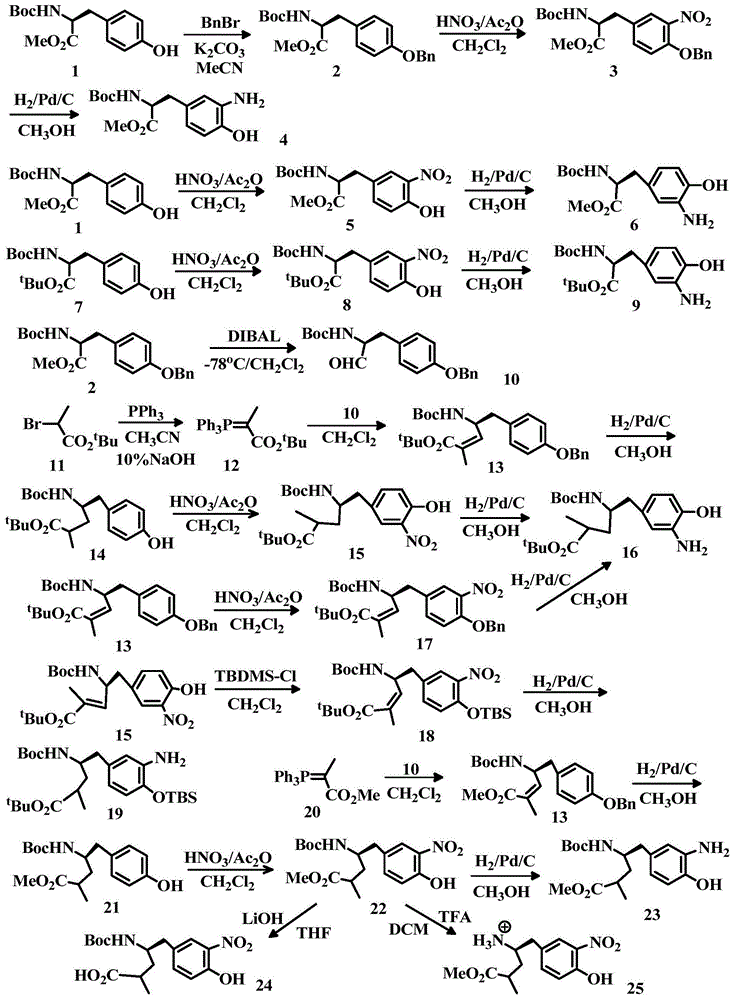
(bpin)2结构_二甲基甲酰胺结构式2,3-二氨基琥珀酰基偶联物连接子的制作方法本发明申请涉及以2,3-二氨基琥珀酰基双连接子(双链连接子)链接细胞毒性药物/分子与细胞结合分子的偶联物。本发明还涉及具有所述连接子的细胞毒性药物/分子与细胞结合分子偶
2,3-二氨基琥珀酰基偶联物连接子的制作方法
 本发明申请涉及以2,3-二氨基琥珀酰基双连接子(双链连接子)链接细胞毒性药物/分子与细胞结合分子的偶联物。本发明还涉及具有所述连接子的细胞毒性药物/分子与细胞结合分子偶联物的制备,尤其是药物具有氨基,羟基,二氨基,氨基羟基,二羟基,羧基,肼,醛和巯基时,可以以特定方式与双连接子结合,以及相应偶联物的治疗用途。 发明背景 抗体药物偶联物(adc),是通过一个有条件稳定的连接子链接的小分子化疗药物与抗体(mabs)的协同组合,可通过受体介导的内吞作用使小分子药物在肿瘤内优先蓄积,而不进入健康的组织,已经成为了一类非常有效的抗癌药物,adc药物目前具有庞大且增长迅速的临床管线。adc的三个组分,单克隆抗体,连接子和细胞毒性药物,均会影响偶联物的功效和毒性。优化每个组分,同时增强adc整体的功能,这一直是adc设计和开发的主要考虑。我们相信,能获得定点释放,有效荷载,最优化学计量和大分子的均质性的连接子技术,对于获得药物良好的药代动力学,功效和耐受性至关重要(lambert,j.和chari,r.,j.med.chem.2014,57,6949-64;ponte,j.等,bioconj.chem.,2016,27(7),1588-98;dovgan,i.等,sci.rep.2016,6,30835;ross,p.l.和wolfe,j.l.j.pharm.sci.105(2),391-7;chen,t.等j.pharm.biomed.anal.,2016,117,304-10;zhao,r.y.等,2011,j.med.chem.54,3606-23)。 先前对抗体药物偶联物(adc)稳定性的研究,由于连接子的相对稳定,主要集中在由于相对稳定的有效负载量(例如美登素)的去偶联而导致的药物释放(piwkoc.等,clin.druginvestig.2015,35(8),487-93;lambert,j.和chari,r.j.med.chem.2014,57,6949-64)。但是上市药物t-dm1(抗体-美登素偶联物)作为her2阳性的、无法切除的局部晚期或转移性乳腺癌的一线治疗方案,和作为her2阳性晚期胃癌的二线治疗方案,在临床试验中均失败,因为相比于其副作用,它对患者的益处有限(ellis,p.a.等,j.clin.oncol.2015,33(2015asco年会附录摘要507);shen,k.等,sci.rep.2016;6:23262;degoeij,b.e.和lambert,j.m.curropinimmunol2016,40,14-23;barrios,c.h.等,j.clin.oncol.2016,34(2016asco年会附录摘要593))。 为解决脱靶毒性问题,研究者在adc分子设计时,试图在单一有效荷载的基础上,扩大连接子-有效载荷和偶联化学的范围,尤其是解决靶向adc上连接子-有效荷载的效能问题(lambert,j.m.ther.deliv.2016,7,279-82;zhao,r.y.等,2011,j.med.chem.54,3606-23)。如今,许多药物开发者和学术机构都非常注重开发新型的可靠的特异性连接子和定点偶联方法,这些adc具有更长的循环半衰期,更高的疗效,可能更低的脱靶毒性,更好的体内药代动力学(pk)特性,以及生产时有更好的批次间一致性(hamblett,k.j.等,clin.cancerres.2004,10,7063-70;adem,y.t.等,bioconjugatechem.2014,25,656-664;boylan,n.j.bioconjugatechem.2013,24,1008–1016;strop,p.等,2013chem.biol.20,161-67;wakankar,a.mabs,2011,3,161–172)。迄今报道的这些特异性偶联方法包括在抗体基因工程改造,引入半胱氨酸(junutula,j.r.等,nat.biotechnol.2008,26,925–32;junutula,j.r.等,2010clin.cancerres.16,4769;美国专利8,309,300;7,855,275;7,521,541;7,723,485;wo2008/),引入硒代半胱氨酸(hofer,t.等,biochemistry2009,48,12047–57;li,x.等,methods2014,65,133–8;美国专利8,916,159),引入含有五氟芳香试剂标签的半胱氨酸(zhang,c.等,nat.chem.2015,8,1–9),引入巯基岩藻糖(okeley,n.m.等,2013bioconjugatechem.24,1650),或引入非天然氨基酸(axup,j.y.等,proc.nat.acad.sci.usa.2012,109,16101-6;zimmerman,e.s.等,2014,bioconjug.chem.25,351–361;wu,p.等,2009proc.natl.acad.sci.106,3000-5;rabuka,d.等,nat.protoc.2012,7,1052-67;美国专利8,778,631;美国专利申请;wo2010/081110,wo2006/069246,wo2007/059312;美国专利7,332,571;7,696,312和7,638,299;wo2007/;美国专利7,632,492和7,829,659),通过二溴马来酰胺(jones,m.w.等j.am.chem.soc.2012,134,1847–52),双砜试剂(badescu,g.等bioconjug.chem.2014,25,1124–36;wo2013/,wo2014/064424),二溴哒嗪二酮(maruani,a.等nat.commun.2015,6,6645)重新桥接还原的分子间二硫化物,通过半乳糖基和唾液酸转移酶(zhou,q.等bioconjug.chem.2014,25,510–520;美国专利申请),甲酰甘氨酸生成酶(fge)(drake,p.m.等bioconj.chem.2014,25,1331–41;carrico,i.s.等,美国专利7,985,783;8,097,701;8,349,910,和美国专利申请,),磷酸泛酰巯基乙胺基转移酶(pptases)(grünewald,j.等bioconjug.chem.2015,26,2554–62),转肽酶a(beerli,r.r.等plosone2015,10,e0)等而偶联,可与streptoverticilliummobaraense转谷氨酰胺酶(mtg)(strop,p.bioconj.chem.2014,25,855–62;strop,p.等,chem.biol.2013,20,161–7;美国专利8,871,908)或与微生物转谷氨酰胺酶(mtgase)(dennler,p.等,2014,bioconjug.chem.25,569–78;siegmund,v.等angew.chemie-int.ed.2015,54,13420–4;美国专利申请;美国专利7,893,019)作用导入谷氨酰胺标签,或通过酶/细菌在蛋白质主链外部形成异肽键-肽键(kang,h.j.等science2007,318,1625–8;zakeri,b.等proc.natl.acad.sci.usa2012,109,e690–7;zakeri,b.&howarth,m.j.am.chem.chem.soc.2010,132,4526–7)而偶联。 我们已经公开了几种桥连天然抗体的链间二硫键被还原产生的一对巯基的偶联方法,例如使用溴代马来酰亚胺和二溴代马来酰亚胺连接子(wo2014/009774),2,3-二取代的琥珀酸/2-单取代的/2,3-二取代的富马酸或马来酸连接子(wo2015/,wo),乙炔二羧酸连接子(wo2015/,wo)或肼连接子(wo2015/)。与通过抗体上的半胱氨酸或赖氨酸残基偶联的传统的、非选择性偶联物相比,用这些连接子和方法制备的adc具有更好的治疗窗口。在本专利申请,我们公开了含2,3-二氨基琥珀酰基的新型双连接子,和它们与细胞毒性分子的偶联方法,特别是细胞毒性分子中含有二氨基,氨基-羟基,二羟基,羧基,醛,肼和巯基等基团时的方法。用双连接子制备的免疫偶联物靶向递送的半衰期延长,并且在血液循环中对非靶细胞,组织或器官的暴露最小,具有更小的脱靶毒性。 技术实现要素: 本发明描述了抗体与细胞毒性分子通过双连接子偶联,特别是当细胞毒性分子具有氨基,羟基,二氨基,氨基-羟基,二羟基,羧基,肼或巯基等两个官能团时。它还提供了双连接子,以特定方式将细胞结合分子与细胞毒性分子偶联的方法。 本发明的一个方面,含有2,3-二氨基琥珀酰基双连接子的偶联物由式(i)、(ii)、(iii)或(iv)表示: 其中: 表示单键; 任选为单键,或可缺省; 任选为单键、双键,或可缺省; n独立地为1-30; q是与r3和r4连接的细胞结合剂/分子,可以是目前已知的,或者即将变为已知的任何种类的分子,可与具有治疗意义或被生物修饰的细胞的片段结合,复合或反应。优选地,细胞结合剂/分子是免疫治疗蛋白,抗体,抗体片段或具有超过四个氨基酸的肽; drug1或/和drug2是细胞毒性分子/剂,是治疗药物,或免疫治疗蛋白质/分子,或用于增强细胞结合剂的结合或稳定细胞结合剂的功能分子,或细胞表面受体结合配体,或抑制细胞增殖的分子; x1和x2相同或不同,独立地选自nh、nhnh、n(r1)、n(r1)n(r2)、o、s、s-s、o-nh.o-n(r1)、ch2-nh、ch2-n(r1)、ch=nh、ch=n(r1)、s(o)、s(o2)、p(o)(oh)、s(o)nh、s(o2)nh、p(o)(oh)nh、nhs(o)nh、nhs(o2)nh、nhp(o)(oh)nh、n(r1)s(o)n(r2)、n(r1)s(o2)n(r2)、n(r1)p(o)(oh)n(r2)、os(o)nh、os(o2)nh、op(o)(oh)nh、c(o)、c(nh)、c(nr1)、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)nh、oc(nh)nh、oc(nr1)nh、nhc(o)nh、nhc(nh)nh、nhc(nr1)nh、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)n(r1)、oc(nh)n(r1)、oc(nr1)n(r1)、nhc(o)n(r1)、nhc(nh)n(r1)、nhc(nr1)n(r1)、n(r1)c(o)n(r1)、n(r1)c(nh)n(r1)、n(r1)c(nr1)n(r1)、或c1-c6烷基、c2-c8烯基,杂烷基、烷基环烷基或杂环烷基、c3-c8芳基、ar-烷基、杂环、碳环、环烷基、杂烷基环烷基、烷基羰基或杂芳基; y1、y2、z1和z2可以相同或不同,独立地连接细胞结合分子q或drug1或drug2的官能团、与之形成二硫化物、醚、酯、硫醚、硫酯、肽、腙、氨基甲酸酯、碳酸酯、胺(仲、叔或季胺)、亚胺、环杂烷基、杂芳族、烷基肟或酰胺键;优选地,y1、y2、z1和z2独立地具有以下结构:c(o)ch、c(o)c、c(o)ch2、arch2、c(o)、nh、nhnh、n(r1)、n(r1)n(r2)、o、s、s-s、o-nh、o-n(r1)、ch2-nh.ch2-n(r1)、ch=nh、ch=n(r1)、s(o)、s(o2)、p(o)(oh)、s(o)nh、s(o2)nh、p(o)(oh)nh、nhs(o)nh、nhs(o2)nh、nhp(o)(oh)nh、n(r1)s(o)n(r2)、n(r1)s(o2)n(r2)、n(r1)p(o)(oh)n(r2)、os(o)nh、os(o2)nh、op(o)(oh)nh、c(o)、c(nh)、c(nr1)、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)nh、oc(nh)nh、oc(nr1)nh、nhc(o)nh、nhc(nh)nh、nhc(nr1)nh、c(o)nh、c(nr1)nh、oc(o)n(r1)、oc(nh)n(r1)、oc(nr1)n(r1)、nhc(o)n(r1)、nhc(nh)n(r1)、nhc(nr1)n(r1)、n(r1)c(o)n(r1)、n(r1)c(nh)n(r1)、n(r1)c(nr1)n(r1);或c1-c8烷基,c2-c8杂烷基,烷基环烷基,杂环烷基;c3-c8芳基、ar-烷基、杂环、碳环、环烷基、杂烷基环烷基、烷基羰基、杂芳基; 优选地,y1、y2、z1和z2与细胞结合剂/分子上的巯基对相连接。巯基优选为通过还原剂将细胞结合剂的链间二硫键还原而产生,还原剂包括二硫苏糖醇(dtt),二硫赤藓糖醇(dte),l-谷胱甘肽(gsh),三(2-羧乙基)膦(tcep),2-巯基乙胺(β-mea),或/和β巯基乙醇(β-me,2-me); r1、r2、r3和r4是包含c,n,o,s,si和p原子的链状结构,最优含0-500个原子,共价连接x和z1,y和z2。r1、r2、r3和r4的各个原子以所有可能的化学方式结合,比如形成亚烷基,亚烯基和亚炔基,醚,聚氧化烯,酯,胺,亚胺,多胺,肼,腙,酰胺,脲,氨基脲,卡巴肼,烷氧胺,氨基甲酸酯,氨基酸,肽,酰氧基胺,异羟肟酸,或上述组合。优选地,r1、r2、r3和r4相同或不同,独立选自o、nh、s、nhnh、n(r5)、n(r3)n(r3’)、如式(och2ch2)por5或(och2ch-(ch3))por5或nh(ch2ch2o)pr5或nh(ch2ch(ch3)o)pr5或n[(ch2ch2o)pr5]-[(ch2ch2o)p’r5’]或(och2ch2)pcoor5或ch2ch2(och2ch2)pcoor5的聚乙烯氧基单,其中p和p’独立地是选自0至约1000的整数,或上述的组合;c1-c8烷基;c2-c8杂烷基,烷基环烷基,杂环烷基;c3-c8芳基,芳烷基,杂环,碳环,环烷基,杂烷基环烷基,烷基羰基或杂芳基; 更优选地,r1、r2、r3、r4、r5和r5’独立地是h,c1-c8烷基,c2-c8杂烷基、烷基环烷基或杂环烷基,c3-c8芳基、ar-烷基、杂环、碳环、杂烷基环烷基、烷基羰基或杂芳基;或c1-c8碳原子酯、醚或酰胺;或1~24个氨基酸;或具有式(och2ch2)p或(och2ch(ch3))p的聚乙烯氧基,其中p是0-约5000的整数,或上述的组合; r1、r2、r3和r4可以任选地包含6-马来酰亚胺基己酰基(“mc”)、马来酰亚胺基丙酰基(“mp”)、缬氨酸-瓜氨酸(“val-cit”或“vc”)、丙氨酸-苯丙氨酸(“ala-phe”或“af”)、对氨基苄氧基羰基(“pab”)、4-硫戊酸酯(“spp”)、4-(n-马来酰亚胺甲基)环己烷-1羧酸酯(“mcc”)、(4-乙酰基)氨基-苯甲酸酯(“siab”)、4-硫代丁酸酯(spdb)、4-硫代-2-羟基磺酰基丁酸酯(2-磺基-spdb)或具有1-8个天然或非天然氨基酸的肽,天然氨基酸优选自天冬氨酸、谷氨酸、精氨酸、组氨酸、赖氨酸、丝氨酸、苏氨酸、天冬酰胺、谷氨酰胺、半胱氨酸、硒代半胱氨酸、酪氨酸、苯丙氨酸、甘氨酸、脯氨酸、色氨酸和丙氨酸; 另外,r1、r2、r3、r4、y1、y2、z1和z2独立地可缺省。 另一方面,本发明提供了含有2,3-二氨基琥珀酰基团的高反应活性的双连接子,如式(v)、(vi)、(vii)和(viii),细胞结合分子的两个或多个基团可以同时或依次与它们反应,形成前文式(i)、(ii)、(iii)和(iv)中的结构: 其中: 任选地是单键或双键或三键,或者可以缺省;当代表三键时,lv1和lv2同时缺省; drug1、drug2、n、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1和z2的定义与式(i)-(iv)中相同; lv1和lv2代表相同或不同的离去基团,可以与细胞结合分子上的巯基、胺、羧酸、硒醇、苯酚或羟基反应。此类离去基团包括但不限于,卤化物(例如氟化物,氯化物,溴化物和碘化物)、甲磺酰基、甲苯磺酰基、三氟甲基磺酰基、三氟甲基磺酸酯、硝基苯氧基、n-琥珀酰亚胺基(nhs)、苯氧基、二硝基苯氧基、五氟苯氧基、四氟苯氧基、三氟苯氧基、二氟苯氧基、一氟苯氧基、五氯苯氧基、1h-咪唑-1-基、一氯苯氧基、二氯苯氧基、三氯苯氧基、四氯苯氧基、n-(苯并三唑基)氧基、2-乙基-5-苯基异恶唑-3′-磺酰基、苯基恶二唑-磺酰基、2-乙基-5-苯基异恶唑基、苯基恶二唑基(oda)、恶二唑基、不饱和键(碳-碳、碳-氮、碳-硫、碳-磷、硫-氮、磷-氮、氧-氮或碳-氧之间的双键或三键),或者与mitsunobu反应的缩合试剂作用产生的中间体分子。 另一方面,本发明提供了如下列式(ix)和(x)的高反应活性的双连接子,其中细胞毒性分子的两个或多个官能团可以同时或依次与之反应形成式(i)、(ii)、(iii)或(iv)中的结构。 其中: q、n、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1和z2的定义和式(i)-(iv)中相同;lv1、lv2、lv1’以及lv2’的定义与lv1与lv2在式(v)-(viii)中的定义相同; 另一方面,本发明提供了如下式(xi)和(xii)的高反应活性的双连接子,细胞毒性分子和细胞结合分子可以独立地、同时或依次与之反应形成式(i)-(iv)中的结构: 其中x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1和z2的定义与式(i)-(iv)中相同;lv1、lv2、lv1’及lv2’的定义与lv1与lv2在式(v)-(viii)中的定义相同; 本发明还涉及制备式(i),(ii),(iii)和(iv)的细胞结合分子-药物偶联物的方法。 附图说明 图1显示了酪氨酸(tyr)和tubutyrosine(tut)类似物的合成,其在苯环上具有氨基或硝基,可与细胞结合分子双链连接。 图2显示了tubulysin类似物片段的合成。 图3显示了tubulysin类似物片段的合成。 图4显示了含有2,3-二氨基琥珀酰基的双连接子和含有具有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成。 图5显示了含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图6显示了含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图7显示了具有含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图8显示了含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联 图9显示了具有含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图10显示了具有含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图11显示了具有含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联,以及澳瑞斯汀片段的合成。 图12显示了含有双连接子的澳瑞斯汀片段的合成。 图13显示了含有双连接子的澳瑞斯汀f的合成及其与抗体的偶联,以及amanitin片段和连接子的合成。 图14显示了含有双连接子的澳瑞斯汀f的合成及其与抗体的偶联。 图15显示了含有双连接子的amanitin类似物的合成。 图16显示了通过抗体上的一对巯基将含有双连接子的amanitin类似物与抗体的偶联。 图17显示了通过抗体上的一对巯基将含有双连接子的amanitin类似物与抗体的偶联。 图18显示了通过抗体的一对巯基和双连接子将tubulysin类似物和cbi二聚体类似物与抗体偶联。 图19显示了含有双连接子的cbi二聚体类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图20显示了含有双连接子的cbi二聚体类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图21显示了含有双连接子的cbi二聚体类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图22显示了含有双连接子的cbi二聚体类似物的合成及其通过抗体的一对巯基与抗体的偶联,以及pbd二聚体片段的合成。 图23显示了含有双连接子的pbd二聚体的合成及其通过抗体的一对巯基与抗体的偶联。 图24显示了含有双连接子的pbd二聚体的合成及其通过抗体的一对巯基与抗体的偶联。 图25显示了含有双连接子的pbd二聚体的合成及其通过抗体的一对巯基与抗体的偶联。 图26显示了含有双连接子的pbd二聚体的合成及其通过抗体的一对巯基与抗体的偶联。 图27比较了偶联物ba-12,ba-14,ba-16,ca-03,ca-04,ca-05,ca-06,ca-07,ca-10,ca-11,ca-12和t-dm1在人胃肿瘤n87细胞模型上的抗肿瘤作用,采用pbs对照,静脉注射,一次给药3mg/kg。除了ca-06以外,所有12种偶联物均显示出抗肿瘤活性。 发明内容 定义 “烷基”是指在烷烃上除去一个或两个氢原子而产生的脂肪烃基团或单价基团。它可以是直链或是支链的,在链中含有c1-c8(1-8个碳原子)。“支链”是指直链烷基上连接有一个或多个低碳数的烷基,如甲基、乙基或丙基。示例性的烷基包括甲基、乙基、正丙基、异丙基、正丁基、叔丁基、正戊基、3-戊基、辛基、壬基、癸基、环戊基、环己基、2,2-二甲基丁基、2,3-二甲基丁基、2,2-二甲基戊基、2,3-二甲基戊基、3,3-二甲基戊基、2,3,4-三甲基戊基、3-甲基-己基、2,2-二甲基己基、2,4-二甲基己基、2,5-二甲基己基、3,5-二甲基己基、2,4-二甲基戊基、2-甲基庚基、3-甲基庚基、正庚基、异庚基、正辛基和异辛基。c1-c8烷基可以是未被取代的或被一个或多个下列基团取代,包括但不限于c1-c8烷基、-o-(c1-c8烷基)、-芳基、-c(o)r’、-oc(o)r’、-c(o)or’、-c(o)nh2,-c(o)nhr’、-c(o)n(r’)2、-nhc(o)r’、-sr’、-s(o)2r’、-s(o)r’、-oh、-卤素、-n3、-nh2、-nh(r’)、-n(r’)2和-cn;其中每个r’独立地选自于c1-c8烷基和芳基。 “卤素”指氟、氯、溴或碘原子;优选氟和氯原子。 “杂烷基”指其中1至4个碳原子独立地被选自o、s和n的杂原子所取代的c2-c8烷基。 “碳环”指含有3到8个碳原子的饱和或不饱和单环,或含有7到13个碳原子的饱和或不饱和双环。单环碳环有3到6个环原子,典型的有5或6个环原子。双环碳环有7到12个环原子,构成[4,5]、[5,5]、[5,6]或[6,6]的双环系统,或有9个或10个环原子,构成[5、6]或[6,6]的双环系统。具有代表性的c3-c8的碳环包括但不限于:-环丙基、-环丁基、-环戊基、-环戊二烯基、-环己基、-环己烯基、-1,3-环己二烯基、-1,4-环己二烯基、-环庚基、-1,3-环庚二烯基、-1,3,5-环庚三烯基、-环辛基和-环辛二烯基。 “c3-c8碳环”可以是未被取代的或被一个或多个下列基团取代,包括但不限于c1-c8烷基、-o-(c1-c8烷基)、-芳基、-c(o)r’、-oc(o)r’、-c(o)or’、-c(o)nh2、-c(o)nhr’、-c(o)n(r’)2、-nhc(o)r’、-sr’、-s(o)r’、-s(o)2r’、-oh、-卤素、-n3、-nh2、-nh(r’)、-n(r’)2及-cn;其中每个r’独立地选自c1-c8烷基和芳基。 “烯基”指含有碳-碳双键的直链或支链脂肪烃基团,链内含有2-8个碳原子。示例性的烯基包括乙烯基、丙烯基、正丁烯基、异丁烯基、3-甲基丁-2-烯基、正戊烯基、己烯基、庚烯基、辛烯基。 “炔基”指含有碳-碳三键的直链或支链脂肪烃基团,链内含有2-8个碳原子。示例性的炔基包括乙炔基、丙炔基、正丁炔基、2-丁炔基、3-甲基丁炔基、5-戊炔基、正戊炔基、己炔基、庚炔基和辛炔基。 “亚烷基”是指含1-18个碳原子的饱和的、支炼或直链或环状烃基,并带有两个通过从母体烷烃的相同或两个不同碳原子上除去两个氢原子而产生的一价自由基。典型的亚烷基包括但不限于:亚甲基(-ch2-)、1,2-乙基(-ch2ch2-)、1,3-丙基(-ch2ch2ch2-)、1,4-丁基(-ch2ch2ch2ch2-)等。 “亚烯基”指含2-18个碳原子的不饱和的、支链或直链或环状烃基,并带有通过从母体烯烃的相同或两个不同碳原子上除去两个氢原子而产生的两个一价自由基。典型的亚烯基包括但不限于:1,2-亚乙基(-ch=ch-)。 “亚炔基”指含2-18个碳原子的不饱和的、支链或直链或环状烃基,并带有通过从母体炔的相同或两个不同碳原子上除去两个氢原子而产生的两个一价自由基。典型的亚炔基包括但不限于:乙炔、炔丙基和4-戊炔基。 “芳基”或“芳香基”指由一个或多个环组成的芳香或杂芳香基团,包含三至十四个碳原子,优选六至十个碳原子。术语“杂芳香基”是指芳香基上的一个或几个碳,最优是一个、两个、三个或四个碳原子,被氧(o)、氮(n)、硅(si)、硒(se)、磷(p)或(s)所取代,优选被氧、硫和氮所取代而产生的基团。术语“芳基”或“芳香基”也指其中一个或几个氢原子独立地被-r’、卤素、-or’、-sr’、-nr’r”、-n=nr’、-n=r’、-nr’r”、-no2、-s(o)r’、-s(o)2r’、-s(o)2or’、-os(o)2or’、-pr’r”、-p(o)r’r”、-p(or’)(or”)、-p(o)(or’)(or”)或-op(o)(or’)(or”)所取代而产生的芳香基团。其中r’和r”独立地为氢、烷基、烯基、炔基、杂烷基、芳基、芳烷基、羰基或其药用盐。 “杂环”指一个环结构,其中一到四个环碳原子独立地被o、n、s、se、b、si或p等杂原子所取代。优选的杂原子是o、n和s。在《化学与物理手册》第78版的225-226页(thehandbookofchemistryandphysics,78thedition,crcpress,inc.,1997-1998,第225页至226页)上也有杂环化合物的相关描述,在此引作参考。优选的非芳基杂环包括环氧基、氮丙啶基、硫杂丙基、吡咯烷基、吡唑烷基、咪唑烷基、环氧乙烷基、四氢呋喃基、二氧戊环基、四氢吡喃基、二噁烷基、二氧戊环基、呱啶基、呱嗪基、吗啉基、吡喃基、咪唑啉基、吡咯啉基、吡唑啉基、噻唑烷基、四氢噻喃基、二噻烷基、硫代吗啉基、二氢吡喃基、四氢吡喃基、二氢吡喃基、四氢吡啶基、二氢吡啶基、四氢嘧啶基、二氢噻喃基、氮杂环庚烷基,以及上述基团与苯基缩合得到的稠环。 术语“杂芳基”或“芳基杂环”是指含3到14,优选5至10个原子的芳香性杂环、包含单环、双环或多环。示例包括吡咯基、吡啶基、吡唑基、噻吩基、嘧啶基、吡嗪基、四唑基、吲哚基、喹啉基、嘌呤基、咪唑基、噻吩基、噻唑基、苯并噻唑基、呋喃基、苯并呋喃基、1,2,4-噻二唑基、异噻唑基、三唑基、四唑基、异喹啉基、苯并噻吩基、异苯并呋喃基、吡唑基、咔唑基、苯并咪唑基、异恶唑基、吡啶基-n-氧化物,以及上述基团与苯基缩合得到的稠环。 “烷基”、“环烷基”、“烯基”、“炔基”、“芳基”、“杂芳基”、“杂环”等也指相应的去除两个氢原子而形成的“亚烷基”、“环亚烷基”、“亚烯基”、“亚炔基”等。 “芳烷基”指烷基上一个与碳原子(通常为末端或sp3碳原子)连接的氢原子被芳基取代而得到的一类非环烷基。典型的芳烷基包括芐基、2-苯基乙-1-基、2-苯基乙烯-1-基、萘基甲基、2-萘基乙-1-基、2-萘基乙-1-基、萘并芐基、2-萘基苯基-1-基等。 “杂芳烷基”指烷基上一个与碳原子(通常为末端或sp3碳原子)连接的氢原子被杂芳基取代而得到的一类非环烷基。杂芳烷基的实例有2-苯并咪唑基甲基、2-呋喃基乙基。 “羟基保护基”的实例包括甲氧基甲基醚、2-甲氧基乙氧基甲基醚、四氢吡喃基醚、芐基醚、对甲氧基芐基醚、三甲基甲硅醚、三乙基硅醚、三异丙基硅醚、叔丁基二甲基硅醚、三苯基甲基硅醚、乙酸酯、取代乙酸酯、特戊酸酯、苯甲酸酯、甲磺酸酯和对甲苯磺酸酯。 “离去基团”指可以被另一个官能团取代的官能团。这些离去基团是本领域公知的,实例包括卤化物(如氯化物、溴化物和碘化物)、甲磺酰基、对甲苯磺酰基和三氟甲磺酰基。优选的离去基团选自硝基苯氧基、n-羟基琥珀酰亚胺基(nhs)、苯氧基、二硝基苯氧基、五氟苯氧基、四氟苯氧基、二氟苯氧基、一氟苯氧基、五氯苯氧基、三氟甲磺酰基、咪唑基、氯酚基、四氯苯氧基、1-羟基苯并三唑基、甲苯磺酰基、甲磺酰基、2-乙基-5-苯基异恶唑-3′-磺酰基,酸酐或与其它酸酐作用形成的酸酐,例如乙酸酐、甲酸酐、或与多肽缩合试剂、mitsunobu反应试剂作用生成的中间体。 以下缩写为本发明所采用,其定义为:boc,叔丁氧基羰基、brop,溴代十四烷基鏻六氟磷酸盐;cdi,1,1′-羰基二咪唑;dcc,二环己基碳二亚胺;dce,二氯乙烷;dcm,二氯甲烷;dead为偶氮二甲酸二乙酯;diad,偶氮二甲酸二异丙基酯;dibal-h,二异丁基氢化铝;dipea或dea,二异丙基乙胺;depc,二乙基氰基磷酸酯;dma,n,n-二甲基乙酰胺;dmap,4-(n,n-二甲基氨基)吡啶;dmf,n,n-二甲基甲酰胺;dmso,二甲基亚砜;dtpa为二亚乙基三胺五乙酸;dtt,二硫苏糖醇;edc,1-(3-二甲基氨基丙基)-3-乙基碳二亚胺盐酸盐;esi-ms,电喷雾质谱;乙酸乙酯,etoac为乙酸乙酯;fmoc,n-(9-芴基甲氧基羰基);hatu,o-(7-氮杂苯并三唑-1-基)-n,n,n’,n’-四甲基脲六氟磷酸盐;hobt,1-羟基苯并三唑;hplc,高效液相色谱;nhs,n-羟基琥珀酰亚胺;mecn为乙腈;meoh为甲醇;mmp,4-甲基吗啉;pab,对氨基苯甲酸;pbs,磷酸盐缓冲液(ph7.0-7.5);ph,为苯基;phe为l-苯丙氨酸;pybrop为溴-三-吡咯烷-鏻六氟磷酸盐;peg,聚乙二醇;sec,尺寸排阻色谱;tcep,三(2-羧乙基)膦;tfa,三氟乙酸;thf,四氢呋喃;val,缬氨酸;tl为薄层色谱;uv为紫外线。 “氨基酸”可以是天然或非天然的,优选α-氨基酸。天然氨基酸由基因所编码,包括丙氨酸、精氨酸、天冬酰胺、天冬氨酸、半胱氨酸、谷氨酸、谷氨酰胺、甘氨酸、组氨酸、异亮氨酸、亮氨酸、赖氨酸、蛋氨酸、苯丙氨酸、脯氨酸、丝氨酸、苏氨酸、酪氨酸、色氨酸和缬氨酸。非天然氨基酸是蛋白质氨基酸的衍生物,包括羟脯氨酸、羊毛硫氨酸、2-氨基异丁酸、脱氢丙氨酸、γ-氨基丁酸(神经递质)、鸟氨酸、瓜氨酸、β-丙氨酸(3-氨基丙酸)、γ-羧基谷氨酸、硒代半胱氨酸(存在于许多非真核以及大多数真核细胞中、但不是由dna直接进行编码)、吡咯赖氨酸(仅在一些古细菌和一种细菌中发现)、n-甲酰基甲硫氨酸(通常是细菌、线粒体和叶绿体中蛋白质中最初的氨基酸)、5-羟色氨酸、l-二羟基苯丙氨酸、三碘甲腺原氨酸、l-3,4-二羟基苯丙氨酸(dopa)和o-磷酸丝氨酸。术语“氨基酸”还包括氨基酸类似物和模拟物。类似物是具有与天然氨基酸相同结构通式h2n(r)chco2h的化合物,其中r在天然氨基酸里未能发现。类似物的实例包括高丝氨酸、正亮氨酸、甲硫氨酸-亚砜和甲硫氨酸甲基锍。更优的是氨基酸模拟物,它是具有与α-氨基酸的化学结构不同、但是功能类似的化合物。天然氨基酸多为“l”立体化学构型,“非天然氨基酸”为“d”构型的氨基酸。在本专利申请中使用1至8个氨基酸时、其序列优选为蛋白水解酶可识别的序列。许多水解酶可识别序列是本领域已知的,可以参见:matayoshi等,science247:954(1990);dunn等,meth.enzymol.241:254(1994);seidah等,meth.enzymol.244:175(1994);thornberry,meth.enzymol.244:615(1994);weber等,meth.enzymol.244:595(1994);smith等,meth.enzymol.244:412(1994)及bouvier等,meth.enzymol.248:614(1995);此处引作参考。特别是选自以下序列:val-cit、ala-val、ala-ala、val-val、val-ala-val、lys-lys、ala-asn-val、val-leu-lys、cit-cit、val-lys、ala-ala-asn、asp-lys、asp-glu、glu-lys、lys、cit、ser及glu。 “糖苷”是糖通过糖苷键在其异头碳上与另一基团键合得到的分子。糖苷可以通过o-、n-、s-或c-糖苷键连接,分别产生o-糖苷、糖基胺、硫代糖苷和c-糖苷。其结构式为cm(h2o)n(其中m可以不同于n,m、n<36)。本发明中的糖苷包括葡萄糖(右旋糖)、果糖(左旋糖)、阿洛糖、阿卓糖、甘露糖、古洛糖、艾杜糖、半乳糖、塔罗糖、半乳糖胺、氨基葡萄糖、唾液酸、n-乙酰氨基葡萄糖、磺基奎诺糖(6-脱氧-6-磺基-d-吡喃葡萄糖)、核糖、阿拉伯糖、木糖、来苏糖、山梨糖醇、甘露醇、蔗糖、乳糖、麦芽糖、海藻糖、麦芽糖糊精、棉子糖、葡萄糖醛酸(葡糖苷酸)和水苏糖。它可以是d或l的构型、5原子环状呋喃糖的形式、6原子环状吡喃糖的形式,或是非环形式、α-异构体(异头碳的-oh在haworth投影碳原子平面之下)、或β-异构体(异头碳的-oh在haworth投影碳原子平面之上),包括单糖、二糖、多醇或含3-6个糖单的低聚糖。 本发明申请中的“抗体”指全长免疫球蛋白分子或全长免疫球蛋白分子的免疫活性部分,如含有抗原结合位点的分子,该结合位点免疫特异性地与靶标抗原或部分靶标抗原结合,靶标包括但不限于,癌细胞或产生与自身免疫疾病相关的自免疫抗体的细胞。本发明中的免疫球蛋白可以是免疫球蛋白的任何类型(例如igg、ige、igm、igd、iga和igy)、类别(例如igg1、igg2、igg3、igg4、iga1和iga2)或子类。免疫球蛋白可以来自任何物种,但优选的免疫球蛋白来源于人、鼠或兔。本发明的抗体优选是单克隆抗体,包括但不限于多克隆、单克隆、双特异性、人、人源化或嵌合抗体,单链抗体,fv、fab片段、f(ab’)片段、f(ab’)2片段、由fab表达库产生的片段,抗独特型(抗id)抗体,cdr和任何能免疫特异性地结合癌细胞抗原、病毒抗原或微生物抗原的上述结构的表位结合片段。 “对映异构体”,也称为“光学异构体”,是两个立体异构体中的一个,它们是彼此的镜像,不可重迭(不等同),就像人的左右手,除非沿着某一平面被翻转,它们是不可重迭的(仅通过改变方向不能让双手重迭)。化合物中的单个手性原子或类似的结构特征使得该化合物具有两种可能的结构,它们不可重迭,是彼此的镜像。在某一化合物中存在的多个手性特征增加了可能存在的构型的数目,其中可能会有一些互为镜像。对映体纯的化合物是指在检测方法的能力范围内,仅具有同一种手性的样品。在对称的环境中,两个对映体可以使平面偏振光(+/-)在相反的方向上等量旋转(偏振光可以被认为是不对称的介质),除此之外,它们具有相同的化学性质和物理性质。由于这个原因,它们有时也被称为光学异构体。光学异构体及其等量的对映体的混合物被称为外消旋体,它对平面偏振光无净旋转,因为每个正旋转(+)都被负旋转(-)完全抵消。通常两个对映异构体与其他的对映异构体物质发生不同的化学反应。由于许多生物分子是对映体,因此有时两种对映体对生物有机体的影响存在显著差异。例如,在药物中,通常只有一种对映体可以发生想要的生理作用,而另一种对映体或是活性较低、或无活性,有时甚至产生不良反应。基于这样的发现,可以开发仅由一种对映体(“对映体纯”)组成的药物以增强药理学效力,有时还可以消除一些副作用。 同位素是特定化学素的质子数相同,中子数不同的不同核素。同一素的所有同位素具有相同数量的质子。一个原子序数指定一个特定的素,但非同位素;特定素原子可以有不同的中子数。核子(质子和中子)的数量是原子的质量数,特定素的每个同位素具有不同的质量数。例如、碳-12、碳-13和碳-14是碳素的三种同位素,质量数分别为12,13和14。碳的原子序数为6,意味着每个碳原子都有6个质子,因此这些同位素的中子数分别为6、7和8。氢原子有三种同位素:氕(1h)、氘(2h)和氚(3h),氘的质量是氕的两倍,氚的质量是氕的三倍。通过动力学同位素效应,同位素替代实验可用于确定化学反应的机理。同位素替代实验还可用于研究外源化合物通过吸收和分布机制进入体内后,身体如何对它产生作用,体内物质的代谢变化(例如通过细胞色素p450或葡萄糖醛酸转移酶等代谢酶的作用),以及药物代谢产物的排泄途径,是为药代动力学(pk)研究。同位素替代实验可用于研究药物的生化和生理作用,包括在动物(包括人类)、微生物或生物组合上所显现出来的作用(例如感染),是为药效学(pd)研究。两者(pk和pd)一起决定药物的剂量、益处及副作用。同位素可以采用一种稳定的(非放射性的)或非稳定的素。药物的同位素取代物还可能具有与原始药物不同的治疗功效。 “药学上”或“药学上可接受的”是指当分子实体和组合物酌情施用于动物或人时,不会产生不利、过敏或其他不良反应。 “药学上可接受的溶剂化物”或“溶剂化物”是指一种或多种溶剂分子与本发明公开的化合物的结合物。形成药学上可接受的溶剂合物的溶剂的实例,包括但不限于水、异丙醇、乙醇、甲醇、dmso、乙酸乙酯、乙酸和乙醇胺。 “药学上可接受的辅料”包括任何载体、稀释剂、佐剂或其它介质,例如防腐剂或抗氧化剂、填充剂、崩解剂、润湿剂、乳化剂、悬浮剂、溶剂、分散介质、包衣剂、抗细菌剂和抗真菌剂、等渗剂和吸收延迟剂等。这些介质和药剂与药物活性物质一起使用在本领域内是熟知的。任何传统介质或药剂,除非与活性成分不兼容,也可以考虑将其用于治疗组合物中。补充活性成分也可以加入组合物中,成为合适的治疗组合。 本发明中,“药用盐”是指此处公开化合物的衍生物,是母体化合物的酸盐或碱盐。药学上可接受的盐包括由无毒无机酸或有机酸与母体化合物形成的常规无毒盐或季铵盐。例如,所述常规无毒盐包括衍生自无机酸(例如盐酸、氢溴酸、硫酸、氨基磺酸、磷酸、硝酸等)的盐;以及由有机酸,例如乙酸、丙酸、琥珀酸、酒石酸、柠檬酸、甲磺酸、苯磺酸、葡萄糖醛酸、谷氨酸、苯甲酸、水杨酸、甲苯磺酸、草酸、富马酸、马来酸及乳酸等制备的盐。另外的盐包括铵盐,如三甲胺、葡甲胺、丙三醇等的盐、金属盐、如钠、钾、钙、锌或镁盐。 本发明中的药用盐可以从包含酸性或碱性片段的母体化合物,用常规的化学方法制成。一般地说,这些盐可以通过在本发明化合物的游离酸或碱的水溶液或有机溶液或两者的混合溶液中,加入其它适当的等当量的碱或酸而形成。非水相的反应介质一般为乙醚,乙酸乙酯,乙醇,异丙醇或者乙腈。可以适用盐的列表可参见《remington’spharmaceuticalsciences》,第17版,mackpublishingcompany,easton,pa,1985,第1418页。 “施用”或“给药”是指以任何方式向受试者转移、递送、引入或运输药物或其他药剂。这些方式包括口服用药、局部接触、静脉内、腹膜内、肌肉内、病灶内、鼻内、皮下或鞘内给药。本发明还考虑使用装置或器械来施用药剂。这种装置可以使用主动或被动型传输,而且可以是缓释或快速释放递送装置。 “治疗有效量”是指有效预防或治疗本文提及的病理状况的,本发明化合物/药物的量。 术语“患者”或“受试者”指受到或可能受到本文所述病理状况影响的动物或人。优选地,患者是人类。 就癌症而言,术语“治疗”包括以下任何一项或全部:阻止肿瘤细胞或癌细胞生长、复制,减轻整体肿瘤量,以及改善与该疾病相关的一个或多个症状。 就自身免疫性疾病而言,术语“治疗”包括以下任一项或全部:阻止与自身免疫性疾病相关的细胞的复制,包括但不限于能够产生自身免疫性抗体的细胞,减轻自身免疫性抗体量和改善自身免疫性疾病的一个或多个症状。 就传染病而言、术语“治疗”包括以下任何一项或全部:阻止引起传染病的病原体的生长、增殖或复制、以及改善传染病的一个或多个症状。 “哺乳动物”或“动物”的实例包括但不限于人、鼠、家鼠、豚鼠、猴、猪、山羊、牛、马、狗、猫、鸟和家禽。 术语“化合物”,“细胞毒剂”,“细胞毒性化合物”,“细胞毒性二聚体”和“细胞毒性二聚体化合物”可互换使用,包括本发明中或参考文献中公开的结构、结构式代表的结构或其衍生物。该术语还包括本发明中公开的化合物的立体异构体、几何异构体、互变异构体、溶剂化物、代谢产物、盐(例如药学上可接受的盐)和前药以及它们的盐。还包括任何上述结构的溶剂化物、水合物和多晶型物。本发明中在某些方面具体列举“立体异构体”、“几何异构体”、“互变异构体”、“溶剂化物”、“代谢物”、“盐”、“前药”、“前药盐”、“偶联物”、“偶联物的盐”、“溶剂化物”、“水合物”或“多晶型物”,不应据此认为,若在本发明的其他方面仅仅使用术语“化合物”,而未列举上述术语时,是有意省略这些形式。 术语“亚胺反应性试剂”是指能够与亚胺基反应的试剂。亚胺反应性试剂的实例包括但不限于亚硫酸盐(h2so3,h2so2或hso3-,so32-,hso2-与阳离子形成的盐),焦亚硫酸盐(h2s2o5或s2o52-与阳离子形成的盐),单,二,三和四硫代磷酸酯(po3sh3、po2s2h3、pos3h3、ps4h3或po3s3-、po2s23-、pos33-、ps43-与阳离子形成的盐),硫代磷酸酯((r5o)2ps(or5)、r5sh、r5soh、r5so2h、r5so3h),各种胺(羟胺(nh2oh)、肼(nh2nh2)、nh2or5、r5nhr5’、nh2r5),nh2-co-nh2、nh2-c(=s)-nh2、硫代硫酸盐(h2s2o3或s2o32-与阳离子形成的盐)、连二亚硫酸盐(h2s2o4或s2o42-与阳离子形成的盐)、二硫代磷酸酯(p(=s)(or5)(sh)(oh)或与阳离子形成的盐)、异羟肟酸(r5c(=o)nhoh或与阳离子形成的盐)、酰肼(r5conhnh2)、甲醛次硫酸盐(hoch2so2h或hoch2so2-与阳离子形成的盐,例如hoch2so2-na+)、糖化核苷酸(例如gdp-甘露糖)、fludarabine或它们的混合物,其中r5和r5’都独立地为具有1至8个碳原子的直链或支链烷基、并被至少一个选自-–n(r5)(r5’)、-co2h、-so3h、和-po3h的取代基取代;r5和r5’可以进一步可选地被本文所述烷基取代基取代;优选地,阳离子是单价阳离子,例如na+或k+。优选地,亚胺反应性试剂选自亚硫酸盐、羟胺、尿素和肼。更优选地,亚胺反应性试剂是nahso3或khso3. “细胞结合剂”或“细胞结合分子”可以是目前已知的或将成为已知的分子,包括肽和非肽。通常,它们可以是抗体(尤其是单克隆抗体)或包含至少一个结合位点的抗体片段、淋巴因子、激素、生长因子、营养转运分子(例如转铁蛋白),或任何其他细胞结合分子或物质(例如维生素)。 可以使用的细胞结合剂的更具体的例子包括:单克隆抗体、单链抗体、抗体的片段,例如fab、fab’、f(ab’)2、fv(parham,j.immunol.131,2895-2902(1983);spring等,j.immunol.,113,470-478(1974);nisonoff等,arch.biochem.biophys.,89,230-244(1960))、fab表达文库产生的片段、抗独特型(anti-id)抗体、cdr、以上任一项的可以其免疫特异性结合癌细胞抗原、病毒抗原或微生物抗原的表位结合片段;干扰素;肽;淋巴因子如il-2、il-3、il-4、il-6;激素,例如胰岛素、trh(促甲状腺激素释放激素)、msh(促黑素细胞刺激激素)、类固醇激素,例如雄激素和雌激素;生长因子和集落刺激因子,例如egf、tgfα、胰岛素样生长因子(igf-i、igf-ii)、g-csf、m-csf和gm-csf(burgess,immunologytoday,5,155-158(1984));维生素,例如叶酸;转铁蛋白(o’keefe等,j.biol.chem.,260,932-937(1985))。 利用单克隆抗体技术可以生产极具选择性的细胞结合剂,特异性的单克隆抗体。在本领域中众所周知的产生单克隆抗体技术是,通过用感兴趣的抗原,例如完整的靶细胞,从靶细胞,全病毒,灭火全病毒,病毒蛋白,如病毒外壳蛋白等分离的抗原,来免疫小鼠,大鼠,仓鼠或任何其他哺乳动物而产生。合适的细胞结合剂的选择是取决于待靶向的特定细胞群,但是通常,如果可以获得合适的单克隆抗体,则优选单克隆抗体。 本专利公开了新型双连接子偶联物,其中的连接子及其合成实例如图1至26和实施例所示。 一种含2,3-二氨基琥珀酰基双链接的细胞结合剂和细胞毒性分子的偶联物 双链接偶联物如结构式(i),(ii),(iii)或(iv)所示: 或其光学异构体、外消旋体、非对映体或对映体; 其中 代表单键; 代表可选为单键或可以缺省; 代表可选为单键,双键,或者可以缺省;n独立地为1到30; q是连接到r3和r4的细胞结合剂/分子,可以是目前已知的,或者即将成为已知的任何种类的分子,可与具有治疗意义或生物学修饰的细胞群的片段结合,复合或反应。优选地,细胞结合剂/分子是免疫治疗蛋白,抗体,单链抗体;与靶细胞结合的抗体片段;单克隆抗体;单链单克隆抗体;或结合靶细胞的单克隆抗体片段;嵌合抗体;与靶细胞结合的嵌合抗体片段;域抗体;与靶细胞结合的域抗体片段;模拟抗体的adnectins;darpins;淋巴因子;激素;维生素;增长因子;集落刺激因子;或营养转运分子(转铁蛋白);含超过四个氨基酸的结合肽,或蛋白质,或抗体,或附着在白蛋白,聚合物,树枝状大分子,脂质体,纳米颗粒,囊泡或(病毒)衣壳上的小的细胞结合分子或配体; drug1或/和drug2是细胞毒性分子/药剂是治疗药物/分子/试剂,或免疫治疗蛋白质/分子,或用于增强细胞结合或稳定细胞结合剂的功能分子,或细胞表面受体结合配体,或抑制细胞增殖分子;或用于监测,检测或研究细胞结合作用的分子。它也可以是免疫治疗化合物、化学治疗化合物的类似物或前药,或药学上可接受的盐,水合物或水合盐,或晶体,或光学异构体,外消旋体,非对映异构体或对映异构体,抗体(probody)或抗体(probody)片段,或sirna、dna分子,或细胞表面结合配体; 优选地,细胞毒性分子是许多小分子药物中的任何一种,包括但不限于tubulysins、卡奇霉素、澳瑞斯汀、美登素、cc-1065类似物、吗啉代多柔比星、紫杉烷、cryptophycins、鹅膏毒素(例如amanitins)、埃坡霉素、艾日布林、格尔德霉素、喜树碱(例如sn-38)、多卡霉素、道诺霉素、甲氨蝶呤、长春地辛、长春新碱和苯并二氮杂卓二聚体(例如吡咯并苯并二氮杂卓(pbd)、托马霉素、吲哚啉并苯并二氮杂卓、咪唑并噻二氮杂卓或恶唑烷并苯并二氮杂卓的二聚体); x1和x2相同或不同,独立地选自nh、nhnh、n(r1)、n(r1)n(r2)、o、s、s-s、o-nh、o-n(r1)、ch2-nh、ch2-n(r1)、ch=nh、ch=n(r1)、s(o)、s(o2)、p(o)(oh)、s(o)nh、s(o2)nh、p(o)(oh)nh、nhs(o)nh、nhs(o2)nh、nhp(o)(oh)nh、n(r1)s(o)n(r2)、n(r1)s(o2)n(r2)、n(r1)p(o)(oh)n(r2)、os(o)nh、os(o2)nh、op(o)(oh)nh、c(o)、c(nh)、c(nr1)、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)nh、oc(nh)nh、oc(nr1)nh、nhc(o)nh、nhc(nh)nh、nhc(nr1)nh、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)n(r1)、oc(nh)n(r1)、oc(nr1)n(r1)、nhc(o)n(r1)、nhc(nh)n(r1)、nhc(nr1)n(r1)、n(r1)c(o)n(r1)、n(r1)c(nh)n(r1)、n(r1)c(nr1)n(r1);或c1-c6烷基;c2-c8烯基、杂烷基、烷基环烷基或杂环烷基;c3-c8芳基、芳烷基、杂环、碳环、环烷基、杂烷基环烷基、烷基羰基或杂芳基; y1、y2、z1和z2是相同或不同的官能团,独立地通过二硫化物,硫醚,硫酯,肽,腙,醚,酯,氨基甲酸酯,碳酸酯,胺(二级,三级或四级),亚胺,环杂烷基,杂芳基,烷氧基或酰胺键,连接至细胞结合分子q;优选地,y1、y2、z1和z2独立地具有以下结构:c(o)ch、c(o)c、c(o)ch2、arch2、c(o)、nh、nhnh、n(r1)、n(r1)n(r2)、o、s、s-s、o-nh、o-n(r1)、ch2-nh.ch2-n(r1)、ch=nh、ch=n(r1)、s(o)、s(o2)、p(o)(oh)、s(o)nh、s(o2)nh、p(o)(oh)nh、nhs(o)nh、nhs(o2)nh、nhp(o)(oh)nh、n(r1)s(o)n(r2)、n(r1)s(o2)n(r2)、n(r1)p(o)(oh)n(r2)、os(o)nh、os(o2)nh、op(o)(oh)nh、c(o)、c(nh)、c(nr1)、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)nh、oc(nh)nh;oc(nr1)nh、nhc(o)nh、nhc(nh)nh、nhc(nr1)nh、c(o)nh、c(nr1)nh、oc(o)n(r1)、oc(nh)n(r1)、oc(nr1)n(r1)、nhc(o)n(r1)、nhc(nh)n(r1)、nhc(nr1)n(r1)、n(r1)c(o)n(r1)、n(r1)c(nh)n(r1)、n(r1)c(nr1)n(r1);或c1-c8烷基、c2-c8杂烷基、烷基环烷基、杂环烷基;c3-c8芳基、芳烷基、杂环、碳环、环烷基、杂环烷基、烷基羰基、杂芳基; 优选地,y1、y2、z1和z2连接到细胞结合剂/分子的巯基对上。巯基优选地是通过选自二硫苏糖醇(dtt)、二硫代三甘醇(dte)、l-谷胱甘肽(gsh)、三(2-羧乙基)磷化氢(tcep)、2-巯基乙胺(β-mea)或/和β-巯基乙醇(β-me,2-me)的还原剂将细胞结合剂的链间二硫键还原而生成的成对硫原子; r1、r2、r3和r4是包含c,n,o,s,si和p原子的链状结构,最优含0-500个原子,共价连接x和z1,y和z2。r1、r2、r3和r4中的各个原子以所有可能的化学方式结合,比如形成亚烷基,亚烯基和亚炔基,醚,聚氧化烯,酯,胺,亚胺,多胺,肼,腙,酰胺,脲,氨基脲,卡巴肼,烷氧胺,氨基甲酸酯,氨基酸,肽,酰氧基胺,异羟肟酸,或上述组合。优选地,r1、r2、r3和r4相同或不同,独立地选自o、nh、s、nhnh、n(r5)、n(r3)n(r3’)、如式(och2ch2)por5、(och2ch-(ch3))por5、nh(ch2ch2o)pr5、nh(ch2ch(ch3)o)pr5、n[(ch2ch2o)pr5]-[(ch2ch2o)p’r5’]、(och2ch2)pcoor5、ch2ch2(och2ch2)pcoor5的聚乙烯氧基单,其中p和p’独立地是选自0至约1000的整数,或上述的组合;c1-c8烷基;c2-c8杂烷基,烷基环烷基,杂环烷基;c3-c8芳基,芳烷基,杂环,碳环,环烷基,杂烷基环烷基,烷基羰基或杂芳基; 更优选的r1、r2、r3、r4、r5和r5’独立地为h、c1-c8烷基、c2-c8杂烷基、烷基环烷基或杂环烷基、c3-c8芳基、芳烷基、杂环、碳环、杂烷基环烷基、烷基羰基或杂芳基;或c2-c8酯、醚或酰胺;或1~24氨基酸;或结构式为(och2ch2)p或(och2ch(ch3))p的聚乙烯氧基单,其中p是0到约5000的整数,或上述组合; r1、r2、r3和r4可任选地由下列一个或多个连接子组分构成:6-马来酰亚胺基己酰基(“mc”)、马来酰亚胺丙酰基(“mp”)、缬氨酸-瓜氨酸(“val-cit”或“vc”)、丙氨酸-苯丙氨酸(“ala-phe”或“af”)、对氨基芐氧基-羰基(“pab”)、4-硫代戊酰基(“spp”)、4-(n-马来酰亚胺甲基)环己烷-1酰基(“mcc”)、(4-乙酰基)氨基苯酰基(“siab”)、4-硫丁酰基(spdb)、4-硫-2-羟基磺酰基-丁酰基(2-sulfo-spdb),或含有1-8个天然或非天然氨基酸单的天然或非天然肽。天然氨基酸最优选自天冬氨酸、谷氨酸、精氨酸、组氨酸、赖氨酸、丝氨酸、苏氨酸、天冬酰胺、谷氨酰胺、半胱氨酸、硒代半胱氨酸、酪氨酸、苯丙氨酸、甘氨酸、脯氨酸、色氨酸和丙氨酸; 此外,r1、r2、r3和r4独立地可包含以下亲水结构之一: 其中是连接位点;x3、x4、x5、x6和x7独立地选自nh、nhnh、n(r5)、n(r5)n(r5’)、o、s、c1-c6烷基、c2-c6杂烷基、烷基环烷基或杂环烷基、c3-c8芳基、芳烷基、杂环、碳环、环烷基、杂环烷基、烷基羰基、杂芳基、或1~8个氨基酸;其中r5和r5’独立地为h、c1-c8烷基、c2-c8杂烷基、烷基环烷基或杂环烷基、c3-c8芳基、芳烷基、杂环、碳环、杂环烷基、烷基羰基或杂芳基、c1-c8酯、醚或酰胺;或具有式(och2ch2)p或(och2ch(ch3))p的聚乙烯氧基,其中p是0到约5000的整数,或其组合; r1、r2、r3、r4、y1、y2、z1和z2独立地可以含有自我毁灭或非自我毁灭的组分,肽单、腙键、二硫化物、酯、肟、酰胺或硫醚键。自我毁灭单包括但不限于,与对氨基芐基氨甲酰基(pab)电子结构相似的芳香化合物,例如2-氨基咪唑-5-甲醇的衍生物、杂环pab类似物、β-葡糖苷酸、以及邻或对氨基芐基缩醛; 优选地,自我毁灭型连接子组分具有以下结构之一: 其中(*)标记的原子是另外的间隔体或可断裂连接子单、或细胞毒性剂和/或结合分子(cba)的连接点;x1、y1、z2和z3独立地为nh、o或s;z1独立地为h、nhr5、or1、sr5、cox1r5,其中x1和r5如前文所定义;v为0或1;u1独立地为h、oh、c1-c6烷基,(och2ch2)n、f、cl、br、i、or5、sr5、nr5r5’、n=nr5、n=nr5、n=r5、nr5r5’、no2、sor5r5’、so2r5、so3r5、so3r5、oso3r5、oso3r5、pr5r5’、po5r5’、po2r5r5’、opo(or5)(or5′)或och2po(or5(or5(or5′)、其中,其中,r5和r5’独立选自h、c1-c8烷基、c2-c8烷基,烯基、杂烷基或氨基酸;c3-c8芳基、烷基、烷基、烷基、或氨基酸;c3-c8芳基、杂环、碳环、环烷基、杂环烷基、杂芳烷基、烷基羰基或糖苷;或药用阳离子盐;; 非自我毁灭型连接子组分具有以下结构之一: 其中(*)标记的原子是另外的间隔体或可释放的连接子单、或细胞毒性剂和/或结合分子的连接点;x1、y1、u1、r5、r5’如前文所定义;r为0~100;m和n独立地为0~6; 进一步优选地,r1、r2、r3和r4独立地包含可释放的连接子组分。术语“可释放的”是指连接子上包含至少一个可在生理条件下被破坏的键,例如ph、酸、碱、氧化作用、代谢、生化或酶不稳定的键。应当理解,导致键断裂不一定是生物或代谢过程、而可能是一个标准化学反应、例如水解或取代反应,这种生理条件的例子有:ph值比细胞浆内ph低的内涵体,恶性细胞内存在的毫摩尔浓度的大量谷胱甘肽(与细胞内巯基发生二硫键交换反应); 可释放连接子组分r1、r2、r3和r4的实例包括但不限于: -(cr5r6)m(aa)r(cr7r8)n(och2ch2)t-、(cr5r6)m(cr7r8)n(aa)r(och2ch2)t-、(aa)r-(cr5r6)m(cr7r8)n(och2ch2)t-、(cr5r6)m(cr7r8)n(och2ch2)r(aa)t-、-(cr5r6)m-(cr7=cr8)(cr9r10)n(aa)t(och2ch2)r-、-(cr5r6)m(nr11co)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m(aa)t(nr11co)(cr9r10)n(och2ch2)r-、-(cr5r6)m(oco)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、-(cr5r6)m(co)(aa)t-(cr9r10)n(och2ch2)r-、-(cr5r6)m(nr11co)(aa)t(cr9r10)n(och2ch2)r-、-(cr5r6)m-(oco)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、-(cr5r6)m(co)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m-苯基co(aa)t(cr7r8)n-、-(cr5r6)m-呋喃co(aa)t(cr7r8)n-、-(cr5r6)m-恶唑co(aa)t(cr7r8)n-、-(cr5r6)m-噻唑基co(aa)t(ccr7r8)n-、-(cr5r6)t-噻吩co(cr7r8)n-、-(cr5r6)t-咪唑co-(cr7r8)n-、-(cr5r6)t-吗啉co(aa)t-(cr7r8)n-、-(cr5r6)t哌嗪-co(aa)t-(cr7r8)n-、-(cr5r6)t-n甲基co(aa)t-(cr7r8)n-、-(cr5r)m-(aa)t苯基-、-(cr5r6)m-(aa)t呋喃、-(cr5r6)m-恶唑(aa)t、-(cr5r6)m-噻唑基(aa)t、-(cr5r6)m-噻吩-(aa)t-、-(cr5r6)m-咪唑(aa)t-、-(cr5r6)m-吗啉(aa)t-、-(cr5r6)m-哌嗪(aa)t-、-(cr5r6)m-n甲基哌嗪(aa)t-、k(cr5r6)m(aa)r(cr7r8)n(och2ch2)t-、k(cr5r6)m(cr7r8)n(aa)r(och2ch2)t-、k(aa)r-(cr5r6)m(cr7r8)n(och2ch2)t-、k(cr5r6)m(cr7r8)n(och2ch2)r(aa)t-、k(cr5r6)m-(cr7=cr8)(cr9r10)n(aa)t(och2ch2)r-、k(cr5r6)m(nr11co)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m(aa)t(nr11co)(cr9r10)n(och2ch2)r-、k(cr5r6)m(oco)(aa)t(cr9r10)n-(och2ch2)r-、k(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m(co)(aa)t-(cr9r10)n(och2ch2)r-、k(cr5r6)m(nr11co)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m-(oco)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、k-(cr5r6)m(co)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m-苯基co(aa)t(cr7r8)n-、k-(cr5r6)m-呋喃co(aa)t-(cr7r8)n-、k(cr5r6)m-恶唑co(aa)t(cr7r8)n-、k(cr5r6)m-噻唑基co(aa)t-(cr7r8)n-、k(cr5r6)t-噻吩co(cr7r8)n-、k(cr5r6)t咪唑-co-(cr7r8)n-、k(cr5r6)t吗啉co(aa)t(cr7r8)n-、k(cr5r6)t哌嗪-co(aa)t-(cr7r8)n-、k(cr5r6)t-n甲基co(aa)t(cr7r8)n-、k(cr5r)m(aa)t苯基、k-(cr5r6)m-(aa)t呋喃-、-k(cr5r6)m-恶唑(aa)t-、k(cr5r6)m-噻唑基(aa)t-、k(cr5r6)m-噻吩-(aa)t-、k(cr5r6)m-咪唑(aa)t-、k(cr5r6)m-吗啉(aa)t-、k(cr5r6)m-哌嗪(aa)t-、k(cr5r6)mn甲基哌嗪(aa)t-;其中aa、m和n定义如前文所描述;t和r独立地为0-100;r3、r4、r5、r6、r7和r8独立地选自h、卤化物、c1-c8烷基、c2-c8芳基、烯基、炔基、醚、酯、胺或酰胺,这些基团均可以被以下基团所取代:一个或多个卤素、cn、nr1r2、cf3、or1、芳基、杂环、s(o)r1、so2r1、-co2h、-so3h、-or1、-co2r1、-conr1、-po2r1r2、-po3h或p(o)r1r2r3;k是nr1、-ss-、-c(=o)-、-c(=o)nh-、-c(=o)o-、-c=nh-o-、-c=n-nh-、-c(=o)nh-nh-、o、s、se、b、het(c3-c8杂环或杂芳环),或含有1-20个相同或不同氨基酸的肽。 更优选地,r1、r2、r3和r4独立地为具有1-18个碳原子的直链烷基,或具有式(och2ch2)p的聚乙烯氧基单,p=1~5000,或含有1~20个氨基酸单(l或d形式)的肽,或上述组合。 此外,y1、y2、r1、r2、r3、r4、z1或z2可独立地由以下一个或多个组分构成: 6-马来酰亚胺己酰胺基(mc)、马来酰亚胺基丙酰胺基(mp)、硫代马来酰胺基、硫代氨基氧代丁酸、硫代氨基氧代丁烯酸、缬氨酸瓜氨酸(val-cit)、丙氨酸苯丙氨酸(ala-phe)、赖氨酸苯丙氨酸(lys-phe)、赖氨酸丙氨酸(lys-ala),p-对氨基苄氧羰基(pab)、4-硫代戊酰基(spp)、4-硫代丁酰基(spdb),4-(n-马来酰亚胺甲基)环已烷基-1-酰基(mcc)、马来酰亚胺乙胺基(me)、4-硫代-2-羟基磺酰基丁酰基(2-磺酰-spdb)、芳基硫基(pys),(4-乙酰基)氨基苯甲酰基(siab)、氧基苄基硫基、氨基苄基硫基、二氧基苄硫基、二氨基苄硫基、氨基氧基苄硫基、烷氧基氨基(aoa)、亚乙基氧基(eo)、4-甲基-4-二硫代戊酰基(mpdp)三唑、二硫代、烷基磺酰基、烷基磺酰胺基、磺胺双酰胺基、磷酸二酰胺基、烷基膦酰胺酸基、次膦酸基、n-甲基烷基膦酰胺酸基、n,n’-二甲基膦酰胺酸基、烷基二膦酰胺基,肼、乙酰亚胺;肟、乙酰乙酰肼、氨基乙胺、氨基乙基-氨基乙基胺,和l-或d-,或含有1-20个氨基酸的天然或非天然肽;其中原子中间的连接键意味着它可以连接相邻的碳原子键;其中波浪线指另外键连接的位点; 或者,y1、y2、r1、r2、r3、r4、z1或z2可以独立地缺省,但是y1、y2、r1、r2、r3、r4、z1和z2不可以同时缺省。 优选地,式(i)、(ii)、(iii)和(iv)的立体异构体可由下列式(ia)、(ib)、(ic)、(iia)、(iib)、(iic)、(iva)、(ivb)和(ivc)表示: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、drug1和drug2与前文定义相同。 优选地,双连接偶联物用以下式(i-01)、(i-02)、(i-03)、(i-04)、(i-05)、(i-06)、(i-07)、(i-08)、(i-09)、(i-10)、(i-11)、(i-12)、(i-13)、(i-14)、(i-15)、(i-16)、(i-17)、(i-18)、(i-19)、(i-20)、(i-21)、(i-22)、(i-23)、(ii-01)、(ii-02)、(ii-03)、(ii-04)、(ii-05)、(ii-06)、(ii-07)、(ii-08)、(ii-09)、(ii-10)、(ii-11)、(ii-12)、(ii-13)、(ii-14)、(ii-15)、(ii-16)、(ii-17)、(ii-18)、(iii-01)、(iii-02)、(iii-03)、(iii-04)、(iii-05)、(iii-06)、(iii-07)、(iii-08)、(iii-09)、(iii-10)、(iii-11)、(iii-12)、(iii-13)、(iii-14)、(iii-15)、(iii-16)、(iii-17)、(iii-18)、(iii-19)、(iii-20)、(iv-01)、(iv-02)、(iv-03)、(iv-04)、(iv-05)、(iv-06)、(iv-07)、(iv-08)、(iv-09)、(iv-10)、(iv-11)、(iv-12)、(iv-13)、(iv-14)、(iv-15)、(iv-16)、(iv-17)、(iv-18)、(iv-19)、和(iv-20)所表示: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、drug1和drug2的定义如前文所述。此外,drug1和drug2中的一个独立地可以缺省,但不能同时缺省。 以含有2,3-二氨基琥珀酰基的连接子双链接的药物和细胞结合分子偶联物的制备 以双链连接药物和细胞结合分子的偶联物的制备途径,示于图1-46和实施例中。 另一方面,本发明提供了含有以下2,3-二氨基琥珀酰基的式(v),(vi),(vii)和(viii)的易于反应的双连接子,其中细胞结合的两个或更多个残基分子可以同时或顺序反应形成上述式(i),(ii),(iii)和(iv): 另一方面,本发明提供了如式v),(vi),(vii)和(viii)所示的,高反应活性的,含有2,3-二氨基琥珀酰基的双连接子,细胞结合分子的两个或多个基团可以同时或依次与之反应,形成式(i),(ii),(iii)和(iv)中的结构: 其中: 任选地可以是单键、双键或三键,或者可以缺省;当代表三键时,lv1和lv2缺省; drug1、drug2、n、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1以及z2与式(i)-(iv)中的定义相同; lv1和lv2为相同或不同的反应官能团,这些官能团可以与细胞结合分子上的硫基、胺、羧酸、硒醇、酚或羟基发生反应。lv1和lv2独立地选自羟基(oh)、氟(f)、氯(cl)、溴(br)、碘(i)、硝基苯氧基、n-羟基琥珀酰亚胺(nhs)基、苯氧基、二硝基苯氧基、五氟苯氧基、四氟苯氧基、三氟苯氧基、二氟苯氧基、一氟苯氧基、五氯苯氧基、三氟甲磺酰基、咪唑基、二氯苯氧基、三氯苯氧基、四氯苯氧基、1-羟基苯并三唑基、甲苯磺酰基、甲磺酰基、2-乙基-5-苯基异恶唑-3’-磺酰基、酸酐或与其它酸酐作用形成的酸酐,例如乙酸酐、甲酸酐,或与多肽缩合试剂、mitsunobu反应试剂作用生成的中间体。缩合剂的例子如下:1-乙基-(3-二甲基氨基丙基)碳二亚胺(edc)、二环己基碳二亚胺(dcc)、n,n’-二异丙基碳二亚胺(dic)、n-环己基-n’-(2-吗啉代-乙基)碳二亚胺甲基对甲苯磺酸盐(cmc或cme-cdi)、1,1′-羰基二咪唑(cdi)、氧-(苯并三唑-1-)基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tbtu)、n,n,n’,n’-四甲基-氧-(1h-苯并三唑-1-基)-六氟磷酸铵(hbtu)、(苯并三唑-1-基氧基)三(二甲基氨基)-六氟磷酸盐(bop)、(苯并三唑-1-基氧基)三吡咯烷基六氟磷酸盐(pybop)、氰基膦酸二乙酯(depc)、氯-n,n,n’,n’-四甲基甲脒六氟磷酸盐、1-[双(二甲基氨基)亚甲基]-1h-1,2,3-三唑并[4,5-b]吡啶3-氧六氟磷酸盐(hatu)、1-[(二甲氨基)(吗啉代)亚甲基]-1h-[1,2,3]三唑并[4,5-b]吡啶-1-鎓3-氧六氟磷酸盐(hdma)、2-氯-1,3-二甲基-咪唑六氟磷酸盐(cip)、六氟磷酸氯代吡咯烷酮鎓(pyclop)、氟-n,n,n’,n’-双(四亚甲基)甲脒六氟磷酸盐(btffh)、n,n,n’,n’-四甲基-s-(1-氧代-2-吡啶基)硫脲六氟磷酸盐、氧-(2-氧代-1(2h)吡啶基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tptu)、s-(1-氧代-2-吡啶基)n,n,n’,n’-四甲基硫脲四氟硼酸盐、氧-[(乙氧基羰基)-氰基甲基氨基]-n,n,n’,n’-六氟磷酸四甲基脲(hotu)、(1-氰基-2-乙氧基-2-氧代乙基氨基氧基)二甲氨基-吗啉代-六氟磷酸盐(comu)、氧-(苯并三唑-1-基)-n,n,n’,n’-双(四亚甲基)六氟磷酸盐(hbpyu)、n-芐基-n’-环己基-碳二亚胺(有或没有聚合物结合)、二吡咯烷基(n-琥珀酰亚胺基氧基)碳鎓六氟磷酸盐(hspyu)、氯二吡咯烷基六氟磷酸盐(pyclu)、2-氯-1,3-二甲基咪唑四氟硼酸盐(cib)、(苯并三唑-1-基氧基)二呱啶碳六氟磷酸盐(hbpipu)、氧-(6-氯苯并三唑-1-基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tctu)、溴代(二甲基氨基)-六氟磷酸盐(brop)、丙基膦酸酐(ppaca、)、2-吗啉代乙基异氰化物(mei)、n,n,n’,n’-四甲基-氧-(n-琥珀酰亚胺基)六氟磷酸盐(hstu)、2-溴-1-乙基-吡啶鎓四氟硼酸盐(bep)、氧-[(乙氧基羰基)氰基-亚甲基氨基]-n,n,n’,n’-四甲基脲四氟硼酸盐(totu)、4-(4,6-二甲氧基-1,3,5-三嗪-2-基)-4-甲基吗啉氯化物(mmtm、dmtmm)、n,n,n’,n’-四甲基-氧-(n-琥珀酰亚胺基)脲四氟硼酸(tstu)、o-(3,4-二氢-4-氧代-1,2,3-苯并三嗪-3-基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tdbtu)、1,1′-(偶氮二羰基)-二呱啶(add)、二-(4-氯芐基)偶氮二羧酸酯(dcad)、偶氮二羧酸二叔丁酯(dbad)、偶氮二羧酸二异丙酯(diad)、偶氮二羧酸二乙酯(dead)。另外,lv1和lv2可以是酸酐,或与其它c1-c8酸酐作用形成的酸酐; 优选的lv1和lv2独立地选自卤化物(例如氟化物、氯化物、溴化物和碘化物)、甲磺酰基(甲磺酰基)、甲苯磺酰基(甲苯磺酰基)、三氟甲基磺酰基(三氟甲磺酸酯)、三氟甲基磺酸酯、硝基苯氧基、n-琥珀酰亚胺基氧基(nhs)、苯氧基;二硝基苯氧基;五氟苯氧基、四氟苯氧基、三氟苯氧基、二氟苯氧基、单氟苯氧基、五氯苯氧基、1h-咪唑-1-基、氯苯氧基、二氯苯氧基、三氯苯氧基、四氯苯氧基、n-(苯并三唑基)氧基、2-乙基-5-苯基异恶唑-3′-磺酰基、苯基恶二唑磺酰基(-砜-oda)、2-乙基-5-苯基异恶唑鎓-基、苯基恶二唑基(oda)、恶二唑基、不饱和碳(碳-碳、碳-氮、碳-硫、碳-磷、硫-氮、磷-氮、氧-氮或碳-氧之间的双键或三键)、或以下结构之一: 二硫化物;卤代乙酰基;酰卤化物;n-羟基丁二酰亚胺酯基;马来酰亚胺基;单取代马来酰亚胺基;单取代丁二酰亚胺基;二取代丁二酰亚胺基;二取代丁二酰亚胺基;-cho醛基;乙烯磺酰基;丙烯酰基;2-(对甲氧基)乙酰基;2-(甲氧基)乙酰基;2-(硝基苯氧基)乙酰基;2-(二硝基苯酚氧基)乙酰基;2-(氟苯氧基)-乙酰基;2-(二氟苯氧基)-乙酰基;2-((三氟甲基)-磺酰氧基)乙酰基;酮或醛基;2-(五氟苯氧基)乙酰基;甲基砜麻黄二唑基(oda);酸酐、烷氧基氨基;叠氮基、炔基、或酰肼,其中x1’为f,cl,br,i或lv3;x2’是o,nh,n(r1)或ch2;r3独立地为h,芳基,杂芳基或芳香基团,其中一个或几个氢原子独立地被-r1,-卤素,-or1,-sr1,-nr1r2,-no2,-s(o)r1,-s(o)2r1或-coor1取代;lv3是离去基团,选自f、cl、br、i;硝基苯氧基;n-羟基琥珀酰亚胺基(nhs);苯氧基;二硝基苯氧基;五氟苯氧基;四氟苯氧基;二氟苯氧基;单氟苯氧基;五氯苯氧基;三氟甲磺酰基;咪唑基;二氯酚基;四氯苯氧基;1-羟基苯并三唑基;甲苯甲磺酰基;甲磺酰基;2-乙基-5-苯基异恶唑-3′-磺酰基,酸酐或与其它酸酐作用形成的酸酐,例如乙酸酐、甲酸酐;或与多肽缩合试剂、mitsunobu反应试剂作用生成的中间体。 式(i)中结构的优选立体异构体由式(va)、(vb)、(vc)、(via)、(vib)、(vic)、(viia)、(viib)、(viic)、(viiia)、(viiib)和(viiic)所示: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、lv1、lv2、drug1和drug2如前文所定义。 优选地,含双链连接子的偶联物如结构式(v-01)、(v-02)、(v-03)、(v-04)、(v-05)、(v-06)、(v-07)、(v-08)、(v-09)、(v-10)、(v-11)、(v-12)、(v-13)、(v-14)、(v-15)、(v-16)、(v-17)、(v-18)、(v-19)、(v-20)、(v-21)、(v-22)、(v-23)、(vi-01)、(vi-02)、(vi-03)、(vi-04)、(vi-05)、(vi-06)、(vi-07)、(vi-08)、(vi-09)、(vi-10)、(vi-11)、(vi-12)、(vi-13)、(vi-14)、(vi-15)、(vi-16)、(vi-17)、(vi-18)、(vii-01)、(vii-02)、(vii-03)、(vii-04)、(vii-05)、(vii-06)、(vii-07)、(vii-08)、(vii-09)、(vii-10)、(vii-11)、(vii-12)、(vii-13)、(vii-14)、(vii-15)、(vii-16)、(vii-17)、(vii-18)、(vii-19)、(vii-20)、(viii-01)、(viii-02)、(viii-03)、(viii-04)、(viii-05)、(viii-06)、(viii-07)、(viii-08)、(viii-09)、(viii-10)、(viii-11)、(viii-12)、(viii-13)、(viii-14)、(viii-15)、(viii-16)、(viii-17)、(viii-18)、(viii-19)、和(viii-20)所示: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、drug1和drug2如前文所定义;x1和x1’独立为h、f、cl、br、i、ots、oms、otf、n3、cho、-c=ch、-c≡c-、arc(=o)r1、c(=o)nhnh2、-o-nh2、硝基苯氧基、n-羟基琥珀酰亚胺(nhs)、苯氧基、二硝基苯氧基、五氟苯氧基、四氟苯氧基、二氟苯氧基、单氟苯氧基、五氯苯氧基、三氟甲磺酰基、咪唑基、二氯酚基、四氯苯氧基、1-羟基苯并三唑基、甲苯甲磺酰基、甲磺酰基,2-乙基-5-苯基异恶唑-3′-,酸酐或与其它酸酐作用形成的酸酐、例如乙酸酐、甲酸酐,o-nhs(on-氢琥珀酰亚胺)、o-咪唑、o-三唑、o-四唑、o-ar、o-arno2、o-ar(no2)2、o-arf4、o-arf3、o-arf5、o-arf2、o-arf、o-arcl4、o-arcl3、o-arcl5、o-arcl2、o-arcl、o-arso3h、o-aropo3h2、o-ar(no2)cooh、s-ar(no2)2cooh、o-吡啶、o-硝基苯氧基、o-二硝基苯氧基、o-五氟苯氧基、o-四氟苯氧基、o-三氟苯氧基、o-二氟苯氧基、o-氟苯氧基、o-五氯苯氧基、o-四氯苯氧基、o-三氯苯氧基、o-二氯苯氧基、o-氯苯氧基、o-吡啶、o-硝基吡啶、o-二硝基吡啶、o-c1-c8烷基、o-三氟甲磺酸盐、o-苯并三唑、s-ar、s-arno2、s-ar(no2)2、s-arf4、s-arf3、s-arf5、s-arf2、s-arf、s-arcl4、s-arcl3、s-arcl5、s-arcl2、s-arcl、s-arso3h、s-aropo3h2、s-ar(no2)cooh、s-ar(no2)2cooh、s-吡啶、ss-吡啶、s-硝基吡啶、s-二硝基吡啶、s-c1-c8烷基、ss-c1-c8烷基、s-三氟甲磺酸酯、s-苯并三唑、其中ar是c3-c8芳环;或与多肽缩合试剂生成的,或与mitsunobu反应偶联试剂生成的中间体分子。 另一方面,本发明提供了如结构式(ix)和(x)的高反应活性双链连接子,细胞毒性分子的两个或多个官能团可以同时或依次与之反应形成如式(i)的结构: 其中: q、n、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、和z2定义如式(i)-(iv);lv1、lv2、lv1’和lv2’的定义如lv1和lv2在式(v)-(viii)中的定义; lv1、lv2、lv1’和lv2’独立地,可以同时或依次与细胞毒性药物的官能团反应分别形成如式(i)、(ii)、(iii)和(iv)的结构; 此外,优选地,lv1、lv2、lv1’和lv2’独立地为二硫化物、马来酰亚胺基、卤代乙酰基、烷氧基胺、叠氮基、酮、醛、肼、氨基、羟基、羧酸盐、咪唑、硫醇或炔烃;或n-羟基琥珀酰亚胺酯、对硝基苯基酯、二硝基苯基酯、五氟苯基酯、五氯苯基酯;四氟苯基酯;二氟苯基酯;单氟苯基酯;或五氯苯基酯、二氯苯基酯、四氯苯基酯或1-羟基苯并三唑酯;三氟甲磺酸酯、甲磺酸酯或甲苯磺酸酯;2-乙基-5-苯基异恶唑-3′-磺酸酯;吡啶基二硫化物或硝基吡啶基二硫化物;马来酰亚胺、卤代乙酸酯、乙炔二羧基或酰卤(氟化物、氯化物、溴化物或碘化物)。优选地,x和y具有以下结构之一:n-羟基琥珀酰亚胺酯;马来酰亚胺;二硫化物;卤代乙酰基;酰卤;乙烯磺酰基;丙烯酰基;2-(甲苯氧基)乙酰基;2-(甲氧基)乙酰基;2-(硝基苯氧基)乙酰基;2-(二硝基苯氧基)乙酰基;2-(氟苯氧基)-乙酰基;2-2-(二氟苯氧基)-乙酰基;2-((三氟甲基)-磺酰基)氧基)乙酰基;酮或醛、2-(五氟苯氧基)乙酰基;甲基砜苯基恶二唑(oda);酸酐、氨基氧烷基;叠氮基、炔基或酰肼。其中x1’是f、cl、br、i或lv3;x2’是o、nh、n(r1)或ch2;r3和r5是h、r1、芳基、杂芳基或其中一个或几个h原子独立地被-r1、-卤素、-or1、-sr1、-nr1r2、-no2、-s(o)r1、-s(o)2r1或-coor1取代的芳基;lv3是选自甲磺酰基(ms)、甲苯磺酰基(ts)、三氟甲基磺酰基、三氟甲基磺酸酯、硝基苯氧基、n-琥珀酰亚胺基氧基(nhs)、苯氧基;二硝基苯氧基;五氟苯氧基、四氟苯氧基、三氟苯氧基、二氟苯氧基、单氟苯氧基、五氯苯氧基、1h-咪唑-1-基、氯苯氧基、二氯苯氧基、三氯苯氧基、四氯苯氧基、n-(苯并三唑基)氧基、2-乙基-5-苯基异恶唑鎓基、苯基恶二唑基(oda)、恶二唑基或与mitsunobu反应缩合试剂反应产生的中间分子,其中r1和r2如前文所定义; 优选地,用于制备偶联物的双链连接子化合物由式(ix-01)、(ix-02)、(ix-03)、(ix-04)、(ix-05)、(ix-06)、(ix-07)、(ix-08)、(ix-09)、(ix-10)、(ix-11)、(ix-12)、(ix-13)、(ix-14)、(ix-15)、(ix-16)、(ix-17)、(ix-18)、(ix-19)、(ix-20)、(ix-21)、(ix-22)、(ix-23)、(x-01)、(x-02)、(x-03)、(x-04)、(x-05)、(x-06)、(x-07)、(x-08)、(x-09)、(x-10)、(x-11)、(x-12)、(x-13)、(x-14)、(x-15)、(x-16)、(x-17)、(x-18)、(x-19)和(x-20)表示: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、lv1、lv2、lv1’和lv2’定义如前文所述。此外,drug1和drug2相互独立,其一可以缺省,但不可同时缺省。 能与药物/细胞毒性剂的末端胺或羟基反应的官能团lv1、lv2、lv1’和lv2’包括但不限于:n-羟基琥珀酰亚胺酯、对硝基苯基酯,二硝基苯基酯,五氟苯基酯,酰氯或羧酸酐;能和细胞毒性剂的末端巯基反应的官能团可以是吡啶二硫化物,硝基吡啶二硫化物,马来酰亚胺基,卤代乙酸酯,甲基砜基苯基恶二唑(oda),酰氯或羧酸酐;能和末端酮或醛反应的官能团可以是,但也不限于胺,烷氧基胺,肼,酰氧基胺或酰肼;和末端叠氮基反应的官能可以是,也不限于炔基。 另一方面,本发明提供了如式(xi)和(xii)的高反应活性的双连接子,细胞毒性分子和细胞结合分子独立地,可以或同时或依序与之反应生成式(i)-(iv)的结构。 其中x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1和z2定义如式(i)-(iv);lv1、lv2、lv1’和lv2’的定义和lv1与lv2在式(v)-(viii)中的定义; 优选地,用于制备偶联物的双连接子化合物进一步由下式表示: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、lv1、lv2、lv1’、lv2’、x1和x1’定义如前文所述; 部分结构式(i),(ii),(iii)和(iv)中分子的制备如图1-26所示或在实施例中描述。为了合成式(i),(ii),(iii)和(iv)中的偶联物,通常药物上或细胞毒性分子上的两个官能团,依次或同时与结构式为(xi)和(xii)的连接子上的lv1’,lv2’,lv1和lv2基团反应,反应在有机溶剂中或含有0.1%-99.5%有机溶剂的水性介质中或完全水性介质中进行,形成结构式如(v),(vi),(vii),或(viii)的化合物。可分离相应的化合物,或者使其立即同时或依次与细胞结合分子上的两个或更多个基团反应,优选的基团为还原细胞结合分子的二硫键而产生的一对游离巯基,形成结构式为(i),(ii),(iii)或(iv)的偶联化合物。反应在0-60℃,ph5-9的水性介质中进行,可添加或不添加0-30%的可与水混溶的有机溶剂,例如dma,dmf,乙醇,甲醇,丙酮,乙腈,thf,异丙醇,二恶烷,丙二醇或乙二醇。 或者,式(i)、(ii)、(iii)或(iv)中的偶联物也可以通过首先使式(xi)或(xii)中的连接子与两个或更多个细胞结合分子上的基团反应,优选在0-60℃,ph5~9水溶液中或者加入0~30%与水混溶的有机溶剂,与细胞结合分子中还原二硫键而产生的一对游离巯基反应,形成如式(ix)或(x)的经修饰的细胞结合分子。巯基对优选是通过选自以下的还原剂将细胞结合剂的链间二硫键还原:二硫苏糖醇(dtt)、二硫赤藓糖醇(dte)、l-谷胱甘肽(gsh)、三(2-羧乙基)膦(tcep)、2-巯基乙胺(β-mea)或/和β-巯基乙醇(β-me、2-me),反应在ph4~9水性介质中进行,可加入或不加入0~30%的与水混溶有机溶剂。式(xi)和(xii)上的反应基团lv1’、lv2’、lv1和lv2各自独立地为二硫化物、硫醇、硫酯、马来酰亚胺基、卤代乙酰基、叠氮化物、1-炔、酮、醛、烷氧基氨基、三氟甲磺酸酯、羰基咪唑、甲苯磺酸酯、甲磺酸酯、2-乙基-5-苯基异恶唑-3′-磺酸酯,或硝基苯酚酯、n-羟基琥珀酰亚胺(nhs)酯、苯酚酯、二硝基苯酚酯、五氟苯酚酯、四氟苯酚酯、二氟苯酚酯、一氟苯酚酯、五氯苯酚酯、二氯苯酚酯、四氯苯酚酯、1-羟基苯并三唑的酯、酸酐或酰肼,或其他酸酯衍生物。然后与药物/细胞毒剂上的一个或两个基团同时或依次,在0-60℃,ph4-9.5的水性介质中加入或不加入0-30%的与水混溶的有机溶剂中反应,经柱纯化或透析后,得到式(i)、(ii)、(iii)或(iv)中的化合物。药物/细胞毒性剂的反应基团以不同方式与式(ix)或(x)中修饰的细胞结合分子反应。例如,若式(i)、(ii)、(iii)或(iv)的细胞结合剂-药物偶联物中含有二硫键,它的形成通过修饰的细胞结合剂(ix)或(x)中的二硫键和具有游离巯基的药物之间的二硫键交换来实现;若式(i)、(ii)、(iii)或(iv)的细胞结合剂-药物偶联物中含有硫醚键,它的形成通过修饰的细胞结合剂(ix)或(x)中的马来酰亚胺基或卤代乙酰基或乙基磺酰基和具有游离巯基的药物反应来实现;若在偶联物中含有酸不稳定腙键,它的形成可以通过药物或式(ix)或(x)化合物上的羰基与式(ix)或(x)化合物或者药物分子上的酰肼反应来实现,该方法为本领域所熟知(例如p.hamann等,cancerres.53,3336-34,1993;b.laguzza等,j.med.chem.32;548-55,1959;p.trail等,cancerres.,57,100-5,1997);若在偶联物中含有三唑键,它的形成可以通过药物或式(ix)或(x)中化合物的1-炔基与另一对应物上的叠氮基通过化学反应来实现(huisgen环加成)(lutz,j-f.等,2008,adv.drugdel.rev.60,958–70;sletten,e.m.等,2011,accchem.research44,666-76)。通过在式(ix)或(x)中修饰的细胞结合剂或药物上的酮或醛与另一对应物上的氧胺反应,实现细胞结合剂-药物偶联物中肟的连接。含巯基的药物可与式(ix)或(x)中带有马来酰亚胺基,卤代乙酰基或乙基磺酰基取代基的修饰的细胞结合分子连接子在水性缓冲液,ph5.5~9.0下反应,得到含硫醚键的如式(i)、(ii)、(iii)或(iv)所示的细胞结合分子-药物偶联物。含巯基的药物可以与带有吡啶基二硫代官能团的式(ix)或(x)中的修饰的连接子进行二硫键交换,得到二硫键连接的偶联物。带有羟基或巯基的药物可以在温和碱,例如ph8.0-9.5环境下,与带有卤素,特别是羧酸酯的α卤化物的如式(ix)或(x)中的修饰的连接子反应,得到醚或硫醚链接的偶联药物。在脱水剂如edc或dcc存在下,药物上的羟基可以与带有羧基的如式(xi)或(xii)所示的连接子缩合,产生酯键,得到的如式(ix)或(x)所示的经药物修饰的桥连接子可以与细胞结合分子偶联。含有氨基的药物可以与如式((ix)或(x)所示的细胞结合分子连接子上的nhs、咪唑、硝基苯酚、n-羟基琥珀酰亚胺(nhs)、苯酚、二硝基苯酚、五氟苯酚、四氟苯酚、二氟苯酚、单氟苯酚、五氯苯酚、三氟甲磺酸酯、咪唑、二氯苯酚、四氯苯酚、1-羟基苯并三唑的酯,甲苯磺酸酯,甲磺酸酯,2-乙基-5-苯基异恶唑-3′-磺酸酯缩合,得到酰胺链接的偶联物。 合成的偶联物可以通过标准生物化学方法纯化,例如在sephadexg25或sephacryls300柱上进行凝胶过滤,吸附色谱,离子交换,或透析。在一些情况下,细胞结合剂为小分子化合物(例如叶酸、黑素细胞刺激激素、egf等),与小分子药物偶联后,可以通过色谱法纯化,例如hplc、中压柱层析法或离子交换色谱法。 为了使结构式(v),(vi),(vii)或(viii)中的细胞毒性分子-双链连接子与细胞结合分子,优选抗体,上的一对游离巯基的偶联反应有更高产率,可能需要在反应混合物中加入少量水溶性有机溶剂或相转移剂。可将式(v),(vi),(vii)或(viii)中的交联剂(连接子),以高浓度如1-500mm溶解于可与水混溶的极性有机溶剂中,例如不同的醇(如甲醇、乙醇和丙醇)、丙酮、乙腈、四氢呋喃(thf)、1,4-二恶烷、二甲基甲酰胺(dmf)、二甲基乙酰胺(dma)或二甲基亚砜(dmso)。同时,将细胞结合分子,如抗体以1~50mg/ml浓度溶解在ph4~9.5,最优ph6~8.5的缓冲液中,再用0.5~20eq.的tcep或dtt处理20分钟至48小时。还原后,dtt可通过sec色谱纯化去除。tcep也可以通过sec色谱法或离子交换色谱法去除,或者留在反应混合物中,无需进一步纯化。此外,以tcep还原抗体或其他细胞结合剂,可以在如式(v),(vi),(vii)或(viii)所示的药物-连接子分子共存时进行,此时药物与细胞结合分子的偶联,可以与tcep还原抗体同时实现。 进行细胞结合剂的修饰的水溶液为ph4至9之间缓冲液,优选在6.0至7.5之间,可以含有适合用于这个ph范围的任何非亲核性缓冲盐。典型的缓冲液包括磷酸盐、乙酸盐、三乙醇胺盐酸盐、hepes和mops缓冲液,也可含有其它组分,例如环糊精、羟丙基-β-环糊精、聚乙二醇、蔗糖和其它盐,如nacl和kcl。在将式(v),(vi),(vii)或(viii)中的药物-连接子加入到已经被还原的细胞结合分子的溶液中后,将反应混合物在4℃至45℃,优选15℃的温度下保温。对反应进程的监测,可以通过测量在某一特定紫外线波长(例如254nm)吸光度的减少,或某一特定紫外线波长(例如280nm)吸光度的增加,或选择其它适当波长。反应完成后,被修饰的细胞结合剂可以以常规方式被分离,例如使用凝胶过滤色谱、离子(阳离子或阴离子)交换色谱、吸附色谱,硅胶或氧化铝柱层析色谱,结晶、制备薄层色谱或hplc方法。 可以通过测量反应生成的硝基吡啶硫酮、二硝基吡啶二硫酮、吡啶硫酮、羧基酰胺基吡啶二硫酮和二羧基酰胺基吡啶二硫酮基团的紫外吸光度,对修饰的程度进行评估。对于没有发色基团分子的偶联反应、修饰或偶联反应可以通过lc-ms监测、优选uplc-qtof质谱或毛细管电泳质谱法(ce-ms)监测。本发明所述的连接子含有多种官能团,可与细胞结合分子,尤其是具有合适取代基的修饰的细胞结合分子反应。例如,带有氨基或羟基的修饰的细胞结合分子,可以与带有n-羟基琥珀酰亚胺(nhs)酯的药物反应,带有巯基的修饰的细胞结合分子,可以与带有马来酰亚胺基或卤代乙酰基的药物反应。另外,带有羰基(酮或醛)基团的细胞结合分子,可以与带有酰肼或烷氧基胺的药物反应。基于连接子上官能团的反应活性,本领域技术人员可以很容易地确定使用哪种连接子分子。 细胞结合剂 本发明的偶联物中的细胞结合分子cb或q,和被修饰的细胞结合分子,是目前已知的或将成为已知的,可与具有治疗学意义或能在生物学意思上被修饰的细胞的片段结合,复合或反应的分子。 细胞结合剂包括但不限于大分子量蛋白质,例如抗体、抗体样蛋白质、全长抗体、多克隆抗体、单克隆抗体、二聚体、多聚体、多特异性抗体(例如双特异性抗体、三特异性抗体或四特异性抗体);单链抗体;抗体片段、例如fab、fab’、f(ab’)2、fv、(parham,j.immunol.-902(1983)),由fab表达文库产生的片段,抗独特型(抗id)抗体、cdr’s、双抗体、三抗体、四抗体、微抗体、前抗体、前抗体片段、小免疫蛋白(sip),和上述任何一种的表位结合片段,能免疫特异性结合癌细胞抗原、病毒抗原、微生物抗原或免疫系统产生的能够识别,结合特定抗原或表现出所需生物活性的蛋白质(miller等,j.immunology,2003,170:4854-61);干扰素(如i型、ii、iii);肽;淋巴因子如il-2、il-3、il-4、il-5、il-6、il-7、il-8、il-9、il-10、il-11、il-12、il-13、il-14、il-5、il-16、il-17、il-18、il-19、il-20、il-21、il-22、il-23、il-24、il-25、gm-csf、干扰素γ(ifn-γ);激素如胰岛素、trh(促甲状腺激素释放激素)、msh(促黑素细胞激素)、类固醇激素如雄激素和雌激素;生长因子和集落刺激因子如表皮生长因子(egf)、粒细胞巨噬细胞集落刺激因子(gm-csf)、转化生长因子(tgf)如tgfα、tgfβ、胰岛素和胰岛素样生长因子(igf-i、igf-ii)、g-csf、m-csf和gm-csf(burgess,immunologytoday5155-8(1984));牛痘生长因子(vgf);成纤维细胞生长因子(fgf);小分子量的蛋白质、多肽、肽和肽激素、如铃蟾肽、胃泌素、胃泌素释放肽;血小板衍生生长因子;白细胞介素和细胞因子、如白细胞介素-2(il-2)、白细胞介素-6(il-6)、白血病抑制因子、粒细胞-巨噬细胞集落刺激因子(gm-csf);维生素、如叶酸;载脂蛋白和糖蛋白、如转铁蛋白(o’keefe等,j.biol.chem.260,932-937(1985));糖结合蛋白或脂蛋白,如凝集素;细胞营养转运分子;和小分子抑制剂,如前列腺特异性膜抗原(psma)抑制剂和小分子酪氨酸激酶抑制剂(tki)、非肽或任何其他细胞结合分子或物质,如生物活性聚合物(dhar等,proc.natl.acad.sci.2008,105,17356-61);生物活性树枝状大分子(lee,等,nat.biotechnol.2005,23,1517-26;almutairi等,proc.natl.acad.sci.2009,106,685-90);纳米颗粒(liong等,acsnano,2008,2,1309-12;medarova等,nat.med.2007,13,372-7;javier等,bioconjugatechem.2008,19,1309-12);脂质体(medinai等,curr.phar.des.2004,10,2981-9);病毒衣壳(flenniken等,virusesnanotechnol.2009,327,71-93)。 通常,如果可获得合适的单克隆抗体,则优选单克隆抗体作为细胞表面结合剂。并且抗体可以是鼠、人、人源化、嵌合或衍生自其他物种。 本发明中使用的抗体的生产涉及体内或体外方法或其组合。用于产生多克隆抗受体肽抗体的方法在本领域中是众所周知的,例如美国专利no.4,493,795(nestor等)。单克隆抗体通常通过将骨髓瘤细胞与已经用所需抗原免疫的小鼠的脾细胞融合来制备(g.和milstein,c.1975,nature256:495-7)。详细方法在《antibodies-alaboratorymanual》,harlow和lane编辑,冷泉港实验室出版社,纽约(1988)中描述,引用并入本文。特别地,可通过用感兴趣的抗原如完整的靶细胞,从靶细胞,全病毒,灭活的全病毒和病毒蛋白中分离的抗原,来免疫小鼠,大鼠,仓鼠或任何其他哺乳动物,来制备单克隆抗体。通常使用聚乙二醇(peg)6000将脾细胞与骨髓瘤细胞融合。通过它们对hat(次黄嘌呤-氨基蝶呤-胸腺嘧啶)的敏感性来选择融合杂种。通过其对特定受体的免疫反应或抑制靶细胞上受体活性的能力,可鉴定适于制备产本发明的单克隆抗体的杂交瘤。 本发明中使用的单克隆抗体可以通过单克隆杂交瘤培养来生产,培养基中含有分泌具有特定抗原特异性的抗体分子的杂交瘤。将培养物保持在特定的条件,保持足够的时间以使杂交瘤将抗体分子分泌到培养基中。然后收集含有抗体的培养基,通过众所周知的技术进一步分离抗体分子,例如使用蛋白a亲和层析,阴离子,阳离子,疏水或尺寸排阻色谱法(尤其是通过蛋白a亲和层析和尺寸排阻色谱法),离心,差别溶解度法或任何其他蛋白质纯化的标准技术。 用于制备抗体的培养基在本领域都是众所周知的,包括合成培养基,市售可得。示例性的合成培养基为:dulbecco的基本必需培养基(dmem;dulbecco等,virol.8,396(1959))中加入4.5mg/l葡萄糖,0~20mm谷氨酰胺,0~20%胎牛血清,若干ppm的重金属盐,如cu、mn、fe或zn等,或/和其他重金属盐,并加入消泡剂,如聚氧乙烯-聚氧乙烯嵌段共聚物。 另外,生产抗体的细胞株也可以通过细胞融合之外的方法得到,比如说用癌基因dna直接转化b淋巴细胞,或者致癌病毒如eb病毒(ebv,也称人疱疹病毒4(hhv-4))或者肉瘤相关疱疹病毒(kshv)转染b淋巴细胞(可参考美国专利4,341,761;4,399,121;4,427,783;4,444,887;4,451,570;4,466,917;4,472,500;4,491,632;4,493,890)。单克隆抗体也可以通过抗-受体多肽或含末端羧基的多肽而得到。具体可见文献:niman等,proc.natl.acad.sci.,1983,80,4949-4953;geysen等,proc.natl.acad.sci.,1985,82,178-182;lei等,biochemistry,1995,34(20),6675-6688等。通常,抗-受体多肽或多肽类似物可以单独或与免疫原载体连接,作为免疫原生产抗-受体多肽单克隆抗体。 还有其他已知的各种技术,可以用来生产本发明里作为结合分子的单克隆抗体。特别有用的是生产全人源抗体的方法。其中一个方法是噬菌体展示技术,此方法通过亲和富集,从大量的人抗体中筛选出特异性结合抗原的抗体。噬菌体展示技术,包括构建和筛选噬菌体展示库是一种非常成熟的技术,具体可以参考:dente等,gene.148(1):7-13(1994);little等,biotechnoladv.12(3):539-55(1994);clackson等,nature352:264-8(1991);huse等,science246:1275-81(1989)。 通过非人源的如老鼠的杂交瘤技术获得的抗体,可以通过人源化以避免注射入人体时产生抗抗体。最常见的人源化抗体的方法是互补决定区嫁接和表面修饰,这些方法在大量文献中都有描述,如美国专利5,859,205;6,797,492;liu等,immunolrev.,2008,222,9-27;almagro等,frontbiosci.,2008,1(13),1619-33;lazar等,molimmunol.,2007,44(8),1986-98;li等,proc.natl.acad.sci.,2006,103(10),3557-62。全人源抗体也可以通过将带有人免疫球蛋白重链、轻链的抗原免疫转基因小鼠、兔子、猴子以及其他转基因哺乳动物而得到。这样的转基因小鼠例子有xenomouse(abgenix/amgen.),humab-mouse(medarex/bms),velocimouse(regeneron),参见美国专利6,596,541;6,207,418;6,150,584;6,111,166;6,075,181;5,922,545;5,661,016;5,545,806;5,436,149和5,569,825。在人体治疗中,通过将鼠源的可变区与人的非可变区融合为“嵌合抗体”,这类抗体比鼠抗在人体中具有更小的免疫原性(kipriyanov等,molbiotechnol.,2004,26,39-60;houdebine,curropinbiotechnol.,2002,13,625-629)。另外,通过可变区的点突变可以使抗体结合抗原的亲和力和特异性提高(brannigan等,nat.rev.mol.cellbiol.,2002,3,964-70;adams等,j.immunol.methods.,1999,231,249-60)。非可变区的替换可以改进抗体介导的结合功能和其细胞毒性。 对恶性细胞抗原免疫特异性的抗体也可以商业获得,或通过本领域技术人员公知的任何方法,如化学合成或重组表达技术生产。对恶性细胞抗原免疫特异性的抗体的核苷酸序列可以商业获得,例如从genbank数据库或类似数据库,文献出版物或通过常规克隆和测序获得。 除抗体外,结合/阻断/靶或以某种其他方式与靶细胞上的表位或相应受体相互作用的肽或蛋白质均可用作结合分子。这些肽或蛋白质可以是对表位或相应受体具有亲和力的任何随机肽或蛋白质,并且它们不一定是免疫球蛋白家族。这些肽可以通过与噬菌体展示抗体类似的技术分离(szardenings,jreceptsignaltransductres.2003,23(4):307-49)。对来自这种随机肽文库的肽的使用可以类似于抗体和抗体片段。肽或蛋白质的结合分子可以与大分子或其它材料偶联或连接,例如,但不限于白蛋白,聚合物,脂质体,纳米颗粒,树枝状大分子,只要这样的附着允许肽或蛋白质保持其抗原结合特异性。 在优选的实施例中,本发明的细胞结合分子是单克隆抗体。用于与本发明的与细胞毒剂偶联的抗体的例子包括,但不限于3f8(抗gd2)、阿巴单抗(抗ca-125)、阿昔单抗(抗cd41(整联蛋白α-iib)、阿达木单抗(抗tnf-α)、adecatumumab(抗epcam、cd326)、阿非莫单抗(抗tnf-α)、afutuzumab(抗cd20)、alacizumab单抗(抗vegfr2)、ald518(抗il-6)、alemtuzumab(campath、mabcampath、抗cd52)、altumomab(抗cea)、anatumomab(抗tag-72)、anrukinzumab(ima-638、抗-il-13)、apolizumab(抗-hla-dr)、阿奇单抗(抗-cea)、阿塞珠单抗(抗-l-选择蛋白cd62l)、atlizumab(tocilizumab、actemra、roactemra、抗-il-6受体)、atorolimumab(抗-rhesus因子)、bapineuzumab(抗-β淀粉样蛋白)、basiliximab(simulect、抗cd25(il-2受体的α链))、bavituximab(抗磷脂酰丝氨酸)、bectumomab(lymphoscan、抗-cd22)、贝利单抗(benlysta、lymphostat-b、抗baff)、benralizumab(抗cd125)、bertilimumab(抗ccl11(eotaxin-1))、besilesomab(scintimun、抗cea相关抗原)、贝伐单抗(avastin、抗vegf-a)、biciromab(fibriscint、抗纤维蛋白iiβ链)、bivatuzumab(抗-cd44v6)、blinatumomab(bite、抗cd19)、brentuximab(cac10、抗-cd30tnrsf8)、briakinumab(抗il-12、il-23)、canakinumab(ilaris、抗il-1)、cantuzumab(c242、抗canag)、capromab、catumaxomab(removab、抗epcam、抗cd3)、cc49(抗tag-72)、cedelizumab(抗cd4)、certolizumab单抗(cimzia抗tnf-α)、西妥昔单抗(爱必妥、imc-c225、抗egfr)、citatuzumabbogatox(抗epcam)、cixutumumab(抗igf-1)、clenoliximab(抗cd4)、clivatuzu-mab(抗muc1)、conatumumab(抗trail-r2)、cr6261(抗流感a血凝素)、dacetuzumab(抗cd40)、daclizumab(zenapax、抗cd25(il-2受体α链))、daratumumab(抗cd38(环adp核糖水解酶)、denosumab(prolia、抗rankl)、detumomab(抗b淋巴瘤细胞)、dorlimomab、dorlixizumab、ecromeximab(抗gd3神经节苷脂)、eculizumab(soliris、抗-c5)、edobacomab(抗内毒素)、edrecolomab(panorex、mab17-1a、抗-epcam)、efalizumab(raptiva、抗lfa-1(cd11a))、efungumab(mycograb、抗hsp90)、elotuzumab(抗slamf7)、elsilimomab(抗il-6)、enlimomab单抗(抗icam-1(cd54))、epitumomab(抗episialin)、依他珠单抗(抗-cd22)、erlizumab(抗-itgb2(cd18))、ertumaxomab(rexomun、抗her2/neu、cd3)、依他拉单抗(abegrin、抗整联蛋白αvβ3)、exbivirumab(抗乙肝表面抗原)、fanolesomab(neutrospec、抗cd15)、faralimomab(抗干扰素受体)、farletuzumab(抗叶酸受体1)、felvizumab(抗呼吸道合胞病毒)、fezakinumab(抗-il-22)、figitumumab(抗-igf-1受体)、fontolizumab(抗-ifn-γ)、foravirumab(抗狂犬病病毒糖蛋白)、fresolimumab(抗tgf-β)、galiximab(抗cd80)、gantenerumab(抗β淀粉样蛋白)、gavilimomab(抗cd147(basigin))、gemtuzumab(抗cd33)、girentuximab(抗碳酸酐酶9)、glembatumumab(cr011、抗gpnmb)、golimumab(simponi、抗-tnf-α)、gomiliximab(抗-cd23(ige受体))、ibalizumab(抗-cd4)、ibritumomab(抗cd20)、igovomab(indimacis-125、抗ca-125)、imciromab(myoscint、抗心肌肌凝蛋白)、infliximab(remicade、抗tnf-α)、intetumumab(抗cd51)、inolimomab(抗cd25(il-2受体α链)、伊珠单抗(抗-cd22)、ipilimumab(抗cd152)、iratumumab(抗cd30(tnfrsf8))、keliximab(抗-cd4)、labetuzumab(cea-cide、抗cea)、lebrikizumab(抗il-13)、lemalesomab(抗nca-90(粒细胞抗原))、lerdelimumab(抗tgfβ2)、lexatumumab(抗trail-r2)、libivirumab(抗乙肝表面抗原)、lintuzumab(抗cd33)、鲁米木单抗(抗cd40)、鲁米单抗(抗cd23(ige受体)、mapatumumab(抗trail-r1)、马西莫单抗(抗t-细胞受体)、马妥珠单抗(抗egfr)、mepolizumab(bosatria、抗il-5)、metelimumab(抗tgfβ1)、milatuzumab(抗cd74)、minretumomab(抗tag-72)、mitumomab(bec-2、抗gd3神经节苷脂)、morolimumab(抗恒河猴因子)、motavizumab(numax、抗呼吸道合胞病毒)、muromonab-cd3(orthocloneokt3、抗cd3)、nacolomab(抗c242)、naptumomab(抗5t4)、那他珠单抗(tysabri、抗整联蛋白α4)、奈巴单抗(抗内毒素)、necitumumab(抗egfr)、nerelimomab(抗-tnf-α)、nimotuzumab(theracim、theraloc、抗-egfr)、nofetumomab、ocrelizumab(抗cd20)、奥利木单抗(afolimomab、抗lfa-1(cd11a))、ofatumumab(arzerra、抗cd20)、olaratumab(抗pdgf-rα)、omalizumab(xolair、抗igefc区)oportuzumab(抗epcam)、oregovomab(ovarex、抗ca-125)、otelixizumab(抗cd3)、pagibaximab(抗脂磷壁酸)、palivizumab(synagis、abbosynagis、抗呼吸道合胞病毒)、帕尼单抗(vectibix、abx-egf、抗egfr)、panobacumab(抗铜绿假单胞菌(pseudomonasaeruginosa))、帕考珠单抗(抗il-4)、pemtumomab(theragyn、抗muc1)、pertuzumab(omnitarg、2c4、抗her2/neu)、pexelizumab(抗c5)、pintumomab(抗腺癌抗原)、priliximab(抗-cd4)、pritumumab(抗波形蛋白)、pro140(抗-ccr5)racotumomab(1e10、抗-n-羟乙酰神经氨酸(neugc、ngna)-神经节苷脂gm3))、rafivirumab(抗狂犬病病毒糖蛋白)、ramucirumab(抗vegfr2)、ranibizumab(lucentis、抗vegf-a)、raxibacumab(抗炭疽毒素、保护性抗原)、regavirumab(抗巨细胞病毒糖蛋白b)、reslizumab(抗-il-5)、rilotumumab(抗-hgf)、rituximab(mabthera、rituxanmab、抗-cd20)、robatumumab(抗-igf-1受体)、rontalizumab(抗ifn-α)、rovelizumab(leukar-rest、抗cd11、cd18)、ruplizumab(antova、抗cd154(cd40l))、satumomab(抗tag-72)、sevirumab(抗巨细胞病毒)、sibrotuzumab(抗fap)、西法木单抗(抗ifn-α)、siltuximab(抗il-6)、siplizumab(抗cd2)、smartmi95(抗cd33)、solanezumab(抗β淀粉状蛋白)、sonepcizumab(抗鞘氨醇-1-磷酸)、sontuzumab(抗-episialin)、stamulumab(抗-myostatin)、sulesomab(leukoscan、抗nca-90(粒细胞抗原))、tacatuzumab(抗α甲胎蛋白)、tadocizumab(抗整联蛋白αiibβ3)、talizumab(抗ige)、tanezumab(anti-ngf)、taplitumomab(抗cd19)、tefibazumab(aurexis、(抗凝聚因子a))、telimomab、tenatumomab(抗腱生蛋白c)、teneliximab(抗cd40)、teplizumab(抗cd3)、tgn1412(抗cd28)、ticilimumab(tremelimumab、抗-ctla-4)、tigatuzumab(抗trail-r2)、tnx-650(抗il-13)、tocilizumab(atlizumab、actemra、roactemra、il-6受体)、toralizumab(抗cd154(cd40l))、tositumomab(抗cd20)、曲妥珠单抗(赫赛汀、抗her2/neu)、tremelimumab(抗ctla-4)、tucotuzumabcelmoleukin(抗epcam)、tuvirumab(抗乙型肝炎病毒)、urtoxazumab(抗大肠杆菌)、ustekinumab(stelara、抗-il-12、il-23)、vapaliximab(抗-aoc3(vap-1))、维多珠单抗(抗整联蛋白α4β7)、维妥珠单抗(抗cd20)、vepalimomab(抗aoc3(vap-1))、visilizumab(nuvion、抗cd3)、vitaxin(抗血管整合素avb3)、volociximab(抗整联蛋白α5β1)、votumumab(humaspect、抗肿瘤抗原ctaa16.88)、zalutumumab(humax-egfr、zanolimumab(humax-cd4、抗-cd4)、ziralimumab(抗-cd147(basigin))、zolimomab(抗-cd5)、依那西普alefaceptabataceptrilonacept(arcalyst)、14f7(抗irp-2(铁调节蛋白2))、14g2a(抗gd2神经节苷脂、源于nat.cancerinst.、治疗黑素瘤和实体瘤)、j591(抗-psma、源于weillcornell医学院、治疗前列腺癌)、225.28s(抗hmw-maa(高分子量黑素瘤相关抗原)、sorinradiofarmacisrl(源于意大利米兰、治疗黑色素瘤)、col-1(抗ceacam3、cgm1、源于natcancerinst.、治疗结肠直肠癌和胃癌)、cyt-356(治疗前列腺癌)、hnk20(oravaxinc.治疗呼吸道合胞病毒感染)、immurait(源于immunomedics、治疗nhl)、lym-1(抗hla-dr10、peregrinepharm)、mak-195f(抗tnf(肿瘤坏死因子、tnfa、tnf-α、tnfsf2、源于abbott/knoll、治疗脓毒症中毒性休克)、medi-500(t10b9、抗cd3、trαβ(t细胞受体α/β)、源于medimmuneinc、用于移植物抗宿主疾病病)、ringscan(抗tag72(肿瘤相关糖蛋白72)、源于neoprobecorp.、用于乳腺癌、结肠癌和直肠癌)、avicidin(抗epcam(上皮细胞粘附分子))、抗-tacstd1(肿瘤相关钙信号转导1)、抗ga733-2(胃肠肿瘤相关蛋白2)、抗egp-2(上皮糖蛋白2)、抗ksa、ks1/4抗原、m4s、肿瘤抗原17-1a、cd326(源于neorx公司、治疗结肠癌、卵巢癌、前列腺癌和nhl)、lymphocide(源于immunomedics,nj)、smartid10(源于proteindesignlabs)、oncolym(源于technicloneinc,ca)、allomune(源于biotransplant,ca)、anti-vegf(源于genentech,ca)、ceacide(源于immunomedics,nj)、imc-1c11(源于imclone,nj)和cetuximab(源于imclone,nj)。 用于结合抗原的其它抗体,包括但不限于抗以下抗原的抗体:氨肽酶n(cd13)、膜联蛋白a1、b7-h3(cd276、各种癌症)、ca125(卵巢癌)、ca15-3(各种癌)、ca19-9(各种癌)、l6(各种癌)、lewisy(各种癌)、lewisx(各种癌)、甲胎蛋白(各种癌)、ca242、胎盘碱性磷酸酶(各种癌)、前列腺特异性抗原(前列腺癌)、前列腺酸性磷酸酶(前列腺癌)、表皮生长因子(各种癌)、cd2(霍奇金病、非霍奇金淋巴瘤的淋巴瘤、多发性骨髓瘤)、cd3的ε(t细胞淋巴瘤、肺癌、乳腺癌、胃癌、卵巢癌、自身免疫性疾病、恶性腹水)、cd19(b细胞恶性肿瘤)、cd20(非霍奇金淋巴瘤)、cd22(白血病、淋巴瘤、多发性骨髓瘤、系统性红斑狼疮)、cd30、cd33、cd37、cd38(多发性骨髓瘤)、cd40(淋巴瘤、多发性骨髓瘤、白血病)、cd51(转移性黑素瘤、肉瘤)、cd52、cd56(小细胞肺癌癌、卵巢癌、merkel细胞癌、以及液体肿瘤、多发性骨髓瘤)、cd66e(癌症)、cd70(转移性肾细胞癌和非霍奇金淋巴瘤)、cd74(多发性骨髓瘤)、cd80(淋巴瘤)、cd98(癌症),粘蛋白(癌)、cd221(实体瘤)、cd227(乳腺癌、卵巢癌)、cd262(非小细胞肺癌和其他癌)、cd309(卵巢癌)、cd326(实体瘤)、ceacam3(大肠癌、胃癌)、ceacam5(癌胚抗原;cea、cd66e)(乳腺癌、结肠直肠癌和肺癌)、dll3(δ状-3)、dll4(δ状-4)、egfr(表皮生长因子受体、各种癌症)、ctla4(黑色素瘤)、cxcr4(cd184、血红素肿瘤、实体肿瘤)、内皮糖蛋白(cd105、实体瘤)、epcam(上皮细胞粘附分子、膀胱癌、头、颈、结肠、前列腺非霍奇金淋巴瘤、和卵巢癌)、erbb2(表皮生长因子受体2;肺癌、乳腺癌、前列腺癌)、fcgr1(自身免疫性疾病)、folr(叶酸受体、卵巢癌)、gd2神经节苷脂(癌症)、g-28(一种细胞表面抗原glyvolipid、黑素瘤)、独特型gd3(癌症)、热休克蛋白(癌症)、her1(肺、胃癌)、her2(乳腺癌、肺癌和卵巢癌)、hla-dr10(nhl)、hla-drb(非霍奇金淋巴瘤、b细胞白血病)、人绒毛膜促性腺激素(癌)、igf1r(胰岛素样生长因子1受体、实体瘤、血液癌症)、il-2受体(白细胞介素2受体、t-细胞白血病和淋巴瘤)、il-6r(白细胞介素6受体、多发性骨髓瘤、类风湿性关节炎、castleman病、il6依赖性肿瘤)、整合素(素αvβ3、α5β1、α6β4、αllβ3、α5β5、αvβ5细胞附着因子、各种癌症)、mage-1(各种癌)、mage-2(各种癌)、mage-3(各种癌)、mage4(各种癌)、抗转铁蛋白受体(各种癌)、p97(黑色素瘤)、ms4a1(跨膜域4亚科a成员1、非霍奇金b细胞淋巴瘤、白血病)、muc1或muc1-klh(乳腺癌、卵巢癌、子宫颈癌、支气管和胃肠道癌症)、muc16(ca125)(卵巢癌)、cea(大肠癌)、gp100(黑色素瘤)、mart1(黑色素瘤)、mpg(黑色素瘤)、ms4a1(跨膜域4蛋白a、小细胞肺癌、非霍奇金淋巴瘤)、核仁、神经癌基因产物(癌)、p21(癌)、抗(n-羟乙酰神经氨酸)抗体结合位(乳腺癌、黑色素瘤)、plap样睾丸碱性磷酸酶(卵巢癌、睾丸癌)、psma(前列腺肿瘤)、psa(前列腺癌)、robo4、tag72(肿瘤相关糖蛋白72、白血病、胃癌、结肠直肠癌、卵巢癌)、t细胞的跨膜蛋白(各种癌症)、tie(cd202b)、tnfrsf10b(肿瘤坏死因子受体超家族成员10b、各种癌症)、tnfrsf13b(肿瘤坏死因子受体超家族成员13b、多发性骨髓瘤、非霍奇金淋巴瘤、以及其他癌症、类风湿性关节炎和系统性红斑狼疮)、tpbg(滋养层糖蛋白、肾细胞癌)、trail-r1(肿瘤坏死凋亡诱导配体受体1、淋巴瘤、非霍奇金淋巴瘤、大肠癌、肺癌)、vcam-1(cd106、黑色素瘤)、血管内皮生长因子、血管内皮生长因子-a、vegf-2(cd309、各种癌症)。抗体识别的一些其他的肿瘤相关抗原可见于各种综述(gerber等,mabs1:3,247-253(2009);novellino等,cancerimmunolimmunother.54(3),187-207(2005);franke等,cancerbiotherradiopharm.2000,15,459-76)。 细胞结合剂,更优选为抗体,是能够抗肿瘤细胞、病毒感染细胞、微生物感染细胞、寄生虫感染细胞、自身免疫细胞、活化细胞、骨髓细胞、活化t细胞、b细胞或黑素细胞的任何试剂。更具体地说,细胞结合剂可以是能够抗以下任何一种抗原或受体的任何试剂/分子:cd2、cd2r、cd3、cd3gd、cd3e、cd4、cd5、cd6、cd7、cd8、cd8a、cd8b、cd9、cd10、cd11a、cd11b、cd11c、cd12、cd12w、cd13、cd14、cd15、cd15s、cd15u、cd16、cd16a、cd16b、cd17、cdw17、cd18、cd19、cd20、cd21、cd22、cd23、cd24、cd25、cd26、cd27、cd28、cd29、cd30、cd31、cd32、cd33、cd34、cd35、cd36、cd37、cd38、cd39、cd40、cd41、cd42、cd42a、cd42b、cd42c、cd42d、cd43、cd44、cd44r、cd45、cd45ra、cd45rb、cd45ro、cd46、cd47、cd47r、cd48、cd49a、cd49b、cd49c、cd49e、cd49f、cd50、cd51、cd52、cd53、cd54、cd55、cd56、cd57、cd58、cd59、cd60、cd60a、cd60b、cd60c、cd61、cd62e、cd62l、cd62p、cd63、cd64、cd65、cd65s、cd66、cd66a、cd66b、cd66c、cd66d、cd66e、cd66f、cd67、cd68、cd69、cd70、cd71、cd72、cd73、cd74、cd74、cd75、cd75s、cd76、cd77、cd78、cd79、cd79a、cd79b、cd80、cd81、cd82、cd83、cd84、cdw84、cd85、cd86、cd87、cd88、cd89、cd90、cd91、cd92、cdw92、cd93、cd94、cd95、cd96、cd97、cd98、cd99、cd99r、cd100、cd101、cd102、cd103、cd104、cd105、cd106、cd107、cd107a、cd107b、cd108、cd109、cd110、cd111、cd112、cd113、cdw113、cd114、cd115、cd116、cd117、cd118、cd119、cdw119、cd120a、cd120b、cd121a、cd121b、cdw121b、cd122、cd123、cdw123、cd124、cd125、cdw125、cd126、cd127、cd128、cdw128、cd129、cd130、cd131、cdw131、cd132、cd133、cd134、cd135、cd136、cdw136、cd137、cdw137、cd138、cd139、cd140a、cd140b、cd141、cd142、cd143、cd144、cd145、cdw145、cd146、cd147、cd148、cd149、cd150、cd151、cd152、cd153、cd154、cd155、cd156a、cd156b、cdw156c、cd157、cd158a、cd158b、cd159a、cd159b、cd159c、cd160、cd161、cd162、cd162r、cd163、cd164、cd165、cd166、cd167、cd167a、cd168、cd169、cd170、cd171、cd172a、cd172b、cd172g、cd173、cd174、cd175、cd175s、cd176、cd177、cd178、cd179、cd180、cd181、cd182、cd183、cd184、cd185、cd186、cdw186、cd187、cd188、cd189、cd190、cd191、cd192、cd193、cd194、cd195、cd196、cd197、cd198、cdw198、cd199、cdw199、cd200、cd200a、cd200b、cd201、cd202、cd202b、cd203、cd203c、cd204、cd205、cd206、cd207、cd208、cd209、cd210、cdw210、cd211、cd212、cd213a1、cd213a2、cd214、cd215、cd216、cdw217、cdw218a、cdw218b、cd219、cd220、cd221、cd222、cd223、cd224、cd225、cd226、cd227、cd228、cd229、cd230、cd231、cd232、cd233、cd234、cd235a、cd235ab、cd235b、cd236、cd236r、cd237、cd238、cd239、cd240、cd240ce、cd240d、cd241、cd242、cd243、cd244、cd245、cd246、cd247、cd248、cd249、cd250、cd251、cd252、cd253、cd254、cd256、cd257、cd258、cd259、cd260、cd261、cd262、cd263、cd264、cd265、cd266、cd267、cd268、cd269、、cd270、cd271、cd272、cd273、cd274、cd275、cd276(b7-h3)、cd277、cd278、cd279、cd280、cd281、cd282、cd283、cd284、cd285、cd286、cd287、cd288、cd289、cd290、cd291、cd292、cdw293、cd294、cd295、cd296、cd297、cd298、cd299、cd300a、cd300c、cd300e、cd301、cd302、cd303、cd304、cd305、cd306、cd307、cd308、cd309、cd310、cd311、cd312、cd314、cd315、cd316、cd317、cd318、cd319、cd320、cd321、cd322、cd323、cd324、cdw325、cd326、cdw327、cdw328、cdw329、cd330、cd331、cd332、cd333、cd334、cd335、cd336、cd337、cdw338、cd339、4-1bb、5ac、5t4(滋养层糖蛋白、tpbg、5t4、wnt激活的抑制因子1或waif1)、腺癌抗原、ags-5、ags-22m6、激活素受体样激酶1、afp、akap-4、alk、α-整合素、αvβ6、氨基肽酶n、淀粉样蛋白β、雄激素受体、血管生成素2、血管生成素3、膜联蛋白a1、炭疽毒素保护性抗原、抗转铁蛋白受体、aoc3(vap-1)、b7-h3、炭疽芽孢杆菌、baff(b细胞活化因子)、b淋巴瘤细胞、bcr-abl、bombesin、boris、c5、c242抗原、ca125(碳水化合物抗原125、muc16)、ca-ix(或caix、碳酸酐酶9)、calla、canag、canislupusfamiliarisil31、碳酸酐酶ix、心肌肌球蛋白、ccl11(c-c基序趋化因子11)、ccr4(c-c趋化因子受体4型、cd194)、ccr5、cd3e(ε)、cea(癌胚抗原)、ceacam3、ceacam5(癌胚抗原)、cfd(因子d)、ch4d5、胆囊收缩素2(cck2r)、cldn18(claudin-18)、结块因子a、cripto、fcsf1r(集落刺激因子1受体、cd115)、csf2(集落刺激因子2、粒细胞-巨噬细胞集落刺激因子(gm-csf))、ctla4(细胞毒性t淋巴细胞相关蛋白4)、ctaa16.88肿瘤抗原、cxcr4(cd184)、c-x-c趋化因子受体4型、环状adp核糖水解酶、细胞周期蛋白b1、cyp1b1、巨细胞病毒、巨细胞病毒糖蛋白b、达比加群、dll3(δ样配体3)、dll4(δ样配体4)、dpp4(二肽基肽酶4)、dr5(死亡受体5)、大肠杆菌志贺毒素型pe-1、大肠杆菌志贺毒素型pe-2、ed-b、egfl7(含egf样结构域的蛋白质7)、egfr、egfrii、egfrviii、内皮糖蛋白(cd105)、内皮素b受体、内毒素、epcam(上皮细胞粘附分子)、epha2、episialin、erbb2(表皮生长因子受体2)、erbb3、erg(tmprss2ets融合基因)、大肠杆菌、etv6-aml、fap(成纤维细胞活化蛋白α)、fcgr1、甲胎蛋白、纤维蛋白ii、β链、纤连蛋白额外结构域-b、folr(叶酸受体)、叶酸受体α、叶酸水解酶、fos相关抗原1、呼吸道合胞病毒f蛋白、卷曲受体、岩藻糖基gm1、gd2神经节苷脂、g-28(细胞表面抗原glyvolipid)、gd3独特型、globoh、磷脂酰肌醇蛋白聚糖3、n-羟乙酰神经氨酸、gm3、gmcsf受体α链、生长分化因子8、gp100、gpnmb(跨膜糖蛋白nmb)、gucy2c(鸟苷酸环化酶2c、鸟苷酸环化酶c(gc-c)、肠鸟苷酸环化酶、鸟苷酸环化酶c受体、热稳定肠毒素受体)、热休克蛋白、血凝素、乙型肝炎表面抗原、乙型肝炎病毒、her1(人表皮生长因子受体1)、her2、her2/neu、her3(erbb-3)、igg4、hgf/sf(肝细胞生长因子/散射因子)、hhgfr、hiv-1、组蛋白复合物、hla-dr(人类白细胞抗原)、hla-dr10、hla-drb、hmwmaa、人绒毛膜促性腺激素、hngf、人分散因子受体激酶、hpve6/e7、hsp90、htert、icam-1(细胞间粘附分子1)、独特型、igf1r(igf-1、胰岛素样生长因子1受体)、ighe、ifn-g、influezahemag-glutinin、ige、igefc区、ighe、白细胞介素(例如il-1、il-2、il-3、il-4、il-5、il-5、il-6、il-6r、il-7、il-8、il-9、il-9、il-10、il-11、il-12、il-13、il-13、il-15、il-17、il-17、il-17a、il-18、il-19、il-20、il-20、il-21、il-22、il-23、il-27、il-27、或il-28)、il31ra、ilgf2(胰岛素样生长因子2)、整合素(α4、αiibβ3、αvβ3、αvβ3、α4β7、α7、α5β1、α5β7、α5β1、α5β7、α5β8、il-α6β4、α7β7、αllβ3、α5β5、αvβ5)、干扰素γ诱导蛋白、itga2、itgb2、kir2d、lck、le、legumain、lewis-y抗原、lfa-1(淋巴细胞功能相关抗原1、cd11a)、lhrh、lingo-1、脂磷壁酸、liv1a、lmp2、lta、mad-ct-1、mad-ct-2、mage-1、mage-2、mage-3、magea1、magea3、mage4、mart1、mcp-1、mif(巨噬细胞移动抑制因子或糖基化抑制因子(gif))、ms4a1(跨膜4域亚家族a成员1)、msln(间皮素)、muc1(粘蛋白1、细胞表面相关(muc1)或多形上皮粘蛋白(pem))、muc1-klh、muc16(ca125)、mcp1(单核细胞趋化蛋白1)、melana/mart1、ml-iap、mpg、ms4a1(跨膜4域亚家族a)、mycn、髓鞘相关糖蛋白、肌肉生长抑制素、na17、narp-1、nca-90(粒细胞抗原)、nectin-4(asg-22me)、ngf、神经凋亡调节蛋白酶1、nogo-a、notch受体、nucleolin、neu癌基因产物、ny-br-1、ny-eso-1、ox-40、oxldl(氧化低密度脂蛋白)、oy-tes1、p21、p53非突变体、p97、page4、pap、抗-(n-羟乙酰神经氨酸)的互补位、pax3、pax5、pcsk9、pdcd1(pd-1、程序性细胞死亡蛋白1、cd279)、pdgf-rα(α型血小板衍生生长因子受体)、pdgfr-β、pdl-1、plac1、plap样睾丸碱性磷酸酶、血小板衍生生长因子受体β、磷酸钠共转运蛋白、pmel17、聚唾液酸、蛋白酶3(pr1)、前列腺癌、ps(磷脂酰丝氨酸)、前列腺癌细胞、铜绿假单胞菌、psma、psa、psca、狂犬病病毒糖蛋白、rhd(rh多肽1(rhpi)、cd240)、恒河猴因子、rankl、rantes受体(ccr1、ccr3、ccr5)、rhoc、ras突变体、rgs5、robo4、呼吸道合胞病毒、ron、肉瘤易位断点、sart3、硬骨素、slamf7(slamfamilymember7)、selectinp、sdc1(syndecan1)、sle(a)、somatomedinc、sip(鞘氨醇-1-磷酸)、生长抑素,精子蛋白17、ssx2、steap1(前列腺的六种跨膜上皮抗原1)、steap2、stn、tag-72(肿瘤相关糖蛋白72)、survivin、t-cellreceptor、tcell跨膜蛋白、tem1(肿瘤内皮标志物1)、tenb2、腱生蛋白c(tn-c)、tgf-α、tgf-β(转化生长因子β)、tgf-β1、tgf-β2(转化生长因子β2)、tie(cd202b)、tie2、tim-1(cdx-014)、tn、tnf、tnf-α、tnfrsf8、tnfrsf10b(肿瘤坏死因子受体超家族成员10b)、tnfrsf13b(肿瘤坏死因子受体超家族成员13b)、tpbg(滋养层糖蛋白)、trail-r1(肿瘤坏死凋亡诱导配体受体1)、trailr2(死亡受体5(dr5))、肿瘤相关钙信号转导2、肿瘤特异性糖基化muc1、tweak受体、tyrp1(糖蛋白75)、trop-2、trp-2、酪氨酸酶、vcam-1(cd106)、vegf、vegf-a、vegf-2(cd309)、vegfr-1、vegfr2或波形蛋白、wt1、xage1或表达任何胰岛素生长因子受体或任何表皮生长因子受体的细胞。 在具体的实施例中,本发明的双链接的偶联物可用于治疗癌症。目标癌症包括但不限于,肾上腺皮质癌、肛门癌、膀胱癌、大脑肿瘤(脑干神经胶质瘤、小脑星形细胞瘤、脑星形细胞瘤、室管膜瘤、成神经管细胞瘤、幕上原始神经外胚层和松果体肿瘤、视觉通路和下丘脑胶质瘤)、乳腺癌、类癌肿瘤、胃肠道癌症、未知小细胞癌、宫颈癌、结肠癌、子宫内膜癌、食道癌、肝外胆管癌、尤因家族肿瘤(pnet)、颅内生殖细胞肿瘤、眼癌、眼内黑色素瘤、胆囊癌、胃癌(胃癌)、性腺外生殖细胞瘤、孕周滋养细胞瘤、头颈癌、下咽癌、胰岛细胞癌、肾癌(肾细胞癌)、喉癌、白血病(急性淋巴细胞,急性髓系,慢性淋巴细胞,慢性粒细胞,毛细胞)、嘴唇和口腔癌症、肝癌、肺癌(非小细胞,小细胞)、淋巴瘤(艾滋病相关,中枢神经系统的,皮肤t细胞的,霍奇金病,非霍奇金病)、恶性间皮瘤、黑色素瘤、梅克尔细胞癌、转移性鳞状颈癌与隐匿性原发性癌、多发性骨髓瘤和其他浆细胞肿瘤、蕈样肉芽肿、骨髓增生异常综合征、骨髓增生异常、鼻咽癌、神经母细胞瘤、口腔癌、口咽癌、骨肉瘤、卵巢癌(上皮、生殖细胞瘤、低恶性肿瘤)、胰腺癌(外分泌,胰岛细胞癌)、副鼻窦和鼻腔癌、甲状旁腺癌、阴茎癌、嗜铬细胞瘤、垂体肿瘤、浆细胞肿瘤、前列腺癌横纹肌肉瘤、直肠癌、肾细胞癌(肾癌)、肾盂和输尿管(移行细胞)、唾腺癌、赛塞里综合症、皮肤癌(皮肤t细胞淋巴瘤,卡波西氏肉瘤,黑色素瘤)、小肠肿瘤、软组织肉瘤、胃癌、睾丸癌、胸腺瘤(恶性)、甲状腺癌、尿道癌症、子宫癌、不寻常的少年的癌症、阴道肿瘤、外阴肿瘤和维尔姆斯瘤。 在另一个具体的实施例中,本发明的偶联物、相应的组合物和方法可以用于治疗或预防自身免疫疾病。自身免疫性疾病包括但不限于,achlorhydra自身免疫性活动性慢性肝炎、急性播散性脑脊髓炎、急性出血性脑白质炎、艾迪生病、无精症、斑秃、肌萎缩侧索硬化症、强直性脊柱炎、抗gbm/tbm肾炎、抗磷脂综合征、抗异常酶综合征、关节炎、特应性过敏、特应性皮炎、自身免疫性再生障碍性贫血、自身免疫性心肌病、自身免疫性溶血性贫血、自身免疫性肝炎、自身免疫性内耳疾病、自身免疫性淋巴组织增生综合征、自身免疫性周围神经病、自身免疫性胰腺炎、自身免疫性多内分泌综合征i、ii和iii型、自身免疫性黄体酮皮炎、自身免疫性血小板减少性紫癜、自身免疫性葡萄膜炎、balo病/balo同心硬化症、bechets综合征、berger氏病、bickerstaff脑炎、blau综合征、大疱性类天疱疮、castleman病、chagas病、慢性疲劳免疫功能障碍综合征、慢性炎性脱髓鞘性多发性神经病、慢性复发性多灶性骨髓炎、慢性莱姆病、慢性阻塞性肺病、churg-strauss综合征、瘢痕性类天疱疮、乳糜泄、cogan综合征、冷凝集素病、补体成分2缺乏症、颅骨动脉炎、crest综合征、crohns病(特发性炎症性肠病)、库欣综合征、皮肤白细胞增多性血管炎、德戈氏病、dercum氏病、疱疹样皮炎、皮肌炎、1型糖尿病、弥漫性皮肤系统性硬化症、dressler综合征、盘状红斑狼疮、湿疹、子宫内膜异位症、附着点炎相关的关节炎、eosinophilic筋膜炎、大疱性表皮松解症、结节性红斑、特发性混合性冷球蛋白血症、伊文氏综合征、纤维发育不良性骨化症、纤维肌痛、纤维化性肌炎、纤维性肺泡炎、胃炎、胃肠类天疱疮、巨细胞动脉炎、肾小球肾炎、古德帕斯丘尔综合征、格雷夫斯病、格林-巴利综合征、桥本氏脑炎、桥本氏甲状腺炎、溶血性贫血、过敏性紫癜、妊娠性肝炎、化脓性汗腺炎、休斯综合征(抗磷脂综合征)、低丙球蛋白血症、特发性炎性脱髓鞘疾病、特发性肺纤维化、特发性血小板减少性紫癜(自身免疫性血小板减少性紫癜)、iga肾病(伯杰氏病)、包涵体肌炎、炎性脱髓鞘性多神经炎、间质性膀胱炎、过敏性肠综合征、少年特发性关节炎、青少年类风湿性关节炎、川崎氏病、朗伯-伊顿重症肌无力综合征、白细胞碎屑性血管炎、扁平苔癣、硬化性硬化症、线状iga疾病(lad)、lougehrig病(也称肌萎缩侧索硬化症)、狼疮性肝炎、红斑狼疮、majeed综合征、美尼尔氏病、显微镜下多动脉炎、米勒-费希尔综合征、混合性结缔组织病、硬斑病、穆罕默德-哈贝曼病、麦考利综合征、多发性骨髓瘤、多发性硬化症、重症肌无力、肌炎、嗜睡症、视神经脊髓炎(devic病)、神经性肌强直、眼睑瘢痕性类天疱疮、opsoclonusmyoclonus综合征、ord甲状腺炎、回文风湿病、pandas(与链球菌相关的小儿自身免疫性神经精神病)、paraneoplastic小脑变性、阵发性睡眠性血红蛋白尿症、parryromberg综合征、parsonnage-turner综合征、睫状体平部炎、天疱疮、寻常型天疱疮、贫血、周围脑脊髓炎、poems综合征、结节性多动脉炎、风湿性多肌痛、多发性肌炎、原发性胆汁性肝硬化、原发性硬化性胆管炎、进行性炎症性神经病变、牛皮癣、牛皮癣性关节炎、坏疽性皮肤炎、纯红细胞再生障碍、rasmussen脑炎、雷诺现象、复发性多软骨炎、赖特综合征、不宁腿综合症、后神经纤维化、类风湿性关节炎、类风湿热、结节病、精神分裂症、施密特综合征、schnitzler综合征、施尼茨勒综合征、巩膜炎、硬皮病、干燥综合征、脊椎关节病、粘稠血症、still病、僵人综合征、亚急性细菌性心内膜炎、苏萨克综合征、sweet综合征、小舞蹈病、交感神经性贫血、takayasu动脉炎、颞动脉炎(巨细胞动脉炎)、tolosa-hunt综合征、横贯性脊髓炎、溃疡性结肠炎(特发性炎性肠病)、未分化结缔组织病、未分化脊柱关节病、血管炎、白癜风、韦格纳肉芽肿病、威尔逊氏综合征、威斯科特-奥尔德里奇综合征。 在另一个具体的实施例中,本发明中双链接偶联物上的结合分子,可用于治疗或预防自身免疫疾病,包括但不限于,抗弹性蛋白抗体、abys抗上皮细胞抗体、抗地下室膜iv型胶原蛋白抗体、抗核抗体、抗dsdna、抗ssdna、抗心磷脂抗体igm、igg、抗乳糜泻抗体、抗磷脂抗体igk、igg、抗sm抗体、抗线粒体抗体、甲状腺抗体、微粒体抗体、t细胞抗体、甲状腺球蛋白抗体、抗scl-70、抗jo、抗u.sub.1rnp、抗la/ssb、抗ssa、抗ssb、抗壁细胞抗体、抗组蛋白、抗rnp、c-anca、p-anca、抗着丝粒、抗纤维蛋白原、抗gbm抗体、抗神经节苷脂抗体、抗desmogein3抗体、抗p62抗体、抗sp100抗体、抗线粒体(m2)抗体、类风湿因子抗体、抗mcv抗体、抗拓扑异构酶抗体、抗中性粒细胞胞质(canca)抗体。 在某些优选的实施例中,本专利申请中偶联物上的结合分子,可以与自身免疫性疾病相关的激活淋巴细胞上表达的受体或受体复合物相结合。受体或受体复合物包含,免疫球蛋白基因超家族成员(例如cd2、cd3、cd4、cd8、cd19、cd20、cd22、cd25、cd27、cd28、cd30、cd33、cd37、cd38、cd56、cd70、cd79、cd79b、cd90、cd152/ctla-4、pd-1、pd-l1或icos)、tnf受体超家族成员(例如cd27、cd40、cd95/fas、cd134/ox40、cd137/4-1bb、inf-r1、tnfr-2、rank、taci、bcma、骨保护素、apo2/trail-r1、trail-r2、trail-r3、trail-r4和apo-3)、整合蛋白、细胞因子受体、趋化因子受体、主要组织相容性蛋白、凝集素(c型、s型或i型)或补体控制蛋白。 在另一个具体实施例中,可用的对病毒或微生物抗原具有免疫特异性的细胞结合配体是人源化或人单克隆抗体。“病毒抗原”包括但不限于,任何能够引发免疫应答的病毒肽,多肽蛋白(例如hivgp120、hivnef、rsvf糖蛋白、流感病毒神经氨酸苷酶、流感病毒血凝素、htlvtax、疱疹单纯疱疹病毒糖蛋白(例如gb、gc、gd和ge)和乙型肝炎表面抗原)。“微生物抗原”包括但不限于,任何能够引发免疫应答的微生物肽、多肽、蛋白质、糖、多糖或脂质分子(例如细菌、真菌、致病原生动物或酵母多肽、包括如lps和荚膜多糖5/8)。可用于治疗病毒或微生物感染的抗体的实例,包括但不限于:帕利珠单抗,它是用于治疗rsv感染的,人源化抗呼吸道合胞病毒单克隆抗体;pro542,是一种cd4融合抗体,用于治疗hiv感染;奥斯他韦,是一种用于治疗乙型肝炎病毒的人抗体;protvir,是一种人源化igg1抗体,用于治疗巨细胞病毒,和抗lps抗体。 以双连接子链接的本发明中的细胞结合分子-药物偶联物可用于治疗感染性疾病。这些感染性疾病包括但不限于,不动杆菌属感染、放线菌病、非洲昏睡病(非洲锥虫病)、艾滋病(获得性免疫缺陷综合症)、阿米巴病、无形体病、炭疽、溶血性耶尔森菌感染、阿根廷出血热、蛔虫病、曲霉病、星状病毒感染、巴贝斯虫病、蜡状芽孢杆菌感染、细菌性肺炎、细菌性阴道炎、类杆菌感染、小袋虫病、蛔虫感染、bk病毒感染、黑色发结节病、人芽囊原虫感染、芽生菌病、玻利维亚出血热、疏螺旋体感染、肉毒中毒(和婴儿肉毒中毒)、巴西出血热、布鲁氏杆菌病、伯克霍尔德氏菌感染、布鲁里溃疡、杯状病毒感染(诺如病毒和沙波病毒)、弯曲杆菌病、念珠菌病(念珠菌病、鹅口疮)、猫抓病、蜂窝组织炎、chagas病(美洲锥虫病)、子囊、水痘、衣原体、肺炎衣原体感染、霍乱、色素母细胞瘤、华支睾吸虫、艰难梭状芽孢杆菌感染、球孢子菌病、科罗拉多蜱热病、普通感冒(急性病毒性鼻咽炎、急性鼻炎)、克雅氏病、克里米亚-刚果出血热、隐球菌病、隐孢子虫病、皮肤幼虫迁徙、环孢子虫病、肠杆菌感染、肠道病毒感染、流行性斑疹伤寒、传染性红斑(第五种疾病)、急疹、姜片虫病、肝片吸虫病、致命性家族性失眠、丝虫病、产气荚膜梭菌食物中毒、自由活体阿米巴感染、梭杆菌感染、气性坏疽(梭菌性肌坏死)、地丝菌病、格斯特曼-斯特拉斯勒-谢克尔病综合征、贾第鞭毛虫病、马鼻疽、淋病、肉芽肿性腹泻(第五性病)、a群链球菌感染、b群链球菌感染、流感嗜血杆菌感染、手足口病(hfmd)、汉坦病毒肺综合征、幽门螺杆菌感染、溶血性尿毒综合征、肾综合征出血热、甲型肝炎、乙型肝炎、丙型肝炎、丁型肝炎、戊型肝炎、单纯性疱疹、组织胞浆菌病、钩虫感染、人类博卡病毒感染、人类ewingii埃里希体病、人类粒细胞无形体病、人类偏肺病毒感染、人类单核细胞埃里希体病、人乳头瘤病毒感染、人副流感病毒感染、膜壳绦虫病、艾巴氏病毒传染性单核细胞增多症(单)、流行性感冒、等孢子虫病、川崎病、角膜炎、金格杆菌感染、库鲁病、拉沙热、军团病(退伍军人症)、军团病(庞蒂亚克热)、利什曼病、莱姆病、淋巴丝虫病(象皮病)、淋巴细胞性脉络丛脑膜炎、疟疾、马尔堡出血热、麻疹、类鼻疽病(惠氏病)、脑膜炎、脑膜炎球菌病、后殖吸虫病、微孢子虫病、传染性软疣、腮腺炎、小鼠斑疹伤寒(地方性斑疹伤寒)、支原体肺炎、足菌肿、蝇蛆病、新生儿结膜炎(新生儿眼病)、变异型克雅氏病(vcjd、nvcjd)、诺卡氏菌病、盘尾丝虫病(河盲症)、副球孢子菌病(南美芽生菌病)、肺吸虫病、巴斯德氏菌病、头虱、体虱、阴虱、盆腔炎、百日咳、鼠疫、肺炎球菌感染、肺孢子虫肺炎、肺炎、脊髓灰质炎、普氏菌感染、原发性阿米巴脑膜脑炎、进行性多灶性白质脑病、鹦鹉热、q热、狂犬病、鼠咬热、呼吸道合胞病毒感染、鼻孢子虫病、鼻病毒感染、立克次体感染、立克次体痘、裂谷热、落基山斑疹热、轮状病毒感染、风疹、沙门氏菌病、sars(严重急性呼吸综合征)、疥疮、血吸虫病、败血症、志贺氏菌病(bacillary痢疾)、带状疱疹(带状疱疹)、天花(天花)、孢子丝菌、葡萄球菌食物中毒、感染金黄色葡萄球菌、粪类圆线虫病、梅毒、绦虫病、破伤风、须癣(barber痒)、头皮癣、体癣、股癣、手癣、掌黑癣、足癣(香港脚)、甲癣(灰指甲)、花斑癣、弓蛔虫病(眼幼虫移行症)、弓蛔虫病(内脏幼虫移行症)、弓形体病、旋毛虫病、滴虫病、鞭虫病(鞭虫感染)、肺结核、兔热病、解脲脲原体感染、委内瑞拉马脑炎、委内瑞拉出血热、病毒性肺炎、西尼罗河热、白毛结节病(白癣)、假结核耶尔森氏菌、耶尔森氏鼠疫杆菌肠道病、黄热病、接合菌病。 本发明的细胞结合剂,更优选为抗体,抗病原菌株包括但不限于,鲍氏不动杆菌、以色列放线菌、放线菌和丙酸杆菌、布氏锥虫、hiv(人免疫缺陷病毒病毒)、溶组织内阿米巴、无形体属、炭疽芽孢杆菌、溶血弧菌、胡宁病毒、蛔虫属、曲霉属、星状病毒科、巴贝虫属、蜡状芽孢杆菌、多种细菌、拟杆菌属、大肠杆菌、蛔虫属、bk病毒、结节菌、人芽囊原虫、皮炎芽生菌、马丘波病毒、疏螺旋体属、肉毒梭菌、清风藤属、布鲁氏菌属、通常为洋葱伯克霍尔德菌和其他伯克霍尔德氏菌种、溃疡分枝杆菌、杯状病毒科、弯曲杆菌属、通常为白色假丝酵母和其他假丝酵母属、汉赛巴尔通体、a群链球菌和葡萄球菌、克氏锥虫、杜克雷嗜血杆菌、vzv、沙眼衣原体、科罗拉多蜱热病毒、鼻病毒、冠状病毒、cjd朊病毒、克里米亚-刚果出血热病毒、新型隐球菌、隐孢子虫属、巴西钩虫、多种寄生虫、环孢子虫、带状绦虫、巨细胞病毒、登革热病毒(den-1、den-2、den-3和den-4)-黄病毒、脆弱双歧杆菌、白喉棒状杆菌、裂头绦虫、麦地那龙线虫、埃博拉病毒、棘球绦虫属、埃立克体肠球菌属、肠道病毒属、普氏立克次体、细小病毒b19、人疱疹病毒6和人疱疹病毒7、布氏姜片虫、肝片吸虫和巨大片吸虫、ffi朊病毒、丝虫目超家族、产气荚膜梭菌、梭杆菌属、其他梭状芽孢杆菌、白地霉、gss朊病毒、肠道贾第虫、伯克霍尔德氏菌、刺孢小芽孢杆菌和革兰氏假丝酵母、淋球菌、肉芽肿克雷伯氏菌、化脓性链球菌、无乳链球菌、流感嗜血杆菌、肠道病毒、主要是柯萨奇a病毒和肠道病毒71、无名病毒、幽门螺旋杆菌、大肠杆菌o157:h7、布尼亚病毒科、甲型肝炎病毒、乙型肝炎病毒、丙型肝炎病毒、丁型肝炎病毒、戊型肝炎病毒、单纯疱疹病毒1、单纯疱疹病毒2、荚膜组织胞浆菌、十二指肠腺瘤和壶腹癌流感嗜血杆菌、人博卡病毒、埃里希体、嗜吞噬细胞无嗜血杆菌、人偏肺病毒、查菲埃里希体、人乳头瘤病毒、人副流感病毒、微小膜壳绦虫和缩小膜壳绦虫、艾巴氏病毒、正粘病毒科家族、贝氏等孢球虫、金格杆菌、肺炎克雷伯菌、克雷伯氏菌、嗜肺军团菌、嗜肺军团菌、嗜肺军团菌、利什曼原虫属、麻风分枝杆菌和结核分枝杆菌、钩端螺旋体属、单核细胞增多性李斯特氏菌、伯氏疏螺旋体和其他疏螺旋体属物种、班氏旋毛虫和马来丝虫、淋巴细胞脉络丛脑膜炎病毒(lcmv)疟原虫属、马尔堡病毒、麻疹病毒、类鼻疽伯克霍尔德氏菌、脑膜炎奈瑟氏球菌、横川后殖吸虫、小孢子虫目门、传染性软疣病毒(mcv)、腮腺炎病毒、伤寒立克次氏体、肺炎支原体、多种细菌和真菌寄生双翅蝇幼虫、沙眼衣原体和淋病奈瑟菌、vcjd朊病毒、诺卡氏菌和其他诺卡氏菌属、盘尾丝虫属、盘鲍拟亚科、副龙属西马尼和其他副属、巴斯德氏菌属、头虱、人体虱、百日咳博德特氏菌鼠疫耶尔森氏菌、肺炎链球菌、肺炎球菌、脊髓灰质炎病毒、普雷沃氏菌属、奈氏格氏杆菌、jc病毒、鹦鹉热衣原体、伯氏考克斯体、狂犬病病毒、单链球菌和螺旋菌、呼吸道合胞病毒、鼻孢子菌、鼻病毒、立克次体属、由小株立克次体、裂谷热病毒、立克次体立克次体、轮状病毒、风疹、沙门氏菌属、sars冠状病毒、人疥螨、血吸虫属、体细胞属、志贺菌属、水痘带状疱疹病毒、天花少校或天花小、申克孢子丝菌、金黄色葡萄球菌属、金黄色葡萄球菌、链球菌化脓、圆线虫、梅毒螺旋体、绦虫属、破伤风、癣属癣音铀、癣属、絮状表皮癣菌、红色毛癣菌、须毛癣菌、红色毛癣菌、威尼克外瓶黴、毛癣菌属属、细胞死亡属、弓箭毒或弓箭毒、刚地弓形虫、旋毛虫、阴道毛滴虫、三丘里三种、结核分枝杆菌、弗朗西拉图拉菌、尿素和马脑炎病毒、委内瑞拉马脑炎病毒、霍乱弧菌、瓜纳里托病毒、西尼罗河病毒、beigelii丝孢、假结核耶尔森氏菌、小肠结肠炎耶尔森氏菌、黄热病病毒、毛霉菌目阶(毛霉菌病)和虫霉目阶(虫霉属真菌病)、毛霉菌目绿脓杆菌、弯曲杆菌(弧菌)、气单胞菌、艾氏菌、耶尔森氏菌、志贺痢疾杆菌、志贺氏杆菌、志贺氏菌、沙门氏菌、伤寒沙门氏菌、雅司螺旋体、奋森氏螺旋体、伯氏疏螺旋体、细螺旋体、卡氏肺孢子虫、流产布鲁氏菌、布鲁杆菌、布鲁氏菌、支原体属、普氏立克次体、恙虫病立克次氏体、衣原体属、致病性真菌(烟曲霉、白色念珠菌、荚膜组织胞浆菌)、原生动物(溶组织内阿米巴、tenas毛滴虫、hominis毛滴虫、冈比亚锥虫、罗得西亚锥虫、罗氏利什曼原虫、热带利什曼原虫、巴西利什曼原虫、肺孢子虫肺炎、间日疟原虫、恶性疟原虫、疟原虫疟疾)或helminiths(日本血吸虫、曼氏血吸虫、埃及血吸虫和钩虫)。 其他用作本发明的细胞结合剂,治疗病毒性疾病的抗体,包括但不限于,抗下列致病性病毒抗原的抗体:痘病毒、疱疹病毒、腺病毒、小黄病毒、肠病毒、小核糖核酸病毒、细小病毒、呼肠病毒、逆转录病毒、流感病毒、副流感病毒、腮腺炎、麻疹、呼吸道合胞病毒、风疹、虫媒病毒、弹状病毒、沙门氏菌、非a/非b型肝炎病毒、鼻病毒、冠状病毒、罗托病毒、致癌病毒、如hbv(肝细胞癌)、人乳头状瘤病毒(宫颈癌、肛门癌)、卡波济氏肉瘤相关的疱疹病毒(卡波济氏肉瘤肉瘤)、人类疱疹病毒第四型(鼻咽癌、伯基特淋巴瘤、原发性中枢神经系统淋巴瘤)、瘤病毒(默克尔细胞癌)、sv40(猿猴病毒40)、hcv(肝细胞癌)、htlv-1(成人t细胞白血病/淋巴瘤);免疫紊乱导致病毒,如人类免疫缺陷病毒(艾滋病)、中枢神经系统病毒,如jcv(进行性多灶性脑白质病)、丙型肝炎病毒(亚急性硬化性全脑炎)、lcv(淋巴细胞性脉络丛脑膜炎)、亚博病毒脑炎、正粘病毒(脑炎性脑炎)、rv(狂犬病)、长鼻病毒、疱疹病毒脑膜炎、拉姆齐亨特综合征ii型、脊髓灰质炎病毒(脊髓灰质炎病毒、后脊髓灰质炎综合征)、htlv-1(热带麻痹性麻痹))、巨细胞病毒(巨细胞病毒视网膜炎、hsv(疱疹性角膜炎)、心血管病毒,如cbv(心包炎、心肌炎)、呼吸系统/急性病毒性鼻内炎/病毒性肺炎,如爱泼斯坦-巴尔病毒(ebv感染/传染性单核病)、巨细胞病毒、非典冠状病毒(严重急性呼吸综合征)或正黏液病毒、流感病毒a/b/c(流感/禽流感)、副粘病毒、人类副流感病毒、rsv(人类呼吸道合胞病毒)、hmpv、消化系统病毒(腮腺炎病毒、巨细胞病毒(巨细胞病毒食管炎)、腺病毒(腺病毒感染)、轮状病毒、诺瓦克病毒、星状病毒、冠状病毒、乙型肝炎病毒、cbv、甲型肝炎病毒、丙型肝炎病毒、丁型肝炎病毒、戊型肝炎病毒、hgv)、泌尿生殖病毒,如bk病毒、muv(腮腺炎)。 更进一步,本发明也包括用本发明中偶联物和可接受的载体,稀释剂或辅料构成的组合物,以治疗癌症、感染或自身免疫性疾病。治疗癌症、感染和自身免疫性疾病的方法可以在体外,体内或离体实施。体外用途的实例包括用它处理细胞培养物,以杀死除了不表达靶抗原的变体以外的所有细胞;或者杀死表达不需要的抗原的变体。离体使用的例子包括在进行移植(hsct)之前对造血干细胞(hsc)进行处理,以杀死患病或恶性肿瘤细胞。例如,在癌症治疗中的自体移植之前或在自身免疫性疾病的治疗中从骨髓中去除肿瘤细胞或淋巴细胞,或在移植之前为了防止移植物抗宿主疾病从同种异体骨髓或组织中除去t细胞和其他淋巴细胞。这样的临床离体治疗可以按如下步骤进行:从患者或其他个体收获骨髓,然后在含有血清的培养基中约37℃下孵育约30分钟至约48小时,在该培养基中加入本发明的偶联物,浓度范围从约1pm至0.1mm。具体的药物浓度和孵育时间应当由专业临床医师决定。孵育后,用含血清的培养基洗涤骨髓细胞,并按照已知的方法通过静脉注射给患者。若患者在骨髓采集和再输注治疗细胞之间,还接受其它治疗(例如消融化疗或全身辐射疗程)的情况下,应使用标准医疗设备将处理后的骨髓细胞在液氮中冷冻储存。 用于偶联的药物/细胞毒性剂 在本发明中,可与细胞结合分子偶联的药物是包括细胞毒性剂在内的小分子药物。本发明中的“小分子药物”泛指分子量为100至4000,更优200至3000的有机、无机或金属有机化合物。这些小分子药物在本领域文献中已被充分描述,如wo0a2和美国专利4,956,303。小分子药物包括已知的药物和即将成为已知的药物。 已知的药物包括但不限于, 1)化疗药物:a)烷基化剂,如氮芥:氯苯那普,氯普那嗪,环磷酰胺,达喀尔巴嗪,雌二醇氮芥,异环磷酰胺,氮芥,盐酸二甲氧胺,氧化二氮芥,盐酸氨氯地平,麦考酚酸,卫矛醇,呱泊溴烷,新氮芥,苯芥胆甾醇,松龙苯芥,噻替呱,曲磷胺对,尿嘧啶;cc-1065(包括其阿多来新、卡折来新、比折来新及其合成类似物);多卡霉素(包括kw-2189和cbi-tmi、及其合成类似物);苯并二氮二聚体(例如吡咯并苯二氮(pbd)或托美霉素,吲哚并苯并二氮杂,咪唑并苯并噻二氮杂或恶唑烷并苯并二氮杂的二聚体);亚硝基脲(卡莫司汀,洛莫司汀,氯化梭菌素,福莫司汀,尼莫司汀,拉莫司汀);烷基磺酸盐(白苏芬、树苏芬、磺胺异丙磺胺和皮苏芬);三氮烯(达喀尔巴嗪);含铂化合物(卡铂,顺铂,奥沙利铂);吖丙啶类,如苯并二氢吡喃酮,卡洛酮,美妥替派和乌雷多巴;乙烯亚胺和甲基三聚氰胺,包括六甲蜜胺,三亚乙基三胺,三乙基磷酰胺,三亚乙基硫代磷酰胺和三羟甲基甲基胺; b)植物生物碱:如长春花生物碱(长春新碱,长春碱,长春地辛,长春瑞滨,去甲长春碱);紫杉醇类(紫杉醇,多西紫杉醇及其类似物);美登素类(dm1、dm2、dm3、dm4、美登素、安沙霉素及其类似物);cryptophycin(特别是cryptophycin1和cryptophycin8);埃博霉素,软珊瑚醇,迪莫利德,草苔虫内酯,海兔毒素,澳瑞斯汀,tubulysins,cephalostatin;pancratistatin;erbulins;sarcodictyin;海绵抑制素; c)dna拓扑异构酶抑制剂,例如依托泊苷替尼(9-氨基喜树碱,喜树碱,克立那托,多拉霉素,依托泊苷,磷酸依托泊苷,伊立替康,米托蒽醌,诺消灵,视黄酸(视黄醇),替尼泊苷,拓扑替康,9-硝基喜树碱(rfs2000));丝裂霉素(丝裂霉素c); d)抗代谢物,例如抗叶酸剂,dhfr抑制剂(甲氨蝶呤,曲麦克特,二甲叶酸,蝶罗呤,氨喋呤(4-氨基苯甲酸)或其他叶酸类似物);imp脱氢酶抑制剂(麦考酚酸,噻唑呋林,利巴韦林,eicar);核糖核苷酸还原酶抑制剂(羟基脲,去铁胺);嘧啶类似物,尿嘧啶类似物(安西他滨,阿扎胞苷,6-氮尿嘧啶,卡培他滨(希罗达),卡莫氟,阿糖胞苷,双脱氧尿苷,脱氧氟尿苷,依诺他滨,5-氟尿嘧啶,氟尿苷,ratitrexed(tomudex);胞嘧啶类似物(阿糖胞苷,胞嘧啶阿拉伯糖苷,氟达拉滨);嘌呤类似物(硫唑嘌呤,氟达拉滨,巯嘌呤,硫胺素,硫鸟嘌呤);叶酸补充剂,如弗洛林酸;和烟酰胺磷酸核糖基转移酶(nampt)的抑制剂; e)激素疗法剂,如受体拮抗剂,抗雌激素(甲地孕酮,雷洛昔芬,他莫昔芬),lhrh兴奋剂(戈斯他林,醋酸亮丙瑞林);抗雄激素药(比卡鲁胺,氟他胺,卡鲁司酮,丙酸倍他雄酮,表雄甾醇,戈舍瑞林,亮丙瑞林,美替利定,尼鲁米特,睾内酯,曲洛司坦及其他雄激素抑制剂);维甲类化合物,维生素d3类似物(cb1093,eb1089,kh1060,胆钙化醇,麦角钙化甾醇);光动力疗法剂(维替泊芬,酞菁,光敏剂pc4,去甲氧基-竹红菌素a);细胞因子(干扰素-α,干扰素-γ,肿瘤坏死因子(tnf),含tnf的人蛋白); f)激酶抑制剂,如bibw2992(抗-egfr/erb2),伊马替尼,吉非替尼,呱加他尼,索拉非尼,达沙替尼,舒尼替尼,厄洛替尼,尼洛替尼,拉帕替尼,阿西替尼,帕唑帕尼,凡德他尼,e7080(抗vegfr2),mubritinib,普纳替尼(ap24534),bafetinib(inno-406),bosutinib(ski-606),卡博替尼,维莫德吉,iniparib,鲁索利替尼,cyt387,阿西替尼,tivozanib,索拉非尼,贝伐单抗,西妥昔单抗,曲妥珠单抗,雷珠单抗,帕尼单抗,伊斯平斯;g)聚(adp-核糖)聚合酶(parp)抑制剂,如奥拉帕里、尼拉帕里、依尼帕里、塔拉佐帕里、维利帕里、维利帕里、cep9722(cephalon)、e7016(eisai)、bgb-290(beigene)、3-氨基苯甲酰酰胺; h)抗生素,如烯二炔类抗生素(加利车霉素,特别是加利车霉素γ1,δ1,α1和β1(参考j.med.chem.1996,39(11),2103-2117;angewchemintl.ed.engl.1994,33:183-186),达因霉素,包括达因霉素a和脱氧米霉素,埃斯培拉霉素,卡塔尔霉素,c-1027,maduropeptin,新卡嗪奥斯汀和相关色蛋白烯二炔抗生素),aclacinomysins,放线菌素,安曲霉素,重氮丝氨酸,博来霉素,卡诺霉素,卡拉霉素,洋红霉素,嗜癌素,色霉素,达金霉素,柔红霉素,去柔红霉素,6-重氮-5-氧代-l-去甲亮氨酸,阿霉素,吗啉-阿霉素,氰基吗啉-阿霉素,2-吡咯啉阿霉素和脱氧柔红霉素,表柔比星,阿柔比星,伊达比星,马可霉素,nitomycin,霉酚酸,诺加霉素,橄榄霉素,peplomycin,potfiromycin,嘌呤霉素,奎拉霉素,罗道霉素,链黑霉素,链脲霉素,杀结核菌素,乌苯美司,净司他丁,佐柔比星; i)其他,如聚酮化合物(番荔素),特别是bullatacin和bullatacinone;吉西他滨,环氧酶素(如卡菲偌米布),硼替佐米,沙利度胺,来那度胺,pomalidomide,tosedostat,zybrestat,plx4032,sta-9090,stimuvax,allovectin-7,xegeva,provenge,yervoy,异戊二烯化抑制剂(如洛伐他汀),多巴胺能神经毒素(如星形孢菌素),放线菌素(如放线菌素d,更生霉素),博莱霉素(如博来霉素a2,博莱霉素b2,培洛霉素),蒽环类抗生素(如柔红霉素),鹅膏毒素,阿霉素(亚德里亚霉素),伊达比星,表柔比星,吡柔比星,佐柔比星,米托蒽醌,mdr抑制剂(如维拉帕米),ca2+atp酶抑制剂(如毒胡萝卜素),组蛋白去乙酰酶抑制剂(伏立诺他,罗米地辛,帕比司他,丙戊酸,mocetinostat(mgcd0103),belinostat,pci-24781,恩替诺特,sb939,resminostat,givinostat,ar-42,cudc-101,萝卜硫素,曲古抑菌素a);塞来昔布,格列酮类,表没食子儿茶素没食子酸酯,双硫仑,salinosporamidea;抗肾上腺药物,如氨鲁米特,米托坦,曲洛司坦,醋葡醛内酯,醛磷酰胺,氨基乙酰丙酸,安吖啶,阿拉伯糖苷,bestrabucil,比生群,edatraxate,defofamine,美可辛,地吖醌,依氟鸟氨酸(dfmo),elfomithine,依利醋铵,依托格鲁,硝酸镓,胞嘧啶,羟基脲,伊班膦酸盐,香菇多糖,氯尼达明,米托胍腙,米托蒽醌,莫呱达醇,二胺硝吖啶,喷司他丁,蛋氨氮芥,吡柔比星,鬼臼酸,2-乙肼,甲基苄肼;呱嗪二酮丙烷;根霉素;西佐;螺环锗;细格孢氮杂酸;三亚胺醌;三氯三乙胺;单端孢霉烯(特别是t-2毒素,疣孢菌素a,杆孢菌素a和anguidine),聚氨酯,sirna,反义药物和核酸分解酶。 2)自身免疫疾病药物,包括但不限于,环孢菌素,环孢菌素a,氨基己酸,硫唑嘌呤,溴隐亭,苯丁酸氮芥,氯喹,环磷酰胺,皮质类固醇(例如安西奈德,倍他米松,布地奈德,氢化可的松,氟尼缩松,丙酸氟替卡松,氟可龙达那唑,地塞米松,曲安奈德,二丙酸倍氯米松),dhea,依那西普,羟基氯喹,英夫利昔单抗,美洛昔康,甲氨蝶呤,麦考酚酸酯,泼尼松,西罗莫司,他克莫司。 3)抗感染性疾病药物,包括但不限于a)氨基糖苷类:阿米卡星,阿司米星,庆大霉素(奈替米星,西索米星,异帕米星),潮霉素b,卡那霉素(阿米卡星,阿贝卡星,氨基脱氧卡那霉素,地贝卡星,妥布霉素),新霉素(framycetin,巴龙霉素,核糖霉素),奈替米星,壮观霉素,链霉素,妥布霉素,甲基姿苏霉素;b)酰胺醇类:迭氮氯霉素,氯霉素,氟苯尼考,甲砜霉素;c)安沙霉素:格尔德霉素,除莠霉素;d)碳青霉烯类:比阿培南,多利培南,厄他培南,亚胺培南/西司他丁,美罗培南,帕尼培南;e)头孢烯:碳头孢烯(洛拉卡比),头孢乙腈,氯氨苄青霉素,头孢拉定,头孢羟氨,头孢洛宁,头孢噻啶,头孢噻吩或头孢金素,头孢氨苄,头孢来星,头孢孟多,头孢匹林,羟胺唑头孢菌素,氟唑头孢菌素,孢西酮,唑啉头孢菌素,头孢拉宗,头孢卡品,头孢达肟,头孢吡,头孢克肟,头孢西丁,头孢罗齐,头孢甲氧环烯胺,头孢替唑,头孢呋辛,头孢克肟,头孢地尼,头孢托仑,头孢吡,头孢他美,头孢甲肟,头孢地嗪,头孢尼西,头孢呱酮,头孢雷特,头孢噻肟,噻乙胺唑头孢菌素,头孢唑兰,头孢氨苄,头孢咪唑,头孢匹胺,头孢匹罗,头孢泊肟,头孢罗齐,头孢喹诺,头孢磺啶,头孢他啶,头孢特仑,头孢布腾,头孢噻林,头孢唑肟,头孢吡普,头孢曲松,头孢呋辛,头孢唑南,头霉素(头孢西丁,头孢替坦,头孢氰唑),氧(碳)头孢烯(氟氧头孢,拉氧头孢);f)糖肽:博来霉素,万古霉素(奥利万星,特拉万星),替考拉宁(达巴万星),雷莫拉宁;g)甘氨酰环素:如替加环素;h)β-内酰胺酶抑制剂:青霉烷(舒巴坦,他唑巴坦),氧青霉烷(克拉维酸);i)林可酰胺:克林霉素,林可霉素;j)脂肽:达托霉素,a54145,钙依赖性抗生素(cda);k)大环内酯类:阿奇霉素,克霉素,克拉霉素,地红霉素,红霉素,氟雷霉素,交沙霉素,酮内酯(泰利霉素,塞红霉素),麦迪霉素,米卡霉素,竹桃霉素,利福霉素(异烟肼、利福平,利福布丁,利福喷汀),罗匹霉素,罗红霉素,大观霉素,螺旋霉素,他克莫司(fk506),醋竹桃霉素,泰利霉素;l)单环胺:氨曲南,替吉莫南;m)恶唑烷酮类:利奈唑胺;n)青霉素类:阿莫西林,氨苄青霉素(匹氨西林,海洛西林,巴氨西林,氨苄青霉素,阿霉素),阿替代西林,阿洛西林,苄青霉素,苄星青霉素苄青霉素,苄星青霉素苯氧甲基青霉素,克洛西林,普鲁卡因青霉素(美替西林),美洛西林,甲氧西林,萘夫西林,苯唑西林,醋甲西林,青霉素,非奈西林,苯氧基甲基青霉素,呱拉西林,氨苄西林,磺苯西林,替莫西林,替卡西林;o)多肽:杆菌肽,粘菌素,多粘菌素b;p)喹诺酮类:阿拉曲沙星,巴洛沙星,环丙沙星,克林沙,达氟沙星,二氟沙星,依诺沙星,恩诺沙星,加雷沙星,加替沙星,吉米沙星,格帕沙星,卡诺曲伐沙星,左氧氟沙星,洛美沙星,麻保沙星,莫西沙星,那氟沙星,诺氟沙星,奥比沙星,氧氟沙星,培氟沙星,曲伐沙星,格帕沙星,西他沙星,司帕沙星,替马沙星,托沙星,曲伐沙星;q)链阳性菌素:普那霉素,奎奴普丁/达福普汀;r)磺胺类:氨芐磺胺,偶氮磺胺,磺胺嘧啶,磺胺甲异唑、磺胺酰亚胺、磺胺吡啶、磺胺异恶唑、甲氧苄啶、磺胺甲恶唑(复方磺胺甲恶唑);s)类固醇抗菌药物:如夫西地酸;t)四环素类:强力霉素,金霉素,氯米西环素,地美环素,雷莫昔林,美西环素,美他环素,米诺环素,土霉素,潘美环素,吡咯烷甲基四环素,四环素,甘氨酰环素(如替加环素);u)其他类型的抗生素:番荔枝素,胂凡纳明,细菌萜醇抑制剂(杆菌肽),danal/ar抑制剂(环丝氨酸),dictyostatin,圆皮海绵内酯,软珊瑚醇,埃博霉素,乙胺丁醇,依托泊苷,法罗培南,夫西地酸,呋喃唑酮,异烟肼,laulimalide,甲硝唑,莫匹罗星,nam合成抑制剂(例如磷霉素),呋喃妥因,紫杉醇,普兰西霉素,吡嗪酰胺,奎奴普丁/达福普汀,利福平,他唑巴坦替硝唑,乌菊花素; 4)抗病毒药物:a)侵入/融合抑制剂:阿帕韦洛,马拉韦罗,vicriviroc,gp41(恩夫韦肽),pro140,cd4(艾巴利珠单抗);b)整合酶抑制剂:雷特格韦,elvite-gravir,globoidnana;c)成熟抑制剂:bevirimat,vivecon;d)神经氨酸酶抑制剂:奥司他韦,扎那米韦,帕拉米韦;e)核苷和核苷酸:阿巴卡韦,阿昔单韦,阿德福韦,阿莫西韦,阿昔单抗,溴夫定,西多福韦,克拉夫定,地塞米松,去羟肌苷(ddi),elvucitabine,恩曲他滨(ftc),恩替卡韦,泛昔洛韦,氟拉西林(5-fu),3’-氟取代的2’,3’-脱氧核苷类似物,如3’-氟-2’,3’-双脱氧胸苷(flt)和3’-氟-2’,3’-双脱氧鸟苷(flg),福米韦生,9-鸟嘌呤,碘苷,拉米夫定(3tc),1-核苷(例如β-1-胸苷和β-1-2′-脱氧胞苷),喷昔洛韦,racivir,利巴韦林,迪替丁,司他夫定(d4t),塔利巴韦林(viramidine),替比夫定,替诺福韦,三氟尿苷伐昔洛韦,缬更昔洛韦,扎西他滨(ddc),齐多夫定(azt);f)非核苷类:金刚烷胺,阿替吡啶,卡普韦林,二芳基嘧啶(依曲韦林,rilpivirine),地拉夫定,二十二烷醇,乙米韦林,依法韦仑,膦甲酸(磷酰基甲酸),咪喹莫特,聚乙二醇干扰素,洛韦胺,洛德腺苷,甲吲噻腙,奈韦拉平,nov-205,长效干扰素α,鬼臼毒素,利福平,金刚乙胺,瑞喹莫德(r-848),醋胺金刚烷;g)蛋白酶抑制剂:安普那韦,阿扎那韦,boceprevir,darunavir,福萨那韦,印地那韦,洛匹那韦,奈非那韦,普来可那立,利托那韦,沙奎那韦,telaprevir(vx-950),替拉那韦;h)其它类型的抗病毒药物:抗体酶,阿比朵尔,calanolidea,ceragenin,氰维林-n,二芳基嘧啶,表没食子儿茶素没食子酸酯(egcg),膦甲酸,格里菲辛,taribavirin(viramidine),羟基脲,kp-1461,米替福新,普来可那立,混成抑制剂,利巴韦林,seliciclib; 5)双链接连接子偶联的药物还包括放射性同位素。放射性同位素(放射性核素)的实例有3h,11c,14c,18f,32p,35s,64cu,68ga,86y,99tc,111in,123i,124i,125i,131i,133xe,177lu,211at或213bi。放射性同位素标记的抗体可用于受体靶向成像实验,或者可用于如本发明的抗体-药物偶联物的靶向治疗(wuetalnaturebiotechnology2005,23(9)1137-1146)。细胞结合分子,例如抗体可以通过本专利的连接子连结配体试剂,进行标记。配体可以用文献(currentprotocolsinimmunology,volumes1和2,coligenetal,ed.wiley-interscience,newyork,n.y.pubs.(1991))所述的方法与放射性金属结合、螯合或生成复合物。可以络合金属离子的螯合配体包括dota,dotp,dotma,dtpa和teta(macrocyclics,dallas,tx)等 6)上述任何药物的药学上可接受的盐,酸或其衍生物,水合物或水合盐;或晶体结构;或任何上述药物的旋光异构体,外消旋物,非对映异构体或对映异构体。 在另一个实施例中,结构式(i)和(ii)中的药物/细胞毒性剂可以是发色分子,得到的偶联物可用于检测,监测或研究细胞结合分子与靶细胞的相互作用。发色分子可以吸收一种光,如紫外光,荧光,红外光,近红外光或可见光;发色分子包括黄色素,红细胞,虹彩色素,白细胞,黑色素和蓝绿色素的一类或一个亚类,荧光分子(吸收光后再发光的荧光化学物质)的一类或一个亚类,视觉光转导分子的一类或一个亚类,光子分子的一类或一个亚类,冷光分子的一类或一个亚类和荧光素化合物的一类或一个亚类。 发色分子可选自,但不限于,非蛋白质有机荧光团,例如氧杂蒽衍生物(荧光素,罗丹明,俄勒冈绿,伊红和德克萨斯红);花青衍生物(花青,吲哚羰花青,氧杂花青,硫代花青和部花青);方酸衍生物和环取代的方酸,包括seta,setau和square染料;萘衍生物(丹酰和氟硅酸钠衍生物);香豆素衍生物;恶二唑衍生物(吡啶基恶唑,硝基苯并恶唑和苯并恶二唑);蒽衍生物(蒽醌类,包括draq5,draq7和cytrak橙);芘衍生物(级联蓝等);恶嗪衍生物(尼罗红,尼罗蓝,甲酚紫,恶嗪170等);吖啶衍生物(黄醇黄素,吖啶橙,吖啶黄等);芳基甲胺衍生物(金胺,结晶紫,孔雀石绿)和四吡咯衍生物(卟吩,酞菁,胆红素)。 生色分子选自以下荧光化合物的任何类似物和衍生物:cf染料(biotium),draq和cytrak探针(bios-tatus),bodipy(invitrogen),alexafluor(invitrogen),dylightfluor(thermoscientific,pierce),atto和tracy(sigmaaldrich),fluoprobes(interchim),abberior染料(abberior),dy和megastokes染料(dyomics),sulfocy染料(cyandye),hilytefluor(anaspec),seta,setau和square染料(biosearchtechnologies),surelight染料(apc,rpepercp,phycobilisomes)(columbiabiosciences),apc,apcxl,rpe,bpe(phyco-biotech)。 广泛使用的可与本发明连接子反应或偶联的荧光化合物的实例有:别藻蓝蛋白(apc),氨基胭脂蛋白,apc-cy7偶联物,bodipy-fl,cascadeblue,cy2,cy3,cy3.5,cy3b,cy5,cy5.5,cy7,荧光素,fluorx,羟基香豆素,丽丝胺罗丹明b,萤光黄,me-甲氧基香豆素,nbd,pacificblue,pacificorange,pe-cy5偶联物,pe-r-藻红蛋白(pe),red613,seta-555-叠氮化物,seta-555-dbco,seta-555-nhs,seta-580-nhs,seta-680-nhs,seta-apc-780,seta-percp-680,seta-r-pe-670,setau-380-nhs,setau-405-马来酰亚胺,setau-405-nhs,setau-425-nhs,setau-647-nhs,texasred,tritc,trured,x-rhodamine。 可以与本发明的连接子相连,用于研究核酸或蛋白质的荧光化合物,选自下列化合物或其衍生物:7-aad(7-氨基放线菌素d,cg-选择性的),吖啶橙,色霉素a3,cytrak橙(biostatus),dapi,draq5,draq7,溴化乙锭,hoechst33258,hoechst33342,lds751,光辉霉素,碘化丙啶(pi),sytox蓝,sytox绿,sytox橙,噻唑橙,to-pro,菁染料单体,toto-1,to-pro-1,toto-3,to-pro-3,yoseta-1,yoyo-1。可以与本发明的连接子相连,用于研究细胞的荧光化合物,选自下列化合物或其衍生物:dcfh(2’,7′-二氯二氢荧光素,氧化形式),dhr(二氢罗丹明123,氧化形式,光催化氧化),fluo-3(am酯,ph>6),fluo-4(am酯,ph7.2),indo-1(am酯,低/高钙(ca2+)),snarf(ph6/9)。优选的荧光化合物选自:别藻蓝蛋白(apc),amcyan1(四聚体,clontech),asred2(四聚体,clontech),蓟绿(单体,mbl),azurite,b-藻红蛋白(bpe),cerulean,cypet,dsred单体(clontech),dsred2(“rfp”,clontech),ebfp,ebfp2,ecfp,egfp(弱二聚体,clontech),emerald(弱二聚体,invitrogen),eyfp(弱二聚体,clontech),gfp(s65a突变),gfp(s65c突变),gfp(s65l突变),gfp(y66h突变),gfp(y66w突变),gfpuv,hcred1,j-red,katusha,kusabiraorange(单聚体,mbl),mcfp,mcherry(单体,mbl),mkate(tagfp635,单体,evrogen),mkeima-red(单体,mbl),mko,morange,mplum,mraspberry,mrfp1(单体,tsien实验室),mstrawberry,mtfp1,mturquoise2,p3(藻胆体复合物),多甲藻黄素-叶绿素-蛋白质复合物(percp),r-phycoerythrin(rpe),t-sapphire,tagcfp(二聚体,evrogen),taggfp(二聚体,evrogen),tagrfp(二聚体,evrogen),tagyfp(二聚体,evrogen),tdtomato(串联二聚体),topaz,turbofp602(二聚体,evrogen),turbofpp635(二聚体,evrogen),turbogfp(二聚体,evrogen),turborfp(二聚体,evrogen),turboyfp(二聚体,evrogen),venus,野生型gfp型,ypet,zsgreen1(四聚体,clontech),zsyellow1(四聚体,clontech)。 通过双链连接子连接的抗体-发色团分子的偶联物的结构的实例如下:ac01,ac02,ac03,ac04,ac05,ac06和ac07,ac08,ac09,ac010和ac11: ac10(ir800cw偶联物)、 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、n的定义与前文相同;r12和r12’独立地为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、o(ch2ch2o)pch2ch2nhso3h、nh(ch2ch2o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh-ar-cooh、nh-ar-nh2,其中p=0-5000,aa是氨基酸,(aa)n包含了相同或不同的天然或非天然氨基酸,n=1-30。 在另一个实施方案中,结构式(i),(ii),(iii)和(iv)中的药物可以是聚亚烷基二醇,哺乳动物给药时,用于延长细胞结合分子的半衰期。聚亚烷基二醇包括但不限于聚乙二醇(peg),聚丙二醇以及环氧乙烷和环氧丙烷的共聚物;优选的是peg,更优选的是单官能活化的羟基peg(例如,单个末端活化的羟基peg,包括羟基peg-活性酯,羟基peg-单醛,羟基peg-单胺,羟基peg-单酰肼,羟基peg-单肼基甲酸酯,羟基peg-单碘乙酰胺,羟基peg-单马来酰亚胺,羟基peg-邻二硫吡啶,羟基peg-单肟,羟基peg-单苯基碳酸酯,羟基peg-单苯基乙二醛,羟基peg-单噻唑烷-2-硫酮,羟基peg-单硫代酯,羟基peg-单巯基,羟基peg-单三嗪和羟基peg-单乙烯基砜)。 在某些实施例中,聚亚烷基二醇分子量为约10da至约200kda,优选约88da至约40kda的分子量;具有两个分支,每个分支分子量为约88da至约50kda;更优选的具有两个分支,每个分支约88da至约20kda。在一个具体实施例中,聚亚烷基二醇是聚乙二醇,分子量为约10kda,20kda,或40kda。在具体的实施例中,peg是直链或支链10kdapeg,直链或支链20kdapeg或直链或支链40kdapeg。许多美国专利公开了直链或支链“非抗原性”peg聚合物及其衍生物或偶联物的制备,见美国专利号;;;;;;;;;;;;;;;;;;;;;;;;和。通过桥连接子连接的抗体-聚亚烷基二醇偶联物的结构如pg01,pg02和pg03: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义与前文相同;优选地y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;p为1-5000;r1和r3与上述r1定义相同,且优选地r1和r3为独立地h、oh、och3、ch3、或oc2h5。 在另一个实施方案中,优选的通过本专利的连接子连接至细胞结合分子的细胞毒剂是tubulysin,美登素,紫杉烷类,cc-1065类似物,柔红霉素和多柔比星化合物,毒伞肽(包括鹅膏毒素),indolecarboxamide,苯并二氮卓二聚体(例如吡咯并苯二氮杂卓(pbd),托美霉素,氨茴霉素,吲哚并苯并二氮,咪唑并苯并噻二氮杂卓或恶唑烷并苯并二氮杂卓的二聚体),加利车霉素类和烯二炔类抗生素,放线菌素,氮丝菌素,博来霉素,表柔比星,他莫昔芬,伊达比星,多拉司汀,澳瑞斯汀(例如mmae,mmaf,澳瑞斯汀pye,澳瑞斯汀tp,澳瑞斯汀2-aq,6-aq,eb(aeb),efp(aefp)和它们的同系物),多卡霉素,格尔德霉素或其它的hsp90抑制剂,centanacycin,甲氨喋呤,噻替派,长春地辛,长春新碱,erbulins,,半米塔林,nazumamides,微晶蛋白,放射敏素,streptonigtin,sn38或其它喜树碱类似物或降解物,alterobactin,microsclerodermins,theonellamides,esperamicin,pnu-及其类似物和衍生物,药学上可接受的盐,酸,衍生物,水合物或水合盐;或晶体结构;或任何上述药物的旋光异构体,外消旋物,非对映异构体或对映异构体。 tubulysin是优选的用于本发明偶联物的细胞毒性剂,其为本领域公知,并可以根据已知方法从天然来源分离或者根据已知方法合成制备,如balasubramanian,r.等,j.med.chem.2009,52,238–240;wipf,p.等,org.lett.2004,6,4057–4060;pando,o.等,j.am.chem.soc.2011,133,7692–7695;reddy,j.a.等,mol.pharmaceutics,2009,6,1518–1525;raghavan,b.等,j.med.chem.2008,51,1530–1533;patterson,a.w.等,j.org.chem.2008,73,4362–4369;pando,o.等,org.lett.2009,11(24),pp5567–5569;wipf,p.等,org.lett.2007,9(8),1605–1607;friestad,g.k.org.lett.2004,6,pp3249–3252;hillarym.peltier,h.m.等,j.am.chem.soc.2006,128,16018–16019;chandrasekhars.等,j.org.chem.2009,74,9531–9534;liu,y.等,mol.pharmaceutics,2012,9,168–175;friestad,g.k.等,org.lett.2009,11,1095–1098;kubicek,k.等,angew.chem.int.ed.eng.,2010.49,4809-12;chai,y.等,chembiol,2010,17296-309;ullrich,a.等,angew.chem.int.ed.eng.,2009,48,4422-5;sani,m.等,angew.chem.int.ed.eng.,2007,46,3526-9;domling,a.等,angew.chem.int.ed.eng.,2006.45,7235-9;zanda,m.等,加拿大专利ca(2011);chai,y.等,欧盟专利(2010),pctwo;leamon,c.等,pctwo,wo;ellman,j.等,pctwo,pctwo,美国专利,;matschiner,g.等,pctwo;vlahov,i.等,pctwo,wo;low,p.等,pctwo;richter,w.pctwo;kjems,j.等,pctwo;davis,m.等,pctwo;diener,j.等,美国专利申请,wo;matschiner,g.等,pctwo;vaghefi,f.等,pctwo;doemling,a.德国专利7,pctwo,wo,wo;stanton,m.等,美国专利申请;hoefle,g.等,德国专利,,;leung,d.等,wo;reichenbach,h.等,德国专利;wolfgang,r.美国专利;chen,h.美国专利申请。在专利申请pct/ib2012/053554中描述了优选的与细胞结合分子偶联的tubulysin的结构。 通过双链连接子连接的抗体-tubulysin偶联物的例子如t01、t02、t03、t04、t05、t06、t07、t08、t09、t10、t11、t12、t13、t14、t15、t16t017、t18、t19、t20、t21、t22及t23: t01, 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、和n的定义如前文所述;优选地y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;mab为抗体,优选地为单克隆抗体;r12为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、nhoh、nhor1、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nhso3h、nh(ch2ch2o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh(ch2ch2nh)pch2ch2nh2、nh(ch2ch2s)pch2ch2nh2、nh(ch2ch2nh)pch2ch2oh、nh(ch2ch2s)pch2ch2oh、nh-r1-nh2、或nh(ch2ch2o)pch2ch2nhpo3h2、其中aa为1-8个氨基酸;n为1-20;p为1-5000;r1、r1’、r2、r3、r4和r5独立地为h、c1-c8直链或支链烷基、酰胺或胺;c2-c8芳基、烯基、炔基、杂芳基、杂烷基、烷基环烷基、酯、醚、杂环烷基或酰氧基胺;或含有1-8个氨基酸的肽或(och2ch2)p或(och2ch(ch3))p、其中p是1到约5000的整数;两个r:r1r2、r2r3、r1r3或r3r4可以形成烷基、芳基、杂芳基、杂烷基或烷基环烷基的3~8环状;x3是h、ch3、ch2ch3、c3h7或x1’r1’,其中x1’是nh、n(ch3)、nhnhnh、o或s;r1’为h或c1-c8直链或支链烷基、芳基、杂芳基、杂烷基、烷基环烷基或酰氧基胺;r3’为h或c1-c6直链或支链烷基;z3为h、coor1、nh2、nhr1、or1、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1、o-糖苷(葡萄糖苷、半乳糖苷、甘露糖苷、葡萄糖醛酸苷/葡糖苷酸、阿洛糖苷、果糖苷等)、nh糖苷、s-糖苷或ch2糖苷;m1和m2独立地是h、na、k、ca、mg、nh4或nr1r2r3。 加利车霉素及其相关的烯二炔抗生素为本发明的细胞结合分子-药物偶联物中优选的细胞毒性分子,可参考文献:nicolaou,k.c.等,science1992,256,1172-1178;proc.natl.acad.sci.usa.1993,90,5881-8;美国专利,,,,,,,,,,,,,,,。通过双连接子连接的抗体-加利车霉素类似物的偶联物的实例如下所示: c01. c02 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;q优选地为单克隆抗体。 优选用于本发明的美登木素生物碱包括美登醇及其类似物,可参考美国专利:、、、、、、、、、、、、、、、、、、、、、、、、、、、、和。通过本专利连接子连接的抗体-美登木素生物碱偶联物的结构实例如下:my01、my02、my03、my04、my05、my06、my07和my08: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文;优选地x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;q优选地为单克隆抗体。 紫杉烷,包括紫杉醇(一种细胞毒性天然产物)和多西紫杉醇(一种半合成衍生物)及其类似物,是本发明优选的细胞毒性分子,在如下文献中有描述:kc.nicolaou等,j.am.chem.soc.117,2409-20,(1995);ojima等,j.med.chem.39:3889-3896(1996);40:267-78(1997);45,5620-3(2002);ojima等,proc.natl.acad.sci.96:4256-61(1999);kim等,bull.koreanchem.soc.20,1389-90(1999);miller等,j.med.chem.47,4802-5(2004);美国专利:,,,,,,6.,,,,,,,,和。 经本发明的连接子连接的抗体-紫杉烷偶联物的实例如tx01、tx02和tx03: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义同前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;优选地,q为单克隆抗体。 cc-1065类似物和多卡霉素类似物也是与本发明的双键连接子连接的优选细胞毒性剂。cc-1065类似物和多卡霉素类似物的实例及其合成可见于:warpehoski等,j.med.chem.31:(1988);d.boger等,j.org.chem66,6654-61,2001;美国专利:、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、,、、、和。由本发明的连接子连接的抗体-cc1065类似物偶联物的结构实例如cc01、cc02、cc03、cc04、cc05、cc06和cc07: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;q优选地为单克隆抗体;z3是h、po(om1)(om2)、so3m1、ch2po(om1)(om2)、ch3n(ch2ch2)2nc(o)-、o(ch2ch2)2nc(o)-、r1或糖苷。 柔红霉素/多柔比星同系物也是优选的,与本发明中的双链连接子连接的细胞毒性剂。其结构及合成可参考:hurwitz,e.等,cancerres.35,1175-81(1975);yang,h.m.reisfeld,r.a.proc.natl.acad.sci.85,1189-93(1988);pietersz,c.a.e.等,cancerres.48,926-311(1988);trouet等,79,626-29(1982);z.brich等,j.controlledrelease,19,245-58(1992);chen等,syn.comm.33,2377-90,2003;king等,bioconj.chem.10,279-88,1999;king等,j.med.chem.45,4336-43,2002;kratz等,jmedchem.45,5523-33,2002;kratz等,biol.pharm.bull.jan.21,56-61,1998;lau等,bioorg.med.chem.3,1305-12,1995;scott等,bioorg.med.chem.lett.6,1491-6,1996;watanabe等,tokaij.experimentalclin.med.15,327-34,1990;zhou等,j.am.chem.soc.126,15656-7,2004;wo01/38318;美国专利:;;;;;;;;;;;。 通过本发明的连接子的链接的抗体-cc-1065类似物的偶联物的结构如下da01、da02、da03、da04、da05、da06、da07、da08、da09、da10和da11: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义如前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;r12为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、nhoh、nhor1、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nh-so3h、nh(ch2ch2o)pch2ch2nh-so3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2-ch2nhpo3h2、nh(ch2ch2o)pch2-ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh(ch2ch2nh)pch2-ch2nh2、nh(ch2ch2s)pch2ch2nh2、nh(ch2ch2nh)pch2ch2oh、nh(ch2ch2s)pch2-ch2oh、nh-r1-nh2、或nh(ch2ch2o)pch2ch2nhpo3h2、其中aa是1-8个氨基酸;p是1-5000;q是抗体,优选地为单克隆抗体。 澳瑞斯汀和多拉司汀是优选的和双链连接子连接的细胞毒性剂。澳瑞斯汀,如澳瑞斯汀e(ae),澳瑞斯汀eb(aeb),澳瑞斯汀efp(aefp),单甲基澳瑞斯汀e(mmae),单甲基澳瑞斯汀f(mmaf),澳瑞斯汀f苯二胺(afp)和mmae的苯丙氨酸变体,是多拉司汀的同系物,在如下文献中有描述:int.j.oncol.15367-72(1999);molecularcancertherapeutics,vol.3,no.8,pp.921-32(2004);美国专利申请:、、,美国专利:、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、。 抗体-澳瑞斯汀通过本发明的连接子连接的偶联物的实例如au01、au02、au03、au04、au05、au06、au07、au08、au09、au10、au11、au12、au13、au14、au15、au16、au17、au18、au19、au20、au21、au22、au23、au24、au25、au26和au27: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义同前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;r12是oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、nhoh、nhor1、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nh-so3h、nh(ch2ch2o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2-ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh(ch2ch2nh)pch2-ch2nh2、nh(ch2ch2s)pch2ch2nh2、nh(ch2ch2nh)pch2ch2oh、nh(ch2ch2s)pch2-ch2oh、nh-r1-nh2或nh(ch2ch2o)pch2ch2nhpo3h2,其中aa为1-8个氨基酸;p为1-5000;q优选为单克隆抗体;r1、r2、r3、r4和r5独立地为h,c1-c8直链或支链烷基,芳基,杂芳基,杂烷基,烷基环烷基,酯,醚,酰胺,胺,杂环烷基或酰氧基胺;或含有1-8个氨基酸的肽,或具有式(och2ch2)p或(och2ch(ch3))p的聚乙烯基氧单,其中p是1至约5000的整数。两个r:r1r2,r2r3,r1r3或r3r4可形成烷基,芳基,杂芳基,杂烷基或烷基环烷基的3~8个成员环;x3为h,ch3或x1’r1’,其中x1’为nh,n(ch3),nhnh,o或s,r1’是h或c1-c8直链或支链烷基,芳基,杂芳基,杂烷基,烷基环烷基,酰氧基胺;r3’是h或c1-c6直链或支链烷基;z3’是h、coor1、nh2、nhr1、or1、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1,r1,或o-糖苷(葡糖苷,半乳糖苷,甘露糖苷,葡糖苷酸/葡糖苷酸,阿洛糖苷,果糖苷等),nh糖苷,s-糖苷或ch2糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 苯并二氮卓二聚体(例如吡咯并苯并二氮卓(pbd)或托霉素的二聚体,吲哚并苯并二氮卓,咪唑并苯并噻吩并二氮卓也是本发明优选的细胞毒性剂,其在本领域中的实例如:美国专利,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,美国专利申请,,。以双链连接子连接的抗体-苯并二氮杂卓二聚体偶联物的实例如:pb01、pb02、pb03、pb04、pb05、pb06、pb07、pb08、pb09、pb10、pb11、pb12、pb13、pb14、pb15、pb16、pb17、pb18、pb19、pb20、pb21、pb22、pb23、pb24、pb25、pb26、pb27、pb28、pb29、pb30、pb31和pb32。 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;r1、r2、r3、r1’、r2’和r3’独立地为h,f,cl,=o,=s,oh,sh,c1-c8直链或支链烷基、芳基、烯基、杂芳基、杂烷基、烷基环烷基、酯(coor5or–oc(o)r5)、醚(or5),酰胺(conr5),氨基甲酸酯(oconr5),胺(nhr5,nr5r5′),杂环烷基或酰氧基胺(-c(o)nhoh,-onhc(o)r5),含20种天然或非天然氨基酸的多肽,或如式(och2ch2)p或(och2ch(ch3))p的聚乙烯氧基单,其中p是1至约5000的整数。两个r:r1r2,r2r3,r1r3,r1’r2’,r2’r3’或r1’r3’可独立形成烷基,芳基,杂芳基,杂烷基或烷基环烷基的3~8个环;x3和y3独立地为n,nh,ch2或cr5,其中r5,r6,r12和r12’独立地为h,oh,nh2,nh(ch3),nhnh2,cooh,sh,oz3,sz3,f,cl,或c1-c8直链或支链烷基,芳基,杂芳基,杂烷基,烷基环烷基,酰氧基胺;z3为h,op(o)(om1)(om2),och2op(o)(om1)(om2),oso3m1或o-糖苷(葡萄糖苷,半乳糖苷,甘露糖苷,葡糖苷酸/葡糖苷酸,阿洛糖苷,果糖等),nh-糖苷,s-糖苷或ch2-糖苷;m1和m2独立地为h,na,k,ca,mg,nh4,nr1r2r3。 鹅膏毒肽包括至少有十种有毒化合物,它们最初在几个有毒蘑菇属中被发现,尤其是伞形毒菌和其他几个蘑菇种类。鹅膏毒肽也是优选的通过本发明连接子链接的细胞毒性分子。目前,十种已知的鹅膏毒肽,α-鹅膏蕈碱,β-鹅膏蕈碱,γ-鹅膏蕈碱,ε-鹅膏蕈碱,鹅膏无毒环肽,一羟基鹅膏毒肽羧酸,鹅膏毒肽酰胺,三羟基鹅膏毒肽和鹅膏毒肽酰胺原均是双环多肽,在合成时经历了一个35个氨基酸的前蛋白,而后被脯氨酰寡肽酶切断,得到最终的八个氨基酸肽(litten,w.scientificamerican1975,232(3)90–101;h.e.hallen等,proc.nat.aca.sci.usa2007,104,19097–101;k.baumann等biochemistry1993,32(15)4043–50;karlson-stiberc,perssonh.toxicon2003,42(4)339–49;horgen,p.a.等,arch.microbio.1978,118(3):317-9)。鹅膏毒肽通过抑制rna聚合酶ii(polii),阻断基因转录和蛋白质生物合成,来杀死细胞(brodner,o.g.和wieland,t.biochemistry1976,15(16)3480–4;fiume,l.,currproblclinbiochem,1977,723-8;karlson-stiberc,perssonh.toxicon2003,42(4)339–49;chafin,d.r.,guo,h.和price,d.h.,j.biol.chem.1995,270(32)19114–19;wieland,int.j.pept.proteinres.1983,22(3)257-76)。鹅膏毒肽可以从采集的伞形毒菌蘑菇中分离得到(yocum,r.r.biochemistry1978,17(18)3786-9;zhang,p.等femsmicrobiol.lett.2005,252(2),223-8),或用担子菌发酵(muraoka,s.和shinozawat.,j.bioscibioeng.2000,89(1)73-6,美国专利)或a.fissa进行发酵获得,或通过培养簇生盔孢菌或黄褐盔孢菌产生(wo/1990/009799,日本专利)。然而,些分离和发酵的产量非常低(低于5mg/l培养物)。在过去的三十年中,有文献报道了鹅膏毒肽及其类似物的几种合成方法(w.e.savige,a.fontana,chem.commun.1976,600–1;zanotti,g.等,int.j.pept.proteinres.,1981.18(2)162-8;wieland,t.等,eur.j.biochem.1981,117,161–4;p.a.bartlett等,tetrahedronlett.1982,23,619–22;zanotti,g.等,biochimbiophysacta,1986.870(3)454-62;zanotti,g.等,int.j.peptideproteinres.1987,30,323–9;zanotti,g.等,int.j.peptideproteinres.1987,30,450–9;zanotti,g.等,int.j.pept.proteinres,1988.32(1)9-20;g.zanotti,t.等,int.j.peptideproteinres.1989,34,222–8;zanotti,g.等,int.j.pept.proteinres.,1990.35(3)263-70;mullersman,j.e.和j.f.preston,3rd,int.j.pept.proteinres.,1991.37(6)544-51;mullersman,j.e.等,int.j.pept.proteinres.,1991.38(5)409-16;zanotti,g.等,int.j.pept.proteinres.,1992.40(6)551-8;schmitt,w.等,j.am.chem.soc.1996,118,4380–7;anderson,m.o.等,j.org.chem.,2005,70(12)4578-84;j.p.may等,j.org.chem.2005,70,8424–30;f.brueckner,p.cramer,nat.struct.mol.biol.2008,15,811–8;j.p.may,d.m.perrin,chem.eur.j.2008,14,3404–9;j.p.may等,chem.eur.j.2008,14,3410–17;q.wang等,eur.j.org.chem.2002,834–9;may,j.p.和d.m.perrin,biopolymers,2007,88(5)714-24;may,j.p.等,chemistry,2008.14(11)3410-7;s.delamomarin等,eur.j.org.chem.2010,3985–9;pousse,g.等,org.lett.,2010.12(16)3582-5;luo,h.等,chem.biol.,2014.21(12)1610-7;zhao,l.等,chembiochem,2015.16(10)1420-5),其中大部分是通过部分合成实现的。由于其极高的效力和独特的细胞毒性机制,鹅膏毒肽已被用作偶联物的有效载荷(fiume,l.,lancet,1969.2(7625)853-4;barbanti-brodano,g.和l.fiume,natnewbiol,1973.243(130)281-3;bonetti,e.,m.等,archtoxicol,1976.35(1)p.69-73;davis,m.t.,preston,j.f.science1981,213,1385–1388;preston,j.f.等,archbiochembiophys,1981.209(1)63-71;h.faulstich等,biochemistry1981,20,6498–504;barak,l.s.等,procnatlacadsciusa,1981.78(5)3034-8;faulstich,h.和l.fiume,methodsenzymol,1985.-37;zhelev,z.,a.等,toxicon,1987.25(9)981-7;khalacheva,k.等,ekspmedmorfol,1990.29(3)26-30;u.bermbach,h.faulstich,biochemistry1990,29,6839–45;mullersman,j.e.和j.f.preston,int.j.peptideproteinres.1991,37,544–51;mullersman,j.e.和j.f.preston,biochemcellbiol,1991.69(7)418-27;j.anderl,h.echner,h.faulstich,beilsteinj.org.chem.2012,8,2072–84;moldenhauer,g.等,j.natl.cancerinst.2012,104,622–34;a.moshnikova等,biochemistry2013,52,1171–8;zhao,l.等,chembiochem,2015.16(10)1420-5;zhou,b.等,biosensbioelectron,2015.68189-96;wo2014/043403,us,ep)。我们也一直在研究鹅膏毒肽的偶联。通过双链连接子连接的抗体—鹅膏毒肽偶联物的实例如am01、am02、am03、am04、am05、am06、am07、am08和am09的结构: 其中x1、x2、q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh,nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、chc(o)nh-nhc(o)、c(o)nr1或缺省;r7、r8和r9独立地为h、oh、or1、nh2、nhr1、c1-c6烷基或缺省;y2为o、o2、nr1、nh或缺省;r10是ch2、o、nh、nr1,nhc(o)、nhc(o)nh、nhc(o)o、oc(o)o、c(o)、oc(o)、oc(o)(nr1)、(nr1)c(o)(nr1)、c(o)r1或缺省;r11为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2-ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nhso3h、nh(ch2ch2-o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2c-h2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、或nh(ch2ch2o)pch2ch2nhpo3h2其中aa为1-20个氨基酸;n和m1独立地为1-30;p为1-5000;z3为h、oh、coor1、nh2、nhr1、or1、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1或o-糖苷(葡萄糖苷,半乳糖苷,甘露糖苷,葡糖苷/葡糖苷酸,阿洛糖苷,果糖苷等)nh糖苷、s-糖苷或ch2-糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 喜树碱(cpts)及其衍生物sn-38,拓扑替康,伊立替康(cpt-11),西利替康(db-67,ar-67),科西特康(bnp-1350),etirinotecan,exatecan,lurtotecan,gimatecan(st1481),贝洛替康(ckd-602),鲁比替康(rubitcan)和其他拓扑异构酶抑制剂,可阻止dna重新连接,因此引起dna损伤并导致细胞凋亡。迄今为止,已有拓扑替康,伊立替康这两种cpt类似物获批用于癌症化疗(palakurthi,s.,expertopindrugdeliv.2015;12(12):1911-21;在临床试验中,sn-38和exatecan还被用作adc偶联物的有效荷载(ocean,a.j.,cancer.2017,123(19):3843-3854;starodub,a.n.等,clincancerres.2015,21(17):3870-8;cardillo,t.m.等,bioconjugchem.2015,26(5):919-31;ogitani,y.等,bioorgmedchemlett.2016,26(20):5069-5072;takegawa,n.等,intjcancer.2017oct15;141(8):1682-1689;美国专利,,,;美国专利申请,,,)。 通过桥连接子连接的抗体-喜树碱类似物的偶联物的实例优选为cp01、cp02、cp03、cp04、cp05和cp06: 其中q、x1,x2,y1、y2、r1,r2,r3,r4,r5,r5’,z1、z2,和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)、c(o)nr1或缺省;z3为h、oh、coor1、nh2、nhr1、or1、ch3、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1、或o-糖苷(葡萄糖苷、半乳糖苷、甘露糖苷、葡糖醛酸苷/葡糖醛酸苷、阿洛糖苷、果糖苷等)、nh-糖苷、s-糖苷或ch2-糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 艾日布林主要与微管正电荷端的少数高亲和位点结合,具有细胞毒性和非细胞毒性作用机制。它的细胞毒性作用与其抗有丝分裂活性有关,在长期且不可逆的有丝分裂阻断后诱导了癌细胞的凋亡(kuznetsov,g.等,cancerresearch.2004,64(16):5760-6;towle,m.j.等,cancerresearch。2010,71(2):496-505)。除了基于细胞毒性、抗有丝分裂的机制外,在人类乳腺癌模型中的临床前研究还表明,艾日布林还对存活的癌细胞和残余肿瘤的生物学功能产生复杂影响,而这些似乎与它的抗有丝分裂作用无关。艾日布林已被美国fda批准用于治疗转移性乳腺癌,病人已接受至少两种针对晚期乳腺癌的前期化疗方案,包括基于蒽环类和紫杉烷类的化疗,以及用于治疗不能通过手术去除(无法切除)或已进展(转移)的脂肪肉瘤(一种软组织肉瘤)。艾日布林也已被用作adc偶联物的有效荷载(us)。通过双链连接子连接抗体-艾日布林偶联物的结构优选为以下eb01和eb02: 其中q、x1、x2、y1、r1、r2、r3、r4、r5、r5’、z1、z2、和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)、c(o)nr1或缺省。 烟酰胺磷酸核糖基转移酶(nampt)抑制剂也是adc有效荷载,因为它们具有独特的高活性的机制(sampathd等,pharmacolther2015;151,16-31)。nampt调节细胞中烟酰胺腺嘌呤二核苷酸(nad)的水平,而nad是维持能量和组成代谢的重要氧化还原辅助因子。nad在新陈代谢中具有几个重要作用。它在氧化还原反应中充当辅酶,在adp-核糖基化反应中作为adp-核糖部分的供体,作为第二信使分子环状adp-核糖的前体,并作为细菌dna连接酶的底物,一类被称为sirtuins的酶使用nad+去除蛋白质中乙酰基。除了这些代谢功能外,nad+还是可以自发地或通过调节机制从细胞中释放出腺嘌呤核苷酸(smythl.m.等,j.biol.chem.2004,279(47),48893–903;billingtonr.a.等,molmed.2006,12,324–7),因此具有重要的细胞外功能(billingtonr.a.等,molmed.2006,12,324–7)。当存在nampt抑制剂时,nad的水平降至代谢所需的水平以下,从而产生能量危机并因此导致细胞死亡。到目前为止,nampt抑制剂候选药物fk-866,chs-828和gmx-1777已经进入临床试验,但每种药物在产生任何客观缓解之前都遇到了剂量限制性毒性(holenk.等,investnewdrugs2008,26,45-51;hovstadiusp.等,clincancerres2002,8,2843-50;pishvaianm.j.等,jclinoncol2009,27,3581)。因此,使用adc靶向递送nampt抑制剂可能会避免系统毒性,从而获得更大的治疗益处。双链连接子链接的抗体-nampt抑制剂偶联物的结构优选为式np01,np02,np03,np04,np05,np06,np07,np08和np09: 其中q、x1、x2、y1、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;x5为f、cl、br、i、oh、or1、r1、opo3h2、oso3h、nhr1、ocor1、nhcor1;优选地,x1、x2、y1和y2为独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)、c(o)nr1或缺省。 在另外的实施例中,可以将免疫毒素通过双链连接子链接至细胞结合分子。免疫毒素是一种大分子药物,通常是由细菌或植物蛋白衍生的细胞毒性蛋白,如白喉毒素(dt)、霍乱毒素(ct)、天花粉蛋白(tcs)、石竹素、假单胞菌外毒素a(eta)、红原毒素、白喉毒素、ab毒素、iii型外毒素等,它也可能是一种剧毒的细菌成孔原毒素,需要蛋白水解激活。这种原毒素的一个例子是前溶氧素及其基因修饰的形式topalysin。topalysin是一种经修饰的重组蛋白,经过工程设计,可以被前列腺中的一种酶选择性激活,从而在不损伤邻近组织和神经的情况下导致局部细胞死亡和组织破坏。 在又一个实施方案中,细胞结合配体或细胞受体激动剂可以通过本专利的双链连接子偶联至细胞结合分子。这些偶联的细胞结合配体或细胞受体激动剂,特别是抗体-受体偶联物,不仅可以用作靶向导体/导向器以将偶联物递送至恶性细胞,而且还可以用于调节或共刺激期望的免疫应答或改变信号传导途径。 在免疫治疗中,细胞结合配体或受体激动剂优选与tcr(t细胞受体)t细胞的抗体偶联,或与car(嵌合抗原受体)t细胞或b细胞受体(bcr),自然杀伤(nk)细胞,或细胞毒性细胞的抗体偶联。这种抗体优选是抗cd3,cd4,cd8,cd16(fcγriii),cd27,cd40,cd40l,cd45ra,cd45ro,cd56,cd57,cd57bright,tnfβ,fas配体,mhci类分子(hla-a,b,c),或nkr-p1。细胞结合配体或受体激动剂选自但不限于:叶酸衍生物(结合叶酸受体,在卵巢癌和其他恶性肿瘤中过表达的蛋白质)(low,p.s.等,2008,acc.chem.res.41,120-9);谷氨酸尿素衍生物(与前列腺特异性膜抗原结合,前列腺癌细胞的表面标志物)(hillier,s.m.等,2009,cancerres.69,6932-40);生长抑素(也称为生长激素抑制激素(ghih)或生长激素释放抑制因子(srif))或生长激素释放抑制激素)及其类似物如奥曲肽(sandostatin)和兰瑞肽(somatuline)(特别用于神经内分泌肿瘤,gh产生性垂体腺瘤,副神经节瘤,无功能性垂体腺瘤,嗜铬细胞瘤)(ginj,m.等,2006,proc.natl.acad.sci.u.s.a.103,16436-41)。一般而言,生长抑素及其受体亚型(sst1,sst2,sst3,sst4和sst5)已在许多类型的肿瘤中被发现,如神经内分泌肿瘤,特别是在分泌gh的垂体腺瘤中(reubij.c.,landolta.m.,1984j.clin.endocrinolmetab–51;reubij.c.,landolta.m.,1987jclinendocrinolmetab6565–73;moysee.等,jclinendocrinolmetab6198–103)和胃肠胰腺肿瘤(reubij.c.等,1987jclinendocrinolmetab–34;reubij.c.等,1990cancerres50,5969–77),嗜铬细胞瘤(epel-baumj,等,1995jclinendocrinolmetab80:1837–44;reubij.c.等,1992jclinendocrinolmetab74,1082–9),成神经细胞瘤(prevostg,1996neuroendocrinology63:188–197;moertel,c.l.等,1994amjclinpath102:752–756),甲状腺髓样癌(reubi,j.c.,等,1991labinvest64:567–573)小细胞肺癌(sagmanu.等,1990cancer66:2129–2133),非神经内分泌肿瘤包括脑肿瘤如脑膜瘤,成神经管细胞瘤或神经胶质瘤(reubij.c.等,1986jclinendocrinolmetab63433–8;reubij.c.等,1987cancerres–64;fruhwald,m.c.等,1999pediatrres45697–708),乳腺癌(reubij.c.等,1990intjcancer46416–20;srkalovicg等,1990jclinendocrinolmetab70661–669),淋巴瘤(reubij.c.等,1992,intjcancer50895–900),肾细胞癌(reubij.c.等,1992,cancerres–6078),间叶组织肿瘤(reubij.c.等,1996cancerres–31),前列腺癌(reubij.c.等,1995,j.clin.endocrinolmetab–14;等,1989,prostate14:191–208;halmosg等,j.clin.endo-crinolmetab–71),卵巢癌(halmos,g.等,2000jclinendocrinolmetab–12;reubij.c.等,1991amjpathol138:1267–72),胃癌(reubij.c.等,1999,intjcancer81376–86;miller,g.v,1992brjcancer66391–95),肝细胞癌(kouroumalise.等,1998gut42442–7;reubij.c.等,1999gut4566–774)和鼻咽癌(lohk.s.等,2002virchowsarch–8);某些芳香磺酰胺类化合物,尤其是碳酸酐酶ix(缺氧和肾细胞癌标志物)(nerid.等,nat.rev.drugdiscov.2011,10,767-7);垂体腺苷酸环化酶激活肽(pacap)(pac1)用于嗜铬细胞瘤和副神经节瘤;血管活性肠肽(vip)及其受体亚型(vpac1,vpac2)用于肺癌,胃癌,结肠癌,直肠癌,乳腺癌,前列腺癌,胰腺导管癌,肝癌,膀胱癌和上皮肿瘤的癌症;各种肿瘤的α-黑素细胞刺激激素(α-msh)受体;胆囊收缩素(cck)/胃泌素受体及其受体亚型(cck1(以前称为cck-a)和cck2),用于小细胞肺癌,甲状腺髓样癌,星形细胞瘤,胰岛素瘤和卵巢癌;蛙皮素(pyr-gln-arg-leu-gly-asn-gln-trp-ala-val-gly-his-leu-met-nh2)/胃泌素释放肽(grp)及其受体亚型(bb1,grp受体亚型(bb2),bb3和bb4)用于肾细胞癌,乳腺癌,肺癌,胃癌和前列腺癌以及神经母细胞瘤(和神经母细胞瘤(ohlssonb.等,1999,scand.j.gastroenterology34(12)1224–9;weberh.c.2009,cur.opin.endocri.diab.obesity16(1)66–71,gonzalezn.等,2008,cur.opin.endocri.diab.obesity15(1),58-64);神经降压素受体及其受体亚型(ntr1,ntr2,ntr3),用于小细胞肺癌,成神经细胞瘤,胰腺癌,结肠癌和尤因肉瘤;物质p受体及其受体亚型(例如神经胶质肿瘤的nk1受体,hennigi.m.等,1995int.j.cancer61,786–792);神经肽y(npy)受体及其受体亚型(y1-y6)用于乳腺癌;归巢肽包括rgd(arg-gly-asp),ngr(asn-gly-arg),二聚和多聚环状rgd肽(例crgdfv)其识别肿瘤表面上的受体(整联蛋白)(laakkonenp.,vuorinenk.,2010,integrbiol(camb),2(7–8)326–337;chenk,chenx.,2011,theranostics.1:189–200;garangere.等,anti-canceragentsmedchem.7(5)552–558;kerrj.s.等,anticancerresearch,19(2a),959-968;thumshirng.等,2003chem.eur.j.9,2717-2725),和taasgvrsmh或ltlrwvglms(硫酸软骨素蛋白多糖ng2受体)和f3肽(结合细胞表面表达的核素受体的31个氨基酸的肽)(zitzmann,s.2002cancerres.62,18,pp.5139–5143,temminga,k.2005,drugresistanceupdates,8,381–402;p.laakkonen和k.vuorinen,2010,integrativebiol,2(7-8),326–337;m.a.burg,1999cancerres.59(12),2869–2874;k.porkka等2002,proc.nat.acad.sci.usa99(11),7444-9);细胞穿透肽(nakasei.等,2012,j.controlrelease.159(2),181–188);肽激素,如促黄体激素释放激素(lhrh)激动剂和拮抗剂,和促性腺激素释放激素(gnrh)激动剂,通过靶向卵泡刺激素(fsh)和黄体生成素(lh)起作用,以及睾酮产物,例如布舍瑞林(pyr-his-trp-ser-tyr-d-ser(otbu)-leu-arg-pro-nhet),戈那瑞林(pyr-his-trp-ser-tyr-gly-leu-arg-pro-gly-nh2),戈舍瑞林(pyr-his-trp-ser-tyr-d-ser(otbu)-leu-arg-pro-azgly-nh2),组氨瑞林(pyr-his-trp-ser-tyr-d-his(n-benzyl)-leu-arg-pro-nhet),醋酸亮丙瑞林(pyr-his-trp-ser-tyr-d-leu-leu-arg-pro-nhet),那法瑞林(pyr-his-trp-ser-tyr-2nal-leu-arg-pro-gly-nh2),曲普瑞林(pyr-his-trp-ser-tyr-d-trp-leu-arg-pro-gly-nh2),德舍瑞林,阿巴瑞克(ac-d-2nal-d-4-氯-d-3-(3-吡啶基)ala-ser-(n-me)tyr-d-asn-leu-异丙基-lys-pro-d-ala-nh2),西曲瑞克(ac-d-2nal-d-4-chloro-phe-d-3-(3-pyridyl)ala-ser-tyr-d-cit-leu-arg-pro-d-ala-nh2),地加瑞克(ac-d-2nal-d-4-氯苯酚-d-3-(3-吡啶基)ala-ser-4-氨基苯丙氨酸(l-hydroorotyl)-d-4-氨基苯丙氨酸(氨基甲酰基)-leu-异丙基赖氨酸-pro-d-ala-nh2)和加尼瑞克(ac-d-2nal-d-4-氯苯酚-d-3-(3-吡啶基)ala-ser-tyr-d-(n9,n10-二乙基)-homoarg-leu-(n9,n10-二乙基)-homoarg-pro-d-ala-nh2)(thundimadathilj.,j.aminoacids,2012,,doi:10.1155/2012/;boccon-gibodl.等,2011,therapeuticadvancesinurology3(3)127–140;debruynef.,2006,futureoncology,2(6),677–696;schallya.v,nagya.,1999eurjendocrinol141:1–14;koppanm.等,1999prostate38:151–158);和模式识别受体(prr),如类toll受体(tlr),c型凝集素和nodlike受体(nlrs)(fukatam.等,2009,semin.immunol.21,242–253;maisonneuvec.等,2014,proc.natl.acad.sci.u.s.a.111,1–6;botosi.等,2011,structure19,447–459;meanst.k.等,2000,lifesci.68,241–258)范围为小分子(咪喹莫特,鸟嘌呤和腺苷类似物)到大而复杂的生物大分子如脂多糖(lps),核酸(cpgdna,polyi:c)和脂肽(pam3csk4)(kasturis.p.等,2011,nature470,543–547;lanet.2001,j.r.soc.med.94,316;hotzc.和bourquinc.,2012,oncoimmunology1,227-228;dudeka.z.等,2007,clin.cancerres.13,7119–25);降钙素受体,一种32-氨基酸神经肽,在很大程度上通过其对破骨细胞和肾脏的作用来调节钙水平(zaidim.等,1990critrevclinlabsci28,109–174;gorna.h.等1995jclininvest95:2680–91);整联蛋白受体及其受体亚型(例如αvβ1,αvβ3,αvβ5,αvβ6,α6β4,α7β1,αlβ2,αiibβ3,等),其通常在血管发生中起重要作用,表现在各种细胞的表面上,特别是破骨细胞,内皮细胞和肿瘤细胞(ruoslahtie.等,1994cell77,477-8;albeldas.m.等,1990cancerres.50,6757-64);短肽,grgdspk和环状rgd五肽,如环(rgdfv)(l1)及其衍生物(环(-n(me)r-gdfv),环(r-sar-dfv),环-(rg-n(me)d-fv),环(rgd-n(me)f-v),环(rgdf-n(me)v)(西仑吉肽))已显示整联蛋白受体的高结合亲和力(dechantsreiterm.a.等,1999j.med.chem.,42,3033-40;goodmans.l.等,2002j.med.chem.45,1045-51)。 细胞结合配体或细胞受体激动剂可以是基于ig的和基于非ig的蛋白质支架分子。基于ig的支架可以选自但不限于纳米抗体(vhh的衍生物(骆驼ig))(muyldermanss.,2013annurevbiochem。82,775–97);域抗体(dab,vh或vl域的衍生物)(holtl.j.等,2003,trendsbiotechnol.21,484–90);双特异性t细胞engager(bite,双特异性双抗体)(baeuerlep.a.等,2009,curr.opin.mol.ther.11,22–30);双亲和重新定位(dart,双特异性双抗体)(moorep.a.p.等2011,blood117(17),4542–51);四价串联抗体(tandab,二聚双特异双抗体)(cochloviusb.等,2000,cancerres.60(16):4336–4341);非ig支架,可以选自但不限于anticalin(lipocalins的衍生物)(skerraa.,2008,febsj.275(11)2677–83;besteg等,1999proc.nat.acad.usa.96(5):1898–903;skerraa.,2000biochimbiophysacta,1482(1-2)337–50;skerraa.,2007,curropinbiotechnol.18(4)295–304;skerraa.,2008,febsj.275(11):2677–83);adnectins(10thfn3(fibronectin))(koidea.等,1998j.mol.biol.284(4):1141–51;batoriv.2002,proteineng.15(12)1015–20;tolchera.w.2011,clin.cancerres.17(2)363–71;hackelb.j.,2010,proteineng.des.sel.23(4)211–19);设计的锚蛋白重复蛋白(darpins)(ankrin重复蛋白的衍生物)(boersmay.l.等,2011curropinbiotechnol.22(6)849–57),如darpinc9,darpinec4和darpine69_lz3_e01(winklerj.等,2009molcancerther.8(9),2674–83;patriciam-k.m.等,clincancerres.2011;17(1):100–10;boersmay.l.等,2011j.biol.chem.286(48),41273–85);avimers(域a/低密度脂蛋白(ldl)受体)(boersmay.l.,2011j.biol.chem.286(48)41273–41285;silvermanj.等,2005nat.biotechnol.23(12):1556–61)。 通过本专利申请的双链连接子链接的抗体-细胞结合配体或抗体-细胞受体激动剂或抗体-药物偶联物的结构实例如下:lb01(叶酸偶联物),lb02(pmsa配体偶联物),lb03(pmsa配体偶联物),lb04(pmsa配体偶联物),lb05(生长抑素偶联物),lb06(生长抑素偶联物),lb07(奥曲肽,生长抑素类似物偶联物),lb08(兰瑞肽,生长抑素类似物偶联物),lb09(伐普肽(sanvar),生长抑素类似物偶联物),lb10(caix配体偶联物),lb11(caix配体偶联物),lb12(胃泌素释放肽受体(grpr),mba偶联物),lb13(促黄体激素释放激素(lh-rh)配体和gnrh偶联物),lb14(促黄体激素释放激素(lh-rh)和gnrh配体偶联物),lb15(gnrh拮抗剂,abarelix偶联物),lb16(钴胺素,维生素b12类似物偶联物),lb17(钴胺素,维生素b12类似物偶联物),lb18(αvβ3整联蛋白受体,环状rgd五肽偶联物),lb19(vegf受体的异二价肽配体偶联物),lb20(神经髓质素b偶联物),lb21(g蛋白偶联受体蛙皮素偶联物),lb22(类toll受体tlr2偶联物),lb23(雄激素受体偶联物),lb24(αv整合素受体西仑吉肽/环(-rgdfv-)偶联物),lb25(利福布汀类似物偶联物),lb26(利福布汀类似物偶联物),lb27(利福布汀类似物偶联物),lb28(氟氢可的松偶联物),lb29(地塞米松偶联物),lb30(丙酸氟替卡松偶联物),lb31(丙酸倍氯米松偶联物),lb32(曲安奈德偶联物),lb33(泼尼松偶联物),lb34(泼尼松龙偶联物),lb35(甲基强的松龙偶联物),lb36(倍他米松偶联物),lb37(伊立替康类似物偶联物),lb38(克唑替尼类似物偶联物),lb39(硼替佐米类似物偶联物),lb40(卡菲佐米类似物偶联物),lb41(卡菲佐米类似物偶联物),lb42(亮丙瑞林类似物偶联物),lb43(曲普瑞林类似物偶联物),lb44(克林霉素偶联物),lb45(利拉鲁肽类似物偶联物),lb46(索马鲁肽类似物偶联物),lb47(瑞他帕林类似物偶联物),lb48(indibulin类似物偶联物),lb49(长春碱类似物偶联物),lb50(利西那肽类似物偶联物),lb51(奥希替尼类似物偶联物),lb52(核苷类似物偶联物),lb53(厄洛替尼类似物偶联物)和lb54(拉帕替尼类似物偶联物),其结构如下所示: lb01(叶酸偶联物) lb02(pmsa-配体偶联物)、 lb03(pmsa-配体偶联物)、 lb04(pmsa-配体偶联物)、 lb05(生长抑素偶联物)、 lb06(生长抑素偶联物) lb07(奥曲肽、生长抑素类似物偶联物)、 lb08(兰瑞肽、生长抑素类似物偶联物)、 lb09(氨肽(sanvar)、生长抑素类似物偶联物)、 lb10(caix配体偶联物)、 lb11(caix配体偶联物)、 lb12(胃泌素释放肽受体(grpr)、mba偶联物)、 lb13(促黄体激素释放激素(lh-rh)配体和和促性腺激素释放激素gnrh配体偶联物)、 lb14(促黄体激素释放激素(lh-rh)和促性腺激素释放激素gnrh配体偶联物)、 lb15(gnrh拮抗剂、阿巴瑞克偶联物)、 lb16(钴胺素、维生素b12类似物偶联物)、 lb17(钴胺素、维生素b12类似物偶联物)、 lb18(环rgd五肽,作用于αvβ3整联蛋白受体)、 lb19(异源二价肽配体偶联物,作用于血管内皮生长因子vegf受体)、 lb20(神经髓质素b偶联物)、 lb21(蛙皮素偶联物,作用于g蛋白偶联受体)、 lb22(tlr2偶联物,作用于类toll受体)、 lb23(雄激素受体)、 lb24(西伦吉肽/环(-rgdfv-)偶联物,作用于αv整合素受体) lb25(利福布丁类似物偶联物)、 lb26(利福布丁类似物偶联物)、 lb27(利福布丁类似物偶联物)、 lb28(氟氢可的松偶联物)、 lb29(地塞米松偶联物)、 lb30(丙酸氟替卡松偶联物)、 lb31(倍氯米松丙酸酯)、 lb32(曲安奈德偶联物)、 lb33(泼尼松偶联物)、 lb34(泼尼松龙偶联物)、 lb35(甲基强的松龙偶联物)、 lb36(倍氟美松偶联物)、 lb37(伊立替康类似物)、 lb38(克唑替尼类似物偶联物)、 lb39(硼替佐米类似物偶联物);其中y5是n、ch、c(cl)、c(ch3)或c(coor1)的r1是h、c1-c6烷基、c3-c8芳基; lb40(卡非佐米类似物偶联物)、 lb41(卡非佐米类似物偶联物)、 lb42(亮丙瑞利类似物)、 lb43(曲普瑞林类似物偶联物)、 lb44(克林霉素偶联物)、 lb45(利拉鲁肽类似物偶联物)、 lb46(索马鲁肽类似物偶联物)、 lb47(瑞他帕林类似物偶联物)、 lb48(丁布尔类似物偶联物)、 lb49(长春碱类似物偶联物)、 lb50(利西森肽类似物偶联物)、 lb51(奥西丁尼类似物偶联物)、 lb52(核苷类似物偶联物)、 lb53(埃罗替尼类似物偶联物)、 lb54(拉帕替尼类似物偶联物)、 其中“—–”、x1、x2、q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;x3为ch2、o、nh、nhc(o)、nhc(o)nh、c(o)、oc(o)、oc(o)(nr3)、r1、nhr1、nr1、c(o)r1或缺省;x4为h、ch2、oh、o、c(o)、c(o)nh、c(o)n(r1)、r1、nhr1、nr1、c(o)r1或c(o)o;x5为h、ch3、f、或cl;m1和m2为独立的h、na、k、ca、mg、nh4、nr1r2r3;r6为5′-脱氧腺苷、me、oh、或cn; 在另一个实施例中,一种,两种或更多种dna,rna,mrna,小干扰rna(sirna),微rna(mirna)和piwi相互作用rna(pirna)通过本专利的双链连接子与细胞结合分子偶联。短链的rna(sirna,mirna,pirna)和长链的非编码反义rna与细胞内的表观遗传变化相关(goodchild,j(2011),methodsinmolecularbiology(clifton,n.j.),7641–15)。本发明中的dna,rna,mrna,sirna,mirna或pirna可以是单链或双链,核苷酸单为一百万至三百万,并且部分核苷酸可以是非天然(合成)形式,例如具有硫代磷酸酯键的寡核苷酸,如fomivirsen,或以硫代磷酸酯键而不是磷酸酯键连接的天然rna和dna的核苷酸,分子中间的糖部分是脱氧核糖,在两端是2′-o-甲氧基乙基修饰的核糖的核苷酸,如mipomersen,或含肽核酸(pna),吗啉代,硫代磷酸酯,硫代磷酰胺,或2′-o-甲氧基乙基(moe),2′-o-甲基,2′-氟,锁核酸(lna),或双环核酸(bna)核糖的寡核苷酸,或糖环中的2′-3’碳键被去除的核酸(whitehead,k.a.等,(2011),annualreviewofchemicalandbiomolecularengineering277–96;bennettc.f.,swayzee.e.,(2010),annu.rev.pharmacol.toxicol.50259–29)。优选地,寡核苷酸的长度为约8至超过200个核苷酸。核苷酸偶联物的例子如下所示: 其中“—–”、q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)和c(o)nr1;是单链或双链的dna、rna、mrna、sirna、mirna或pirna。 在另一个实施方案中,igg抗体与一种,两种或多种不同功能的分子或药物偶联,优选通过轻链和重链之间的一对巯基(通过还原二硫键),或轻重链之间一对巯基,或两个重链之间的上部一对巯基,以及两个重链之间的下部一对巯基特异性偶联,结构如st1,st2,st3,st4,st5或st6所示: st2、 st4、 st6、 其中“—–”、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选的x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)和c(o)nr1;m1、m2、m3和m4独立地为1-30。 此外,含有相同或不同双链连接子的药物或细胞毒性分子,依次地与细胞结合分子偶联,或者,含有相同或不同双链连接子的不同细胞毒性分子,逐步加入含有细胞结合分子的偶联反应混合物中反应,在细胞结合分子的不同偶联位点处的细胞毒性分子和y1,、y2,、r1,、r2,、r3,、r4,、r5,、r5’,、z1,、z2和n可以是不同的。 偶联物的制剂及其应用 本专利申请的偶联物被配制成液体,冻干后可被复溶成液体的形态。在病人上施用时,不产生高水平抗体聚集的制剂配方包含0.1克/升-300克/升的偶联物活性成分、一种或多种多醇(例如糖)、ph值为4.5至7.5的缓冲液、表面活性剂(如聚山梨酸20或80)、抗氧化剂(例如抗坏血酸和/或蛋氨酸)、强化剂(如甘露醇、山梨醇或氯化钠)、螯合剂(如edta)、金属络合物(如锌-蛋白络合物)、可生物降解聚合物(如聚酯)、防腐剂(如苯甲醇)和/或游离氨基酸。 用于制剂的合适缓冲液包括但不限于,有机酸盐,例如柠檬酸、抗坏血酸、葡糖酸、碳酸、酒石酸、琥珀酸、乙酸或邻苯二甲酸的钠、钾、铵或三羟乙基氨基盐,氨基丁三醇盐酸、硫酸或磷酸缓冲液。此外,氨基酸阳离子也可用作缓冲液。这些氨基酸包括但不限于,精氨酸、甘氨酸、甘氨酰甘氨酸和组氨酸。精氨酸缓冲液包括精氨酸乙酸盐、精氨酸氯化物、精氨酸磷酸盐、精氨酸硫酸盐,精氨酸琥珀酸盐等。在一个实施例中,精氨酸缓冲液是精氨酸乙酸盐。组氨酸缓冲液的实例包括组氨酸氯化物-精氨酸氯化物、组氨酸乙酸盐-精氨酸乙酸盐、组氨酸磷酸盐-精氨酸磷酸盐、组氨酸硫酸盐-精氨酸硫酸盐、组氨酸琥珀酸盐-精氨酸琥珀酸盐等。缓冲液的ph是4.5至ph7.5,优选约4.5至约6.5,更优选约5.0至约6.2。在一些实施例中,缓冲液中有机酸盐的浓度为约10mm至约500mm。 在制剂中可选地含有的“多醇”是具有多个羟基的物质。多醇可用作液体和冻干制剂中的稳定辅料和/或等渗剂。多醇可以保护生物药物免受物理和化学降解。最好能被排除的共溶剂增加了蛋白质接口处溶剂的有效表面张力,能量最有利的结构构像是表面积最小的那些溶剂。多醇包括糖(还原和非还原糖)、糖醇和糖酸。“还原糖”是指含有半缩醛基团的糖,它能够还原金属离子,或与蛋白质中的赖氨酸和其他氨基发生反应,“非还原糖”是指不具有还原糖性质的糖。还原糖的例子有果糖、甘露糖、麦芽糖、乳糖、阿拉伯糖、木糖、核糖、鼠李糖、半乳糖和葡萄糖。非还原糖包括蔗糖、海藻糖、山梨糖、松解糖和棉子糖。糖醇选自甘露醇、木糖醇、赤藓糖醇、麦芽糖醇、乳糖醇、赤藓糖醇、苏糖醇、山梨醇和甘油。糖酸包括l-葡萄糖酸盐及其金属盐。液体配方或冻干制剂中的多醇含量,按重量计,为0.0%-20%。在配方中优选浓度约为0.1%到15%的非还原糖,蔗糖或海藻糖,其中由于海藻糖的溶液稳定性,海藻糖更优。 在制剂中可选的表面活性剂可选自聚山梨醇酯(聚山梨醇酯20、聚山梨醇酯40、聚山梨醇酯65、聚山梨醇酯80、聚山梨醇酯81、聚山梨醇酯85等);泊洛沙姆(如泊洛沙姆188、聚(环氧乙烷)-聚(环氧丙烷)、泊洛沙姆407或聚丙二醇-丙二醇等);triton;十二烷基硫酸钠(sds);月桂基硫酸钠;辛基糖苷钠;十二烷基、肉荳蔻酰基、亚油基或硬脂基磺基甜菜碱;十二烷基、肉荳蔻酰基、亚油基或硬脂基肌氨酸;亚油酸、肉荳蔻基或十六烷基甜菜碱;月桂酰胺基丙基、椰油酰胺丙基、亚油酰胺基丙基、肉荳蔻酰基丙基、棕榈酰基丙基或异硬脂酰胺基丙基-甜菜碱(例如月桂酰胺丙基);肉荳蔻酰胺丙基、棕榈酰丙基或异硬脂酰胺基丙基-二甲胺;甲基椰油酰基钠或甲基油基牛磺酸二钠;十二烷基甜菜碱、十二烷基二甲基氧化胺、椰油酰胺丙基甜菜碱和可可两性甘氨酸酯;monaquattm系列(如异硬脂基乙基亚胺鎓乙基硫酸盐);聚乙二醇,聚丙二醇,乙二醇和丙二醇的共聚物(如pluronic、pf68等)。优选的表面活性剂是聚氧乙烯山梨糖醇脂肪酸酯,如聚山梨醇酯20、40、60或80(吐温tween20、40、60或80)。制剂中表面活性剂的浓度范围,按照重量计,为0.0%至约2.0%。在某些特定实施例中,表面活性剂浓度为约0.01%至约0.2%。在一个实施例中,表面活性剂浓度为约0.02%。 在制剂中可选的“防腐剂”是从根本上可以减小其中细菌的化合物。防腐剂的实例包括十八烷基二甲基芐基氯化铵、六甲基氯化铵、苯扎氯铵(烷基芐基二甲基氯化铵的混合物,其中烷基为长链烷基)和芐索氯铵。其他类型的防腐剂包括芳香醇如苯酚,丁基和芐基醇,对羟基苯甲酸烷基酯,如甲酯或丙酯,儿茶酚、间苯二酚、环己醇、3-戊醇和间甲酚。液体配方或冻干粉末中的防腐剂含量,按照重量计,为0.0%-5.0%。在一个实施例中,所用防腐剂是苯甲醇。 在制剂中合适的游离氨基酸,选自但不限于精氨酸、胱氨酸、甘氨酸、赖氨酸、组氨酸、鸟氨酸、异亮氨酸、亮氨酸、丙氨酸、甘氨酸谷氨酸或天冬氨酸中的一种或多种。优选碱性氨基酸为精氨酸、赖氨酸和/或组氨酸。如果组成中包含组氨酸,它可以充当缓冲剂和游离氨基酸,但是当使用组氨酸缓冲液时,通常还要包含一个非组氨酸的游离氨基酸,如赖氨酸。氨基酸可以以d-和/或l-型存在,但l-型比较常见。氨基酸可以任何合适的盐的形式存在,如精氨酸盐酸盐。液体配方或冻干粉末中的氨基酸含量,以重量计,为0.0001%-15.0%,优选为0.01%至5%。 可选地,制剂还包含甲硫氨酸或抗坏血酸作为抗氧化剂,浓度为约0.01至5毫克/毫升;可选地,制剂包含金属螯合剂,例如edta,egta等,浓度为约0.01至2mm。 最终的制剂可以用缓冲调节剂(如一种酸,包括hcl、h2so4、乙酸,h3po4、柠檬酸等,或是碱,如naoh、koh、nh4oh、乙醇胺、二乙醇胺或三乙醇胺、磷酸钠、磷酸钾、柠檬酸三钠、氨基丁三醇等)调节至优选的ph值。制剂还应当被调节至“等渗”,即目标制剂具有与人血基本相同的渗透压。等渗制剂渗透压通常为250至350mosm。可以使用蒸气压或冰冻型渗透压计测量等渗性。 在液体或冻干制剂中可能有用的其他辅料包括,例如,岩藻糖、纤维二糖、麦芽三糖、褪黑糖、辛酮糖、核糖、木糖醇、精氨酸、组氨酸、甘氨酸、丙氨酸、蛋氨酸、谷氨酸、赖氨酸、咪唑、甘氨酸、甘露糖基甘油酯、tritonx-100、puloronicf-127、纤维素、环糊精、(2-羟丙基)-β-环糊精、右旋糖酐(10、40和/或70kd)、聚葡萄糖、麦芽糊精、无花果胶、明胶、羟丙基甲基、磷酸钠、磷酸钾、氯化锌、锌、氧化锌、柠檬酸钠、柠檬酸三钠、氨丁三胺、铜、纤维粘连蛋白、肝素、人血清白蛋白、鱼精蛋白、甘油、edta、间甲酚、苯甲醇、苯酚、多醇、被还原的糖、其中一羰基被还原为一级或二级醇。 其它可以在本专利申请的液体制剂中使用的辅料还包括:例如调味剂、抗微生物剂、甜味剂、抗氧化剂、抗静电剂、脂质如磷脂或脂肪酸脂、类固醇如胆固醇、蛋白质辅料如血清白蛋白(人血清白蛋白)、重组人白蛋白、明胶、酪蛋白、成盐反离子如钠等。这些和另外的适用于本发明制剂的,已知的药物辅料和/或加入剂为本领域公知,如在由美国医药协会罗威(rowe)等人编著的第四版《药用辅料手册》(thehandbookofpharmaceuticalexcipients)中所列;以及由威尔金斯出版公司出版(2005),热纳罗(gennaro)等人编著的第21版《雷明顿:药学科学与实践》(remington:thescienceandpracticeofpharmacy)中所列。 在更进一步的实施例中,本发明提供了制剂的制备方法,包括以下步骤:(a)将包含偶联物,辅料和缓冲体系的制剂冻干至粉末状;(b)在介质中复溶步骤(a)中的冻干混合物,以使得复溶的制剂稳定。步骤(a)中的液体可进一步包含稳定剂和一种或多种辅料,选自前述填充剂、盐、表面活性剂和防腐剂。稀释的有机酸或水,例如无菌水、注射用抑菌水(bwfi)、可以用作复溶介质。复溶介质可选用水,如无菌水、抑菌性注射用水(bwfi)、乙酸、丙酸、琥珀酸、氯化钠、氯化镁溶液、氯化钠的酸性溶液、氯化镁的酸性溶液或精氨酸的酸性溶液,其浓度为约10-约250mm。 本专利申请的偶联物的液体制剂应具有各种设定的特征。需要考虑的主要问题之一是其稳定性,因为蛋白质/抗体在制造和储存期间,常会形成可溶及不溶的聚集体。此外,溶液中会发生各种化学反应(脱酰胺、氧化、剪切、异构化等),导致降解产物水平增加和/或生物活性丧失。液体或冻干制剂中的偶联物最好应在25℃下,具有超过18个月的货架期。更优的液体或冻干制剂中的偶联物应在25℃下具有超过24个月的货架期。最为优选的液体制剂应该在2-8℃下具有约24-36个月的货架期,冻干粉末在2-8℃下,应该具有长达约60个月的货架期。液体制剂和冻干制剂优选地具有在-8℃,-20℃或-70℃下至少两年货架期。 在一些实施例中,该制剂在冷冻(例如-20℃或-70℃)和融化之后是稳定的,例如在1、2或3个冷冻和融化循环之后是稳定的。可以用不同的方式定性和/或定量地评估稳定性,包括评估药物/抗体(蛋白质)的比例和聚集体的形成(例如,使用uv、尺寸排阻色谱法、通过测量浊度和/或通过目测);通过使用阳离子交换色谱、图像毛细管等电聚焦(icief)或毛细管区带电泳评估电荷异质性;进行氨基末端或羧基末端序列分析、质谱分析或基质辅助激光解吸电离/飞行时间质谱(maldi/tofms),hplc-ms/msce-sds或sds-page分析以比较还原抗体和完整抗体;进行肽图分析(例如胰蛋白酶或lys-c);评估抗体的生物学活性或抗原结合功能。不稳定可能涉及以下一种或多种:聚集、脱酰胺作用(例如asn脱酰胺作用)、氧化作用(例如met氧化作用)、异构化作用(例如asp异构化作用)、剪切/水解/断裂作用(例如铰链区断裂)、生成琥珀酰亚胺、未成对半胱氨酸、n末端延伸、c末端加工、糖基化差异等。 稳定的偶联物应当在药物制剂中“保持其生物学活性”,例如,如果偶联物的生物活性在给定时间内,例如12个月,按照抗原结合测定和/或体外细胞毒性测定的方法,生物活性可以保持在相差20%以内,优选10%(在测定误差内)。 药物容器或容器用于容纳专利申请的任何偶联物的药物制剂。该容器是小瓶,瓶子,预填充注射器或预填充自动注射器注射器。 对于临床体内使用,偶联物给药方式的实例如下:每天一次、每周一次、每两周一次、每三周一次、每次四周一次或每月一次、共周,静脉推注。注射的剂量是在50-1000ml生理盐水中,可任选地向其中加入人血清白蛋白(例如0.5-1ml人血清白蛋白浓缩溶液,100mg/ml)。每周一次、每两周一次、每三周一次的剂量约为50μg/kg-30mg/kg体重,静脉推注(每次注射10μg-200mg/kg的范围)。治疗后周,患者可能会接受第二个疗程。关于给药方式,辅料,稀释剂,剂量,时间等的具体临床方案可以由熟练的临床医生确定。 可以根据体内或体外的方法杀死选定的细胞群进行治疗的医学病症,包括任何类型的癌症的恶性肿瘤,自身免疫性疾病,移植排斥和感染(病毒,细菌或寄生虫)。 获得满意的生物学效应所需的偶联物的量将取决于许多因素,包括偶联物的化学特性,效力和生物利用度,疾病类型,患者的种族,患者的疾病状态,给药途径,这些决定了所需剂量,给药方式和给药方案。 一般而言,可以通过包含本发明的药物为含0.1-10%w/v偶联物的生理缓冲水溶液,用于肠胃外施用。典型剂量范围为1μg/kg-0.1g/kg体重,每天、每周、每两周、每三周或每月一次,优选的剂量范围是人体等效剂量0.01mg/kg-30mg/kg体重,每周,每两周,每三周或每月一次。待给药物的优选剂量可能取决于下列变量,如疾病的类型或病症的进展,患者的总体健康状况,所选化合物的相对生物学功效,药物的制剂,给药方式(静脉内,肌肉内或其他),药物在确定的给药途径的药代动力学特性,给药速度(推注或连续输注)和给药方案(在给定时间内重复次数)。 通过本发明的连接子的偶联物也能够以单位剂量形式给药,其中术语“单位剂量”是指能够给予患者并且可以容易地处理和包装的单一剂量,保持为物理和化学稳定的单位剂量,包括活性偶联物本身,或作为药学上可接受的组合物,如下所述。因此,典型的每日/每周/双周/每月总剂量范围为0.01-100mg/kg体重。通过一般指导,人体的单位剂量范围为每天1毫克-3000毫克,或每周,每两周(两周),三周或每月一次。优选地,单位剂量范围为每月施用1-4次1-500mg,甚至更优选1mg-100mg,每周一次或每两周一次或每三周一次。本文提供的偶联物可以通过与一种或多种药学上可接受的辅料混合而配制成药物组合物。这种单位剂量组合物可以制备成通过口服给药使用,特别是以片剂,简单胶囊或软凝胶胶囊的形式;或鼻内,特别是以粉末,滴鼻剂或气溶胶的形式;或皮肤,例如局部用软膏,乳膏,乳液,凝胶或喷雾剂,或通过透皮贴剂。 在又一个实施方案中,包含治疗有效量的式(i)偶联物或通过本专利描述的任何偶联物的药物组合物可以与其它治疗剂例如化学治疗剂、放射疗法、免疫治疗剂、用于协同有效治疗或预防癌症、自身免疫疾病或传染病的自身免疫疾病剂、抗感染剂或其他偶联物。协同剂优选选自以下一种或几种药物:阿巴西普、abemaciclib、乙酸阿比特龙、abraxane、阿杜卡奴单抗、对乙酰氨基酚/氢可酮、阿卡替尼、阿杜卡奴单抗、阿达木单抗、adxs31-142、adxs-her2、阿法替尼二马来酸盐、阿地白介素、阿乐替尼、阿伦单抗、艾力替尼、alitretinoin、ado-trastuzumabemtansine、安非他明/右旋安非他明、阿那曲唑、apatinib、阿立哌唑、蒽环类药物、阿立哌唑、atazanavir、阿特朱单抗、阿托伐他汀、avelumab、avxs-101、axicabtageneciloleucel、阿西替尼、贝利司他、bcg-live、贝伐单抗、贝沙罗汀、blinatumomab、硼替佐米、波舒替尼、本妥昔单抗、布格替尼、布地奈德、布地奈德/福莫特罗、丁丙诺啡、byl719(α特异性pi3k抑制剂)、卡巴他赛、卡博替尼、卡马替尼、卡培他滨、卡非佐米、嵌合抗原受体工程t(car-t)细胞、塞来昔布、色瑞替尼、西妥昔单抗、西奥罗尼、西达本胺、环孢素、cinacalcet、克唑替尼、考比替尼、cosentyx、克唑替尼、tisagenlecleucel、达比加群、达拉菲尼、达卡巴嗪、达利珠单抗、达科替尼、达托霉素、达拉木单抗、darbepoetinalfa、darunavir、达沙替尼、denileukindiftitox、地诺单抗、depakote、dexlansoprazole、dexmethylphenidate、地塞米松、l-3、4-二羟基苯基丙氨酸、dinutuximab、阿法链道酶、强力霉素、度洛西汀、德卫利昔、度伐鲁单抗、依托珠单抗、emicizumab、emtricibine/利匹韦林/替诺福韦、地索普西富马酸、恩曲他滨/替诺福韦/依非韦伦、依诺肝素、恩沙替尼、恩杂鲁胺、易吡替尼、阿法依伯汀、厄洛替尼、埃索美拉唑、eszopiclone、依那西普、依维莫司、依西美坦、依维莫司、艾塞那肽er、依泽替米贝、依泽替米贝/辛伐他汀、法米替尼、非诺贝特、非戈替尼、非格司亭、芬戈莫德、氟马替尼、丙酸氟替卡松、氟替卡松/沙美特罗、呋喹替尼、氟维司群、gazyva、吉非替尼、醋酸格拉替雷、醋酸戈舍瑞林、gsk(bcma-adc)、henatinib、埃克替尼、伊马替尼、替伊莫单抗、依鲁替尼、埃克替尼、艾代拉里斯、异环磷酰胺、英夫利昔单抗、咪喹莫特、immunocyst、immunobcg、iniparib、门冬胰岛素、地特胰岛素、甘精胰岛素、赖脯胰岛素、干扰素α、干扰素α-1b、干扰素α-2a、干扰素α-2b、干扰素β、干扰素β1a、干扰素β1b、干扰素γ-1a、拉帕替尼、易普利姆玛、异丙托溴铵/沙丁胺醇、伊沙唑米、卡努玛、莱地鲁单伉、醋酸兰瑞肽、来那度胺、来那度胺、甲磺酸乐伐替尼、来曲唑、左旋甲状腺素、左旋甲状腺素、利多卡因、利奈唑胺、利拉鲁肽、lisdexamfetamine、ln-144(肿瘤浸润淋巴细胞)、lorlatinib、德立替尼/delitinib、美金刚、甲氧基聚乙二醇epoetin-beta、哌醋甲酯、美托洛尔、曲美替尼、美西他滨/利匹韦林/替诺福韦、莫达非尼、莫米松、mycidac-c、霉酚酸、耐昔妥珠单抗、诺拉替尼、尼罗替尼、尼拉帕尼、尼沃鲁单抗、奥法木单抗、奥比曲妥珠单抗、奥瑞珠单抗、奥拉帕尼、奥美沙坦、奥美沙坦/氢氯苯噻哒嗪、奥马珠单抗、omega-3脂肪酸乙酯、oncorine、奥司他韦、奥希替尼、羟考酮、奥扎莫德、帕波克利、帕利珠单抗、帕尼单抗、帕比司他、帕唑帕尼、派姆单抗、pd-1抗体、pd-l1抗体、培美曲塞、帕妥珠单抗、吡非尼酮、肺炎球菌结合疫苗、泊马度胺、普瑞巴林、proscavax、普萘洛尔、普喹替尼、吡咯替尼、喹硫平、雷贝拉唑、氯化镭223、雷洛昔芬、raltegravir、雷莫芦单抗、雷珠单抗、瑞戈非尼、瑞博西尼、瑞莎珠单抗、利妥昔单抗、利伐沙班、罗米地辛、罗苏伐他汀、磷酸鲁索替尼、沙丁胺醇、索凡替尼、索马鲁肽、sevelamer、西地那非、司妥昔单抗、西莫替尼、西帕替尼/cipatinib、辛波莫德、sipuleucel-t、西他列汀、西他列汀/二甲双胍、solifenacin、索兰珠单抗、索尼吉布、索拉非尼、磺胺替尼、舒尼替尼、他克莫司、tacrimus、他达那非、他莫昔芬、甲磺酸达拉非尼、talimogenelaherparepvec、talazoparib、特拉瑞韦、talazoparib、替莫唑胺、替西罗莫司、替奈普酶、替诺福韦/恩曲他滨、富马酸替诺福韦酯、睾酮凝胶、替加卡托/依伐卡托、沙利度胺、theliatinib、ticebcg、噻托溴铵、tisagenlecleucel、托珠单抗、托瑞米芬、曲美替尼、曲妥珠单抗、曲贝替定(海鞘素743)、曲美替尼、替西木单抗、trifluridine/tipiracil、维甲酸、乌帕替尼、uro-bcg、优特克单抗、valoctocogeneroxaparvovec、缬沙坦、veliparib、凡德他尼、威罗菲尼、维特克拉、维莫德吉、索凡替尼、伏立诺他、阿柏西普、zostavax及其类似物、衍生物、药学上可接受的盐、载体、稀释剂或其辅料,或其以上的组合。 用本申请的连接子偶联的药物/细胞毒性剂可以是本专利中描述的的任何药物/细胞毒性剂类似物和/或衍生物。药物/细胞毒性剂领域的技术人员可以理解,本文所述的每种药物/细胞毒性剂都可以被修饰,使所得化合物仍保留起始化合物的特异性和/或活性。技术人员还应当理解,可以使用这些类似物或衍生物来代替本文所述的药物/细胞毒性剂。因此,本发明的药物/细胞毒性剂包括这些类似物和衍生物。 本发明以下列实施例做进一步说明,但不仅限于以下实施例。 实施例 以下实施例进一步说明本发明,但这些实施例无意于限制本发明的范围。以下示例中所述的细胞系,除非另有说明,根据美国典型培养物保藏中心(atcc)或德国deutschesammlungvonmikroorganismenundzellkulturengmbh(dmsz)或中国科学院上海细胞培养研究所指定的条件进行培养。除非另有说明,否则细胞培养试剂来自invitrogencorp.。所有无水溶剂都可以通过商业途径获得,并在氮气下储存在sure-seal瓶中。购买的所有其他试剂和溶剂均为可用的最高等级,无需进一步纯化即可使用。用varainprestarhplc进行制备hplc分离。nmr光谱在bruker500mhz仪器上分析测得。化学位移(δ)以百万分数(ppm)为单位报告,为对四甲基硅烷(0.00ppm)的相对值,偶合常数(j)以hz为单位报告。质谱数据是在装有watersacquityuplc分离模块和acquitytuv检测器的watersxevoqtof质谱上获得的。 实施例1.2,5-二氧代-2,5-二氢-1h-吡咯-1-羧酸甲酯的合成。 在0℃下,向马来酰亚胺(6.35g,65.4mmol,1.0eq)的乙酸乙酯(120ml)溶液中加入n-甲基吗啉(8.6ml,78.5mmol,1.2eq)和氯甲酸甲酯(6.0ml,78.5mmol,1.2eq)。在0℃下将反应搅拌30分钟,室温搅拌1小时。滤出固体,浓缩滤液。将残余物溶于ch2cl2中并通过硅胶过滤,并用ch2cl2洗脱以洗去颜色。浓缩适当的组分,将得到的固体用10%乙酸乙酯/石油醚打浆,得到白色固体(9.00g,收率89%)。 实施例2.(s)-3-((叔丁氧羰基)氨基)-2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酸的合成。 在0℃,向h-dap(boc)-oh(1.00g,4.9mmol)和饱和碳酸氢钠(20ml)溶液中加入2,5-二氧代-2,5-二氢-1h-吡咯-1-羧酸甲酯(2.30g,14.7mmol)。将反应在0℃下搅拌1小时,然后升温至室温并再搅拌1小时。然后加入1nkhso4以将ph调节至~6,并将所得混合物用乙酸乙酯(2×50ml)萃取。将合并的有机层用硫酸钠干燥,过滤并浓缩,得到标题化合物(0.42g,收率30%)。esim/zc12h15n2o6[m-h]-计算值:283.10,实测值:283.10。 实施例3.(2-(2,5-二氧代-2-,5-二氢-1h-吡咯-1-基)乙基)氨基甲酸叔丁酯的合成。 将n-boc-乙二胺(5.6ml,35.4mmol,1.1eq)和饱和碳酸氢钠(60ml)的混合物冷却至0℃,向其中分批加入2,5-二氧代-2,5-二氢-1h-吡咯-1-羧酸甲酯(5.00g,32.2mmol,1.0eq)。在0℃下搅拌30分钟后,将反应升温至室温并搅拌1小时。将沉淀物过滤收集并用冷水洗涤,然后溶于乙酸乙酯并用盐水洗涤,用无水硫酸钠干燥并浓缩,得到标题化合物,为白色固体(6.69g,收率87%)。 实施例4.(2-(1,3-二氧代-3a,4,7,7a-四氢-1h-4,7-环氧异吲哚-2(3h)-基)乙基)氨基甲酸叔丁酯的合成。 将(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙基)氨基甲酸叔丁酯(6.00g,25.0mmol),呋喃(18.0ml)的甲苯溶液(120ml)在高压管中加热回流并搅拌16小时。无色溶液在反应过程中变黄。然后将混合物冷却至室温并浓缩,将得到的白色固体用乙醚打浆,得到标题化合物(6.5g,收率84%)。 实施例5.2-(2-氨基乙基)-3a,4,7,7a-四氢-1h-4,7-环氧异吲哚-1,3(2h)-二酮盐酸盐的合成。 将(2-(1,3-二氧代-3a,4,7,7a-四氢-1h-4,7-环氧异吲哚-2(3h)-基)乙基)氨基甲酸叔丁酯(9.93g,32.2mmol)溶于二噁烷(15ml)中,并在室温下与浓hcl(15ml)搅拌3小时。浓缩反应物,过滤收集所得固体,用乙酸乙酯洗涤滤饼。将固体在烘箱(50℃)中干燥过夜,得到标题化合物(6.94g,收率88%)。 实施例6.2,8-二氧代-1,5-恶唑烷-5-羧酸叔丁酯的合成。 在4℃,向3,3′-氮杂二基二丙酸(10.00g,62.08mmol)的1.0mnaoh(300ml)溶液中加入二碳酸二叔丁酯(22.10g,101.3mmol)的四氢呋喃(200ml)溶液。加入后,将混合物在4℃下搅拌2小时。用0.2mh3po4将混合物小心酸化至ph~4,真空浓缩,用ch2cl2萃取,用硫酸钠干燥,蒸发并用快速sio2色谱纯化,用acoh/甲醇/二氯甲烷(0.01:1:5)洗脱,得到3,3′-((叔丁氧基羰基)氮杂二基)二丙酸(13.62g,收率84%)。esimsm/z:c11h19no6[m+h]+计算值:262.27,实测值:262.40。 在0℃下,向3,3′-(叔丁氧基羰基)氮杂二基)二丙酸(8.0g,30.6mmol)的二氯甲烷(500ml)溶液中加入五氧化二磷(8.70g,61.30mmol)。将混合物在0℃下搅拌2小时,然后搅拌1小时,通过短sio2柱过滤,并用乙酸乙酯/二氯甲烷(1:6)冲洗柱。浓缩滤液并用乙酸乙酯/正己烷打浆,得到标题化合物(5.64g,收率74%)。esimsm/z:c11h17no5[m+h]+,计算值:244.11,实测值:244.30。 实施例7.3-(2-(2-(2-(2-(甲苯磺酰氧基)乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 将3-(2-(2-(2-羟基乙氧基)乙氧基)丙酸叔丁酯(10.0g,35.95mmol)的乙腈(50.0ml)和吡啶(20.0ml)混合。然后在30分钟内通过加料漏斗滴加甲苯磺酰氯(7.12g,37.3mmol)的50ml乙腈溶液。5小时后tlc分析显示反应完成。滤出已形成的吡啶盐酸盐并除去溶剂。通过用20%乙酸乙酯的己烷溶液洗脱,用纯乙酸乙酯在硅胶上纯化残余物,得到11.2g(76%收率)标题化合物。1hnmr:1.40(s,9h),2.40(s,3h),2.45(t,2h,j=6.4hz),3.52-3.68(m,14h),4.11(t,2h,j=4.8hz),7.30(d,2h,j=8.0hz),7.75(d,2h,j=8.0hz);esimsm/z:c20h33o8s(m+h)计算值:433.18,实测值:433.30。 实施例8.3-(2-(2-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 一边搅拌一边向50mldmf中加入3-(2-(2-(2-(2-(甲苯磺酰氧基)乙氧基)乙氧基)乙氧基)丙酸叔丁酯(4.0g,9.25mmol)和叠氮化钠(0.737g,11.3mmol)。将反应加热至80℃。4小时后,tlc分析表明反应完成。将反应冷却至室温,并用水(25ml)淬灭。分离水层,并萃取到乙酸乙酯(3×35ml)中。合并的有机层经无水硫酸镁干燥,过滤,并真空除去溶剂。叠氮化物粗产物(2.24g,收率98%,hplc纯度约93%)无需进一步纯化即可用于下一步。1hnmr(cdcl3):1.40(s,9h),2.45(t,2h,j=6.4hz),3.33(t,2h,j=5.2hz),3.53-3.66(m,12h)。esimsm/z:c13h26n3o8(m+h),计算值:304.18,实测值:304.20。 实施例9.3-(2-(2-(2-(叠氮基乙氧基)乙氧基)乙氧基)丙酸的合成。 向在1,4-二氧六环(40ml)中的3-(2-(2-(2-叠氮基乙氧基)乙氧基)丙酸叔丁酯(2.20g,7.25mmol)中加入hcl(12m,10ml)。将混合物搅拌40分钟,用1,4-二氧六环(20ml)和甲苯(40ml)稀释,蒸发并与14-二氧六环(20ml)和甲苯(40ml)共蒸发至干,得到标题产物粗品,无需进一步纯化(1.88g,收率105%,hplc纯度约92%)。esimsm/z:c9h18n3o5[m+h]+计算值:248.12,实测值:248.40。 实施例10.13-氨基-4,7,10-三氧杂十二烷酸叔丁酯和13-氨基双(4,7,10-三氧杂十二烷酸叔丁酯)的合成。 在氢化反应容器内,将叠氮化物3-(2-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)丙酸(5.0g,约14.84mmol)粗品溶解在乙醇(80ml)中,向其中加入300mg10%pd/c。将该系统抽真空,并在剧烈搅拌下充入2atm的氢气。然后将反应在室温下搅拌过夜,tlc显示原料消失。将反应粗品用短硅藻土垫过滤,用乙醇洗。浓缩滤液,在硅胶柱上使用含1%三乙胺的甲醇/二氯甲烷混合物(5%至15%)作为洗脱剂纯化,得到13-氨基-4,7,10-三氧杂十二烷酸叔丁酯(1.83g,44%产率,esimsm/z:c13h27no5(m+h),计算值278.19,实测值278.30)和13-氨基-双(4,7,10-三氧杂十二烷酸叔丁酯)(2.58g,32%产率,esimsm/z:c26h52no10(m+h),计算值538.35,实测值538.40)。 实施例11.3-(2-(2-(2-氨基乙氧基)乙氧基)乙氧基)丙酸盐酸盐的合成。 在搅拌下向13-氨基-4,7,10-三氧杂十二烷酸叔丁酯(0.80g,2.89mmol)的1,4-二氧六环(30ml)溶液中加入10mlhcl(36%)。0.5小时后,tlc分析显示反应完成,浓缩反应混合物,并与乙醇和乙醇/甲苯共浓缩,得到标题盐酸盐(>90%纯度,0.640g,86%产率),无需进一步纯化。esimsm/z:c9h20no5(m+h),计算值222.12,实测值222.20。 实施例12.13-氨基-双(4,7,10-三氧杂十二烷酸)盐酸盐。 在搅拌下向13-氨基-双(4,7,10-三氧杂十二烷酸叔丁酯)(1.00g,1.85mmol)的1,4-二氧六环(30ml)溶液中加入10mlhcl(36%)。0.5小时后,tlc分析显示反应完成,浓缩反应混合物,并与乙醇和乙醇/甲苯共浓缩,得到标题产物盐酸盐(>90%纯度,0.71g,91%产率),无需进一步纯化。esimsm/z:c18h36no10(m+h),计算值426.22,实测值426.20。 实施例13.3-(2-(2-(2-(2-羟基乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 向2,2’-(乙烷-1,2-二基双(氧基))二乙醇(55.0ml,410.75mmol,3.0eq.)的无水四氢呋喃(200ml)溶液中加入钠块(0.1g)。搅拌混合物直至钠块消失,然后滴加丙烯酸叔丁酯(20.0ml,137.79mmol,1.0eq.)。将混合物搅拌过夜,然后在0℃下用盐酸(20.0ml,1n)淬灭。通过旋转浓缩除去四氢呋喃,加入盐水(300ml)并将所得混合物用乙酸乙酯(3×100ml)萃取。将有机层用盐水(3×300ml)洗涤,经无水硫酸钠干燥,过滤并浓缩,得到无色油状物(30.20g,79.0%产率),其不经进一步纯化而直接使用。esimsm/z:c13h27o6[m+h]+计算值278.1729,实测值278.1730。 实施例14.3-(2-(2-(2-(2-(甲苯磺酰氧基)乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 在0℃下,向3-(2-(2-(2-羟基乙氧基)乙氧基)乙氧基)丙酸叔丁酯(30.20g,108.5mmol,1.0eq.)和tscl(41.37g,217.0mmol,2.0eq.)的无水二氯甲烷(220ml)溶液中加入三乙胺(30.0ml,217.0mmol,2.0eq.)。将混合物在室温下搅拌过夜,然后用水(3×300ml)和盐水(300ml)洗涤,经无水硫酸钠干燥,过滤,浓缩并通过硅胶柱层析(3:1正己烷/乙酸乙酯)纯化得到无色油状物(39.4g,产率84.0%)。esimsm/z:c20h33o8s[m+h]+计算值433.1818,实测值433.2838。 实施例15.3-(2-(2-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 将3-(2-(2-(2-(甲苯磺酰氧基)乙氧基)乙氧基)乙氧基)丙酸叔丁酯(39.4g,91.1mmol,1.0eq.)溶解于无水dmf(100ml),接着加入nan3(20.67g,316.6mmol,3.5eq.)。将混合物在室温下搅拌过夜。加入水(500ml)并用乙酸乙酯(3×300ml)萃取。将合并的有机层用水(3×900ml)和盐水(900ml)洗涤,用无水硫酸钠干燥,过滤,浓缩并通过硅胶柱层析(5:1正己烷/乙酸乙酯)纯化,得到浅黄色油状物(23.8g,85.53%产率)。esimsm/z:c13h25o3n5na[m+na]+计算值326.2,实际值326.2。 实施例16.3-(2-(2-(2-(2-氨基乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 将raney-ni(7.5g,悬浮于水中)用水(三次)和异丙醇(三次)洗涤,并与异丙醇中的3-(2-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)丙酸叔丁酯(5.0g,16.5mmol)混合。在室温下,氢气球下搅拌该混合物16小时,然后用硅藻土垫过滤,用异丙醇洗涤垫。浓缩滤液并通过柱层析(5-25%甲醇/二氯甲烷)纯化,得到浅黄色油状物(2.60g,57%产率)。esimsm/z:c18h23no2na[m+na]+计算值279.19,实测值279.19。 实施例17.2-(2-(二(苄基氨基)乙氧基)乙醇的合成。 将2-(2-氨基乙氧基)乙醇(21.0g,200mmol)和碳酸钾(83.0g,600mmol)混合于乙腈(350ml)中,加入苄基溴(57.0ml,480mmol)。将混合物回流过夜后,加入水(1l),用乙酸乙酯(3×300ml)萃取。将合并的有机层用饱和食盐水(1000ml)洗涤,用无水硫酸钠干燥,过滤,浓缩并通过硅胶柱色谱(4:1石油醚/乙酸乙酯)纯化,得到无色油状物(50.97g,产率89.2%)。esimsm/z:c18h23no2na[m+na]+计算值:309.1729,实测值:309.1967。 实施例18.3-(2-(2-(2-(二苄氨基)乙氧基)乙氧基)丙酸叔丁酯的合成。 向2-(2-(二苄基氨基)乙氧基)乙醇(47.17g,165.3mmol),丙烯酸叔丁酯(72.0ml,495.9mmol)和四丁基碘化铵(6.10g,16.53mmol)的二氯甲烷(560ml)溶液中加入50%氢氧化钠水溶液(300ml)。将混合物搅拌过夜。分离有机层,水层用乙酸乙酯(3×100ml)萃取。合并有机层并用水(3×300ml)和饱和食盐水(300ml)洗涤,用无水硫酸钠干燥,过滤,浓缩并通过硅胶柱色谱(7:1石油醚/乙酸乙酯)纯化,得到无色油状物(61.1g,89.4%产率)。esimsm/z:c25h36no4[m+h]+计算值:414.2566,实测值:414.2384。 实施例19.3-(2-(2-(2-氨基乙氧基)乙氧基)丙酸叔丁酯的合成。 在氢化反应瓶中向3-(2-(2-(2-(二苄基氨基)乙氧基)乙氧基)丙酸叔丁酯(20.00g,48.36mmol,1.0eq.)的四氢呋喃(30ml)和甲醇(60ml)溶液中加入pd/c(2.00g,10wt%)。将混合物在氢气环境中(1atm)振荡过夜,通过硅藻土(助滤剂)过滤,浓缩滤液,得到无色油状物(10.58g,93.8%产率)。esimsm/z:c11h24no4[m+h]+:计算值234.1627,实测值234.1810。 实施例20.3-(2-(2-(2-羟基乙氧基)乙氧基)丙酸叔丁酯的合成。 向2,2’-氧代二乙醇(19.7ml,206.7mmol,3.0eq.)的无水四氢呋喃(100ml)溶液中加入钠(0.1g)。搅拌混合物直至钠块消失,然后滴加丙烯酸叔丁酯(10.0ml,68.9mmol,1.0eq.)。将混合物搅拌过夜,加入盐水(200ml)并用乙酸乙酯(3×100ml)萃取。将有机层用盐水(3×300ml)洗涤,经无水硫酸钠干燥,过滤,浓缩并通过硅胶柱层析(1:1正己烷/乙酸乙酯)纯化,得到无色油状物(8.10g,49.4%产率)。esimsm/z:c11h23o5[m+h]+的计算值235.1467,实测值235.1667。 实施例21.3-(2-(2-(甲苯磺酰氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 在0℃下,向3-(2-(2-羟基乙氧基)乙氧基)丙酸叔丁酯(6.24g,26.63mmol,1.0eq.)和tscl(10.15g,53.27mmol,2.0eq.)的无水二氯甲烷(50ml)溶液中加入吡啶(4.3ml,53.27mmol,2.0eq.)。将混合物在室温下搅拌过夜,然后用水(100ml)洗涤,水层用二氯甲烷(3×50ml)萃取。将合并的有机层用盐水(300ml)洗涤,经无水硫酸钠干燥,过滤,浓缩并通过硅胶柱层析(5:1正己烷/乙酸乙酯)纯化,得到无色油状物(6.33g,61.3%产率)。esimsm/z:c18h27o7s[m+h]+计算值389.1556,实测值389.2809。 实施例22.3-(2-(2-(2-叠氮基乙氧基)乙氧基)丙酸叔丁酯的合成。 向3-(2-(2-(甲苯磺酰氧基)乙氧基)乙氧基)丙酸叔丁酯(5.80g,14.93mmol,1.0eq.)的无水dmf(20ml)溶液中加入nan3(5.02g,77.22mmol),5.0eq.)。将混合物在室温下搅拌过夜,加入水(120ml)并用乙酸乙酯(3×50ml)萃取。将合并的有机层用水(3×150ml)和盐水(150ml)洗涤,用无水硫酸钠干燥,过滤,浓缩并通过硅胶柱层析(5:1正己烷/乙酸乙酯)纯化,得到无色油状物(3.73g,产率69.6%)。esimsm/z:c11h22o3n4na[m+h]+计算值260.1532,实测值260.2259。 实施例23.3-(2-(2-(2-氨基乙氧基)乙氧基)丙酸叔丁酯的合成。 将3-(2-(2-叠氮基乙氧基)乙氧基)丙酸叔丁酯(0.18g,0.69mmol)溶于甲醇(3.0ml,含60μl浓盐酸)中,并与pd/c(10wt%,20mg)氢化反应30分钟。将催化剂通过硅藻土垫过滤,用甲醇洗涤硅藻土垫。浓缩滤液,得到无色油状物(0.15g,93%产率)。esimsm/z:c11h24no4[m+h]+的计算值234.16,实测值234.14。 实施例24.3-(2-(2-叠氮基乙氧基)乙氧基)丙酸的合成。 将3-(2-(2-叠氮基乙氧基)乙氧基)丙酸叔丁酯(2.51g,9.68mmol)溶解于1,4-二恶烷(30ml)中并与10ml浓盐酸在室温下搅拌35分钟,用乙醇(30ml)和甲苯(30ml)稀释,并在真空下浓缩。将粗品在硅胶柱上使用甲醇/二氯甲烷(5%至10%)(含1%甲酸)纯化,得到标题化合物(1.63g,83%产率),esimsm/z:c7h12n3o4[m-h]-计算值202.06,实测值202.30。 实施例25.2,5-二氧吡咯烷基-1-基3-(2-(2-叠氮基乙氧基)乙氧基)丙酸酯的合成。 在搅拌下向3-(2-(2-叠氮基乙氧基)乙氧基)丙酸(1.60g,7.87mmol)的二氯甲烷(30ml)溶液中加入nhs(1.08g,9.39mmol)和edc(3.60g,18.75mmol)。8小时后tlc分析显示反应完成,浓缩反应混合物并在硅胶上纯化,乙酸乙酯/二氯甲烷(5%-10%)洗脱,得到标题化合物(1.93g,收率82%)。esimsm/z:c11h17n4o6[m+h]+,计算值:301.11,实测值:301.20。 实施例26.2,5-二氧代吡咯烷-1-基3-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)丙酸酯的合成。 向3-(2-(2-(2-叠氮基乙氧基)乙氧基)丙酸(4.50g,18.21mmol)的二氯甲烷(80ml)溶液中加入nhs(3.0g,26.08mmol)和edc(7.60g,39.58mmol),搅拌8小时后tlc分析显示反应完成,浓缩反应混合物并在硅胶上纯化,乙酸乙酯/二氯甲烷(5%-10%)洗脱,得到标题化合物(5.38g,收率86%)。esimsm/z:c13h20n4o7[m+h]+,计算值:345.13,实测值:345.30。 实施例27.(14s,17s)-1-叠氮基-17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-((叔丁氧基羰基)-氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸。 向(s)-2-((s)-2-氨基-6-((叔丁氧基羰基)氨基)己酰胺基)-4-(叔丁氧基)-4-氧代丁酸(2.81g,6.73mmol)在dma(70ml)和0.1mnah2po4(50ml,ph7.5)的混合物中加入2,5-二氧代吡咯烷-1-基3-(2-(2-叠氮基乙氧基)乙氧基)丙酸酯(3.50g,10.17)。将混合物搅拌4小时,真空蒸发,在硅胶上纯化,以甲醇(5%-15%)在含有0.5%乙酸的二氯甲烷溶液作为洗脱液,得到标题化合物(3.35g,收率77%)。esimsm/z:c28h51n6o11[m+h]+,计算值:647.35,实测值:647.80。 实施例28.(14s,17s)-1-叠氮基-14-(4-((叔丁氧基羰基)-氨基)丁基)-17-((4-(羟甲基)苯基)氨基甲酰基)-12,15-的合成二氧代-3,6,9-三氧杂-13,16-二氮杂癸烷-19-酸叔丁酯。 向(14s,17s)-1-叠氮基-17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-((叔丁氧基羰基)-氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸(3.30g,5.10mmol)和(4-氨基苯基)甲醇(0.75g,6.09)的dma(25ml)溶液中加入edc(2.30g,11.97mmol))。将混合物搅拌过夜,真空蒸发,使用甲醇/二氯甲烷(5%-8%)作为洗脱剂在硅胶上纯化,得到标题化合物(3.18g,收率83%)。esimsm/z:c35h58n7o11[m+h]+,计算值:752.41,实测值:752.85。 实施例29.(14s,17s)-1-氨基-14-(4-((叔丁氧基羰基)-氨基)丁基)-17-((4-(羟甲基)苯基)氨基甲酰基)-12,15-的合成二氧代-3,6,9-三氧杂-13,16-二氮杂并癸烷-19-酸叔丁酯。 向(14s,17s)-1-叠氮基-14-(4-((叔丁氧基羰基)氨基)丁基)-17-((4-(羟甲基)苯基)氨基甲酰基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂萘并癸烷-19-酸叔丁酯(1.50g,1.99mmol)的四氢呋喃(35ml)溶液中加入pd/c(200mg,10%pd,50%水)。将混合物在1psi的h2下振荡过夜,通过硅藻土(助滤剂)过滤,浓缩滤液,得到标题化合物(1.43g,99%收率),无需进一步纯化,立即用于下一步骤。esimsm/z:c35h60n5o11[m+h]+,计算值:726.42,实测值:726.70。 实施例30.(s)-15-叠氮基-5-异丙基-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十五烷-1-酸的合成。 向(s)-2-(2-氨基-3-甲基丁酰胺基)乙酸(val-gly)(1.01g,5.80mmol)的dma(50ml)和0.1mnah2po4(50ml,ph7.5)溶液中加入2,5-二氧代吡咯烷-1-基3-(2-(2-叠氮基乙氧基)乙氧基)丙酸酯(1.90g,6.33)。将混合物搅拌4小时,真空蒸发,在硅胶上纯化,以甲醇(5%-15%)在含有0.5%乙酸的二氯甲烷溶液作为洗脱液,得到标题化合物(1.52g,收率73%)。esimsm/z:c14h26n5o6[m+h]+,计算值:360.18,实测值:360.40。 实施例31.(s)-2,5-二氧代吡咯烷-1-基15-叠氮基-5-异丙基-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十五烷-1-酸酯的合成 向(s)-15-叠氮基-5-异丙基-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十五烷-1-酸(1.50g,4.17mmol)的二氯甲烷(40ml)溶液中加入nhs(0.88g,7.65mmol)和edc(2.60g,13.54mmol)。8小时后tlc分析显示反应完成,将反应混合物浓缩并在硅胶柱上纯化,使用5%至20%乙酸乙酯的二氯甲烷溶液作为洗脱液,得到标题化合物(1.48g,78%收率)。esimsm/z:c18h29n6o8[m+h]+,计算值:457.20,实测值:457.50. 实施例32.4-((苄氧基)羰基)氨基)丁酸的合成。 在0°c,将4-氨基丁酸(7.5g,75mmol)和naoh(6g,150mmol)溶解于水(40ml),加入氯甲酸苄酯(16.1g,95mmol)的四氢呋喃(32ml)溶液。将反应在0℃搅拌1小时,室温3小时。减压蒸馏除去四氢呋喃,用浓盐酸调节水溶液ph值至3。用乙酸乙酯萃取,饱和食盐水洗,无水硫酸钠干燥,浓缩得到白色固体(16.4g,92%)。msesim/z:c12h16no5[m+h]+计算值:238.10,实测值:238.08。 实施例33.4-(((苄氧基)羰基)氨基)丁酸叔丁酯的合成。 将dmap(0.8g,6.56mmol)和dcc(17.1g,83mmol)加入到4-((((苄氧基)羰基)氨基)丁酸(16.4g,69.2mmol)和叔丁醇(15.4g,208mmol)的二氯甲烷(100ml)溶液中。室温搅拌过夜,将反应物过滤并浓缩滤液。将残留物溶于乙酸乙酯中,用1nhcl,饱和食盐水洗涤,用硫酸钠干燥,过滤,浓缩后通过柱色谱(10至50%乙酸乙酯/石油醚)纯化,得到目标化合物(7.5g,37%产率)msesim/z:c16h23no4na[m+na]+计算值:316.16,实测值:316.13。 实施例34.4-氨基丁酸叔丁酯的合成。 将4-(((苄氧基)羰基)氨基)丁酸叔丁酯(560mg,1.91mmol)溶于甲醇(50ml)中,与pd/c催化剂(10wt%,100mg)混合,然后氢化(1atm)反应3小时。滤出催化剂,减压蒸馏除去所有挥发物,得到标题化合物(272mg,90%产率)。msesim/zc8h18no2[m+h]+计算值:160.13,实测值:160.13。 实施例35.3,3′-(苄基氮杂二基)二丙酸二叔丁酯的合成。 在80℃下,将苯基甲胺(2.0ml,18.29mmol,1.0eq.)和丙烯酸叔丁酯(13.3ml,91.46mmol,5.0eq.)的混合物回流过夜,然后浓缩。通过硅胶柱(20:1正己烷/乙酸乙酯)纯化粗产物,得到标题化合物,为无色油状物(5.10g,77%产率)。esimsm/z:c21h34no4[m+h]+计算值:364.2,实测值:364.2。1hnmr(400mhz,cdcl3)δ7.38–7.21(m,5h),3.58(s,2h),2.76(t,j=7.0hz,4h),2.38(t,j=7.0hz,4h),1.43(s,17h)。 实施例36.3,3′-氮杂二丙基二丙酸二叔丁酯的合成。 在氢化反应瓶中,向3,3′-(苄基氮杂二基)二丙酸二叔丁酯(1.37g,3.77mmol,1.0eq.)的甲醇(10ml)溶液中加入pd/c(0.20g,10%pd/c,含水50%)。将混合物在h2气中振荡过夜,然后通过硅藻土垫过滤。浓缩滤液得到标题化合物,为无色油状物(1.22g,89%产率)。esimsm/z:c14h28no4[m+h]+计算值:274.19,实测值:274.20。 实施例37.4-(2-(((苄氧基)羰基)氨基)丙酰胺基)-丁酸叔丁酯的合成。 在0℃下,向4-氨基丁酸叔丁酯(1.00g,6.28mmol,1.0eq.)和z-l-丙氨酸(2.10g,9.42mmol,1.5eq.)的无水二氯甲烷(50ml)溶液中加入hatu(3.10g,8.164mmol,1.3eq.)和三乙胺(2.6ml,18.8mmol,3.0eq.)。将反应物在0℃下搅拌10分钟,然后加热至室温并搅拌过夜。将混合物用二氯甲烷稀释,用水和盐水洗涤,经无水硫酸钠干燥,浓缩,并通过硅胶柱(10:3石油醚/乙酸乙酯)纯化,得到标题化合物,为无色油状物(1.39g,61%产率)。esimsm/z:c19h29n2o5na[m+h]+计算值387.2,实测值387.2。 实施例38.4-(2-氨基丙酰胺基)丁酸叔丁酯的合成。 在氢化反应瓶中,向4-(2-(((苄氧基)羰基)氨基)丙酰胺基)丁酸叔丁酯(1.39g,3.808mmol,1.0eq.)的甲醇(12ml)溶液中加入pd/c(0.20g,10wt%)。将混合物在氢气中振荡2小时,然后通过硅藻土(助滤剂)过滤,浓缩,得到标题化合物,为浅黄色油状物(0.838g,95%产率)。esimsm/z:c11h23n2o3[m+h]+计算值231.16,实测值231.15。 实施例39.3-(2-(2-(二苄基氨基)乙氧基)乙氧基)丙酸的合成。 在室温下,向3-(2-(2-(二苄基氨基)乙氧基)丙酸叔丁酯(2.3g,5.59mmol,1.0eq)的二氯甲烷(10ml)溶液中加入tfa(5ml)。搅拌90分钟后,将反应混合物用无水甲苯稀释并浓缩,重复该操作三次,得到标题化合物,为浅黄色油状物(2.0g,理论收率),将其直接用于下一步。esimsm/zc21h28no4[m+h]+计算值:358.19,实测值:358.19。 实施例40.五氟苯基3-(2-(2-(二苄基氨基)乙氧基)乙氧基)-丙酯的合成。 在0℃下,向3-(2-(2-(二苄基氨基)乙氧基)乙氧基)丙酸(2.00g,5.59mmol,1.0eq.)在无水二氯甲烷(30ml)的溶液中加入dipea直至ph为中性,然后加入五氟苯酚(1.54g,8.38mmol,1.5eq.)和dic(1.04ml,6.70mmol,1.2eq.)。10分钟后,将反应升温至室温并搅拌过夜。将混合物过滤,浓缩并通过硅胶柱柱色谱(15:1石油醚/乙酸乙酯)纯化,得到标题化合物,为无色油状物(2.10g,72%产率)。esimsm/z:c27h27f5no4[m+h]+计算值:524.2,实测值:524.2。 实施例41.2-苄基-13-甲基-11,14-二氧代-1-苯基-5,8-二氧杂-2,12,15-三氮杂十九烷-19-叔丁酯的合成。 0℃时,向4-(2-氨基丙酰胺基)丁酸叔丁酯(0.736g,3.2mmol,1.0eq.)和五氟苯基3-(2-(2-(二苄基氨基)乙氧基)乙氧基)丙酯(2.01g,3.84mmol,1.2eq.)的无水dma(20ml)溶液中加入dipea(1.7ml,9.6mmol,3.0eq.)。在0℃下搅拌10分钟,将反应升温至室温并搅拌过夜。加入水(100ml)并将混合物用乙酸乙酯(3×100ml)萃取。将合并的有机层用水(3×200ml)和盐水(200ml)洗涤,用无水硫酸钠干燥,过滤,浓缩并通过硅胶柱层析(25:2二氯甲烷/甲醇)纯化,得到标题化合物,为浅黄色油状物(1.46g,80%产率)。esimsm/z:c32h48n3o6[m+h]+计算值:570.34,实测值:570.33。 实施例42.2-苄基-13-甲基-11,14-二氧代-1-苯基-5,8-二氧杂-2,12,15-三氮杂十九烷-19-酸的合成。 在室温下,向2-苄基-13-甲基-11,14-二氧代-1-苯基-5,8-二氧杂-2,12,15-三氮杂十九烷-19-酸叔丁酯(0.057g,0.101mmol,1.0eq.)的二氯甲烷(3ml)溶液中加入tfa(1ml)并搅拌40分钟。用无水甲苯稀释反应物,然后浓缩。重复该操作三次,得到标题化合物,为无色油状物(0.052g,理论产率),将其直接用于下一步骤。esimsm/z:c28h40n3o6[m+h]+计算值:514.28,实测值:514.28。 实施例43.2-(2-(((苄氧基)羰基)氨基)丙酰胺基)-乙酸叔丁酯的合成。 将2-(((苄氧基)羰基)氨基)丙酸(0.84g,5mmol),2-氨基乙酸叔丁酯(0.66g,5mmol),hobt(0.68g,5mmol),edc(1.44g,7.5mmol)溶于二氯甲烷(20ml),然后加入dipea(1.7ml,10mmol)。将反应混合物在室温下搅拌过夜,用水(100ml)洗涤,并将水层用乙酸乙酯萃取。合并有机层,用硫酸镁干燥,过滤,减压浓缩,残余物在硅胶柱上纯化,得到标题产物(0.87g,52%)。esim/z:c17h25n2o5[m+h]+:计算值:337.17,实测值:337.17。 实施例44.2-(2-((苄氧基)羰基)氨基)丙酰胺基)乙酸的合成。 将2-(2-(((苄氧基)羰基)氨基)丙酰胺基)乙酸叔丁酯(0.25g,0.74mmol)溶于二氯甲烷(30ml)中,然后加入tfa(10ml)。将混合物在室温搅拌过夜,浓缩,得到标题化合物,其不经进一步纯化直接用于下一步。esim/z:c13h17n2o5[m+h]+:计算值:281.11,实测值:281.60。 实施例45.3-(2-(2-(2-羟基乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 在搅拌下向350ml无水四氢呋喃中加入80mg(0.0025mol)金属钠和三乙二醇(150.1g,1.00mol)。在钠完全溶解后,加入丙烯酸叔丁酯(24ml,0.33mol)。将溶液在室温下搅拌20小时,然后用8ml1.0mhcl中和。真空除去溶剂,将残余物悬浮在盐水(250ml)中,用乙酸乙酯(3×125ml)萃取。将合并的有机层用盐水(100ml)洗,水(100ml)洗,用硫酸钠干燥,除去溶剂。将得到的无色油状物真空干燥,得到69.78g(76%产率)标题产物。1hnmr:1.41(s,9h),2.49(t,2h,j=6.4hz),3.59-3.72(m,14h)。esimsm/zc13h25o6(m-h)计算值:277.17,实测值:277.20。 实施例46.2,5,8,11,14,17,20,23,26,29-十二氧杂三十一烷-31-酸叔丁基酯的合成。 将nah(60%,8.0g,200mmol)加入到2,5,8,11,14,17,20,23,26-九氧杂二十八烷-28-醇(42.8g,100mmol)的四氢呋喃(1.0l)溶液中。在室温搅拌30分钟后,向混合物中加入2-溴乙酸叔丁酯(48.8g,250mmol),并在室温下搅拌1小时。然后将混合物倒入冰水中,用二氯甲烷萃取,用盐水洗涤有机层,用无水硫酸钠干燥。用柱层析法(0%~5%甲醇:二氯甲烷)纯化,得到黄色油状化合物432(32g,收率59%)。 实施例47.2,5,8,11,14,17,20,23,26,29-十二氧杂三十一烷-31-酸的合成。 将2,5,8,11,14,17,20,23,26,29-十二氧杂三十一烷-31-酸叔丁酯(40.0g,73.8mmol)溶解于二氯甲烷(400ml)中,然后加入甲酸(600ml)。将所得溶液在25℃下搅拌过夜。在真空下除去所有挥发物,得到的标题产物,为黄色油状物(36.0g,理论收率)。esim/zc21h43o12[m+h]+计算值:487.27,实测值:487.24。 实施例48.2,5,8,11,14,17,20,23,26,29-十二氧杂三十一烷-31-酰氯的合成。 向2,5,8,11,14,17,20,23,26,29-十二氧杂三十一烷-31-酸(36.0g,73.8mmol)的二氯甲烷(640ml)溶液中加入(cocl)2(100ml)和dmf(52g,0.74mmol)。在室温下将所得溶液搅拌4小时。在真空下除去所有挥发物,得到黄色油状标题产物。 实施例49.(s)-37-(苄氧)羰基)氨基)-31-氧代-2,5,8,11,14,17,20,23,26,29-十二氧杂-32-氮杂三十八烷-38-酸的合成。 将z-l-lys-oh(41.4g,147.6mmol),na2co3(23.4g,221.4mmol)和naoh(5.9g,147.6mmol)溶于水(720ml)中。将混合物冷却至0℃,向其中加入2,5,8,11,14,17,20,23,26,29-十二氧杂三十一烷-31-酰氯(37.2g,73.8mmol)的四氢呋喃(20ml)溶液。将所得混合物在室温下搅拌1小时。在真空下除去四氢呋喃,并将浓hcl加入冰冷下的水溶液中直至ph达到3。用二氯甲烷萃取后,将有机层用盐水洗涤,用硫酸钠干燥并浓缩,得到标题产物,为黄色油状物(55g,收率99%)。esimsm/zc35h60n2o15[m+h]+:计算值:749.40,实测值:749.39。 实施例50.(s)-13-(2-(((苄氧基)羰基)氨基)-5-(叔丁氧基)-5-氧代戊烷酰胺基)十三烷酸叔丁酯的合成。 向(s)-2-(((苄氧基)羰基)氨基)-5-(叔丁氧基)-5-氧代戊酸(3.50g,10.38mmol)和13-氨基十三烷酸叔丁酯(3.00g,10.51mmol)的dmf(70ml)溶液中加入edc(10.00g,52.08mmol)和tea(1.60ml,11.16mmol)。将反应在室温下搅拌8小时,真空浓缩,用饱和盐水(80ml)和乙酸乙酯(100ml)稀释,分离。水层用乙酸乙酯(50ml×3)萃取,合并的有机相用100ml饱和盐水洗涤一次,然后用无水硫酸钠干燥,过滤并浓缩。通过硅胶柱色谱(乙酸乙酯/二氯甲烷,1:15)纯化残余物,得到标题化合物(5.45g,收率87%),esimsm/z:c34h57n2o7[m+h]+:计算值:605.41,实测值:605.38。 实施例51.(s)-13-(2-氨基-5-(叔丁氧基)-5-氧代戊烷酰胺基)十三烷酸叔丁酯的合成。 向13-(2-(((苄氧基)羰基)氨基)-5-(叔丁氧基)-5-氧代戊烷酰胺基)十三烷酸叔丁酯(2.80g,4.63mmol)的dma(100ml)溶液中加入10%pd/c(0.41g),将混合物在氢气下室温中搅拌18小时。然后通过硅藻土过滤除去pd/c,并用dma洗涤滤床。浓缩滤液,得到黄色泡沫状产物,其无需进一步纯化即可用于下一步(2.19g,收率101%)。esimsm/z:c26h51n2o5[m+h]+计算值:471.37,实测值:471.80。 实施例52.2,2-二甲基-4,17-二氧代-3,7,10,13,20,23,26-七氧杂-16-氮杂二十九烷-29-酸的合成 在3-(2-(2-(2-氨基乙氧基)乙氧基)丙酸叔丁酯(6.00g,21.64mmol)和3,3′-(氧代双(乙烷-2,1-二基))双(氧基))二丙酸(21.01g,84.00mmol)的dma(200ml)溶液中加入edc(18.00g,93.75mmol)和dipea(5.00g,38.75mmol)。将混合物搅拌过夜,然后浓缩并通过硅胶柱色谱法纯化(甲醇:二氯甲烷=1:12至1:5),得到标题化合物,为白色油状物(9.15g,86%收率)。esimsm/z:c23h44no11[m+h]+计算值:510.28,实测值:510.55。 实施例53.1-苄基39叔丁基14,26-二氧代-4,7,10,17,20,23,30,33,36-壬氧基-13,27-二氮杂三十九烷-1,39-二酯的合成。 在(s)-叔丁基13-(2-氨基-5-(叔丁氧基)-5-氧代戊烷酰胺基)十三烷酯(5.11g,10.03mmol)和3-(2-(2-氨基乙氧基)乙氧基)乙氧基)丙酸酯(3.21g,10.31mmol)的dma(100ml)溶液中加入edc(8.02g,41.77mmol)和dipea(3.00g,23.25mmol)。将混合物搅拌过夜,然后浓缩并通过硅胶柱色谱法纯化(乙酸乙酯:二氯甲烷=1:8至1:3),得到标题化合物,为白色油状物(7.01g,87%收率)。esimsm/z:c39h67n2o15[m+h]+计算值:803.44,实测值:803.80。 实施例54.3,16,28-三氧代-1-苯基-2,6,9,12,19,22,25,32,35,38-十氧杂-15,29-二氮杂四十一烷-41-酸的合成。 将1-苄基39叔丁基14,26-二氧代-4,7,10,17,20,23,30,33,36-十三烷-13,27-二氮杂三十九烷-1,39-二酯(6.90g,8.60mmol)溶于hcooh(50ml)中并在0-4℃下搅拌1小时。将反应混合物用甲苯(50ml)稀释,浓缩并与甲苯共蒸发两次,并将残余物置于真空泵上得标题化合物(6.45g,产率约101%,粗产物)。esimsm/z:c35h59n2o15[m+h]+计算值:747.38,实测值:747.50。 实施例55.1-苄基39-(2,5-二氧代吡咯烷-1-基)14,26-二氧代-4,7,10,17,20,23,30,33,36-九氧杂-13,27-二氮杂三十九烷-1,39-二酯。 在3,16,28-三氧代-1-苯基-2,6,9,12,19,22,25,32,35,38-十氧杂-15,29-二氮杂四十一烷-41-酸(4.01g,5.37mmol)和nhs(n-羟基琥珀酰亚胺)(0.68g,5.91mmol)的dma(100ml)溶液中加入edc(1.52g,7.92mmol)和dipea(0.50g,3.87mmol)。将混合物搅拌过夜,然后浓缩并通过硅胶柱色谱法纯化(乙酸乙酯:二氯甲烷=1:8至1:4),得到标题化合物,为白色泡沫状物(4.17g,收率92%)。esimsm/z:c39h62n3o17[m+h]+计算值:844.40,实测值:844.85。 实施例56.(s)-47-(((苄氧基)羰基)氨基)-3,16,28,41-四氧代-1-苯基-2,6,9,12,19,22,25,32,35,38-十氧杂-15,29,42-三氮四十八烷-48-酸的合成。 向(s)-6-氨基-2-(((苄氧基苄氧基)羰基)氨基)氨基)己酸(1.38g,4.92mmol)的dma(30ml)和100mmnah2po4,ph7.5缓冲液(40ml)中,在2小时内分4份加入1-苄基39-(2,5-二氧代吡咯烷-1-基)14,26-二氧代-4,7,10,17,17,20,23,30,33,33,36-九氧杂-13,27-二氮杂三十九烷-1,39-二酯(4.15g,4.92mmol)。将混合物搅拌4小时,然后浓缩并通过硅胶柱色谱法纯化(甲醇:二氯甲烷=1:7至1:4),得到标题化合物,为白色泡沫状物(4.07g,收率82%)。esimsm/z:c49h77n4o18[m+h]+计算值:1009.51,实测值:1009.90。 实施例57.(s)-1-苄基51-(2-(三甲基甲硅烷基)乙基)45-(((苄氧基)-羰基)氨基)-14,26,39,46-四氧代-4,7,10,17,20,23,30,33,36-九氧杂-13,27,40,47-四氮杂五十一烷-1,51-二酯的合成。 向(s)-47-(((苄氧基)羰基)氨基)-3,16,28,41-四氧代-1-苯基-2,6,9,12,19,22,25,32的溶液中加入35,38-十氧杂-15,29,42-三氮杂四十八烷-48-酸(4.00g,3.96mmol)和2-(三甲基甲硅烷基)4-氨基丁酸乙酯(0.90g,4.43mmol)的dma(25ml)溶液中,加入edc(2.03g,10.57mmol)。将混合物搅拌6小时,然后浓缩并通过硅胶柱色谱法纯化(甲醇:二氯甲烷=1:15至1:8),得到标题化合物,为白色泡沫状物(3.97g,收率84%)。esimsm/z:c58h96n5o19si[m+h]+计算值:1194.64,实测值:1194.90。 实施例58.12-氨基-2,2-二甲基-6,11,18,31,43-五氧代-5,21,24,27,34,37,40,47,50,53-十氧代-10,17,30,44-四氮杂-2-五十六烷-56-酸的合成。 在氢化瓶中向(s)-1-苄基51-(2-(三甲基甲硅烷基)乙基)45-(((苄氧基)-羰基)氨基)-14,26,39,46-四氧代-4,7,10,17,20,23,30,33,36-九氧杂-13,27,40,47-四氮杂苯基戊烷-1,51-二酯(3.90g,3.33mmol)的甲醇(40ml)溶液中加入pd/c(10wt%,0.20g)。将混合物在40psi氢气下振荡2小时,通过硅藻土(助滤剂)过滤,浓缩滤液,得到标题化合物(3.16g,收率98%),其不经进一步纯化直接用于下一步。esimsm/z:c43h83n5o17si[m+h]+计算值:970.55,实测值:970.70。 实施例59.2,5-二氧代吡咯烷-1-基4-((3ar,7r,7as)-1,3-二氧代-3a,4,7,7a-四氢-1h-4,7-环氧异吲哚-2(3h))-基)丁酸酯的合成。 在压力容器中将4-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丁酸(10.0g,54.62mmol)和呋喃(5ml,68.74mmol)的乙醚(90ml)溶液在170℃加热6小时,然后将溶液冷却至室温,真空浓缩并在etoh/正己烷中结晶,得到4-((3ar,7r,7as)-1,3-二氧代-3a,4,7,7a-四氢-1h-4,7-环氧异吲哚-2(3h)-基)丁酸(11.24g,44.76mmol,收率82%)。然后重新溶解在二氯甲烷(100ml)中,加入nhs(7.00g,60.86mmol)和edc(25.00g,130.20mmol)。将混合物搅拌6小时,然后浓缩并通过硅胶柱色谱法纯化(乙酸乙酯:二氯甲烷=1:8至1:5),得到标题化合物,为白色泡沫状物(13.57g,收率87%)。esimsm/z:c16h17n2o7[m+h]+:计算值:349.09,实测值:349.55。 计算值60.2,3-双(2-溴乙酰氨基)琥珀二酰氯的合成。 向thf/h2o/dipea(125ml/125ml/8ml)的混合物中加入2,3-二氨基琥珀酸(5.00g,33.77mmol)和2-溴乙酰溴(25.0g,125.09mmol)。将混合物搅拌过夜,蒸发并通过硅胶柱色谱法(水/乙腈5:95)纯化,得到浅黄色油状物2,3-双(2-溴乙酰氨基)琥珀酸(9.95g,收率76%)。esimsm/z:c8h11br2n2o6[m+h]+计算值:388.89,实测值:388.68。 向2,3-双(2-溴乙酰氨基)琥珀酸(3.50g,9.02mmol)的二氯甲烷(80ml)溶液中加入草酰氯(5.80g,46.05mmol)和dmf(0.01ml)。将混合物搅拌2.5小时,用甲苯稀释,浓缩并与二氯乙烷(2×20ml)和甲苯(2×15ml)共蒸发至干,得到2,3-双(2-溴乙酰氨基)琥珀二酰氯(粗品,不稳定),用于下一步而无需进一步纯化(3.90g,收率102%)。esimsm/z:c8h9br2cl2n2o4[m+h]+计算值:424.82,实测值:424.90。 实施例61.2,3-双(((苄氧基)羰基)氨基)琥珀酸的合成。 向2,3-二氨基琥珀酸(4.05g,27.35mmol)的四氢呋喃(250ml)和nah2po4(0.1m,250ml,ph8.0)的混合物中,在两小时内分4份加入苄基氯甲酸酯(15.0g,88.23mmol)。将混合物再搅拌6小时,浓缩并上样到硅胶柱上,用含有1%甲酸的水/乙腈(1:9)洗脱,得到标题化合物(8.65g,收率76%,纯度~95%)。esimsm/z:c20h21n2o8[m+h]+计算值:417.12,实测值:417.60。 实施例62.双(2,5-二氧代吡咯烷-1-基)2,3-双(((苄氧基)羰基)-氨基)琥珀酸酯的合成。 向2,3-双(((苄氧基)羰基)氨基)琥珀酸(4.25g,10.21mmol)的dma(70ml)溶液中加入nhs(3.60g,31.30mmol)和edc(7.05g,36.72mmol)。将混合物搅拌过夜,浓缩并上样到硅胶柱上,用乙酸乙酯/二氯甲烷(1:6)洗脱得到标题化合物(5.42g,收率87%,纯度~95%)。esimsm/z:c28h27n4o12[m+h]+计算值:611.15,实测值:611.60。 实施例63.4,4′-((2,3-双(((苄氧基)羰基)氨基)-琥珀酰基)双(氮杂二基))丁酸二叔丁酯的合成。 向2,3-双(((苄氧基)羰基)氨基)琥珀酸(4.25g,10.21mmol)的dma(70ml)混合物中加入4-氨基丁酸叔丁酯(3.25g,20.42mmol))和edc(7.01g,36.70mmol)。浓缩并上样到硅胶柱上,用乙酸乙酯/二氯甲烷(1:10)洗脱,得到标题化合物(6.56g,收率92%,纯度~95%)。esimsm/z:c36h51n4o10[m+h]+计算值:699.35,实测值:699.55。 实施例64.4,4′-((2,3-二氨基琥珀酰基)双(氮杂二基))-丁酸二叔丁酯的合成。 向4,4′-((2,3-双(((苄氧基)羰基)氨基)-琥珀酰基)双-(氮杂二基))二丁酸二叔丁酯(2.50g,3.58mmol)的甲醇(100ml)溶液中加入10%pd/c(0.30g,50%湿),将混合物在氢气中室温下搅拌18小时。然后通过硅藻土过滤除去pd/c,并用甲醇(~70ml)洗涤滤床。浓缩滤液,得到黄色泡沫状产物,其无需进一步纯化即可用于下一步(1.55g,收率101%)。esimsm/z:c20h39n2o6[m+h]+计算值:431.28,实测值:431.40。 实施例65.4,4′-((2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯的合成。 向3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酸(1.25g,7.39mmol)的dma(60ml)溶液中加入4,4′-((2,3-二氨基琥珀酰基)双(氮杂二基))-二丁酸二叔丁基酯(1.55g,)和edc(2.41g,12.61mmol)。将混合物搅拌过夜,浓缩并上样到硅胶柱上,用乙酸乙酯/二氯甲烷(1:10)洗脱,得到标题化合物(2.33g,收率89%)。esimsm/z:c34h49n6o12[m+h]+计算值:733.33,实测值733.50。 实施例66.4,4′-((2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸的合成。 向搅拌的4,4′-((2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯(2.30g,3.14mmol)的1,4-二氧六环(20ml)溶液中加入hcl(36%,7.0ml)。将混合物搅拌30分钟,用甲苯(20ml)稀释,浓缩并上样到硅胶柱上,用甲醇/二氯甲烷(1:10至1:4)洗脱,得到标题化合物(1.67g,收率85%)。esimsm/z:c26h33n6o12[m+h]+计算值:621.21,实测值:621.55。 实施例67.4,4′-((2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯的合成。 向2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酸(1.12g,7.22mmol)的dma(60ml)溶液中加入4,4′-((2,3-二氨基琥珀酰基)双-(氮杂二基))二丁酸二叔丁基酯(1.55g,~3.58mmol)和edc(2.40g,12.56mmol)。将混合物搅拌过夜,浓缩并上样到硅胶柱上,用乙酸乙酯/二氯甲烷(1:10)洗脱,得到标题化合物(2.27g,收率90%)。esimsm/z:c32h45n6o12[m+h]+计算值:704.30,实测值:704.55。 计算值68.4,4′-((2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)琥珀酰基)双(氮杂二基))二丁酸的合成。 向4,4′-((2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯(2.20g,3.12mmol)的1,4-二氧六环(20ml)溶液中加入hcl(36%,7.0ml)。将混合物搅拌30分钟,用甲苯(20ml)稀释,浓缩并上样到硅胶柱上,用甲醇/二氯甲烷(1:10至1:4)洗脱,得到标题化合物(1.67g,85%收率)。esimsm/z:c24h29n6o12[m+h]+593.18,found593.50。 实施例69.双(2,5-二氧代吡咯烷-1-基)4,4′-(2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)琥珀酰基)双(氮杂二基))二丁酸酯。 向4,4′-((2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-琥珀酰基)双(氮杂二基))二丁酸(1.10g,1.85mmol)的dma(30ml)溶液中加入nhs(1-羟基吡咯烷-2,5-二酮)(0.55g,4.78mmol)和edc(1.25g,6.54mmol)。将混合物搅拌过夜,浓缩并上样到硅胶柱上,用乙酸乙酯/二氯甲烷(1:10)洗脱,得到标题化合物(1.28g,收率88%)。esimsm/z:c32h35n8o16[m+h]+计算值:787.21,实测值:787.50。 实施例70.2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸的合成。 向2,3-二氨基琥珀酸(5.00g,33.77mmol)的thf/h2o/dipea(125ml/125ml/2ml)的混合溶液中加入马来酸酐(6.68g,68.21mmol)。将混合物搅拌过夜,蒸发,得到2,3-双((z)-3-羧基丙烯酰胺基)琥珀酸(11.05g,收率99%),为白色固体。esimsm/z:c12h13n2o10[m+h]+计算值:345.05,实测值:345.35。 向2,3-双((z)-3-羧基丙烯酰胺基)琥珀酸(11.05g,33.43mmol)在hoac(70ml),dmf(10ml)和甲苯(50ml)的混合溶液中的乙酸酐(30毫升)。将混合物搅拌2小时,用dean-stark分水器在100℃回流6小时,浓缩,用etoh(2×40ml)和甲苯(2×40ml)共浓缩,并在硅胶柱上纯化。水/乙腈(1:10)洗脱,得到标题化合物(7.90g,收率76%,纯度~95%)。esimsm/z:c12h9n2o8[m+h]+计算值:309.03,实测值:309.30。 实施例71.双(2,5-二氧代吡咯烷-1-基)2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸酯的合成。 向2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸(4.00g,12.98mmol)的dmf(70ml)混合溶液中加入nhs(3.60g,31.30mmol)和edc(7.05g,36.72mmol)。将混合物搅拌过夜,浓缩并上样到硅胶柱上,用乙酸乙酯/二氯甲烷(1:6)洗脱,得到标题化合物(5.73g,收率88%,hplc纯度~96%)。esimsm/z:c20h15n4o12[m+h]+计算值:503.06,实测值:503.45。 实施例72.(3s,6s,39s,42s)-6,39-二叔丁基(4-((叔丁氧基羰基)氨基)丁基)-22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,42-双((4-(羟甲基)苯基)氨基甲酰基)-5,8,21,24,37,40-六氧代-11,14,17,28,31,34-六氧杂-4,7,20,25,38,41-六氮杂四十四烷-1,44-二酯的合成。 向(14s,17s)-叔丁基1-氨基-14-(4-((叔丁氧羰基)氨基)丁基)-17-((4-(羟甲基)苯基)氨基甲酰基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十九烷-19-酯(1.43g,1.97mmol)和2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸的dma(25ml)溶液中,加入edc(1.30g,6.77mmol)。将混合物搅拌过夜,真空蒸发,减压浓缩,在硅胶柱上纯化,用甲醇/二氯甲烷(5%-8%)洗脱,得到标题化合物(1.33g,80%产率)。esimsm/z:c82h123n12o28[m+h]+,计算值1722.85,实测值1722.98。 实施例73.1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸叔丁酯的合成。 向3-(2-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)丙酸(1.55g,6.27mmol),2-(2-氨基丙酰胺基)丙酸叔丁酯(1.35g,6.27mmol)的dma(60ml)溶液中,加入edc(3.05g,15.88mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:3)洗脱,得到标题化合物(2.42g,86%产率,hplc纯度约95%)。esimsm/z:c19h36n5o7[m+h]+计算值446.25,实测值446.60。 实施例74.1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸的合成。 向1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸叔丁酯(2.20g,4.94mmol)的1,4-二恶烷(40ml)溶液中加入浓hcl(12m,10ml)。将混合物搅拌40分钟,用二恶烷(20ml)和甲苯(40ml)稀释,浓缩,并与二恶烷(20ml)和甲苯(40ml)共浓缩至干,得到标题粗产物,用于下一步,无需进一步纯化(1.92g,100%产率,hplc纯度约94%)。esimsm/z:c15h28n5o7[m+h]+计算值390.19,实测值390.45。 实施例75.21,22-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧代-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二酸的合成。 在氢化反应器中,向1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸(1.90g,4.88mmol)的dma(40ml)溶液中加入pd/c(0.20克,含水50%)。将系统在真空下抽空,并在剧烈搅拌下通入2atm的氢气,在室温下搅拌6小时,tlc显示原料消失。将反应粗品通过短硅藻土垫过滤,用乙醇洗。滤液减压浓缩,得到粗产物1-氨基-1,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸的dma溶液,直接用于下一步。esimsm/z:c15h30n3o7(m+h),计算值364.20,实测值364.30。 向上述氨基化合物的dma(~30ml)溶液中加入0.1mnah2po4(ph7.5,20ml),然后加入双(2,5-二氧代吡咯烷-1-基)2,3-双(2,5-)二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸酯(1.30g,2.59mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用含8%水的乙腈溶液洗脱,得到标题化合物(1.97g,81%产率)。esimsm/z:c42h63n8o20[m+h]+,计算值999.41,实测值999.95。 实施例76.双(2,5-二氧代吡咯烷-1-基)21,22-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧代-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二酯的合成。 向21,22-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧代-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二酸(1.50g,1.50mmol)的dma(10ml)的溶液中加入nhs(0.60g,5.21mmol)和edc(1.95g,10.15mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:4至2:1)洗脱,得到标题化合物(1.50g,83%产率,hplc纯度约95%)。esimsm/z:c50h69n10o24[m+h]+计算值1193.44,实测值1193.95。 实施例77.(s)-2-(羟甲基)吡咯烷-1-羧酸叔丁酯的合成。 将溶解在50ml四氢呋喃中的boc-l-脯氨酸(10.0g,46.4mmol)冷却至0℃,向其中小心地加入bh3的四氢呋喃溶液(1.0m,46.4ml)。将混合物在0℃下搅拌1.5小时,然后倒入冰水中并用乙酸乙酯萃取。将有机层用盐水(50ml)洗涤,经无水硫酸钠干燥,并在减压下浓缩,得到标题化合物(8.50g,91%产率),为白色固体。1h-nmr(500mhz,cdcl3)δ3.94(dd,j=4.9,2.7hz,2h),3.60(ddd,j=18.7,11.9,9.3hz,2h),3.49–3.37(m,1h),3.34–3.23(m,1h),2.06–1.91(m,1h),1.89–1.69(m,2h),1.65–1.51(m,1h),1.49–.40(m,9h)。 实施例78.(s)-2-甲酰基吡咯烷-1-羧酸叔丁酯的合成。 向(s)-2-(羟甲基)吡咯烷-1-羧酸叔丁酯(13.0g,64.6mmol)的二甲基亚砜(90ml)的溶液中加入三乙胺(40ml),搅拌15分钟。将混合物在冰浴上冷却,并在40分钟内分批加入三氧化硫-吡啶络合物(35.98g,226mmol)。将反应升温至室温并搅拌2.5小时。加入冰(250g)后,将混合物用二氯甲烷(150ml×3)萃取。将有机相用50%柠檬酸溶液(150ml),水(150ml),饱和碳酸氢钠溶液(150ml)和盐水(150ml)洗涤,经无水硫酸钠干燥。在真空中除去溶剂,得到标题醛(10.4g,81%产率),为稠油状物,不经进一步纯化而使用。1h-nmr(500mhz,cdcl3)δ9.45(s,1h),4.04(s,1h),3.53(dd,j=14.4,8.0hz,2h),2.00–1.82(m,4h),1.44(d,j=22.6hz,9h)。 实施例79.(4r,5s)-4-甲基-5-苯基-3-丙酰基恶唑烷-2-酮的合成。 在-78℃,n2条件下,向正丁基锂的正己烷(21.6ml,2.2m,47.43mmol)溶液中滴加4-甲基-5-苯基恶唑烷-2-酮(8.0g,45.17mmol)的四氢呋喃(100ml)溶液。将溶液在-78℃保持1小时,然后缓慢加入丙酰氯(4.4ml,50.59mmol)。将反应混合物升温至-50℃,搅拌2小时,然后用饱和氯化铵溶液(100ml)淬灭。真空除去有机溶剂,用乙酸乙酯(3×100ml)萃取水溶液。用饱和碳酸氢钠溶液(100ml)和盐水(100ml)洗涤有机相,无水硫酸钠干燥,过滤并减压浓缩。通过柱层析(20%乙酸乙酯/正己烷)纯化残余物,得到标题化合物,为稠油状物(10.5g,98%产率)。1h-nmr(500mhz,cdcl3)δ7.45–7.34(m,3h),7.30(d,j=7.0hz,2h),5.67(d,j=7.3hz,1h),4.82–4.70(m,1h),2.97(dd,j=19.0,7.4hz,2h),1.19(t,j=7.4hz,3h),0.90(d,j=6.6hz,3h)。 实施例80.(s)-2-((1r,2r)-1-羟基-2-甲基-3-((4r,5s)-4-甲基-2-氧代-5-苯基恶唑烷-3-基))-3-氧代丙基)吡咯烷-1-羧酸叔丁基酯的合成。 在0℃下,向(4r,5s)-4-甲基-5-苯基-3-丙酰基恶唑烷-2-酮(9.40g,40.4mmol)的二氯甲烷(60ml)溶液中加入三乙胺(6.45ml,46.64mmol),然后加入1m二丁基硼三氟甲磺酸酯的二氯甲烷(42ml,42mmol)溶液。将混合物在0℃下搅拌45分钟,冷却至-70℃,然后在30分钟内缓慢加入(s)-2-甲酰基吡咯烷-1-羧酸叔丁酯(4.58g,22.97mmol)的二氯甲烷(40ml)溶液。将反应混合物在-70℃下搅拌2小时,0℃下搅拌1小时,室温下搅拌15分钟,然后用磷酸盐缓冲溶液(ph7,38ml)淬灭。在低于10℃下加入甲醇-30%h2o2溶液(2:1,100ml),搅拌20分钟后,加入水(100ml)并将混合物减压浓缩。向残余物中加入更多的水(200ml),用乙酸乙酯(3×100ml)萃取混合物。用1nkhso4(100ml),碳酸氢钠溶液(100ml)和盐水(100ml)洗涤有机相,用无水硫酸钠干燥并减压浓缩。通过快速柱层析(10%-50%乙酸乙酯/正己烷)纯化残余物,得到标题化合物,为白色固体(7.10g,71%产率).1h-nmr(500mhz,cdcl3)δ7.39(dt,j=23.4,7.1hz,3h),7.30(d,j=7.5hz,2h),5.67(d,j=7.1hz,1h),4.84–4.67(m,1h),4.08–3.93(m,3h),3.92–3.84(m,1h),3.50(d,j=9.0hz,1h),3.24(d,j=6.7hz,1h),2.15(s,1h),1.89(dd,j=22.4,14.8hz,3h),1.48(d,j=21.5hz,9h),1.33(d,j=6.9hz,3h),0.88(d,j=6.4hz,3h)。 实施例81.(s)-2-((1r,2r)-1-甲氧基-2-甲基-3-((4r,5s)-4-甲基-2-氧代-5-苯基恶唑烷-3-基)的合成)-3-氧代丙基)吡咯烷-1-羧酸叔丁酯。 在n2中,向(s)-2-((1r,2r)-1-羟基-2-甲基-3-((4r,5s)-4-甲基-2-氧代-5-苯基恶唑烷-3-基)-3-氧代丙基)吡咯烷-1-羧酸叔丁基酯(5.1g,11.9mmol)和分子筛(5g)的混合物中加入无水二氯乙烷(30ml)。将混合物在室温下搅拌20分钟并冷却至0℃,加入质子海绵(6.62g,30.9mmol),然后加入三甲基氧鎓四氟硼酸盐(4.40g,29.7mmol)。在0℃下继续搅拌2小时,在室温下搅拌48小时。过滤反应混合物,浓缩滤液,并通过柱层析(20-70%乙酸乙酯/正己烷)纯化,得到标题化合物,为白色固体(1.80g,35%产率)。1h-nmr(500mhz,cdcl3)δ7.46–7.27(m,5h),5.65(s,1h),4.69(s,1h),3.92(s,1h),3.83(s,1h),3.48(s,3h),3.17(s,2h),2.02–1.68(m,5h),1.48(d,j=22.3hz,9h),1.32(t,j=6.0hz,3h),0.91–0.84(m,3h)。 实施例82.(2r,3r)-3-((s)-1-(叔丁氧基羰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸的合成。 在0℃下,在5分钟内向(s)-2-((1r,2r)-1-甲氧基-2-甲基-3-((4r,5s)-4-甲基-2-氧代-5-苯基恶唑烷-3-基)-3-氧代丙基)吡咯烷-1-甲酸-(3)-氧代丙基)吡咯烷-1-羧酸叔丁酯(1.80g,4.03mmol)的四氢呋喃(30ml)和水(7.5ml)溶液中加入30%h2o2(1.44ml,14.4mmol)。然后加入lioh(0.27g,6.45mmol)的水溶液(5ml)。在0℃下搅拌3小时后,加入1n亚硫酸钠(15.7ml)并将混合物升温至室温且搅拌过夜。真空除去四氢呋喃,水相用二氯甲烷(3×50ml)洗涤,除去恶唑烷酮助剂。用1n盐酸将水相酸化至ph3并用乙酸乙酯(3×50ml)萃取。用盐水(50ml)洗涤有机层,用无水硫酸钠干燥,过滤并减压浓缩,得到标题化合物,为无色油状物(1.15g,98%产率)。1h-nmr(500mhz,cdcl3)δ3.99–3.74(m,2h),3.44(d,j=2.6hz,3h),3.23(s,1h),2.60–2.45(m,1h),1.92(tt,j=56.0,31.5hz,3h),1.79–1.69(m,1h),1.58–1.39(m,9h),1.30–1.24(m,3h)。 实施例83.(2r,3r)-3-甲氧基-2-甲基-3-((s)-吡咯烷-2-基)丙酸甲酯的合成。 在0℃下,向(2r,3r)-3-((s)-1-(叔丁氧基羰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸(0.86g,2.99mmol)的甲醇(10ml)溶液中缓慢加入氯化亚砜(1.08ml,14.95mmol)。将反应升温至室温并搅拌过夜。将混合物减压浓缩,与甲苯共浓缩,得到标题化合物(0.71g,100%产率),为白色固体,无需进一步纯化即可用于下一步。hrms(esi)m/z:c10h20no3[m+h]+计算值202.14,实测值202.14。 实施例84.(4s,5s)-4-((叔丁氧基羰基)氨基)-5-甲基-3-氧代庚酸乙酯的合成。 向用冰冷却的n-boc-l-异亮氨酸(4.55g,19.67mmol)的四氢呋喃(20ml)溶液中加入1,1’-羰基二咪唑(3.51g,21.63mmol)。待气体停止产生后,将所得混合物升温至室温,搅拌3.5小时。 5℃下,向新制备的异丙基溴化镁的四氢呋喃(123mmol,30ml)溶液中滴加预冷至(0℃)的丙二酸单乙酯(6.50g,49.2mmol)溶液。然后将混合物在室温下搅拌1.5小时。将该烯醇镁溶液在冰水浴上冷却,并在1小时内通过双头针向其中加入咪唑化物溶液。将所得混合物在0℃下搅拌30分钟,然后在室温下搅拌64小时。通过加入10%柠檬酸水溶液(5ml)淬灭反应,并用另外的10%柠檬酸水溶液(110ml)酸化至ph3。用乙酸乙酯(3×150ml)萃取混合物。将有机萃取液用水(50ml),饱和碳酸氢钠水溶液(50ml)和饱和氯化钠水溶液(50ml)洗涤,用无水硫酸钠干燥,并减压浓缩。残留物通过硅胶柱层析纯化,用乙酸乙酯/正己烷(1:4)作为洗脱液,得到标题化合物(5.50g,93%产率)。1h-nmr(500mhz,cdcl3)δ5.04(d,j=7.8hz,1h),4.20(p,j=7.0hz,3h),3.52(t,j=10.7hz,2h),1.96(d,j=3.7hz,1h),1.69(s,2h),1.44(s,9h),1.28(dd,j=7.1,2.9hz,3h),0.98(t,j=6.9hz,3h),0.92–0.86(m,3h)。 实施例85.(3r,4s,5s)-4-((叔丁氧基羰基)氨基)-3-羟基-5-甲基庚酸乙酯的合成。 在-60℃下向(4s,5s)-4-((叔丁氧基羰基)氨基)-5-甲基-3-氧代庚酸乙酯(5.90g,19.83mmol)的乙醇(6ml)溶液中一次性加入硼氢化钠(3.77g,99.2mmol)。将反应混合物在-55℃下搅拌5.5小时,然后用10%柠檬酸水溶液(100ml)淬灭。用另外的10%柠檬酸水溶液将所得溶液酸化至ph2,然后用乙酸乙酯(3×100ml)萃取。用饱和氯化钠水溶液(100ml)洗涤有机物,用无水硫酸钠干燥,并减压浓缩。通过柱层析(10-50%乙酸乙酯/正己烷)纯化残余物,得到标题化合物,为非对映异构体(2.20g,37%产率)和两种非对映异构体的混合物(2.0g,34%产率,约9:1比率)。1h-nmr(500mhz,cdcl3)δ4.41(d,j=9.3hz,1h),4.17(tt,j=7.1,3.6hz,2h),4.00(t,j=6.9hz,1h),3.55(dd,j=11.7,9.3hz,1h),2.56–2.51(m,2h),2.44(dd,j=16.4,9.0hz,1h),1.79(d,j=3.8hz,1h),1.60–1.53(m,1h),1.43(s,9h),1.27(dd,j=9.3,5.0hz,3h),1.03–0.91(m,7h)。 实施例86.(3r,4s,5s)-4-((叔丁氧基羰基)氨基)-3-羟基-5-甲基庚酸的合成。 向(3r,4s,5s)-4-((叔丁氧基羰基)氨基)-3-羟基-5-甲基庚酸乙酯(2.20g,7.20mmol)的乙醇(22ml)溶液中加入1n氢氧化钠(7.57ml,7.57mmol)。将混合物在0℃下搅拌30分钟,然后在室温下搅拌2小时,通过加入1n盐酸水溶液将所得溶液酸化至ph4,然后用乙酸乙酯(3×50ml)萃取。将有机萃取液用1n硫酸氢钾水溶液(50ml)和饱和氯化钠水溶液(50ml)洗涤,用无水硫酸钠干燥,并减压浓缩,得到化合物(1.90g,95%产率)。1h-nmr(500mhz,cdcl3)δ4.50(d,j=8.7hz,1h),4.07(d,j=5.5hz,1h),3.59(d,j=8.3hz,1h),2.56–2.45(m,2h),1.76–1.65(m,1h),1.56(d,j=7.1hz,1h),1.45(s,9h),1.26(t,j=7.1hz,3h),0.93(dd,j=14.4,7.1hz,6h)。 实施例87.(3r,4s,5s)-4-(((叔丁氧羰基)(甲基)氨基)-3-甲氧基-5-甲基庚酸的合成。 向(3r,4s,5s)-4-((叔丁氧基羰基)氨基)-3-羟基-5-甲基庚酸(1.90g,6.9mmol)的四氢呋喃(40ml)溶液中加入氢化钠(在0℃下,60%矿物油中,1.93g,48.3mmol)。搅拌1小时后,加入碘甲烷(6.6ml,103.5mmol)。在0℃下继续搅拌40小时,然后加入饱和碳酸氢钠水溶液(50ml)淬灭反应,接着加入水(100ml)。将混合物用乙醚(2×50ml)洗涤,并将水层用1n硫酸氢钾水溶液酸化至ph3,然后用乙酸乙酯(3×50ml)萃取。将合并的有机萃取液用5%硫代硫酸钠水溶液(50ml)和饱和氯化钠水溶液(50ml)洗涤,用无水硫酸钠干燥,减压浓缩,得到标题化合物(1.00g,48%产率)。1h-nmr(500mhz,cdcl3)δ3.95(d,j=75.4hz,2h),3.42(d,j=4.4hz,3h),2.71(s,3h),2.62(s,1h),2.56–2.47(m,2h),1.79(s,1h),1.47(s,1h),1.45(d,j=3.3hz,9h),1.13–1.05(m,1h),0.96(d,j=6.7hz,3h),0.89(td,j=7.2,2.5hz,3h)。 实施例88.boc-n-me-l-val-oh的合成。 在0℃下,向boc-l-缬氨酸-oh(2.00克,9.2mmol)和碘甲烷(5.74ml,92mmol)的无水四氢呋喃(40ml)溶液中加入氢化钠(3.68克,92mmol)。将反应混合物在0℃下搅拌1.5小时,然后升温至室温并搅拌24小时。用冰水(50ml)淬灭反应,加入水(100ml)后,将反应混合物用乙酸乙酯(3×50ml)洗涤,将水溶液酸化至ph3,然后用乙酸乙酯(3×50ml)萃取。将合并的有机相用无水硫酸钠干燥并浓缩,得到白色固体boc-n-me-val-oh(2.00g,94%产量)。1h-nmr(500mhz,cdcl3)δ4.10(d,j=10.0hz,1h),2.87(s,3h),2.37–2.13(m,1h),1.44(d,j=26.7hz,9h),1.02(d,j=6.5hz,3h),0.90(t,j=8.6hz,3h)。 实施例89.(2r,3r)-3-((s)-1-((3r,4s,5s)-4-((叔丁氧羰基)-(甲基)氨基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸甲酯的合成。 在0℃下,向(2r,3r)-3-甲氧基-2-甲基-3-((s)-吡咯烷-2-基)丙酸甲酯(0.71g,2.99mmol)和(3r,4s,5s)-4-((叔丁氧基羰基)(甲基)氨基)-3-甲氧基-5-甲基庚酸(1g,3.29mmol)的dmf(10ml)溶液中加入氰基膦酸二乙酯(545μl,3.59mmol),然后加入三乙胺(1.25ml,8.99mmol)。将反应混合物在0℃下搅拌2小时,然后升温至室温并搅拌过夜。反应混合物用乙酸乙酯(50ml)稀释,用1n硫酸氢钾水溶液(20ml),水(20ml),饱和碳酸氢钠水溶液(20ml)和饱和氯化钠水溶液(20ml)洗涤,用硫酸钠干燥,并减压浓缩。将残余物在硅胶柱色谱上纯化,用乙酸乙酯/正己烷(1:5至2:1)洗脱,得到标题化合物(0.9g,62%产率),为白色固体。hrms(esi)m/z:c25h46n2o7[m+h]+计算值487.33,实测值487.32。 实施例90.(s)-2-((1r,2r)-1-甲氧基-3-(((s)-1-甲氧基-1-氧代-3-苯基丙-2-基)氨基)-2-甲基-3-氧代丙基)吡咯烷-1-羧酸叔丁酯的合成。 在0℃下,向(2r,3r)-3-((s)-1-(叔丁氧基羰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸(100mg,0.347mmol)和l-苯丙氨酸甲酯盐酸盐(107.8mg,0.500mmol)的dmf(5ml)溶液中加入氰基膦酸二乙酯(75.6μl,0.451mmol),然后加入三乙胺(131μl,0.94mmol)。将反应混合物在0℃下搅拌2小时,然后升温至室温并搅拌过夜。然后将反应混合物用乙酸乙酯(80ml)稀释,用1n硫酸氢钾水溶液(40ml),水(40ml),饱和碳酸氢钠水溶液(40ml)和饱和氯化钠水溶液(40)洗涤。用无水硫酸钠干燥,减压浓缩。通过柱层析(15-75%乙酸乙酯/正己烷)纯化残余物,得到标题化合物(130mg,83%产率),为白色固体。1h-nmr(500mhz,cdcl3)δ7.28(dd,j=7.9,6.5hz,2h),7.23(t,j=7.3hz,1h),7.16(s,2h),4.81(s,1h),3.98–3.56(m,5h),3.50(s,1h),3.37(d,j=2.9hz,3h),3.17(dd,j=13.9,5.4hz,2h),3.04(dd,j=14.0,7.7hz,1h),2.34(s,1h),1.81–1.69(m,2h),1.65(s,3h),1.51–1.40(m,9h),1.16(d,j=7.0hz,3h)。 实施例91.用三氟乙酸去除boc官能团的一般操作。 向n-boc-氨基酸(1.0mmol)的二氯甲烷(2.5ml)的溶液中加入三氟乙酸(1.0ml)。在室温下搅拌1-3小时后,反应混合物在真空中浓缩。与甲苯共蒸发得到脱保护产物,未经进一步纯化即可使用。 实施例92.(2r,3r)-甲基3-((s)-1-((3r,4s,5s)-4-((s)-2-((叔丁氧羰基)氨基)-n,3-二甲基丁胺基)-3-甲氧基-5-甲基庚烷酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸酯的合成。 在0℃下,向(2r,3r)-3-甲氧基-3-((s)-1-((3r,4s,5s)-3-甲氧基-5-甲基-4-(甲氨基)庚酰基)吡咯烷-2-基)甲酯-2-甲基丙酸甲酯(715mg,1.85mmol)去boc保护产物和boc-val-oh(1.2g,5.56mmol)的二氯甲烷(20ml)溶液中加入brop(1.08g,2.78mmol)),然后加入二异丙基乙胺(1.13ml,6.48mmol)。将混合物在暗处,0℃下搅拌30分钟,然后在室温下搅拌48小时。反应混合物用乙酸乙酯(50ml)稀释,用1n硫酸氢钾水溶液(20ml),水(20ml),饱和碳酸氢钠水溶液(20ml)和饱和氯化钠水溶液(20ml))洗涤,用硫酸钠干燥,并减压浓缩。将残余物在硅胶柱上纯化,用乙酸乙酯/正己烷(1:5至4:1)洗脱,得到标题化合物(0.92g,85%产率),为白色固体。hrms(esi)m/z:c30h55n3o8[m+h]+计算值586.40,实测值586.37。 实施例93.(2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丁酰胺)-3-甲氧基-5-甲基庚基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸甲酯。 在0℃时,向(2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((叔丁氧基羰基)氨基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸甲酯(50mg,0.085mmol)的去boc保护产物和五氟苯基2-(二甲基氨基)-2-甲基丙酸酯(74.5mg,0.25mmol)的dmf(2ml)溶液中加入dipea(44μl,0.255mmol)。将反应混合物升温至室温并搅拌2小时,然后用乙酸乙酯(30ml)稀释,用水(10ml)和饱和氯化钠水溶液(10ml)洗涤,经硫酸钠干燥,并减压浓缩。将残余物在硅胶柱上纯化,用乙酸乙酯/正己烷(1:5至5:1)洗脱,得到标题化合物(50mg,100%产率)。hrms(esi)m/z:c31h58n4o7[m+h]+计算值599,实测值599。 实施例94.(2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丁胺基)-3-甲氧基-5-甲基庚烷酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸的合成。 在0-4℃下,向(2r,3r)-甲基3-((s)-1-((3r,4s,5s)-4-((s)-2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丁胺基)-3-甲氧基-5-甲基庚烷酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸酯(50mg,0.0836mmol)的1,4-二氧六环(3ml)溶液,逐滴加入氢氧化锂(14mg,0.334mmol)的水溶液(3ml)。将反应混合物升温至室温,搅拌2小时,用1nhcl酸化至ph7,真空浓缩,无需进一步纯化,直接用于下一步。hrms(esi)m/zc30h57n4o7[m+h]+计算值:585.41,实测值:585.80。 实施例95.(2r,3r)-五氟苯基3-((s)-1-((3r,4s,5s)-4-((s)-2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丁胺基)-3-甲氧基-5-甲基庚烷酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸酯的合成。 在0℃时,向(2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丁酰胺)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸(0.0836mmol)和五氟苯酚(18.5mg,0.1mmol)的二氯甲烷(2ml)溶液中加入dic(12.7mg,0.1mmol)。将混合物升温至室温并搅拌过夜。将反应混合物减压浓缩,不经进一步纯化即用于下一步。hrms(esi)m/z:c36h56f5n4o7[m+h]+计算值751.40,实测值751.70。 实施例96.(s)-2-((叔丁氧羰基)氨基)-3-(4-羟基-3-硝基苯)丙酸甲酯的合成。 向boc-l-酪氨酸甲酯(5g,16.9mmol)的四氢呋喃(50ml)溶液中加入亚硝酸叔丁酯(10ml,84.6mmol),然后将反应混合物在室温下搅拌5小时。浓缩反应混合物,并通过硅胶柱纯化,用乙酸乙酯/正己烷(1:10至1:5)洗脱,得到化合物(4.5g,78%产率),为黄色固体。hrms(esi)m/z:c15h21n2o7[m+h]+计算值341.13,实测值341.30。 实施例97.3-(3-氨基-4-羟基苯基)-2-(叔丁氧羰基)氨基)丙酸甲酯的合成。 向(s)-3-(3-氨基-4-羟基苯基)-2-(叔丁氧基羰基氨基)丙酸甲酯(2g,6.44mmol)的乙酸乙酯(20ml)溶液中加入pd/c(0.2g),在氢气环境下搅拌2小时。过滤混合物,减压浓缩滤液,得到标题化合物(1.7g,95%产率),为白色固体。hrms(esi)m/z:c15h23n2o5[m+h]+计算值311.15,实测值311.30。 实施例98.(2s)-甲基3-(8,9-双(3-(2,5-二氧基-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15-四氧基-3,4,5,6,7,8,9,10,11,12,13,14,15,16-十四氢-2h-苯并[b][1,4,9,14]氧杂三氮杂环十八烷-18-基)-2-((叔丁氧羰基)氨基)丙酸酯的合成。 于0℃下向4,4’-((2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰胺基)-琥珀酰)双(氮杂二酰基))二丁酸(108.0mg,0.182mmol)和(s)-3-(3-氨基-4-羟基苯基)-2-(叔丁氧基羰基氨基)丙酸甲酯(56.6mg,0.182mmol)的dmf(5ml)溶液中加入edc(130mg,0.678mmol),随后加入dipea(64μl,0.365mmol)。将反应混合物升温至室温并搅拌过夜。将混合物用乙酸乙酯(30ml)稀释,用水(10ml)和饱和氯化钠水溶液(10ml)洗涤,用硫酸钠干燥并真空浓缩。将残余物在硅胶柱色谱上纯化,用二氯甲烷/甲醇(20:1至10:1)洗脱,得到标题化合物(110.6mg,收率68%)。hrms(esi)m/zc41h51n8o15[m+h]+计算值:895.34,实测值:895.30。 实施例99.(2s)-2-氨基-3-(8,9-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15-四氧代-3,4,5,6,7,8,9,10,11,12,13,14,15,16-十四氢-2h-苯并[b][1,4,9,14]氧代三氮杂环十八烷-18-基)丙酸甲酯的合成。 在0℃,向(2s)甲基-3-(8,9-双(3-(3-(2,5,5-二氧代-2,5,5,5-二甲基-1-1-吡咯-1-基)丙炔基)-2,7,7,10,15,15-四氧代-3,5,6,7,8,9,10,11,12,13,14,15,15,16-十四氢-2h-苯并[b][1,4,9,9,14]氧代三氮杂环十八烷基-18-基)-2-((叔丁氧基羰基)氨基)氨基)丙酸酯(100.2mg,100.2mg,0.112mmol)的二氯甲烷(6ml)溶液中加入tfa(2ml)。将反应混合物升温至室温并搅拌30分钟,用甲苯稀释,浓缩,用甲苯共蒸发,然后无需进一步纯化即可用于下一步。hrms(esi)m/zc36h43n8o13[m+h]+计算值:795.29,实测值:795.45。 实施例100.(2s)-甲基3-(8,9-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15-四氧代-3,4,5,6,7,8,9,10,11,12,13,14,15,16-十四氢-2h-苯并[b][1,4,9,14]氧代三氮杂环十八烷-18-基)-2-(((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-(2-(甲基氨基)-(2-甲基丙酰胺基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)丙酸酯(a-01)的合成。 在0℃下,向(2r,3r)-五氟苯基3-((s)-1-((3r,4s,5s)-4-((s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸酯(20mg,0.027mmol)和(2s)-2-氨基-3-甲基(8),9-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15-四氧代-3,4,5,6,7,8,9,10,11,12,13,14,15,16-十四氢-2h-苯并[b][1,4,9,14]氧杂三氮杂-环十八烷基-18-基)丙酸甲酯(31.7mg,0.04mmol)的dma(2ml)溶液中加入dipea(9μl,0.053mmol)。将反应混合物升温至室温并搅拌30分钟。将混合物真空浓缩并通过制备hplc纯化(c-18,250mm×10mm,用水/乙腈,9ml/分钟,40分钟内从90%调整到40%洗脱),得到标题化合物(16mg,收率43%)。hrms(esi)m/zc66h97n12o19[m+h]+计算值:1361.69实测值:1361.50。 实施例101.(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((叔丁氧基羰基)(甲基)氨基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯的合成。 在0℃下,向(s)-2-((1r,2r)-1-甲氧基-3-(((s)-1-甲氧基-1-氧代-3-苯基丙-2-基)氨基)-2-甲基-3-氧代丙基)吡咯烷-1-羧酸叔丁基酯(0.29mmol)和(3r,4s,5s)-4-((叔丁氧基羰基)(甲基)氨基)-3-甲氧基-5-甲基庚酸(96.6mg,0.318mmol)的dmf(5ml)溶液中加入氰基磷酸二乙酯(58μl,0.347mmol),然后加入et3n(109μl,0.78mmol)。将反应混合物在0℃下搅拌2小时,然后升温至室温并搅拌过夜。将反应混合物用乙酸乙酯(80ml)稀释,用1n硫酸氢钾水溶液(40ml),水(40ml),饱和碳酸氢钠水溶液(40ml)和饱和氯化钠水溶液(40ml)洗涤,用硫酸钠干燥并真空浓缩。通过柱色谱法(15-75%乙酸乙酯/正己烷)纯化残余物,得到标题化合物(150mg,81%收率),为白色固体。lc-ms(esi)m/zc34h55n3o8[m+h]+计算值:634.40,实测值:634.40。 实施例102.(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((叔丁氧基羰基)氨基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯的合成。 在0℃下,向(s)-甲基2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((叔丁氧羰基)(甲基)氨基)-3-甲氧基-5-甲基庚酰基)-吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸酯(0.118mmol)和boc-val-oh(51.8mg,0.236mmol)的dcm(5ml)溶液中加入brop(70.1mg,0.184mmol),然后加入二异丙基乙胺(70μl,0.425mmol)。将混合物避光,并在0℃下搅拌30分钟,然后在室温下搅拌2天。将反应混合物用乙酸乙酯(80ml)稀释,用1n硫酸氢钾水溶液(40ml),水(40ml),饱和碳酸氢钠水溶液(40ml)和饱和氯化钠水溶液(40ml)洗涤。用硫酸钠干燥并真空浓缩,残余物通过柱色谱法纯化(20-100%乙酸乙酯/正己烷),得到标题化合物(67mg,收率77%),为白色固体。lc-ms(esi)m/zc39h64n4o9[m+h]+计算值:733.47,实测值:733.46。 实施例103.(s)-2-((2r,3r)-3-((s)-1-((6s,9s,12s,13r)-12-((s)-仲丁基)-6,9-二异丙基-13-甲氧基-2,2,5,11-四甲基-4,7,10-三氧代-3-氧杂-5,8,11-三氮杂十五烷-15-基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯的合成。 在0℃下,向(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((叔丁氧基羰基)氨基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯(0.091mmol)的boc-脱保护产物和boc-n-me-val-oh(127mg,0.548mmol)的dmf(5ml)溶液中加入氰基磷酸二乙酯(18.2μl,0.114mmol),然后加入n-甲基吗啉(59μl,0.548mmol)。将反应混合物在0℃下搅拌2小时,然后升温至室温并搅拌过夜。将反应混合物用乙酸乙酯(80ml)稀释,用1n硫酸氢钾水溶液(40ml),水(40ml),饱和碳酸氢钠水溶液(40ml)和饱和氯化钠水溶液洗涤。用硫酸钠干燥,真空浓缩。通过柱色谱法(20-100%乙酸乙酯/己烷)纯化残余物,得到标题化合物(30mg,收率39%),为白色固体。lc-ms(esi)m/zc45h75n5o10[m+h]+计算值:846.55,实测值:846.56。 实施例104.(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-n,3-二甲基-2-((s)-3-甲基-2-(甲基氨基)丁酰胺基)丁酰胺基)-3-甲氧基-5-甲基-庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯的合成。 向(s)-甲基2-((2r,3r)-3-((s)-1-((6s,9s,12s,13r)-12-((s)-仲丁基)-6,9-二异丙基-13-甲氧基-2,2,5,11-四甲基-4,7,10-三氧代-3-氧杂-5,8,11-三氮杂十五烷-15-酰)吡咯烷-2-基)-3-甲氧基-2-甲基丙氨酰基)-3-苯基丙酸甲酯(75.0mg,0.0886mmol)的二氯甲烷(5ml)溶液中加入三氟乙酸(2ml),在室温下搅拌1小时后,真空浓缩反应混合物。与甲苯共蒸发得到脱保护的标题产物,无需进一步纯化即可使用。 实施例105.(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-n,3-二甲基-2-((s)-3-甲基-2-(甲基氨基)丁酰胺基)丁酰胺基)-3-甲氧基-5-甲基庚酰基)-吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸的合成。 将(s)-甲基2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-n,3-二甲基-2-((s)-3-甲基-2-(甲基氨基)丁酰胺基)丁酰胺基)-3-甲氧基-5-甲基-庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸酯(25mg,0.030mmol)的浓盐酸(0.3ml)和1,4-二氧六环(0.9ml)的溶液,在室温下搅拌35分钟。将混合物用etoh(1.0ml)和甲苯(1.0ml)稀释,浓缩并与etoh/甲苯共蒸发(2:1),得到标题化合物,为白色固体(22mg,收率约100%),其不经进一步纯化即用于下一步。lc-ms(esi)m/zc39h66n5o8[m+h]+计算值:732.48,实测值:732.60。 实施例106.(2s)-2-((2r,3r)-3-((2s)-1-((11s,14s,17s)-1-叠氮基-17-((r)-仲丁基)-11,14-二异丙基-18-甲氧基-10,16-二甲基-9,12,15-三氧代-3,6-二氧杂-10,13,16-三氮杂二十烷-20-酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸的合成。 向(s)-2-((2r,3r)-3-((s)-1-((3r,4s,4s,5)-4-((s)-n,3-二甲基-2-((s)-3-甲基-2-(甲基氨基)丁酰胺基)丁酰氨基)-3-甲氧基-5-甲基庚酰基基)-吡咯烷基-2-基-3-甲氧基-2-甲基丙甲酰氨基)-3-甲氧基-3-甲氧基-3-甲基丙酰胺基)-3-苯基丙酸(22mg,0.030毫摩尔)粗品在dma(0.8ml)和nah2po4缓冲溶液(ph7.5,1.0m,0.7ml)中,在2小时内分四次加入2,5-二氧代吡咯烷-1-基3-(2-(2-叠氮基乙氧基)丙酸酯(18.0mg,0.060mmol),搅拌过夜,浓缩并用硅胶柱色谱法纯化(ch3oh/二氯甲烷/hoac1:8:0.01),得到标题化合物(22.5mg,82%收率)。lc-ms(esi)m/zc46h77n8o11[m+h]+计算值:917.56,实测值:917.60。 实施例107.(2s)-2-((2r,3r)-3-((2s)-1-((11s,14s,17s)-1-氨基-17-((r)-仲丁基)-11,14-二异丙基-18-甲氧基-10,16-二甲基-9,12,15-三氧基-3,6-二氧基-10,13,16-三氮杂二十烷-20-酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸的合成。 在氢化瓶中,向(2s)-2-((2r,3r)-3-((2s)-1-((11s,14s,17s)-1-叠氮基-17-((r)-叔丁基)-11,14-二异丙基-18-甲氧基-10,16-二甲基-9,12,15-三氧-3,6-氧代-3,6-二氧杂-10,13,16-三氮杂-20-基-20-基基)吡咯烷基-2-基)-3-甲氧基-2-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸(22.0mg,0.024mmol)的甲醇(5ml)溶液中,加入pd/c(5mg,10%pd,50%水)。抽真空并导入h2(25psi)后,将混合物振荡4小时,通过硅藻土过滤。浓缩滤液,得到粗标题产物(~20mg,收率92%),用于下一步,无需进一步纯化。esimsm/zc46h79n6o11(m+h)计算值:891.57,实测值:891.60。 实施例108.(s)-2-((2r,3r)-3-((s)-1-((6s,9s,12s,13r)-12-((s)-仲丁基)-6,9-二异丙基-13-甲氧基-2,2,5,11-四甲基-4,7,10-三氧代-3-氧杂-5,8,11-三氮杂十五碳-15-基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸。 向(s)-(2r,3r)-3-((s)-1-((6s,9s,12s,13r)-12-((s)-仲丁基)-(s)-6,9-二异丙基-13-甲氧基2,2,5,1-1四甲基-4,7,10-三氧代-3-氧杂-5,8,11-三氮杂十五烷-15酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯(30mg,0.035mmol)的四氢呋喃(1.0ml)溶液中加入lioh水溶液(1.0m,0.8ml)。将混合物在室温下搅拌35分钟,用0.5mh3po4调节ph至6,浓缩并在硅胶柱上纯化(甲醇/二氯甲烷/hoac1:10:0.01),得到标题化合物(25.0mg,85%产率)。lc-ms(esi)m/z:c44h74n5o10[m+h]+计算值832.54,实测值832.60。 实施例109.(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-n,3-二甲基-2-(s)-3-甲基-2-(甲基氨基)丁酰胺基)丁酰胺基)-3-甲氧基-5-甲基庚酰基)-吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸的合成。 向(s)-2-((2r,3r)-3-((s)-1-((6s,9s,12s,13r)-12-((s)-仲丁基)-6,9-二异丙基-13-甲氧基-2,2,5,11-四甲基-4,7,10-三氧代-3-氧杂-5,8,11-三氮杂十五烷-15-酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸(25mg,0.030mmol)的二恶烷(2.0ml)溶液中加入浓盐酸(12n,0.6ml)。将混合物在室温下搅拌30分钟,用二恶烷(4ml)和甲苯(4ml)稀释,浓缩并用c18hplc纯化,用甲醇和水洗脱(l200mm×φ20mm,9ml/min,40分钟从5%甲醇至40%甲醇),得到标题化合物(20.0mg,90%产率)。lc-ms(esi)m/z:c39h66n5o8[m+h]+计算值732.48,实测值732.90。 实施例110.(s)-2-((2r,3r)-3-((s)-1-((5s,8s,11s,14s,15r)-14-((s)-仲丁基)-8,11-二异丙基-15-甲氧基-5,7,13三甲基-3,6,9,12-四氧代-1-苯基-2-氧杂-4,7,10,13-四氮杂十七烷-17-酰基)吡咯烷吡啶-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯的合成。 在0℃下,依次向mmaf-ome(0.132g,0.178mmol,1.0eq.)和z-l-丙氨酸(0.119g,0.533mmol,3.0eq.)的无水二氯甲烷(10ml)溶液中加入hatu(0.135g,0.356mmol,2.0eq.)和nmm(0.12ml,1.07mmol,6.0eq.)。将反应物在0℃下搅拌10分钟,然后升温至室温并搅拌过夜。将混合物用二氯甲烷稀释,用水和盐水洗涤,经无水硫酸钠干燥,浓缩,并通过硅胶柱色谱(20:1二氯甲烷/甲醇)纯化,得到标题化合物,为白色泡沫状固体(0.148g,88%产率)。esimsm/z:c51h79n6o11[m+h]+计算值951.6,实测值951.6。 实施例111.(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-((s)-2-氨基-n-甲基丙酰胺基)-3-甲基丁酰胺基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基庚基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯的合成。 在氢化反应瓶中,将pd/c(0.100g,10%pd/c,含水50%)加入到(s)-2-((2r,3r)-3-((s)-1-((5s,8s,11s,14s,15r)-14-((s)-仲丁基)-8,11-二异丙基-15-甲氧基-5,7,13三甲基-3,6,9,12-四氧代-1-苯基-2-氧杂-4,7,10,13-四氮杂十七烷-17-酰基)吡咯烷吡啶-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯(0.148g,0.156mmol,1.0eq.)的甲醇(5ml)溶液中。将混合物在氢气中振荡5小时,然后通过硅藻土垫过滤。浓缩滤液,得到标题化合物,为白色泡沫状固体(0.122g,96%产率)。esimsm/z:c43h73n6o9[m+h]+计算值817.5,实测值817.5。 实施例112.(2s)-2-(((2r,3r)-3-((2s)-1-((46s,49s,52s,55s,56r)-55-((s)-仲-丁基)-37,38-双(2-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)乙酰氨基)-1-羟基-49,52-二异丙基-56-甲氧基-46,48,54-三甲基-31,36,39,44,47,50,53-七氧代-3,6,9,12,15,18,21,24,27-九氧杂-30,35,40,45,48,51,54-七氮杂五十八烷-58-酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯(a-02)。 (a-2) 和(副产物) 向(s)-甲基2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-((s)-2-氨基-n-甲基丙酰胺基)-3-甲基丁酰胺基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基-庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸酯(0.122g,0.149mmol,1.0eq)和4,4′-((2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯)-1-基乙酰胺基)-琥珀酰基)双(氮杂二基)二丁酸(0.177g,0.298mmol,4.0eq)的无水dma(10ml)溶液中加入hatu(0.270g,0.712mmol)和nmm(0.030ml,0.267mmol)。将反应搅拌2小时,然后加入29-氨基-3,6,9,12,15,18,21,24,27-九氧杂烷-1-醇(0.205mg,0.448mmol)。将反应混合物继续搅拌过夜,然后真空浓缩并通过硅胶柱色谱(10:1至5:1,二氯甲烷/甲醇)纯化,得到标题化合物(a-2),为白色泡沫状固体(0.128g,47%收率,esimsm/z:c87h140n13o29[m+h]+计算值1830.98,实测值1830.70)和副产物2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-n1,n4-双(1-羟基-31-氧代-3,6,9,12,15,18,21,24,27-九氧杂-30-氮杂三十四烷-34-基)琥珀酰胺(84mg,收率38%),esimsm/z:c64h111n8o30[m+h]+计算值:1471.73,实测值:1471.95)。 实施例113.(2s)-2-(((2r,3r)-3-((2s)-1-((56s,59s,62s,63r)-62-((s)-仲丁基)-37,38-双(2-(2-,2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-1-羟基-56,59-二异丙基-63-甲氧基-55,61-二甲基-31,36,39,44,54,57,60-七氧代-3,6,9,12,15,18,21,24,27,48,51-十一烷-30,35,40,45,55,58,61-七氮杂六十五烷-65-酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸(a-3)的合成。 向(2s)-2-(((2r,3r)-3-((2s)-1-((11s,14s,17s)-1-氨基-17-((r)-仲丁基)-11,14-二异丙基-18-甲氧基-10,16-二甲基-9,12,15-三氧-3,6-二氧杂-10,13,16-三氮杂-20-酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸(0.155g,0.174mmol,1.0eq)的dma(10ml)和pbs缓冲液(10ml,0.1mnah2po4,ph5.0)的混合溶液中,加入双(2,5-二氧杂吡咯烷-1-基)4,4′-(((2,3-双(2-(2,5-二氧杂-2,5-二氢-1h-吡咯-1-基)乙酰氨基)琥珀酰基)双(氮杂二氮杂)二丁酸酯(0.275g,0.349mmol,4.0eq)。将混合物搅拌4小时,然后加入29-氨基-3,6,9,12,15,18,21,24,27-壬氧杂环戊烷-1-醇(0.205mg,0.448mmol)。用饱和碳酸氢钠溶液将反应混合物调节至ph7.5并继续搅拌过夜。将混合物真空浓缩并通过反相hplc(250mm×20mm,c18柱,10-80%乙腈/水,40分钟,v=10ml/min)纯化,得到标题化合物(142.1mg,收率43%),esimsm/z:calcdforc90h146n13o31[m+h]+计算值:1905.02,实测值:1905.80)和副产物2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-n1,n4-双(1-羟基-31-氧代-3,6,9,12,15,18,21,24,27-九氧杂-30-氮杂三十四烷-34-基)琥珀酰胺(89mg,收率35%),esimsm/z:c64h111n8o30[m+h]+计算值:1471.73,实测值:1471.95。 实施例114.(2s,2’s)-2,2′-((((2r,2’r,3r,3’r)-3,3′-((2s,2’s)-1,1′-((3r,4s,7s,10s,47s,50s,53s,54r)-4,53-二((s)-仲丁基)-28,29-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-7,10,47,50-四异丙基-3,54-二甲氧基-5,11,46,52-四甲基-6,9,12,22,27,30,35,45,48,51-十氧杂-15,18,39,42-四氧杂-5,8,11,21,26,31,36,46,49,52-十氮杂五十六烷-1,56-二芳基双(吡咯烷-2,1-二基)双(3-甲氧基-2-甲基丙酰基)双(氮杂二基)双(3-苯基丙酸)(a-04)的合成。 向(2s)-2-((2r,3r)-3-((2s)-1-((11s,14s,17s)-1-氨基-17-((r)-仲丁基)-11,14-二异丙基-18-甲氧基-10,16-二甲氧基-9,12,15-三氧基-3,6-二氧代-10,13,16-三氮杂-20-甲氧基-2-基吡啶-2-基)-3-甲氧基-2-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸(0.155g,0.174mmol,0.1eq)的dma(10ml)和pbs缓冲液(10ml,0.1mnah2po4,ph7.5)的混合溶液中,加入双(2,5-二氧代吡咯烷-1-基)4,4′-(2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰胺基)琥珀酰基)双(氮杂二基))二丁酸酯(0.068g,0.087mmol,1.0eq)。将混合物搅拌8小时,真空浓缩并通过反相hplc(250mm×20mm,c18柱,10-80%乙腈/水,40分钟,v=10ml/min)纯化,得到标题化合物(138.1mg,收率68%)。esimsm/z:c116h181n18o32[m+h]+计算值:2338.30,实测值:2338.90。 实施例115.(s,e)-2-甲基-n-(3-甲基丁-2-亚基)丙烷-2-磺酰胺的合成。 在n2保护下,室温向(s)-叔丁基亚磺酸胺(100g,0.825mol)的四氢呋喃(1l)溶液中加入ti(oet)4(345ml,1.82mol)和3-甲基-2-丁酮(81ml,0.825mol)。加热反应液,回流16小时后冷却至室温,然后倒入冰水(1l)。过滤并且用乙酸乙酯洗滤饼。分离滤液中的有机相,无水硫酸钠干燥后减压浓缩,其残留物减压蒸馏(15-20torr,95℃)得目标产物(141g,90%产率),为黄色油状物。1hnmr(500mhz,cdcl3)δ2.54–2.44(m,1h),2.25(s,3h),1.17(s,9h),1.06(dd,j=6.9,5.1hz,6h)。esimsm/z:c9h19nanos[m+na]+:计算值212.12,实测值212.11。 实施例116.(2s,3s)-2-叠氮-3-甲基戊酸的合成。 将nan3(20.0g,0.308mol)溶于水(50ml),加入二氯甲烷(80ml)并冷却至0℃,向该溶液中加入tf2o(10ml,59.2mmol)。加完后在0℃下继续搅拌2小时。分离出有机相,水相用二氯甲烷萃取(2×40ml)。合并有机相,用饱和碳酸氢钠(3×80ml)洗。室温下将此二氯甲烷溶液加入到(l)-异亮氨酸(4.04g,30.8mmol),碳酸钾(6.39g,46.2mmol),五水硫酸铜(77.4mg,0.31mmol)的混合甲醇/水(1:2v/v,300ml)溶液中。加料过程中反应体系内温度会稍微升高。混合液在室温下搅拌16小时,减压蒸去溶剂,水相用水(250ml)稀释,用浓盐酸(大约280ml)酸化至ph6,然后用磷酸盐缓冲液稀释(0.25m,ph6.2,250ml),用乙酸乙酯(5×100ml)洗去磺酸胺副产物。水相用浓盐酸酸化至ph2后用乙酸乙酯(3×150ml)萃取。合并有机相,无水硫酸钠干燥,过滤浓缩得标题化合物(4.90g,99%产率),为亮黄色油状物。1hnmr(500mhz,cdcl3)δ12.01(s,1h),3.82(d,j=5.9hz,1h),2.00(ddd,j=10.6,8.6,5.5hz,1h),1.54(dqd,j=14.8,7.5,4.4hz,1h),1.36–1.24(m,1h),1.08–0.99(m,3h),0.97–0.87(m,3h)。 实施例117.d-n-甲基哌啶酸的合成。 向d-呱啶酸(10.0g,77.4mmol,1.0eq)的甲醇(100ml)溶液中加入甲醛(37%水溶液,30.8ml,154.8mmol,2.0eq)和pd/c(10wt%,1.0g)。将该反应液在h2(1atm)环境中搅拌过夜,而后用硅藻土过滤,用甲醇洗涤滤垫。减压浓缩滤液,获得标题化合物,为白色固体(10.0g,收率90%)。 实施例118.(r)-五氟苯基1-甲基哌啶-2-羧酸酯的合成。 向d-n-甲基呱啶酸(2.65g,18.5mmol)的乙酸乙酯(50ml)溶液中加入五氟苯酚(3.75g,20.4mmol)和dcc(4.21g,20.4mmol)。反应在室温下搅拌16小时,硅藻土过滤,用10ml乙酸乙酯洗。滤液不用进一步纯化,直接使用。esimsm/z:c13h13f5no2[m+h]+计算值309.08;实测值309.60。 实施例119.五氟苯基2-(二甲基氨基)-2-甲基丙酸酯的合成。 在0℃下向2-(二甲基氨基)-2-甲基丙酸(5.00g,38.10mmol)的乙酸乙酯(200ml)溶液中加入2,3,4,5,6-五氟苯酚(10.4g,57.0mmol),然后加入dic(8.8ml,57.0mmol)。将反应混合物升温至室温,搅拌过夜并过滤。浓缩滤液,得到标题化合物(12.0g,>100%产率),不经进一步纯化即用于下一步。esimsm/z:c12h13f5no2[m+h]+计算值298.08;实测值298.60。 实施例120.2,2-二乙氧基乙烷硫代酰胺的合成。 将二乙氧基乙腈(100g,0.774mol)溶解于甲醇(1.5l),在室温下加入(nh4)2s(48%水溶液,143ml,1.05mol)。搅拌16h后,浓缩反应液。向残留物中加入二氯甲烷,用饱和碳酸氢钠溶液洗,饱和食盐水洗,之后用无水硫酸钠干燥,过滤后减压浓缩。粗品用石油醚和二氯甲烷打浆,真空抽滤,收集固体并用石油醚洗涤。总共得到100g(79%产率)目标产物,为白色固体。1hnmr(500mhz,cdcl3)δ7.81(d,j=71.1hz,2h),5.03(s,1h),3.73(dq,j=9.4,7.1hz,2h),3.64(dq,j=9.4,7.0hz,2h),1.25(t,j=7.1hz,6h)。 实施例121.2-(二乙氧基甲基)噻唑-4-羧酸乙酯的合成。 将分子筛(90g)加入2,2-二乙氧基乙烷硫代酰胺(100g,0.61mol,1.0eq)和3-溴丙酮酸乙酯(142ml,1.1mol,1.8eq.)的乙醇溶液(1l)。随后将反应液加热至回流(反应液温度约60℃)并搅拌1h,旋蒸除去乙醇。向残留物中加入二氯甲烷,过滤,滤液浓缩,通过硅胶柱纯化(1:5-1:3乙酸乙酯/石油醚),得到黄色油状物,为目标化合物(130g,82%产率)。 实施例122.2-甲酰基噻唑-4-羧酸乙酯的合成。 向2-(二乙氧基甲基)噻唑-4-羧酸乙酯(130g,0.50mol)的丙酮(1.3l)溶液中加入2nhcl溶液(85ml,0.165mmol),加热至回流(反应液温度约60℃)。tlc显示起始原料反应完全后(约1-2h),减压除去丙酮,残留物用二氯甲烷稀释(1.3l),并依次用饱和碳酸氢钠水溶液、水和食盐水洗,然后用无水硫酸钠干燥。滤出干燥剂后浓缩有机相,所得粗产品用石油醚/乙醚溶液打浆,析出的固体经真空过滤收集,得白色固体(40g,43%产率)。1hnmr(500mhz,cdcl3)δ10.08–10.06(m,1h),8.53–8.50(m,1h),4.49(q,j=7.1hz,2h),1.44(t,j=7.1hz,3h)。esimsm/z:c7h8no3s[m+h]+:计算值186.01,实测值186.01。 实施例123.2-((r,e)-3-(((s)-叔丁基亚硫酰基)亚氨基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯的合成。 在n2保护下,于-78℃下向二异丙胺(121ml,0.86mol)的四氢呋喃溶液中加入正丁基锂溶液(2.5m,302ml,0.76mol)。反应在30分钟内升温至0℃然后重新冷却至-78℃,向其中加入(s,e)-2-甲基-n-(3-甲基丁-2-亚基)丙烷-2-磺酰胺(57g,0.30mol)的四氢呋喃(200ml)溶液。搅拌1小时后滴加clti(oipr)3(168.5g,0.645mol)的四氢呋喃(350ml)溶液。搅拌1小时后再缓慢滴入2-甲酰基噻唑-4-羧酸乙酯(40g,0.215mol)的四氢呋喃(175ml)溶液,所得溶液在-78℃继续搅拌2小时。tlc监测反应进行完全后,用乙酸和四氢呋喃(体积比1:4,200ml)的混合液淬灭反应,而后将反应液倒入冰水,用乙酸乙酯萃取(4×500ml)。有机相用水和食盐水洗,无水硫酸钠干燥,过滤并浓缩。残留物经柱层析(二氯甲烷/乙酸乙酯/石油醚2:1:2)纯化,得标题化合物(60g,74%产率),为无色油状物。1h-nmr(500mhz,cdcl3)δ8.13(s,1h),6.63(d,j=8.2hz,1h),5.20–5.11(m,1h),4.43(q,j=7.0hz,2h),3.42–3.28(m,2h),2.89(dt,j=13.1,6.5hz,1h),1.42(t,j=7.1hz,3h),1.33(s,9h),1.25–1.22(m,6h)。esimsm/z:c16h26nan2o4s2[m+na]+计算值397.13,实测值397.11。 实施例124.2-((1r,3r)-3-((s)-1,1-二甲基乙基亚磺酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯的合成。 将2-((r,e)-3-(((s)-叔丁基亚磺酰基)亚氨基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯(23.5g,62.7mol)溶于四氢呋喃(200ml),冷却至-45℃,向其中缓慢加入ti(oet)4(42.9ml,188mol),加完后搅拌1小时。然后分批加入nabh4(4.75g,126mmol),反应在-45℃搅拌3小时。tlc监测发现起始原料仍有剩余。将反应用hoac/thf(v/v1:4,25ml)淬灭,缓慢加入乙醇(25ml),将反应液倒入冰水(100g),升至室温。经过硅藻土过滤,分离有机相,水洗、饱和食盐水洗、无水硫酸钠干燥,过滤并浓缩。残留物经柱层析(乙酸乙酯/石油醚1:1)纯化得标题化合物(16.7g,71%产率),为白色固体。1hnmr(500mhz,cdcl3)δ8.10(s,1h),5.51(d,j=5.8hz,1h),5.23–5.15(m,1h),4.41(q,j=7.0hz,2h),3.48–3.40(m,1h),3.37(d,j=8.3hz,1h),2.29(t,j=13.0hz,1h),1.95–1.87(m,1h),1.73–1.67(m,1h),1.40(t,j=7.1hz,3h),1.29(s,9h),0.93(d,j=7.3hz,3h),0.90(d,j=7.2hz,3h)。esimsm/z:计算值c16h28nan2o4s2[m+na]+:399.15,实测值399.14。 实施例125.2-((1r,3r)-3-氨基-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯盐酸盐的合成。 在0℃下向2-((1r,3r)-3-((s)-1,1-二甲基乙基亚磺酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯(6.00g,16.0mmol)的乙醇(40ml)溶液中加入4nhcl的1,4-二氧六环(40ml)溶液。反应逐渐升至室温后搅拌2.5小时。浓缩后用乙醚打浆,得白色固体,共4.54g(92%产率),并将其用于下一步。 实施例126.2-((1r,3r)-3-((2s,3s)-2-叠氮基-3-甲基戊胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯的合成。 将(2s,3s)-2-叠氮基-3-甲基戊酸(5.03g,28.8mol,2.0eq)溶于四氢呋喃(120ml)并冷却至0℃,依次加入nmm(6.2ml,56.0mmol)和氯甲酸异丁酯(3.7ml,28.8mol)。在0℃搅拌30分钟,室温1h,在0℃下,分批加入2-((1r,3r)-3-氨基-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯盐酸盐(4.54g,14.7mmol)。在0℃搅拌30分钟后,逐渐升至室温并继续搅拌2小时。反应在0℃下加冰水淬灭并用乙酸乙酯萃取三遍。合并有机相用1nhcl洗,饱和碳酸氢钠洗和食盐水洗,无水硫酸钠干燥。过滤浓缩,残留物经柱层析(0-30%乙酸乙酯/石油醚)纯化得到白色固体(4.55g,74%产率)。 实施例127.2-((1r,3r)-3-((2s,3s)-2-叠氮基-3-甲基戊胺基)-4-甲基-1-((三乙基甲硅烷基)氧基)戊基)噻唑-4-羧酸乙酯的合成。 在0℃下向2-((1r,3r)-3-((2s,3s)-2-叠氮基-3-甲基戊酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯(5.30g,12.8mmol)的二氯甲烷(50ml)溶液中依次加入咪唑(1.75g,25.6mmol)和三乙基氯硅烷(4.3ml,25.6mol)。反应液历时1小时升至室温后,继续搅拌1小时。加入饱和食盐水淬灭,分出有机相,水相用乙酸乙酯萃取。合并后的有机相经干燥、过滤、浓缩后用柱层析(15-35%乙酸乙酯/石油醚)纯化得标题化合物(6.70g,99%产率),为白色固体。1hnmr(500mhz,cdcl3)δ8.12(s,1h),6.75(d,j=8.0hz,1h),5.20–5.12(m,1h),4.44(q,j=7.0hz,2h),4.06–3.97(m,1h),3.87(d,j=3.8hz,1h),2.14(d,j=3.8hz,1h),2.01–1.91(m,3h),1.42(t,j=7.1hz,3h),1.34–1.25(m,2h),1.06(d,j=6.8hz,3h),1.00–0.93(m,18h),0.88(dd,j=19.1,6.8hz,6h)。esimsm/z:c24h44n5o4ssi[m+h]+:计算值526.28,实测值526.28。 实施例128.2-((1r,3r)-3-((2s,3s)-2-叠氮基-n,3-二甲基戊酰胺基)-4-甲基-1-((三乙基甲硅烷基)氧基)戊基)噻唑-4羧酸乙酯的合成。 将2-((1r,3r)-3-((2s,3s)-2-叠氮基-3-甲基戊酰胺基)-4-甲基-1-((三乙基甲硅烷基)氧基)戊基)噻唑-4-羧酸乙酯(5.20g,9.9mmol,1.0eq.)的四氢呋喃(50ml)溶液冷却至-45℃,加入khmds(1m甲苯溶液,23.8ml,23.8mmol,2.4eq.)。将所得混合物在-45℃下搅拌20分钟,然后加入碘甲烷(1.85ml,29.7mmol,3.0eq.)。将反应混合物升温至室温,搅拌超过4.5小时,然后用乙醇(10ml)淬灭反应。粗产物用乙酸乙酯(250ml)稀释并用盐水(100ml)洗涤。水层用乙酸乙酯(3×50ml)反萃取。将有机层干燥,过滤,浓缩并通过柱层析法用15-35%乙酸乙酯/石油醚梯度洗脱,得到标题产物(3.33g,63%产率),为浅黄色油状物。1hnmr(500mhz,cdcl3)δ8.09(s,1h),4.95(d,j=6.6hz,1h),4.41(q,j=7.1hz,2h),3.56(d,j=9.5hz,1h),2.98(s,3h),2.27–2.06(m,4h),1.83–1.70(m,2h),1.41(t,j=7.2hz,3h),1.29(ddd,j=8.9,6.8,1.6hz,3h),1.01(d,j=6.6hz,3h),0.96(dt,j=8.0,2.9hz,15h),0.92(d,j=6.6hz,3h),0.90(d,j=6.7hz,3h);esimsm/z:c25h46n5o4ssi[m+h]+计算值540.30,实测值540.30。 实施例129.2-((3s,6r,8r)-3-((s)-仲丁基)-10,10-二乙基-6-异丙基-5-甲基-1-((r)-1-甲基哌啶-2-基)-1,4-二氧代-9-氧杂-2,5-二氮杂-10-硅杂十二烷-8-基)噻唑-4-甲酸乙酯的合成。 向五氟苯基酯的乙酸乙酯溶液中加入干的pd/c(10wt%,300mg)和2-((1r,3r)-3-((2s,3s)-2-叠氮基-n,3-二甲基戊酰胺基)-4-甲基-1-乙基((三乙基甲硅烷基)氧基)戊基)噻唑-4-羧酸乙酯(3.33g,6.61mmol)。反应液在氢气(1atm)环境中搅拌27小时,而后用硅藻土过滤,乙酸乙酯洗。滤液旋干经柱层析(0-5%甲醇/乙酸乙酯)纯化得标题化合物(3.90g,86%产率)。esimsm/z:c32h59n4o5ssi[m+h]+计算值639.39,实测值639.39。 实施例130.2-((1r,3r)-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)戊酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯的合成。 将2-((3s,6r,8r)-3-((s)-仲丁基)-10,10-二乙基-6-异丙基-5-甲基-1-((r)-1-甲基哌啶-2)-)-1,4-二氧代-9-氧杂-2,5-二氮杂-10-基十二烷-8-基)噻唑-4-羧酸乙酯(3.90g,6.1mmol)溶于acoh/水/四氢呋喃(v/v/v3:1:1,100ml)中,并在室温下搅拌48小时。然后浓缩,残留物经柱层析(2:98至15:85甲醇/乙酸乙酯)纯化得到标题化合物(2.50g,两步产率72%)。esimsm/z:c26h45n4o5s[m+h]+计算值525.30,实测值525.33。 实施例131.2-((1r,3r)-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)戊酰胺基)-1-羟基-4-甲基戊基)噻唑-4-酸的合成。 在0℃下,将lioh水溶液(0.4n,47.7ml,19.1mmol,4.0eq.)加入到2-((1r,3r)-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)-戊酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯(2.50g,4.76mmol,1.0eq.)的1,4-二氧六环(47.7ml)溶液中。室温搅拌2小时后浓缩。残留物经柱层析(100%二氯甲烷至二氯甲烷/甲醇/氨水80:20:1)纯化,得到标题化合物(2.36g,99%产率),为无定形固体。esimsm/z:c24h41n4o5s[m+h]+计算值497.27,实测值497.28。 实施例132.2-((1r,3r)1-乙酰氧基-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)戊酰胺基)-4-甲基戊基)噻唑-4-酸的合成。 在0℃,向2-((1r,3r)-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)戊基)-1-羟基-4-甲基戊基)噻唑-4-羧酸(2.36g,4.75mmol)的吡啶(50ml)溶液中,缓慢加入乙酸酐(2.25ml,24mmol)。反应经2小时逐渐升至室温,并继续搅拌24小时。将反应浓缩并将残余物通过反相hplc(c18柱,50×250mm,50ml/min,10-90%乙腈/水,45分钟)纯化,得到标题化合物(2.25g,88%产率),呈无定形白色固体。esimsm/z:c26h43n4o6s[m+h]+计算值539.28,实测值539.28。 实施例133.(1r,3r)-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)戊烷基)-4-甲基-1-(4-(全氟苯甲酰基)噻唑-2-基)戊基乙酸酯的合成。 在0℃下,向2-((1r,3r)-1-乙酰氧基-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基-哌啶-2-甲酰胺基)戊酰胺的溶液)-4-甲基戊基)噻唑-4-羧酸(860mg,1.60mmol,1.0eq.)在二氯甲烷(20ml)的溶液中,加入五氟苯酚(440mg,2.40mmol,1.5eq.)和n,n’-二异丙基碳二亚胺(220mg,1.75mmol,1.1eq.)。将反应混合物升温至室温并搅拌过夜。减压除去溶剂后,将反应混合物用乙酸乙酯(20ml)稀释,然后经硅藻土过滤。浓缩滤液,在硅胶柱上纯化(1:10至1:3乙酸乙酯/二氯甲烷),得到标题化合物(935.3mg,82%产率),将其直接用于下一步骤。esimsm/z:c32h42f5n4o6s[m+h]+计算值704.28,实测值704.60。 实施例134.2-((6s,9r,11r)-6-((s)-仲丁基)-13,13-二乙基-9-异丙基-2,3,3,8-四甲基-4,7-二氧代-12-氧杂-2,5,8-三氮杂-13-硅十五烷-11-基)噻唑-4-羧酸乙酯的合成。 将干燥pd/c(10wt%,300mg)和2-((1r,3r)-3-((2s,3s)-2-叠氮基-n,3-二甲基戊酰胺基)-4-甲基-1-乙基((三乙基甲硅烷基)氧基)戊基)噻唑-4-羧酸乙酯(3.33g,6.16mmol)加到五氟苯基2-(二甲基氨基)-2-甲基丙酸酯(约2.75g,1.5eq.)的乙酸乙酯溶液中。将反应混合物在氢气下搅拌27小时,然后通过硅藻土过滤,并用乙酸乙酯洗涤滤垫。将合并的有机相浓缩并通过柱层析,用0-5%甲醇/乙酸乙酯溶液梯度洗脱,得到标题产物(3.24g,84%产率)。esimsm/z:c31h59n4o5ssi[m+h]+计算值626.39,实测值626.95。 实施例135.2-((1r,3r)-3-((2s,3s)-2-(2-(二甲胺基)-2-甲基丙酰胺)-n,3-二甲基戊烯基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯的合成。 将2-((6s,9r,11r)-6-((s)-仲丁基)-13,13-二乙基-9-异丙基-2,3,3,8-四甲基-4,7-二氧代-12-氧杂-2,5,8-三氮杂-13-硅杂十五烷-11-基)噻唑-4-羧酸乙酯(3.20g,5.11mmol)溶于脱氧的acoh/水/四氢呋喃(v/v/v3:1:1,100ml)中,并在室温下搅拌48小时。然后浓缩反应物并通过硅胶柱纯化(2:98至15:85甲醇/乙酸乙酯),得到标题化合物(2.33g,89%产率)。esimsm/z:c25h45n4o5s[m+h]+计算值512.30,实测值512.45。 实施例136.2-((1r,3r)-3-((2s,3s)-2-(2-(二甲胺基)-2-甲基丙酰胺)-n,3-二甲基戊烯基)-1-羟基-4-甲基戊基)噻唑-4-羧酸的合成。 在0℃,将lioh水溶液(0.4n,47.7ml,19.1mmol,4.0eq.)加入到2-((1r,3r)-3-((2s,3s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基戊酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯(2.30克,4.50毫摩尔,1.0eq.)的二恶烷(50毫升)溶液中,将反应混合物在室温下搅拌2小时,然后浓缩。用硅胶柱纯化(先用100%二氯甲烷,然后用二氯甲烷/甲醇/nh4oh80:20:1洗脱),得到标题化合物(2.13g,98%产率),为无定形固体。esimsm/z:c23h41n4o5s[m+h]+计算值485.27,实测值485.55。 实施例137.2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧基-12-氧杂-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸的合成。 在0℃下,向2-((1r,3r)-3-((2s,3s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丙酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸(2.10g,4.33mmol)的吡啶(50ml)溶液中缓慢加入乙酸酐(2.25ml,24mmol)。2小时使反应混合物升温至室温,并在室温下搅拌24小时。将反应浓缩并将残余物通过反相hplc(c18柱,50mm×250,50ml/min,10-90%乙腈/水,45分钟)纯化,得到呈无定形白色固体的标题化合物(1.95g,86%产率)。esimsm/z:c25h43n4o6s[m+h]+计算值526.28,实测值526.80。 实施例138.五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸酯的合成。 在0℃下,向2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸(1.90g,3.61mmol,1.0eq.)的二氯甲烷(70ml)溶液中,加入五氟苯酚(1.00g,5.43mmol,1.5eq.)和n,n’-二异丙基碳二亚胺(512mg,3.96mmol,1.1eq.)。将反应混合物升温至室温并搅拌过夜。在减压下除去溶剂后,将反应混合物用乙酸乙酯(80ml)稀释,然后用硅藻土过滤。浓缩滤液,在硅胶柱上纯化(1:10至1:3乙酸乙酯/二氯甲烷),得到标题化合物(2.09mg,84%产率),将其直接用于下一步骤。esimsm/z:c31h42f5n4o6s[m+h]+计算值693.27,实测值693.60。 实施例139.2-(三苯基亚正膦基)丙酸叔丁酯的合成。 将2-溴代丙酸叔丁酯(15.5g,74.1mmol,1.0eq.)和三苯基膦(19.4g,74.1mmol,1.0eq.)在无水乙腈(45ml)中的混合物在室温下搅拌18小时。减压除去乙腈,加入甲苯使白色沉淀析出。倾倒出甲苯,将白色固体溶于二氯甲烷(100ml)中并转移至分液漏斗中。向漏斗中加入10%naoh(100ml),振荡后有机层立即变黄。将有机层分离,并将水层用二氯甲烷(30ml)萃取一次。将二氯甲烷层合并,用盐水(50ml)洗涤一次,然后用硫酸钠干燥,过滤并浓缩,得到叶立德,为黄色固体(16.8g,58%)。 实施例140.(s)-3-(4-(苄氧基)苯基)-2-((叔丁氧基羰基)氨基)丙酸甲酯的合成。 向boc-l-tyr-ome(20.0g,67.7mmol,1.0eq)、k2co3(14.0g,101.6mmol,1.5eq)和ki(1.12g,6.77mmol,0.1eq)在丙酮(100ml)中的混合物中缓慢加入bnbr(10.5ml,81.3mmol,1.2eq)。然后将混合物回流一夜。加入水(250ml),用乙酸乙酯(3×100ml)萃取反应混合物。用盐水(300ml)洗涤组合有机层,用无水硫酸钠干燥,通过硅胶柱层析(4:1己烷/乙酸乙酯)过滤、浓缩和纯化,得到白色固体标题化合物(26.12g,收率99%)。1hnmr(500mhz,cdcl3)δ7.44–7.41(m,2h),7.41–7.36(m,2h),7.35–7.30(m,1h),7.04(d,j=8.5hz,2h),6.93–6.89(m,2h),5.04(s,2h),4.97(d,j=7.7hz,1h),4.55(d,j=6.9hz,1h),3.71(s,3h),3.03(dd,j=14.4,5.7hz,2h),1.44(d,j=18.6hz,10h)。esimsm/z:c22h27no5na[m+na]+计算值:408.18,实测值:408.11。 实施例141.((s)-(1-(4-(苄氧基)苯基)-3-氧代丙-2-基)氨基甲酸叔丁酯的合成。 在-78℃时,1小时内向(s)-3-(4-(苄氧基)苯基)-2-((叔丁氧基羰基)氨基)-丙酸甲酯(26.1g,67.8mmol,1.0eq.)的无水二氯甲烷(450ml)溶液中加入dibal(1.0m正己烷溶液,163ml,2.2eq.)。将混合物在-78℃下搅拌3小时,然后用50ml乙醇淬灭。滴加1nhcl直至达到ph4。使得到的混合物升温至0℃,再进行分层,水层进一步用乙酸乙酯(3×100ml)萃取。将合并的有机溶液用盐水洗涤,经无水硫酸钠干燥并浓缩。用石油醚/乙酸乙酯打浆并过滤,得到标题化合物,为白色固体(18.3g,76%产率)。esimsm/z:c22h27no5na[m+na]+计算值378.11,实测值378.11。 实施例142.(s,z)-5-(4-(苄氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊-2-烯酸叔丁酯。 将(s)-(1-(4-(苄氧基)苯基)-3-氧代丙-2-基)氨基甲酸叔丁酯(0.84g,2mmol,1.0eq.)溶解于无水二氯甲烷(50ml)中,向其中加入2-(三苯基-亚磷酰基)丙酸叔丁酯(1.6g,4mmol,2.0eq.),将溶液在室温下搅拌1.5小时,用tlc确定反应完成。通过柱层析法(10-50%乙酸乙酯/正己烷)纯化反应液,得到标题化合物(1.16g,98%产率)。 实施例143.(4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基苯基)-2-甲基戊酸叔丁酯的合成。 将(s,z)-5-(4-(苄氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊-2-烯酸叔丁酯(467mg,1mmol)溶于甲醇(30ml)中,与pd/c催化剂(10wt%,250mg)混合,在室温下氢化(1atm)过夜。滤出催化剂,减压浓缩滤液,得到标题化合物(379mg,99%产率)。 实施例144.(4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸叔丁酯的合成。 将(4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基苯基)-2-甲基戊酸叔丁酯(379mg,1mmol,1.0eq.)溶于四氢呋喃(20ml)中,向其中加入亚硝酸叔丁酯(315mg,3mmol,3.0eq.)的四氢呋喃(2ml)溶液。将反应物在室温下搅拌3小时,然后倒入水中,用乙酸乙酯(2×50ml)萃取,将合并的有机相用盐水(50ml)洗涤,用无水硫酸钠干燥,过滤并浓缩。通过柱层析法(10-50%乙酸乙酯/正己烷)纯化,得到标题化合物(300mg,71%产率)。 实施例145.(4r)-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸叔丁酯(200mg,0.47mmol)溶于乙酸乙酯(30ml)并与钯催化剂(10wt%,100mg)混合,然后在室温下氢化(1atm)2小时。滤出催化剂,并在真空下除去所有挥发物,得到标题化合物(185mg,99%)。 或者,将(4r)4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸叔丁酯(56mg,0.132mmol)溶于乙酸乙酯(20ml)并与pd/c催化剂(10wt%,50mg)混合并在室温下氢化(1atm)3小时。滤出催化剂,真空除去所有挥发物,得到标题化合物(52mg,99%产率)。esimsm/z:c21h35n2o5[m+h]+计算值:395.25,实测值:395.26。 实施例146.(4r)-4-((叔丁氧基羰基)氨基)-5-(4-((叔丁基二甲基甲硅烷基)氧基)-3-硝基苯基)-2-甲基戊酸叔丁酯的合成。 向(4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸叔丁酯(424mg,1mmol)的二氯甲烷(20ml)溶液中加入咪唑(408mg,6mmol)和叔丁基二甲基氯硅烷(602mg,4mmol)。在室温下持续搅拌所得溶液3小时。之后,反应混合物用盐水(50ml)洗涤,用无水硫酸钠干燥,浓缩并通过柱色谱法(10%至30%乙酸乙酯/正己烷)纯化,得到标题化合物(344mg,64%产率)。 实施例147.(4r)-5-(3-氨基-4-((叔丁基二甲基甲硅烷基)氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(4r)-4-((叔丁氧基羰基)氨基)-5-(4-((叔丁基二甲基甲硅烷基)氧基)-3-硝基苯基)-2-甲基戊酸叔丁酯(200mg,0.37mmol)溶于乙酸乙酯(30ml)中,与钯碳催化剂(10wt%,100mg)混合,并在室温氢化反应(1atm)2小时。滤出催化剂,真空除去所有挥发物,得到标题化合物(187mg,99%产率)。 实施例148.2-(1-叠氮基-14,17二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)-4-((2r)-5-(叔丁氧基)-2–((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酯的合成 向1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-1,1,16-二氮杂十八烷-18-酸(1.50g,3.85mmol)和(4r)-叔丁基-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸酯(0.75g,1.90mmol)的dma(40ml)溶液中加入edc(2.05g,10.67mmol)和dipea(0.70ml,4.0mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:5至1:1)洗脱,得到标题化合物(2.01g,82%产率,hplc纯度约95%)。esimsm/z:c51h85n12o17[m+h]+计算值1137.61,实测值1137.90。 实施例149.(4r)-5-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂-七氮杂环四十六烷-46-基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将2-(1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)-4-((2r)-5-(叔丁氧基)-2–((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸酯(900mg,0.79mmol)溶于乙酸乙酯(30ml)中,与钯碳催化剂(10wt%,100mg)混合,并在室温下氢化反应(1atm)4小时。滤除催化剂并在真空下除去所有挥发物,得到2-(1-氨基-1,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)-4-((2r)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基1-氨基-1,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酯(815mg,96%产量),无需进一步纯化即可使用。esimsm/z:c51h88n8o17[m+h]+计算值1085.62,实测值1085.95。 将edc(1.25g,6.51mmol)和dipea(0.35ml,2.0mmol)加入到上述二氨基化合物(810mg,0.75mmol)和2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸(231mg,0.75mmol)的dma(10毫升)溶液中。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:5至1:1)洗脱,得到标题化合物(844mg,83%产率,hplc纯度约95%)。esimsm/z:c63h92n10o23[m+h]+计算值1357.63,实测值1357.95。 实施例150.(2r)-1-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂-七氮杂环四十六烷-46-基)-4-羧基戊-2-铵的合成。 将(4r)-5-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂-七氮杂环四十六烷-46-基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(840mg,0.62mmol)溶解在二氯甲烷(6ml)和tfa(4ml)的混合物中。将混合物搅拌过夜,用甲苯(10ml)稀释,浓缩,得到标题化合物(7.43g,100%产率,hplc纯度约91%),其不经进一步纯化即用于下一步骤。esimsm/z:c54h76n10o21[m+h]+计算值1200.51,实测值1200.95。 实施例151.(4r)-4-(2-((1r,3r)-1-乙酰氧基-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-基)甲酰胺基)戊酰胺基)-4-甲基戊基)噻唑-4-甲酰胺基)-5-(3-(3-(2-(2-叠氮基乙氧基)乙氧基)丙酰胺基)-4-羟基苯基)-2-甲基戊酸的合成。 向(4r)-4-(2-((1r,3r)-1-乙酰氧基-3-((2s,3s)-n,3-(二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)戊酰胺基)-4-甲基戊基)噻唑-4-甲酰胺基)-5-(3-氨基-4-羟基苯基)-2-甲基戊酸(100mg,0.131mmol)(huangy.等,medchem.#44,249thacsnationalmeeting,denver,co,mar.22-26,2015;wo)的dma(10ml)和nah2po4缓冲溶液(ph7.5,1.0m,0.7ml)的混合溶液中,两小时内分四次加入2,5二氧代吡咯烷-1-基3(2(2叠氮基乙氧基)乙氧基)丙酸酯(80.0mg,0.266mmol)。将混合物搅拌过夜,浓缩并在制备型hplc(3.0×25cm,25ml/min)上纯化,在45分钟内用80%水/甲醇至10%水/甲醇洗脱,得到标题化合物(101.5mg,82%产率)。lc-ms(esi)m/z:c45h70n9o11s[m+h]+计算值944.48,实测值944.70。 实施例152.(4r)-4-(2-((1r,3r)-1-乙酰氧基-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基-哌啶-2-羧酰胺基)戊酰胺基)-4-甲基戊基)噻唑-4-甲酰胺基)-5-(3-(3-(2-(2-氨基乙氧基)乙氧基)丙酰胺基)-4-羟基苯基)-2-甲基戊酸的合成。 在氢化反应瓶中,向(4r)-4-(2-((1r,3r)-1-乙酰氧基-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-基)甲酰胺基)戊酰胺基)-4-甲基戊基)噻唑-4-甲酰胺基)-5-(3-(3-(2-(2-叠氮基乙氧基)乙氧基)丙酰胺基)-4-羟基苯基)-2-甲基戊酸(100.0mg,0.106mmol)的含有0.1%hcl的甲醇(25ml)溶液中,加入pd/c(25mg,10%pd,含水50%)。将容器中的空气抽真空后,加入35psi的氢气,将混合物振荡4小时,通过硅藻土过滤。将滤液浓缩并且在制备性hplc(3.0×25cm,25ml/min)上纯化,在45分钟内用85%水/甲醇至15%水/甲醇洗脱,得到标题化合物(77.5mg,79%产率)。lc-ms(esi)m/z:c45h72n7o11s[m+h]+计算值918.49,实测值918.60。 实施例153.(4r)-5-(4-乙酰氧基-3-硝基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 在0℃下,向(4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸叔丁酯(107.1mg,0.252mmol)的二氯甲烷(4.0ml)溶液中依次加入乙酸酐(0.11ml,1.17mmol)和三乙胺(0.16ml)。然后将反应物升温至室温并搅拌1小时,用二氯甲烷稀释并用水和盐水洗涤,用无水硫酸钠干燥,过滤并浓缩。通过柱层析(0-15%乙酸乙酯/石油醚)纯化残余物,得到无色油状物(120.3mg,理论产率)。esimsm/z:c23h35n2o8[m+h]+计算值467.23,实测值467.23。 实施例154.(4r)-5-(4-乙酰氧基-3-氨基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(4r)-5-(4-乙酰氧基-3-硝基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(120.3mg,0.258mmol)溶于乙酸乙酯(5ml)和乙酸(0.5ml)中。向其中加入pd/c(10wt%,10mg),在室温下,在氢气球下搅拌该混合物30分钟,然后通过硅藻土垫过滤,并用乙酸乙酯洗涤硅藻土垫。将滤液浓缩并通过柱层析(0-25%乙酸乙酯/石油醚)纯化,得到黄色油状物(120.9mg,理论产量)。esimsm/z:c23h37n2o6[m+h]+计算值437.26,实测值437.28。 实施例155.(4r)-5-(3-(4-(((苄氧基)羰基)氨基)丁酰胺基)-4-((叔丁基二甲基甲硅烷基)氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸乙酯。 将2,5-二氧代吡咯烷-1-基4-(((苄氧基)羰基)氨基)丁酸酯(0.396g,1.2mmol)和(4r)-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸乙酯(0.44g,1.2mmol)溶于乙醇(10ml)中,然后加入磷酸盐缓冲溶液(ph=7.5,0.1m,2ml)。反应混合物在室温下搅拌过夜,然后减压除去溶剂,并将残余物通过硅胶柱层析纯化,得到标题产物(0.485g,70%)。esimsm/z:c31h44n3o8[m+h]+计算值:586.31,实测值:586.31。 实施例156.(4r)-5-(3-(4-氨基丁酰胺基)-4-((叔丁基二甲基甲硅烷基)氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸乙酯的合成。 将(4r)-5-(3-(4-(((苄氧基)羰基)氨基)丁酰胺基)-4-((叔丁基二甲基-甲硅烷基)氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸乙酯(0.35g,0.5mmol)溶于甲醇(5ml)中,然后加入pd/c(10wt%,35mg)。将反应混合物在室温下,在氢气球下搅拌过夜,然后通过硅藻土过滤,并将滤液减压浓缩,得到标题产物(0.22g,79%产率)。esimsm/z:c29h52n3o6si[m+h]+计算值:566.35,实测值:566.35。 实施例157.(2r,3s)-2,3-双(((苄氧基)羰基)氨基)琥珀酸的合成。 向(2r,3s)-2,3-二氨基琥珀酸(4.03g,27.30mmol)的四氢呋喃(250ml)和nah2po4(0.1m,250ml,ph8.0)的混合物中,在2小时内分4份加入碳酸氯苄酯(15.0g,88.23mmol)。将混合物搅拌6小时,浓缩并在硅胶柱上纯化,用含有1%甲酸的水/乙腈(1∶9)洗脱,得到标题化合物(8.63g,收率75%)。esimsm/z:c20h21n2o8[m+h]+计算值:417.12,实测值:417.50。 实施例158.(2r,3s)-双(2,5-二氧杂吡咯烷-1-基)2,3-双(((苄氧基)-羰基)氨基)琥珀酸酯的合成。 向(2r,3s)-2,3-双((((苄氧基)羰基)氨基)琥珀酸(4.25g,10.21mmol)的dma(70ml)溶液中加入nhs(3.60g,31.30mmol)和edc(7.00g,36.65mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶6)洗脱,得到标题化合物(5.48g,88%收率)。esimsm/z:c28h27n4o12[m+h]+计算值:611.15,实测值:611.45。 实施例159.4,4′-((((2r,3s)-2,3-双(((苄氧基)羰基)-氨基)琥珀酰基)双(氮杂二基))二丁酸二叔丁基酯的合成。 向(2r,3s)-2,3-双((((苄氧基)羰基)氨基)琥珀酸(4.25g,10.21mmol)的dma(70ml)溶液中加入4-氨基丁酸叔丁酯(3.25g,20.42mmol)和edc(7.00g,36.65mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶10)洗脱,得到标题化合物(6.50g,收率91%)。esimsm/z:c36h51n4o10[m+h]+计算值:699.35,实测值:699.55。 实施例160.4,4′-((((2r,3s)-2,3-双(((苄氧基)羰基)-氨基)琥珀酰基)双(氮杂二基))二叔丁基酯。 向4,4′-(((((2r,3s)-2,3-双(((苄氧基)羰基)氨基)-琥珀酰基)双(氮杂二烷基))二丁酸二叔丁基酯(2.50g,3.58mmol)的甲醇(100ml)溶液中加入10%pd/c(0.30g,50%wet),将混合物在氢气下于室温搅拌18小时。然后通过硅藻土过滤除去pd/c,并用甲醇洗涤滤床。浓缩滤液,得到黄色泡沫状产物,其无需进一步纯化即可用于下一步骤(1.54g,收率100%)。esimsm/z:c20h39n2o6[m+h]+计算值:431.28,实测值:431.50。 实施例161.4,4′-(((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))丁酸二叔丁酯的合成。 向3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酸(1.25g,7.39mmol)的dma(60ml)溶液中加入二叔丁基4,4′-(((2r,3s)-2,3-二氨基琥珀酰基)-双(氮杂二基))二丁酸酯(1.54g,~3.57mmol)和edc(2.40g,12.56mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶10)洗脱,得到标题化合物(2.35g,收率90%)。esimsm/z:c34h49n6o12[m+h]+计算值:733.33,实测值:733.60。 实施例162.4,4′-(((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸的合成。 向4,4′-(((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基))丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯(2.30g,3.14mmol)的1,4-二氧六环(20ml)溶液搅拌加入hcl(36%,7.0ml)。将混合物搅拌30分钟,用甲苯(20ml)稀释,浓缩并硅胶柱上纯化,用甲醇/二氯甲烷(1:10至1:4)洗脱,得到标题化合物(1.69g,收率86%)。esimsm/z:rc26h33n6o12[m+h]+计算值:621.21,实测值:621.70。 实施例163.4,4′-((((2r,3s)-2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-)酰基)乙酰胺基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯的合成。 向2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酸(1.12g,7.22mmol)的dma(60ml)溶液中加入4,4′-二叔丁基(((2r,3s)-2,3-二氨基琥珀酰)-双(氮杂二基))二丁酸二叔丁酯(1.54g,3.58mmol)和edc(2.40g,12.56mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:10)洗脱,得到标题化合物(2.29g,收率91%)。esimsm/z:c32h45n6o12[m+h]+计算值:704.30,实测值:704.60。 实施例164.4,4′-(((2r,3s)-2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰胺基)琥珀酰)双(氮杂二酰基))二丁酸的合成。 向4,4′-(((2r,3s)-2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基))乙酰氨基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯(2.20g,3.12mmol)的1,4-二氧六环(20ml)溶液中加入hcl(36%,7.0ml)。将混合物搅拌30分钟,用甲苯(20ml)稀释,浓缩并在硅胶柱上纯化,并用甲醇/二氯甲烷(1:10至1:4)洗脱,得到标题化合物(1.69g,收率86%)。esimsm/z:c24h29n6o12[m+h]+计算值:593.18,实测值:593.40。 实施例165.双(2,5-二氧代吡咯烷-1-基)4,4′-(((2r,3s)-2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰胺基)琥珀酰基)双(氮杂二基))二丁酸酯的合成。 向4,4′-(((2r,3s)-2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)琥珀酰基)双(氮杂二基))二丁酸(1.10g,1.85mmol)的dma(30ml)溶液中加入nhs(1-羟基吡咯烷-2,5-二酮)(0.55g,4.78mmol)和edc(1.25g,6.54mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:10)洗脱,得到标题化合物(1.30g,收率90%)。esimsm/z:c32h35n8o16[m+h]+计算值:787.21,实测值:787.60。 实施例166.(2s,3s)-2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸的合成。 向(2r,3r)-2,3-二氨基琥珀酸(5.00g,33.77mmol)在thf/h2o/dipea(125ml/125ml/2ml)中加入马来酸酐(6.68g,68.21mmol)。将混合物搅拌过夜,蒸发,得到(2s,3s)-2,3-双((z)-3-羧基丙烯酰胺基)琥珀酸(11.05g,收率99%),为白色固体。esimsm/z:c12h13n2o10[m+h]+计算值:345.05,实测值:345.35。 向(2s,3s)-2,3-双((z)-3-羧基丙烯酰胺基)琥珀酸(11.05g,33.43mmol))的hoac(70ml),dmf(10ml)和甲苯(50ml)混合溶液中加入乙酸酐(30毫升)。将混合物搅拌2小时,用dean-stark分水器在100℃下回流6小时,浓缩,与乙醇(2×40ml)和甲苯(2×40ml)共浓缩,并在硅胶柱上纯化,用水/乙腈(1∶10)洗脱,得到标题化合物(8.10g,收率78%)。esimsm/z:c12h9n2o8[m+h]+计算值:309.03,实测值:309.50。 实施例167.(2s,3s)-双(2,5-二氧杂吡咯烷-1-基)2,3-双(2,5-二氧杂-2,5-二氢-1h-吡咯-1-基)琥珀酸酯的合成。 向(2s,3s)-2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸(4.00g,12.98mmol)的dmf溶液(70ml)中加入nhs(3.60g,31.30mmol)和edc(7.00g,36.65mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶6)洗脱,得到标题化合物(5.79g,收率89%,hplc纯度约为96%)。esimsm/z:c20h15n4o12[m+h]+计算值:503.06,实测值:503.60。 实施例168.(4r)-5-(3-(4-((((苄氧基)羰基)氨基)-丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将hatu(39.9g,105mmol)加入到4-(((苄氧基)羰基)氨基)丁酸(26.1g,110mmol)的dmf(300ml)溶液中。在室温下搅拌后30分钟后,将混合物加入到(4r)5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(39.4g,100mmol)和tea(20.2g,200mmol)的dmf(300毫升)溶液中。将得到的混合物在室温搅拌2小时。然后加入水,用乙酸乙酯萃取,有机层用盐水洗涤,用硫酸钠干燥。通过柱色谱法纯化(20%至70%乙酸乙酯/石油醚),得到标题产物,为白色固体(45g,收率73%)。esim/z:c33h48n3o8[m+h]+计算值:614.34,实测值614.15。 实施例169.(4r)-5-(3-(4-(4-氨基丁亚氨基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(4r)-5-(3-(4-((((苄氧基)羰基)氨基)-丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(100g,163mmol)溶于甲醇(500ml)中,并在室温下与pd/c催化剂(10wt%,10g)氢化(1atm)过夜。滤出催化剂,减压浓缩滤液,得到标题化合物(75.8g,收率97%),为棕色泡沫状固体。1hnmr(400mhz,cdcl3)δ7.11(s,1h),6.83(d,j=10.3hz,2h),5.04–4.52(m,6h),3.90–3.56(m,1h),2.81(d,j=5.3hz,2h),2.63(dd,j=12.5,6.1hz,2h),2.54-2.26(dd,j=14.0,7.6hz,4h),1.94-1.64(m,3h),1.44–1.36(m,18h),1.08(d,j=6.9hz,3h)。esimsm/z:c25h42n3o6[m+h]+计算值:480.30,实测值:480.59。 实施例170.(4r)-5-(3-((s)-37-((((苄氧基)羰基)氨基)氨基)-31,38-二氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32,39-二氮杂四十三酰胺基)-4-羟基苯基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯的合成。 在0℃下,向(4r)5-(3-(4-(4-氨基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(130g,174mmol,1.1eq)的dmf(500ml)溶液中依次加入tea(66ml,474mmol,3eq)和hatu(72g,190mmol,1.2eq)。然后将反应混合物升温至室温并搅拌2小时。在0℃下将(s)-37-((((苄氧基)羰基)氨基)-31-氧-2,5,8,11,14,17,20,23,26,29-十氧杂-32-氮杂三十八烷-38-酸(75.8g,158mmol,1.0eq)的dmf(500ml)溶液加入反应混合物,在室温搅拌1小时。将反应混合物倒入水(4l)中,水层用乙酸乙酯(3×500ml)萃取,合并有机层,用盐水(2l)洗涤,经硫酸钠干燥,浓缩,得到粗标题产物(190g),直接用于下一步。esimsm/z:c60h100n5o20[m+h]+计算值:1210.69,实测值:1210.69。 实施例171.(4r)-叔丁基5-(3-((s)-37-氨基-31,38-二氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32,39-二氮杂四十三酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸酯的合成。 将(4r)-叔丁基5-(3-((s)-37-(((苄氧基)羰基)氨基)-31,38-二氧基-2,5,8,11,14,17,20,23,26,29-癸氧基-32,39-二氮杂四十三酰胺基)-4-羟基苯基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸盐(190g)的粗产物溶解在甲醇(900ml)中,并和pd/c催化剂(10wt%,19g)混合,在室温下氢气(1atm)中搅拌过夜。过滤催化剂,减压浓缩滤液,将粗产物通过硅胶柱纯化,用(二氯甲烷/甲醇)梯度纯化,得到标题产物(105g,两步收率62%)为褐色油状物。esimsm/z:c52h95n5o18[m+h]+计算值:1077.65,实测值:1077.65。 实施例172.2-((6s,9s,12r,14r)-9-((s)-仲丁基)-14-羟基-6,12-二异丙基-2,2,5,11-四甲基-4,7,10-三氧基-3-氧代-5,8,11-三氮杂十四烷-14-基)噻唑-4-羧酸的合成。 向boc-n-me-l-val-oh(33mg,0.14mmol)的乙酸乙酯溶液中加入五氟苯酚(39mg,0.21mmol)及dcc(32mg,0.154mmol)。在室温下将反应混合物搅拌16小时,然后在硅藻土垫上过滤,并用乙酸乙酯洗涤。滤液浓缩并在dma(2ml)中重新溶解,然后加入2-((1r,3r)-3-((2s,3s)-2-氨基-n,3-二甲基戊酰胺)-1-羟基-4-甲基戊基)噻唑-4-羧酸(52mg,0.14mmol)和dipea(48.5μl,0.28mmol)。反应混合物在室温搅拌24小时,然后通过反相高效液相色谱(c18柱,10-100%乙腈/水)浓缩和纯化得到标题化合物(40.2mg,收率49%)。esimsm/z:c28h49n4o7s[m+h]+计算值:585.32,实测值:585.32。 实施例173.2-((6s,9s,12r,14r)-9-((s)-仲丁基)-6,12-二异丙基-2,2,5,11-四甲基-4,7,10,16-四氧杂-3,15-二氧杂-5,8,11-三氮杂十七烷-14-基)噻唑-4-羧酸的合成。 在0℃下,将2-((6s,9s,12r,14r)-9-((s)-仲丁基)-14-羟基-6,12-二异丙基-2,2,5,11-四甲基-4,7,10将(三氧杂-3-氧杂-5,8,11-十四烷-14-基)噻唑-4-甲酸(40mg,0.069mmol)溶解于吡啶(8ml)中,加入乙酸酐(20.4mg,0.2mmol),使反应物升温至室温并搅拌过夜,将混合物浓缩,通过硅胶柱纯化,用甲醇/二氯甲烷梯度洗脱,得到标题产物(48.1mg,收率)。esimsm/z:c30h51n4o8s[m+h]+计算值:627.33,实测值:627.33。 实施例174.(4r)-4-(2-(((6s,9s,12r,14r))-9-((s)-仲丁基)-6,12-二异丙基-2,2,5,11-四甲基-4,7,10,16-四氧代-3,15-二氧杂-5,8,11-三氮杂十四烷-14-基)噻唑-4-羧酰胺基)-2-甲基-5-苯基戊酸的合成。 将五氟苯酚(21.2mg,0.115mmol)和dcc(17.4mg,0.085mmol)加入到2-((6s,9s,12r,14r)-9-((s)-仲丁基)-6,12-二异丙基-2,2,5,11-四甲基-4,7,7,10,16-四氧基-3,15-二氧杂-5,8,11-三氮杂十七烷-14-基)噻唑-4-羧酸(48.1mg,0.077mmol)的乙酸乙酯溶液中。在室温下将反应混合物搅拌16小时,然后在硅藻土垫上过滤,并用乙酸乙酯洗涤。滤液浓缩并在dma(4ml)中重新溶解,然后加入(4r)-4-氨基-2-甲基-5-苯基戊酸(20.7mg,0.1mmol)和dipea(26.8μl,0.154mmol)。反应混合物在室温下搅拌24小时,然后通过反相hplc(c18柱,10-100%乙腈/水)浓缩和纯化,得到标题化合物(63mg,收率~100%)。esimsm/z:c42h66n5o9s[m+h]+计算值:816.45,实测值:816.45。 计算值175.(4r)-4-(2-((3s,6s,9r,11r)-6-((s)-仲丁基)-3,9-二异丙基-8-甲基-4,7,13-三氧基-12-氧杂-2,5,8-三氮杂十四烷-11-基)噻唑-4-甲酰胺基)-2-甲基-5-苯基戊酸盐酸盐的合成。 向(4r)-4-(2-((6s,9s,12r,14r)-9-((s)-仲丁基)-6,12-二异丙基-2,2,5,11-四甲基-4,7,10,16-四氧代-3,15-二氧杂-5,8,11-三氮杂十四烷-14-基)噻唑-4-甲酰氨基)-2-甲基-5-苯基戊酸(60mg,0.073mmol)的乙酸乙酯溶液(3ml)中加入盐酸(0.8ml,12m)。将混合物搅拌30分钟并用甲苯(5ml)和1,4-二氧六环(5ml)稀释。将混合物蒸发并与1,4-二氧六环(5ml)和甲苯(5ml)共蒸发至干。得到的粗标题产物(57.1mg,收率103%),不经纯化直接应用于下一步。esimsm/z:c37h58n5o7s[m+h]+计算值:716.40,实测值:716.60。 实施例176.(4r)-叔丁基-5-(3-(2-(2-((苄氧基)羰基)氨基)-丙酰胺基)乙酰氨基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸酯的合成。 将2-(2-((((苄氧基)羰基)氨基)丙酰胺基)乙酸(0.2g,0.7mmol),(4r)-叔丁基-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基氨基)-2-甲基戊酸酯(0.19g,0.48mmol)和hatu(0.18g,0.48mmol)溶解在二氯甲烷(20ml)中,然后加入tea(134ul,0.96mmol)。将反应混合物在室温搅拌过夜,减压浓缩并将残余物在硅胶柱上纯化,得到标题产物(0.3g,95%)。esimsm/z:c34h49n4o9[m+h]+计算值:657.34,实测值:657.34。 实施例177.(4r)-叔丁基-5-(3-(2-(2-(2-氨基丙酰胺基)乙酰氨基)-4-羟苯基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸酯的合成 在氢化瓶中,将pd/c(0.1g,33wt%,50%水),(4r)-叔丁基-5-(3-(2-(2-((((苄氧基))羰基)氨基)丙酰胺基)乙酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸酯(0.3g,0.46mmol)和甲醇(10ml)混合。将混合物在1个大气压的h2下振摇过夜,然后将通过硅藻土(助滤剂)过滤,并浓缩,得到标题化合物(0.21g,87%),其无需进一步纯化即可用于下一步。esimsm/z:c26h43n4o7[m+h]+计算值:523.31,实测值:523.31。 实施例178.2-羧基-n,n,n-三甲基丙烷-2-氨基溴化物的合成。 向2-溴-2-甲基丙酸(3.00g,17.9mmol)的四氢呋喃(30ml)的溶液中加入三甲胺(1mthf溶液,17.9ml,35.9mmol)。反应混合物在室温下搅拌过夜。通过过滤收集沉淀物,并用乙酸乙酯洗涤,得到呈白色固体的标题化合物(4.00g,理论产率)。esimsm/z:c7h16no2[m+h]+计算值:146,实测值:146。 实施例179.n,n,n,2-四甲基-1-氧代-1-(五氟苯氧基)丙-2-溴化铵的合成。 向2-羧基-n,n,n,n-三甲基丙烷-2-溴化铵(1.55g,6.9mmol)和五氟苯酚(2.50g,13.8mmol)的二氯甲烷(20ml)溶液中加入dcc(2.80g,13.8)。将反应混合物在室温搅拌过夜,将反应过滤,并在真空下浓缩,得到无色油状标题化合物,将其直接用于下一步。esimsm/z:c13h15f5no2[m+h]+计算值:312,实测值:312。 实施例180.(5r,7r,10s)-10-(仲丁基)-5-(4-(乙氧基羰基)噻唑-2-基)-3,3-二乙基-7-异丙基-n,n,n,8,13-五甲基-9,12-二氧代-4-氧杂-8,11-二氮杂-3-硅酸酯十三烷-13-铵的合成。 在0℃下,向2-((1r,3r)-3-((2s)-2-氨基-n,3-二甲基戊酰胺)-4-甲基-1-((三乙基甲硅烷基)氧基)戊)噻唑-4-乙基羧酸乙酯(1.78g,3.4mmol)和n,n,n,2-四甲基-1-氧-1-(五氟苯氧基)丙烷-2-铵溴化物(6.9mmol,10.4mmol)的dmf(20ml)中加入dipea(1.8ml)。将反应混合物升温至室温并搅拌1小时,然后在真空下浓缩,并通过硅胶柱(100:1至5:1二氯甲烷/甲醇)纯化,得到泡沫状标题化合物(1.20g,收率54%)。esimsm/z:c32h61n4o5ssi[m+h]+计算值:642,实测值:642。 实施例181.1-(((2s)-1-((1r,3r)-1-(4-(乙氧羰基)噻唑-2-基)-1-羟基-4-甲基戊烷-3-基)(甲基)氨基)-3-甲基-1-氧代戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-胺的合成。 将(5r,7r,10s)-10-(仲丁基)-5-(4-(乙氧基羰基)噻唑-2-基)-3,3-二乙基-7-异丙基-n,n,8,13-五甲基-9,12-二氧基-4-氧杂-8,11-二氮杂-3-十三烷-13-胺(1,20g,1,86mmol)溶解于acoh/thf/h2o(v/v/v3:1:1,20ml)并搅拌过夜。然后在真空下浓缩反应物,用于下一步,无需进一步纯化。esimsm/z:c26h47n4o5s[m+h]+计算值:527,实测值:527。 实施例182.1-(((2s)-1-(((1r,3r)-1-(4-羧基噻唑-2-基)-1-羟基-4-甲基戊烷-3-基)(甲基)氨基)-3-甲基-1-氧代戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-铵的合成。 向1-(((2s)-1-((((1r,3r)-1-(4-(乙氧基羰基)噻唑-2-基)-1-羟基-4-甲基戊基-3-基)(甲基)氨基)-3-甲基-1-氧代戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-铵(1.86mmol)的1,4-二氧六环(10ml)溶液加入1nnaoh(9.3ml)。然后将反应混合物搅拌2小时并在真空下浓缩。将残余物用水(10ml)稀释,并加入1nhcl以将ph调节至4。将混合物真空浓缩,得到标题化合物,为白色固体。esimsm/z:c24h43n4o5s[m+h]+计算值:499,实测值499。 实施例183.1-(((2s)-1-((1r,3r)-1-乙酰氧基-1-(4-羧噻唑-2-基)-4-甲基戊烷-3-基)(甲基)氨基)-3-甲基-1-氧代戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-铵的合成。 在0℃下,向1-(((2s)-1-(((1r,3r)-1-(4-羧基噻唑-2-基)-1-羟基-4-甲基戊烷-3-基-甲基)-3-甲基-3-甲基-1-氧代戊烷-2-基)-氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-铵(1.86mmol)的吡啶(10ml)溶液中加入乙酸酐(884μl,9.36mmol)。然后升温至室温并搅拌过夜。反应在真空下浓缩,然后用水(20ml)稀释并用乙酸乙酯(3×10ml)洗涤。在真空下浓缩水层,使标题化合物为黄色固体。esimsm/z:c26h45n4o6s[m+h]+计算值:541,实测值:541。 实施例184.1-(((2s)-1-((1r,3r)-1-乙酰氧基-4-甲基-1-(4-((五氟苯酚氧基)羰基)噻唑-2-基)戊烷-3-基)(甲基)氨基)-3-甲基-1-氧代戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-铵的合成。 向1-(((2s)-1-((((1r,3r)-1-乙酰氧基-1-(4-羧基噻唑-2-基)-4-甲基戊三-3-基)(甲基)氨基)-3-甲基-1-氧戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧丙烷-2-铵(150mg,0.277mmol)和五氟苯酚(76.5mg,0.415mmol)的二氯甲烷(2ml)溶液中加入edci(63.7mg,0.33mmol),将反应混合物搅拌小时并真空浓缩,得到标题化合物,为黄色油状物。esimsm/z:c32h44f5n4o6s[m+h]+计算值:707,实测值:707。 实施例185.(s)-4-异丙基-3-丙酰基丙二唑烷-2-酮的合成。 在约-70℃,n2中向(s)-4-异丙基恶唑烷-2-酮(400g,3.09mol,1.0eq)的四氢呋喃(8l)溶液中加入正丁基锂(2.5m正己烷溶液,1.36l,3.4mol,1.1eq)。将混合物在-70℃下搅拌1小时,然后缓慢加入丙酰氯(315g,3.4mol,1.1eq)。再将此混合物在-70℃下搅拌1小时,并逐渐升温至室温。将反应混合物加入到冰冷的饱和氯化铵溶液(7l)中,并用乙酸乙酯(3×2l)萃取。有机层用水(2l)和盐水(2l)依次洗涤,用硫酸钠干燥,过滤,浓缩并通过柱色谱法纯化(3kg硅胶,纯石油醚至5:1石油醚/乙酸乙酯),得标题化合物,为无色油状物(500g,收率87%)。esimsm/z:c9h16no3[m+h]+计算值:186.10,实测值:186.10。 实施例186.(s)-3-(4-(苄氧基)苯基)-2-((叔丁氧羰基)氨基)丙酸甲酯的合成。 向boc-l-tyr-ome(900g,3.05mol,1.0eq),k2co3(632g,4.58mol,1.5eq)和ki(20g,0.150mol,0.05eq)的乙腈混合物(3l)中缓慢加入苄基溴(547g,3.20mol,1.05eq)。然后将混合物回流并通过tlc监测。4小时后,将反应冷却至室温并过滤,将滤液浓缩并用水(3l)和乙酸乙酯(3.5l)稀释,分离有机相,用乙酸乙酯(2×1.5l)萃取水相。洗涤合并的有机层,依次用盐水(2×3l)洗涤,用硫酸钠干燥,过滤并浓缩。将从4批900g的和一批400g初始原料得到的产物混合,称重为5.4kg,然后用石油醚分18批打浆(每批4l石油醚)。收集固体,滤液浓缩后用硅胶柱层析法(4:1正己烷/乙酸乙酯)纯化,合并组分得到标题化合物,总重量为4.85千克白色固体(收率93%)。1hnmr(500mhz,cdcl3)δ7.43(d,j=7.0hz,2h),7.38(t,j=7.4hz,2h),7.32(t,j=7.2hz,1h),7.04(d,j=8.5hz,2h),6.91(d,j=8.6hz,2h),5.04(s,2h),4.55(d,j=6.9hz,1h),3.71(s,3h),3.03(qd,j=14.0,5.8hz,2h),1.43(s,9h)。esimsm/z:c22h28no5[m+h]+计算值:386.19,实测值:386.19。 实施例187.(s)-叔丁基(1-(4-(苄氧基)苯基)-3-氧代丙烷-2-基)氨基甲酸酯的合成。 在-78℃下,向(s)-3-(4-(苄氧基)苯基)-2-((叔丁氧基羰基)氨基)丙酸甲酯(288g,0.74mol,1.0eq.)的无水二氯甲烷中缓慢加入的dibal(在甲苯中1.5m,1.0l,2.0eq),加入完成后,继续搅拌2小时,然后将反应混合物倒入冰水(2l)中。加入2nhcl(2l)以溶解形成的白色沉淀。分离有机相,水相用二氯甲烷(2×500ml)萃取。将合并的有机相用2nhcl(500ml)和水(500ml)洗涤,用无水硫酸钠干燥,过滤并浓缩。将粗产物溶于二氯甲烷(1l)中并上样到硅胶柱(1kg硅胶),用二氯甲烷洗脱。浓缩洗脱溶液并用石油醚/乙酸乙酯打浆,得到标题化合物的白色固体(152g,收率57%)。1hnmr(500mhz,cdcl3)δ9.65(s,1h),7.45(d,j=7.1hz,2h),7.41(t,j=7.4hz,2h),7.35(t,j=7.1hz,1h),7.11(d,j=8.6hz,2h),6.95(d,j=8.6hz,2h),5.07(s,2h),4.42(dd,j=12.4,6.1hz,1h),3.09(d,j=6.2hz,2h),1.46(s,9h)。esimsm/z:c21h26no4[m+h]+计算值:356.18,实测值:356.19。在柱子上也收集到了过度还原的产物醇(65克)。 实施例188.((2s,3s,4s)-1-(4-(苄氧基)苯基)-3-羟基-5-((s)-4-异丙基-2-氧代恶唑烷-3-基)-4-甲基-5-氧代戊烷-2-基)氨基甲酸叔丁酯的合成。 在室温下,向(s)-4-异丙基-3-丙酰基丙二唑烷-2-酮(92.6g,0.50mol,1.1eq)的无水二氯甲烷溶液(1.5l)中加入dipea(70.5g,0.54mol,1.2eq)。将混合物冷却至-10℃,并在n2下加入n-bu2botf(在1.0m二氯甲烷中,500ml,1.1eq)。在加入期间,反应混合物的温度保持在0℃以下。然后将反应在0℃下搅拌1小时,然后冷却至-78℃,逐滴加入(s)-4-异丙基-3-丙酰基恶唑烷丁-2-酮(161g,0.45mol,1.0eq)的二氯甲烷(1l)溶液。在加入期间,反应混合物的温度控制在0℃以下。将混合物在-78℃下搅拌2小时,然后缓慢升温至室温并搅拌过夜。加入pbs(0.1m,ph7.0,2l)。相分离后,将水相进一步用二氯甲烷(2×500ml)萃取。合并的有机层经无水硫酸钠干燥,过滤并浓缩。将粗产物再溶解于甲醇(2l)中,冷却至0℃,然后与h2o2(30%水溶液,500ml)混合并搅拌1小时。通过旋转蒸发除去甲醇,并加入水(3l)。所得混合物用二氯甲烷(3×800ml)萃取。用水(500ml),饱和碳酸氢钠(500ml)和盐水(500ml)洗涤合并有机层,用无水硫酸钠干燥,过滤并浓缩。将残余物与400g硅胶混合,并通过柱色谱法纯化(2kg硅胶,石油醚至5:1石油醚/乙酸乙酯),得到标题化合物,为泡沫状固体(150g,收率61%)。1hnmr(400mhz,cdcl3)δ7.36(ddd,j=24.2,14.2,7.1hz,5h),7.12(d,j=8.4hz,2h),6.90(d,j=8.5hz,2h),5.02(s,2h),4.69(d,j=9.0hz,1h),4.45(d,j=4.1hz,1h),4.33(t,j=8.4hz,1h),4.15(d,j=8.6hz,1h),3.90(dd,j=16.6,8.0hz,1h),3.85–3.77(m,2h),2.81(d,j=7.6hz,2h),2.27(dd,j=11.4,6.7hz,1h),1.35(s,9h),0.89(dd,j=14.3,6.9hz,6h)。esimsm/z:c30h41n2o7[m+h]+计算值:541.28,实测值:541.30。 实施例189.o-((2s,3s,4s)-5-(4-(苄氧基)苯基)-4-((叔丁氧基羰基)氨基)-1-((s)-4-异丙基-2-氧杂恶唑烷-3-基)-2-甲基-1-氧杂戊烷-3-基)1h-咪唑-1-碳硫酸酯的合成。 将((2s,3s,4s)-1-(4-(苄氧基)苯基)-3-羟基-5-((s)-4-异丙基-2-氧恶唑烷-3-基)-4-甲基-5-氧杂戊烷-2-基)氨基甲酸叔丁酯(200g,0.37mol,1.0eq)和1,1′-硫代羰基二咪唑(198g,1.11mol,3.0eq)在无水四氢呋喃(3.5l)中得混合物回流8小时。之后补充加入1,1’-硫代羰基二咪唑(65g,0.37mol,1.0eq),并将混合物回流过夜。通过旋转蒸发除去四氢呋喃,将残余物与500g硅胶混合,并通过柱色谱法纯化(2kg硅胶,石油醚至3:1石油醚/乙酸乙酯),得到标题化合物,为黄色泡沫状物(170g,收率83%)。1hnmr(400mhz,cdcl3)δ8.41(s,1h),7.67(s,1h),7.36(dt,j=16.0,6.9hz,6h),7.09(s,1h),7.05(d,j=8.4hz,2h),6.86(d,j=8.4hz,2h),6.32(d,j=9.5hz,1h),5.01(s,2h),4.56–4.43(m,2h),4.32(ddd,j=16.2,15.6,7.8hz,3h),4.19(d,j=8.7hz,1h),2.96(dd,j=14.6,4.4hz,1h),2.49(dd,j=14.5,10.5hz,1h),2.29(td,j=13.4,6.7hz,1h),1.73(s,1h),1.29(s,9h),0.91(dd,j=13.9,6.9hz,6h)。esimsm/z:c34h43n4o7s[m+h]+计算值:651.27,实测值:651.39。 实施例190.((2r,4s)-1-(4-(苄氧基)苯基)-5-((s)-4-异丙基-2-氧代恶唑烷-3-基)-4-甲基-5-氧戊烷-2-基)氨基甲酸叔丁酯的合成。 向o-((2s,3s,4s)-5-(4-(苄氧基)苯基)-4-((叔丁氧羰基)氨基)-1-((s)-4-异丙基-2-氧杂恶唑烷-3-基)-2-甲基-1-氧杂戊烷-3-基)1h-咪唑-1-碳硫酸酯(210g,0.323mol,1.0eq)的无水甲苯(3l)溶液中依次加入n-bu3snh(182g,0.646mol,2.0eq)和偶氮二异丁腈(0.5g,3.23mmol,0.1eq)。将混合物回流1.0小时,然后浓缩。将残余物与500g硅胶混合并通过柱色谱法纯化(2kg硅胶,石油醚至5:1石油醚/乙酸乙酯),得到标题化合物,为白色泡沫状物(141g,收率83%)。1hnmr(400mhz,cdcl3)δ7.36(ddd,j=24.5,14.5,7.1hz,5h),7.08(d,j=8.5hz,2h),6.90(d,j=8.5hz,2h),5.04(d,j=5.1hz,2h),4.48(d,j=4.2hz,1h),4.33(t,j=8.4hz,1h),4.22(d,j=9.7hz,1h),4.15(d,j=8.8hz,1h),3.81(s,2h),2.73(dd,j=14.1,5.9hz,1h),2.61(dd,j=14.0,7.2hz,1h),2.29(dq,j=13.5,6.8hz,1h),2.11–2.00(m,1h),1.60(dd,j=15.2,6.2hz,2h),1.35(s,9h),1.20(d,j=6.9hz,3h),0.89(dd,j=14.0,6.9hz,6h)。esimsm/z:c30h41n2o6[m+h]+计算值:525.28,实测值:525.37。 实施例191.(2s,4r)-5-(4-(苄氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸的合成。 在0℃下,向((2r,4s)-1-(4-(苄氧基)苯基)-5-((s)-4-异丙基-2-氧代恶唑烷-3-基)-4-甲基-5-酮戊烷-2-基)氨基甲酸叔丁酯(208g,0.39mol,1.0eq)的四氢呋喃(2.1l)和水(700ml)溶液中加入lioh(23.7g,0.99mmol,2.5eq)的h2o2溶液(30%水溶液,336ml,2.97mol,7.6eq)。在0℃下搅拌3小时后,加入亚硫酸氢钠溶液(1.5m,2l)以淬灭反应,滴加2nhcl直至达到ph4。然后用乙酸乙酯(3×800ml)萃取反应混合物。乙酸乙酯溶液用水(500ml)和盐水(500ml)洗涤,用无水硫酸钠干燥,过滤并浓缩。将残余物与硅胶(400g)混合并通过柱色谱(2kg硅胶,石油醚至3:1石油醚/乙酸乙酯)纯化,得到标题化合物,为白色固体(158g,收率96%)。1hnmr(400mhz,cdcl3)δ7.46–7.28(m,5h),7.07(d,j=7.7hz,2h),6.91(d,j=7.8hz,2h),5.04(s,2h),4.52(d,j=8.5hz,1h),3.87(d,j=41.8hz,1h),2.82–2.43(m,3h),1.85(t,j=12.2hz,1h),1.41(s,9h),1.17(d,j=6.9hz,3h)。esimsm/z:c24h32no5[m+h]+计算值:414.22,实测值:414.21。 实施例192.(2s,4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基苯基)-2-甲基戊酸的合成。 将(2s,4r)-5-(4-(苄氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸(158g,0.38mol,1.0eq.)和pd/c(10%,15g)的甲醇(1.5l)溶液在1atmh2下反应16小时,然后通过硅藻土(助滤剂)过滤。浓缩滤液,得到标题化合物,为白色固体(123g,收率>100%)。1hnmr(400mhz,cdcl3)δ7.00(d,j=7.5hz,2h),6.80(s,2h),4.51(d,j=9.0hz,1h),3.88(s,1h),2.66(dd,j=65.6,22.6hz,4h),1.88(t,j=12.2hz,1h),1.42(s,9h),1.14(d,j=6.6hz,3h)。esimsm/z:c17h26no5[m+h]+计算值:324.17,实测值:324.16。 实施例193.(2s,4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸的合成。 向(2s,4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基苯基)-2-甲基戊酸(113g,0.35mol,1.0eq.)的四氢呋喃(1.5l)溶液中逐滴加入t-buono(360g,3.5mol,10.0eq),并在室温下搅拌3小时,然后与硅胶(300g)混合并浓缩,装载在柱(1.5kg硅胶)上,用石油醚洗脱(5:1石油醚/乙酸乙酯和2:1石油醚/乙酸乙酯),得到标题化合物,为黄色固体(85g,收率61%)。1hnmr(400mhz,dmso)δ12.00(s,1h),10.68(s,1h),7.67(s,1h),7.34(d,j=8.4hz,1h),7.03(d,j=8.4hz,1h),6.69(d,j=8.9hz,1h),3.56(d,j=3.8hz,1h),2.67(dd,j=13.5,5.1hz,1h),2.41(dd,j=13.8,6.6hz,1h),1.78–1.65(m,1h),1.27(s,9h),1.18(s,1h),1.05(d,j=7.1hz,3h)。esimsm/z:c17h25n2o7[m+h]+计算值:369.15,实测值:369.14。 实施例194.(2s,4r)-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸的合成。 将(2s,4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸(51.6g,0.14mol,1.0eq.)和pd/c(10wt%,5g)的甲醇(500ml)溶液在室温下氢化(1atm)反应2小时,然后通过硅藻土(助滤剂)过滤。浓缩滤液,得到标题化合物,为棕色泡沫状物(43.8g,收率93%)。esimsm/z:c17h27n2o5[m+h]+计算值:339.18,实测值:339.17。 实施例195.4-((苄氧基)羰基)氨基)丁酸的合成。 在-20℃下,向naoh(23.3g,0.58mol,2.0eq)的水(140ml)溶液中加入4-氨基丁酸(30.0g,0.29mol,1.0eq)和四氢呋喃(60ml),然后逐滴加入cbzcl(54ml,0.38mol,1.3eq)的四氢呋喃(57ml)溶液。将反应混合物在室温下搅拌4小时,然后浓缩并用乙酸乙酯(4×100ml)洗涤。加入浓盐酸调节溶液ph至3,用乙酸乙酯(4×150ml,2×100ml)萃取,合并的有机相用盐水洗涤,用无水硫酸钠干燥,过滤并浓缩,得到标题化合物,为白色固体(48.3g,70.3%)。esimsm/z:c12h16no4[m+h]+计算值:238.1,实测值:238.1。 实施例196.4-(((苄氧基)羰基)氨基)丁酸叔丁酯的合成。 在0℃下,向4-((((苄氧基)羰基)氨基)丁酸(48.0g,0.2mol,1.0eq)和t-buoh(58.0ml,0.6mol,3.0eq)的无水二氯甲烷(480ml)溶液中加入dcc(50.0g,0.24mol,1.2eq)和dmap(2.5g,0.02mol,0.1eq),然后将混合物升温至室温并搅拌过夜。滤出固体并将滤液浓缩,然后用乙酸乙酯(400ml)稀释,并用5%碳酸氢钠溶液和盐水洗涤,经无水硫酸钠干燥,过滤,然后浓缩。残余物通过硅胶柱色谱纯化(石油醚/乙酸乙酯=5∶1),得到标题化合物,为无色油状物(32.8g,55.1%)。esimsm/z:c16h24no4[m+h]+计算值:294.2,实测值:294.2。 实施例197.4-氨基丁酸叔丁酯的合成。 在氢化瓶中,向4-((((苄氧基)羰基)氨基)丁酸叔丁酯(29.0g,0.099mol,1.0eq.)的甲醇(100ml)溶液中加入pd/c(2.9g,10%pd/c,50%水)。将混合物在1atmh2下振动过夜。将反应混合物过滤,并将滤液浓缩,得到标题化合物,为无色油状物(13.8g,收率83.7%)。esimsm/z:c8h18no2[m+h]+计算值:160.1,实测值:160.1。 实施例198.2,5,8,11,14,17,20,23,26-壬氧二十八烷-28-酸叔丁酯的合成。 将nah(60%,24g,600mmol)加入到八乙二醇单甲醚(115g,300mmol)的四氢呋喃(3.0l)溶液中。在室温搅拌后搅拌1小时,将2-溴乙酸叔丁酯(146g,750mmol)加入到混合物中,并在室温搅拌1小时。然后将混合物用二氯甲烷(4l)稀释并倒入冰水(2kg)中。分离有机相,水相用二氯甲烷(1l)萃取。合并的有机相用水洗涤,用无水硫酸钠干燥。通过柱色谱法纯化(20%乙酸乙酯/石油醚,然后纯二氯甲烷至5%甲醇/二氯甲烷洗脱),得到标题化合物,为黄色油状物(108g,收率72%)。 实施例199.2,5,8,11,14,17,20,23,26-九氧杂二十八烷-28-酸的合成。 将2,5,8,11,14,17,20,23,26-九氧杂二十八烷-28-叔丁酯(210g,422mmol)溶解在二氯甲烷(400ml)和无水甲酸(1l)中。将所得溶液在室温搅拌,过夜。真空除去所有挥发物,得到标题化合物,为黄色油状物(200g,收率>100%)。 实施例200.2,5,8,11,14,17,20,23,26-九氧杂二十八烷-28-酰氯的合成。 于室温下将2,5,8,11,14,17,20,23,26-九氧杂二十八烷-28-酸(198g,422mmol)溶于二氯甲烷(2.6l),加入(cocl)2(275ml)和dmf(0.5ml)。将所得溶液在室温持续搅拌3小时。真空除去所有挥发物,得到标题化合物,为黄色油状物(210g,收率>100%)。 实施例201.(s)-34-(((苄氧基)羰基)氨基)-28-氧-2,5,8,11,14,17,20,23,26-九氧杂-29-氮杂三十五烷-35-酸的合成。 将z-l-lys-oh(236g,844mmol),na2co3(89.5g,844mmol)和naoh(33.8g,844mmol)溶于水(1.6l)中。并将混合物用冰盐浴冷却至0℃以下,向其中加入2,5,8,11,14,17,20,23,26-九氧杂二十八烷-28-酰氯(210g,422mmol)的四氢呋喃溶液(160ml)。将所得混合物在室温下搅拌1小时,然后用乙酸乙酯(1l)稀释。分离水层,在冰浴上使用浓hcl将ph调节至3。用二氯甲烷萃取,将有机层用盐水洗涤,用硫酸钠干燥并浓缩,得到标题化合物,为黄色油状物(290g,收率97%)。 实施例202.(s)-五氟苯基34-(((苄氧基)羰基)氨基)-28-氧代-2,5,8,11,14,17,20,23,26-九氧杂-29-氮杂三十五烷-35-酯的合成。 向(s)-34-(((苄氧基)羰基)氨基)-28-氧杂-2,5,8,11,14,17,20,23,26-九氧杂-29-氮杂三十五烷-35-酸(183g,260mmol)的二氯甲烷(2l)溶液中加入五氟苯酚(95.4g,520mmol)和dic(131g,1.04mol)。将反应在室温下搅拌1小时,然后浓缩,得到粗标题产物(430g)。 实施例203.(s)-34-(((苄氧基)羰基)氨基)-28,35-二氧代-2,5,8,11,14,17,20,23,26-九氧杂-29,36-二氮杂四十烷-40-叔丁酯的合成。 在0℃下,向4-氨基丁酸叔丁酯(62.0g,390mmol)的dmf(1.5l)溶液中加入dipea(134g,1.04mol),然后在10-20℃下加入(s)-五氟苯基34-((苄氧基)羰基)-氨基)-28-氧代-2,5,8,11,14,17,20,23,26-九氧杂-29-氮杂三十五烷-35-酯(430g,粗制),将所得混合物在室温下搅拌1小时。在真空下除去dmf,残留物用二氯甲烷稀释,用水洗涤。水相用二氯甲烷反萃取。合并的有机相用0.2nhcl和盐水洗涤,用无水硫酸钠干燥,过滤并浓缩。柱色谱(25%乙酸乙酯/石油醚至纯乙酸乙酯,然后0-5%甲醇/二氯甲烷)纯化,得到黄色油状标题化合物(180g,收率82%)。 实施例204.(s)-34-氨基-28,35-二氧代-2,5,8,11,14,17,20,23,26-九氧杂-29,36-二氮杂四十烷-40-叔丁酯的合成。 向(s)-34-(((苄氧基)羰基)氨基)-28,35-二氧代-2,5,8,11,14,17,20,23,26-九氧杂-29,36-二氮杂四十烷-40-叔丁酯(78.0g,92.3mmol,1.0eq.)的甲醇(500ml)溶液中加入pd/c(13g,10%pd/c,50%水)。将混合物在1atmh2下室温反应过夜,然后过滤并浓缩。通过柱色谱法(0-20%甲醇/二氯甲烷)纯化残余物,得到标题化合物,为绿黄色油状物(70.2g,收率92%)。 实施例205.11-(苄氧基)-11-氧杂十一烷酸的合成。 向十一烷二酸(1.73g,8mmol)的dmf(30ml)溶液中加入k2co3(1.1g,8mmol)和bnbr(1.36g,8mmol)。将混合物在室温搅拌过夜,然后浓缩,并通过柱色谱法(石油醚/乙酸乙酯)纯化,得到标题化合物(1.1g,收率45%)。esimsm/z:c18h27o4[m+h]+计算值:307.18,实测值307.15。 实施例206.3-(2-(2-(二(苄基氨基)乙氧基)乙氧基)丙酸的合成。 向3-(2-(2-(2-(二(苄基氨基)乙氧基)乙氧基)丙酸叔丁酯(2.00g,4.84mmol)的二氯甲烷(5ml)溶液中加入hco2h(5ml)。将反应物在室温下搅拌过夜,然后浓缩至干,并与二氯甲烷共蒸发两次,并将残余物置于油泵上抽干,得到标题化合物(1.72g,收率)。esimsm/z:c21h27no4[m+h]+计算值:358.19,实测值:358.19。 实施例207.2-苄基-11-氧代-1-苯基-5,8,15,18-四氧杂-2,12-二氮杂二十一烷-21-叔丁酯的合成。 在0℃下,向3-(2-(2-(2-(二苄基氨基)乙氧基)乙氧基)丙酸(1.12g,4.83mmol)和3-(2-(2-(2-氨基乙氧基)乙氧基)丙酸叔丁酯(1.72g,4.83)的二氯甲烷(30ml)溶液中加入hatu(1.83g,4.83mmol)和tea(0.68ml,4.83mmol)。反应升温至室温,并搅拌1小时,然后用50ml二氯甲烷稀释,倒入装有50ml水的分液漏斗中。分离有机相,并用盐水(50ml)洗涤,经无水硫酸钠干燥,过滤并浓缩。残余物通过柱色谱法(甲醇/二氯甲烷)纯化,得到标题化合物(2.21g,收率80%)。esimsm/z:c32h48n2o7[m+h]+计算值:573.35,实测值573.35。 实施例208.1-氨基-9-氧代-3,6,13,16-四氧杂-10-氮杂十九烷-19-叔丁酯的的合成。 在氢化瓶中,向2-苄基-11-苄基-1-氧-1-苯基叔丁基-5,8,15,18-四氧杂-2,12-二氮杂二十烷-21-叔丁酯(2.21g,3.86mmol)的甲醇(20ml)溶液中加入pd/c(10wt%,0.2g)。将混合物在1atmh2下搅拌过夜,通过硅藻土(助滤剂)过滤,并将滤液浓缩,得到标题化合物(1.5g,收率)。esimsm/z:c18h36n2o7[m+h]+计算值:393.25,实测值:393.25。 实施例209.31-苄基1-叔丁基11,21-二氧代-4,7,14,17-四氧杂-10,20-二氮杂三十一烷-1,31-二酯的合成。 向1-氨基-9-氧代-3,6,13,16-四氧杂-10-氮杂十九烷-19-叔丁酯(1.50g,3.86mmol)和11-(苄氧基)-11-氧杂十一酸(1.10g,3.6mmol)的二氯甲烷(50ml)溶液中加入hatu(1.48g,3.9mmol)和tea(0.55ml,3.9mmol)。将反应混合物在室温下搅拌1小时,然后用50ml二氯甲烷稀释并倒入含有50毫升水的分液漏斗中。分离有机相,用盐水(50ml)洗涤,用无水硫酸钠干燥,过滤并浓缩。通过柱色谱法(甲醇/二氯甲烷)纯化残余物,得到标题化合物(1.50g,61%收率)。esimsm/z:c36h61n2o10[m+h]+计算值:681.42,实测值:681.42。 实施例210.3,13,23-三氧-1-苯基-2,17,20,27,30-五氧杂-14,24-二氮杂三十三烷-33-酸的合成。 向31-苄基1-11,21-二氧代-4,7,14,17-四氧杂-10,20-二氮杂三十一烷-1,31-二酯(1.50g,2.2mmol)的二氯甲烷(1ml)溶液中加入tfa(3ml)。将反应在室温下搅拌1小时,然后浓缩至干并用二氯甲烷共浓缩两次,并将残余物置于油泵上抽干,得到标题化合物(0.09g,2.2mmol,粗产物)。esimsm/z:c32h53n2o10[m+h]+计算值:625.36,实测值:625.35。 实施例211.(s)-39-(((苄氧基)羰基)氨基)-3,13,23,33-四氧代-1-苯基-2,17,20,27,30-五氧杂-14,24,34-三氮杂四十烷-40-酸的合成。 向3,13,23-三氧代-1-苯基-2,17,20,27,30-五氧杂-14,24-二氮杂三十三烷-33-酸(1.50g,2.20mmol)和z-lys-oh(0.62g,2.20mmol)的二氯甲烷(50ml)溶液中加入hatu(0.84g,2.20mmol)和tea(0.31ml,2.20mmol)。将反应混合物在室温下搅拌1小时,然后用50ml二氯甲烷稀释,倒入含有100ml水的分液漏斗中。分离有机相,并用盐水(100ml)洗涤,经无水硫酸钠干燥,过滤并浓缩。残余物通过柱色谱法(甲醇/二氯甲烷)纯化,得到标题化合物(1.00g,收率53%)。esimsm/z:c46h71n4o13[m+h]+计算值:887.49,实测值:887.50。 实施例212.(s)-5-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-3,11,21,31-四氧-1-苯基-2,14,17,24,27-五氧杂-4,10,20,30-四氮杂四十一烷-41-苄酯的合成。 向(s)-39-((((苄氧基)羰基)氨基)氨基)-3,13,23,33-四氧-1–1-苯基-2,17,20,27,30-五氧杂-14,24,34-三氮杂四十烷-40-酸(0.50g,0.56mmol)的dmf(5ml)溶液中加入hatu(0.21g,0.56mmol),在室温下搅拌反应30分钟。之后在0℃下,依次加入(2s,4r)5-(3-(4-(氨基氨基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.27g,0.56mmol))的dmf(5ml)的溶液和tea(85μl,0.6mmol),并将反应搅拌1小时。将反应混合物倒入装有100ml水的分液漏斗中,并用50ml乙酸乙酯萃取两次。将有机相用100ml盐水洗涤一次,用无水硫酸钠干燥,过滤并浓缩。通过柱色谱(甲醇/二氯甲烷)纯化残余物,得到标题化合物(0.40g,收率55%)。esimsm/z:c71h110n7o18[m+h]+计算值:1348.78,实测值:1348.78。 实施例213.(s)-5-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基甲酰基)-3,11,21,31-四氧代-1-苯基-2,14,17,24,27-五氧杂-4,10,20,30-四氮四十一烷-41-苄酯的合成。 向(s)-39-(((苄氧基)羰基)氨基)-3,13,23,33-四氧代-1-苯基-2,17,20,27,30-五氧杂-14,24,34-三氮杂四十烷-40-酸(0.50g,0.56mmol)的dmf(5ml)溶液中加入hatu(0.21g,0.56mmol),并将反应在室温下搅拌30分钟。之后在0℃下,加入(2s,4r)-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.22g,0.56mmol)的dmf(5ml)溶液和tea(85μl,0.60mmol)。搅拌1小时后,将反应混合物倒入含有100ml水的分液漏斗中,用50ml乙酸乙酯萃取两次。分离有机相并用100ml盐水洗涤,用无水硫酸钠干燥,过滤并浓缩。通过柱色谱法(甲醇/二氯甲烷)纯化残余物,得到标题化合物(0.20g,收率26%)。esimsm/z:c67h103n6o17[m+h]+计算值:1263.73,实测值:1263.73。 实施例214.3,3′-((氧基双(乙烷-2,1-二基))双(氧化))丙二酸二叔丁酯的合成。 向二甘醇(20g,0.188mol)的四氢呋喃(200ml)溶液中加入na(0.43g,0.018mol)。在室温下搅拌1小时后,加入丙烯酸叔丁酯(48g,0.376mol)并将反应混合物在室温下搅拌2天。将反应物真空浓缩并通过柱色谱纯化,得到标题化合物(34g,收率50%)。esimsm/z:c18h35o7[m+h]+计算值:363.23,实测值:363.23。 实施例215.3,3′-((氧基双(乙烷-2,1-二基))双(氧基))二丙酸的合成。 在室温下,将3,3′-((氧双(乙烷-2,1-二基))双(氧))二丙酸二叔丁酯(34g,0.093mol)溶解在甲酸(100ml)中并搅拌过夜,将反应真空浓缩,得到标题化合物。esimsm/z:c10h19o7[m+h]+计算值:251.11,实测值:251.11。 实施例216.2,2-二甲基-4、14、24-三氧杂-3、7、10、17、20、27、30、33-八氧杂-13、23-二氮杂三十六烷-36-酸的合成。 向1-氨基-9-氧代-3,6,6,16-四氧杂-10-氮杂十九烷-19-叔丁酯(1.50g,3.82mmol)和3,3′-((氧化双(乙烷-2,1,1-二基))双(氧基))丙二酸(1.90g,7.64mmol)的dmf(10ml)溶液中加入hatu(1.45g,3.82mmol)和dipea(0.66ml,3.82mmol)。在0℃下将反应混合物升温至室温并搅1小时,然后用二氯甲烷(80ml)稀释,用水(10ml)洗涤,用硫酸钠干燥,过滤,浓缩并通过硅胶柱色谱法纯化,得到标题化合物,为无色液体(1.75g,收率75%)。esimsm/z:c28h53n2o13[m+h]+计算值:625.35,实测值:625.35。 实施例217.1-叔丁基33-(2,5-二氧代吡咯烷-1-基)11,21-二氧代-4,7,14,17,24,27,30-七氧杂-10,20-二氮杂三恶烷-1,33-二酯的合成。 在0℃下,向2,2-二甲基-4,14,24-三氧杂-3,7,10,17,20,27,30,33-八氧杂-13,23-二氮杂三十六烷-36-酸(1.75g,2.8mmol)的二氯甲烷(20ml)溶液中加入edci(1.07g,5.6mmol)和nhs(0.64g,5.6mmol)。将反应升温至室温并搅拌过夜,然后用二氯甲烷(80ml)稀释,用水(10ml)洗涤,再用硫酸钠干燥,过滤并真空浓缩,得到标题化合物(2.00g,收率约100%)。esimsm/z:c32h56n3o15[m+h]+计算值:722.36,实测值:722.36。 实施例218.(s)-42-(((苄氧基)羰基)氨基)-2,2-二甲基-4,14,24,36-四氧代-3,7,10,17,20,27,30,33-八氧杂-13,23,37-三氮杂四十三烷-43-酸的合成。 向n-α-cbz-l-赖氨酸(1.17g,4.2mmol)的水(10ml)溶液中加入碳酸氢钠(0.47g,5.6mmol),将反应混合物冷却至5℃,之后加入1-叔丁基33-(2,5-二氧代吡咯烷-1-基)11,21-二氧代-4,7,14,17,24,27,30-七氧杂-10,20-二氮杂三恶烷-1,33-二酯(2.00g,2.8mmol)的1,4-二氧六环(10ml)溶液。将反应升温至室温并搅拌1小时,加入1nhcl将ph调节至3,用二氯甲烷(50ml×3)萃取。将有机萃取物用水(20ml)洗涤,用硫酸钠干燥,过滤并浓缩,得到标题产物(2.3g,收率92%)。esimsm/z:c42h71n4o16[m+h]+计算值:887.48,实测值:887.48。 实施例219.(s)-5-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-3,11,23,33-四氧代-1-苯基-2,14,17,20,27,30,37,40-八氧杂-4,10,24,34-四氮杂四十三烷-43-叔丁酯的合成。 在0℃下,向(2s,4r)-5-(3-(4-氨基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(1.87g,3.9mmol)和(s)-42-(((苄氧基)-羰基)氨基)-2,2-二甲基-4,14,24,36-四氧代-3,7,10,17,20,27,30,33-十氧杂-13,23,37-三氮杂四十三烷-43-酸(2.3g,2.59mmol)的二氯甲烷(30ml)中加入hatu(0.98g,2.59mmol)和dipea(450μl,2.59mmol)。将反应混合物升温至室温并搅拌1小时,然后真空浓缩并通过硅胶柱色谱纯化,得到标题化合物(2.4g,70%收率)。esimsm/z:c67h110n7o21[m+h]+计算值:1348.77,实测值:1348.77。 实施例220.(s)-43苄基1-叔丁基7-(((苄氧基)羰基)氨基)-6,13,23,33-四氧代-16,19,26,29-四氧杂-5,12的合成,22,32-四氮杂四十三烷-1,43-二酯的合成。 将(s)-39-((苄氧基)羰基)氨基)-3,13,23,33-四氧代-1-苯基-2,17,20,27,30-五氧杂-14,24,34-三氮杂十四烷-40-酸(200mg,0.225mmol)溶于dmf(5ml)中并冷却至0℃,依次加入4-氨基丁酸叔丁酯(71.8mg,0.45mmol)和edc(86.2mg,0.45mmol)。将反应升温至室温并搅拌过夜,倒入冰水中,并用二氯甲烷(3×10ml)萃取。将合并的有机相用水(5ml),盐水(5ml)洗涤,用无水硫酸钠干燥,过滤并浓缩,得到标题化合物(231mg,100%收率)。esimsm/z:c54h86n5o14[m+h]+计算值:1028.61,实测值:1028.61。 实施例221.(s)-43苄基1-(2-((s)-39-(((苄氧基)羰基)氨基)-3,13,23,33,40-五氧代-1-苯基-2,17,20,27,30-五氧杂-14,24,34,41-四氮杂四十五酰胺基)-4-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基)7-((苄氧基)羰基)氨基)-6,13,23,33-四氧代-16,19,26,29-四氧杂-5,12,22,32-四氮杂四十三烷-1,43-二酯的合成。 将(s)-43-苄基1-叔丁基7-((((苄氧基)羰基)氨基)-6,13,23,33-四氧代-16,19,26,29-四氧杂-5,12,22,32-四氮杂四十三烷-1,43-二酯(231mg,0.225mmol)溶于二氯甲烷(3ml)中,并在室温下于tfa(3ml)反应1小时。将反应浓缩并重新溶解在dmf(5ml)中,冷却至0℃,向(2s,4r)-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(44mg,0.112mmol)中依次加入hatu(86mg,0.225mmol)和dipea(39μl,0.225mmol)。将反应升温至室温并搅拌过夜,倒入冰水中,并用二氯甲烷(3×10ml)萃取。将合并的有机相用1nhcl(5ml),水(5ml),盐水(5ml)洗涤,用无水硫酸钠干燥,过滤并浓缩,通过硅胶柱色谱法(0-5%甲醇/二氯甲烷),得到白色泡沫状物(209mg,收率81%)。esimsm/z:c121h185n12o31[m+h]+计算值:2302.32,实测值:2302.80。 实施例222.(s)-7-氨基-1-((2-((r)-7-氨基-42-羧基-6,13,23,33-四氧代-16,19,26,29-四氧代-5,12,22,32-四氮杂-1-酰基)氧基)-5-((2r,4s)-5-(叔丁氧基)-2-(叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基)氨基-1,6,13,23,33-五氧杂-16,19,26,29-四氧杂-5,12,22,32-四氮杂四十三烷-43-酸的合成 将(s)-43苄基1-(2-((s)-39-((((苄氧基)羰基)氨基)-3,13,23,33,40-五氧代-1-苯基-2,17,20,27,30-五氧杂-14,24,34,41-四氮杂戊四酮氨基)-4-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基)7-((苄氧基)-羰基)氨基)-6,13,23,33-四氧代-16,19,26,29-四氧杂-5,12,22,32-四氮杂四十三烷-1,43-二酯(206mg,0.089mmol)溶于甲醇(5ml)中,并与pd/c(10wt%,20mg)混合,在1atm压力h2下反应过夜。然后将混合物通过硅藻土(助滤剂)过滤,浓缩滤液,得到标题化合物(166mg,收率100%)。esimsm/z:c91h161n12o27[m+h]+计算值:1854.15,实测值:1854.80。 实施例223.1,1′-(((8r,27s)-36-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5)-氧代戊基)-17,18-双(2-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)乙酰基)-2,7,10,15,20,25,28,33-八氧代-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34-十二烷二氢-2h-苯并[b][1,4,9,12,17,20,21,24,29,32]氧杂九氮杂环三十六烷-8,27-二基)双(6,16,26-三氧代-9,12,19,22-四氧杂-5,15,25-三氮杂三十六烷-36-酸)的合成。 在0℃下,向(s)-7-氨基-1-((2-((r)-7-氨基-42-羧基-6,13,23,33-四氧代-16,19,26,29-四氧杂-5,12,22,32-四氮杂四十二烷-1-酰基)氧基)-5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基)氨基)-1,6,13,23,33-五氧杂-16,19,26,29-四氧杂-5,12,22,32-四氮杂四十三烷-43-酸(165mg,0.089mmol)的乙醇(10ml)溶液中加入双(2,5-二氧吡咯烷-1-基)4,4′-((2,2′-(1,2-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰基)肼-1,2-二(乙酰基))双(氮杂二酰基))二丁酯(70mg,0.089mmol)和磷酸盐缓冲液(0.5m,ph7.5,3ml)。将反应物在室温下搅拌过夜,然后浓缩并通过硅胶柱色谱法(0-6%甲醇/二氯甲烷)纯化,得到标题化合物666(130mg,收率62%)。esimsm/z:c115h185n18o37[m+h]+计算值:2410.31,实测值:2410.60。 实施例224.1,1′-((8r,27s)-36-((2r,4s)-2-氨基-4-羧基戊基)-17,18-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰基)-2,7,10,15,20,25,28,33-八氧代-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34-三十二烷-2h-苯并[b][1,4,9,12,17,20,21,24,29,32]氧杂九氮杂环三十六烷-8,27-二基)双(6,16,26-三氧杂-9,12,19,22-四氧杂-5,15,25-三氮杂三十烷-36-酸)的合成。 将1,1′-((8r,27s)-36-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-17,18-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰基)-2,7,10,15,20,25,28,33-八氧代-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34-三十二烷-2h-苯并[b][1,4,9,12,17,20,21,24,29,32]氧杂七氮杂环三十六烷-8,27-二基)双(6,16,26-三氧-9,12,19,22-四氧杂-5,15,25-三氮杂三十六烷-36-酸(128mg,0.053mmol)溶于二氯甲烷(3ml)中,并在室温下与tfa(3ml)反应2小时。将反应浓缩并与二氯甲烷共浓缩3次,得到标题化合物(120mg,收率100%)。esimsm/z:c106h169n18o35[m+h]+计算值:2254.19,实测值:2254.30。 实施例225.1,1′-(((8r,27s)-36-((2r,4s)-2-(2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧杂-12-氧杂-2,5,8-三氮杂异烟酸酯-11-基)噻唑-4-羧酰胺基)-4-羧基戊基)-17,18-双(2-(2-,2,5-二氧-2-,5-二氢-1h-吡咯-1-基)乙酰基)-2,7,10,15,20,25,28,33-八氧-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34-十二烷二氢-2h-苯并[b][1,4,9,12,17,20,21,24,29,32]-氧杂杂氮杂环六三十烷-8,27-二基)双(6,16,26-三氧代-9,12,19,22-四氧代-5,15,25-三氮杂三十烷-36-酸)(b-01)的合成。 将1,1′-(((8r,27s)-36-((2r,4s)-2-(2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧杂-12-oxa-2,5,8-三氮杂异烟酸酯-11-基)噻唑-4-羧酰胺基)-4-羧基戊基)-17,18-双(2-(2-,2,5-二氧-2-,5-二氢-1h-吡咯-1-基)乙酰基)-2,7,10,15,20,25,28,33-八氧-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34-十二烷二氢-2h-苯并[b][1,4,9,12,17,20,21,24,29,32]-氧杂氮杂环六三十烷-8,27-二基)双(6,16,26-三氧代-9,12,19,22-四氧代-5,15,25-三氮杂三十烷-36-酸)(120mg,0.053mmol)和41a(36.6mg,0.053mmol)溶于dma(5ml)中,冷却至0℃。加入dipea(18μl,0.106mmol),并将反应升温至室温,搅拌1小时。浓缩反应混合物后,将残余物通过制备型hplc纯化(c18,10-90%乙腈/水),得到标题化合物(b-1)(70mg,收率49%)。esimsm/z:c131h209n22o40s[m+h]+计算值:2762.46,实测值:2762.85。 实施例226.(7s,10r,11s,14s)-10,11-二叔丁基(((苄氧基)-羰基)氨基)-6,9,12,15-四氧代-7,14-双(31-氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32-氮杂三十六烷-36-基)-5,8,13,16-四氮杂二十烷-1,20-二酯的合成。 将(s)-叔丁基37-(((苄氧基)羰基)氨基)-31,38-二氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32,39-二氮杂四十三烷-43-酯(5.98g,6.73mmol)和pd/c(10wt%,0.6g)的甲醇(30ml)溶液在1atmh2压力下氢化过夜,然后通过硅藻土过滤(助滤剂)。浓缩滤液并重新溶于四氢呋喃(60ml)中,在0℃下,加入(2r,3s)-2,3-双(((苄氧基)羰基)氨基)琥珀酸(1.01g,2.42mmol),hobt(817mg,6.05mmol)dcc(1.25g,6.05mmol)和dipea(2.1ml,12.10mmol)。将反应物在室温下搅拌过夜,然后用乙酸乙酯(400ml)稀释,并用0.1nhcl,饱和碳酸氢钠和盐水洗涤,用无水无水硫酸钠干燥,过滤,浓缩并通过硅胶柱色谱法(24:1二氯甲烷/甲醇)纯化,得到标题化合物(5.65g,收率49%)。esimsm/z:c90h154n8o34[m+h]+计算值:1892.06,实测值:1892.60。 实施例227.(7s,10r,11s,14s)-10,11-二氨基-6,9,12,15-四氧代-7,14-双(31-氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32-氮杂三十六烷-36-基)-5,8,13,16-四氮杂二十烷-1,20-二叔丁酯的合成。 将(7s,10r,11s,14s)-10,11-双((((苄氧基)-羰基)氨基)-6,9,12,12,15-四氧-7,14-双(31-氧代2、5、8、11、14、17、20、23、26、29-十氧杂-32-氮杂三十六烷-36-基)-5、8、13、16-四氮杂二十烷-1,20-二叔丁酯(3.71g,1.96mmol)和pd/c(10wt%,0.40g)的甲醇(50ml)溶液在1atmh2压力反应过夜,然后通过硅藻土(助滤剂)过滤,得到标题化合物(3.18g,收率100%)。esimsm/z:c74h142n8o30[m+h]+计算值:623.98,实测值:1624.50。 实施例228.(7s,10r,11s,14s)-10,11-双(4-(2,5-二氧2-,5-二氢-1h-吡咯-1-基)丁酰胺基)-6,9,12、15-四氧杂-7、14-双(31-氧杂-2,5,8,11,14,17,20,23,26,29-十氧杂-32-氮杂三十六烷-36-基)-5,8、13、16-四氮杂二十烷-1、20-二酸的合成。 向(7s,10r,11s,14s)-二叔丁基10,11-二氨基-6,9,12,12,15-四氧-7,14-双(31-氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32-氮杂三十六烷-36-基)-5、8、13、16-四氮杂二十烷-1、20-二酯(315mg,0.194mmol))的dma(10ml)溶液中加入edc(150mg,0.785mmol)和4-马来酰基丁酸(72mg,0.57mmol)。将混合物在室温搅拌12小时,浓缩并通过硅胶柱色谱法纯化(1:4甲醇/二氯甲烷),得到油状物(329mg,收率87%),将其溶于二氯甲烷(25ml)中并与tfa(5ml)在室温下反应1小时,然后浓缩,得到标题化合物(309mg,收率99%)。esimsm/z:c82h140n10o36[m+h]+计算值:1841.94,实测值:1842.50。 实施例229.(2s,4r)-5-(((8s,11s,12r,15s)-11,12-双(4-(2,5-二氧代-2,5-二氢代-1h-))吡咯-1-基)丁酰胺基)-2,7,10,13,16,21-六氧代-8,15-双(31-氧代-2,5,8,11,14,17,20,23,26,29-十氧代-32-氮杂六三十烷-36-基)-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22-二十二氢-2h-苯并[b][1、4、9、12、17、20]氧杂五氮杂环二十四烷-24-基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(7s、10r、11s、14s14s)-10,11-11-双(4-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基-正丁胺基亚基)-6,9,12,12,15-四氧代-7,14-双(31-氧代-2,5,8,11,14,17,20,20,23,26,29,29-十氧代烷-32-氮杂三十六烷-36-基]-5,8,13,16-四氮杂二十烷-1,20-二酸(154mg,0.0837mmol)和(2s,4r)-5-(3-氨基-4-羟基苯基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯(33mg,0.0837mmol)的dmf(6ml)溶液冷却至0℃,并依次加入hatu(64mg,0.167mmol)和tea(46μl,0.335mmol)。将反应搅拌1小时,然后用水(100ml)稀释,并用乙酸乙酯(3×100ml)萃取。用盐水洗涤乙酸乙酯溶液,在无水无水硫酸钠上干燥,过滤,浓缩并通过硅胶柱层析法(6:1二氯甲烷/甲醇)纯化,得到标题化合物(95mg,收率52%)。esimsm/z:c103h170n12o39[m+h]+计算值:2200.17,实测值:2200.90。 实施例230.(2s,4s)-5-(((8s,11s,12r,15s)-11,12-双(4-(2,5-二氧代-2,5-二氢-1h-吡咯-1)-基)丁酰胺基)-2,7,10,13,16,21-六氧代-8,15-双(31-氧代-2,5,8,11,14,17,20,23,26,29-十氧代-32-氮杂三十六烷-36-基)-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22-icosahydro-2h-苯并[b][1、4、9、12、17、20]氧杂五氮杂环二十四烷24-基)-4-(2-((6s,9r,11r)-6-((s)-仲-丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧十二烷基-氧杂-2,5,8-三氮杂十一烷-11-基)噻唑-4-甲酰胺基)-2-甲基戊酸的合成(b-02)。 向(2s,4r)-5-(((8s,11s,12r,15s)-11)-1-基)丁酰胺基)-2,7,10,13,16,21-是氧代-8,15-双(31-氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32-氮杂三十六烷-36-基)-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22-二十氢-2h-苯并[b][1,4,9,12,17,20]氧杂五氮杂环二十四烷24-基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯(98mg,0.045mmol)的二氯甲烷(3ml)溶液中加入tfa(6ml)。将反应混合物在室温搅拌1小时,然后浓缩并重新溶于dma(1ml),加入2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧杂十二-氧代-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸酯(31mg,0.045mmol)和dipea(12μl,0.068mmol)。将反应混合物在室温搅拌90分钟,然后浓缩,并通过反相hplc(c18柱,10-100%乙腈/水)纯化,得到标题化合物(b-2)(36.2mg,62%产率)。esimsm/z:c119h194n16o42s[m+h]+计算值:1276.66,实测值:1276.65。 实施例231.(s)-11-(5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-5-氧戊二酰氨基)十一酸的合成。 向boc-glu(otbu)-oh(0.50g,1.65mmol)的dmf(10ml)溶液中加入hatu(0.69g,1.82mmol)和tea(0.26ml,1.82mmol)。搅拌30分钟后,加入11-氨基十一酸(0.33g,1.65mmol)的dmf(10ml)溶液,并将反应混合物在室温搅拌1小时,然后倒入装有200ml1nhcl的分液漏斗中,并用二氯甲烷(3×50ml)萃取。有机相用100ml盐水洗涤一次,然后用无水无水硫酸钠干燥,过滤并浓缩。残余物通过柱色谱法(甲醇/二氯甲烷)纯化,得到标题化合物(1.0g,收率>100%)。esimsm/z:c25h47n2o7[m+h]+计算值:487.33,实测值:487.34。 实施例232.(s)-11-(2-氨基-4-羧基丁二酰胺基)十一酸的合成。 向(s)-11-(5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-5-氧戊二酰氨基)十一酸(1.0g,2.05mmol)的二氯甲烷(20ml)溶液中加入tfa(5ml)。将反应在室温下搅拌30分钟,然后浓缩至干,并用二氯甲烷共旋蒸干燥两次。最后置于真空泵上抽干,得到标题化合物(0.68g,2.06mmol,收率100%)。esimsm/z:c16h31n2o5[m+h]+计算值:331.22,实测值:331.22。 实施例233.(2s,4r)-5-(3-(2-((((苄氧基)羰基)氨基)-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(2s,4r)5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.2g,0.51mmol),2-(((苄氧基)将羰基)氨基)-3-甲基丁酸(0.13g,0.51mmol),hatu(0.20g,0.51mmol)溶解于二氯甲烷(20ml)中,然后加入tea(110μl,0.8mmol)。将反应混合物在室温搅拌过夜。然后减压除去溶剂,用硅胶柱纯化,得到标题产物(0.30g,91%)。esimsm/z:c34h50n3o8[m+h]+计算值:628.35,实测值:628.45。 实施例234.(2s,4r)5-(3-(3-(2-氨基-3-甲基丁亚氨基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 在氢化瓶中,将pd/c(0.1g,33wt%,50%水)加入到(2s,4r)-5-(3-(2-(((苄氧基)羰基)氨基)-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.29g,0.46mmol)的甲醇(10ml)溶液中。将混合物在1atmh2下振摇过夜,然后通过硅藻土(助滤剂)过滤。浓缩滤液,得到标题化合物(0.23g,),无需进一步纯化即可用于下一步。esimsm/z:c26h44n3o6[m+h]+计算值:494.64,实测值494.75。 实施例235.(2s,4r)-5-(3-(2-(2-(((((苄氧基)羰基)氨基)丙酰胺基)-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(2s,4r)5-(3-(2-氨基-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.23g,0.46mmol),2-(((苄氧基)羰基)-氨基丙酸(0.10g,0.46mmol)和hatu(0.18g,0.46mmol)溶解在二氯甲烷(20ml)中,然后加入tea(110ul,0.8mmol)。将反应混合物在室温下搅拌过夜,在减压下浓缩,并在硅胶柱上纯化,得到标题产物(0.3g,95%)。esimsm/z:c37h55n4o9[m+h]+计算值:699.39,实测值:699.50。 实施例236.(2s,4r)-5-(3-(2-(2-(2-氨基丙酰胺基)-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 在氢气瓶中,将pd/c(0.1g,33wt%,50%wet)加到(2s,4r)-5-(3-(2-(2-(((苄氧基于甲醇(10ml)中的(羰基)氨基)丙酰胺基)-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.3g,0.43mmol)。将混合物在1atmh2下振摇过夜,然后通过硅藻土(助滤剂)过滤,浓缩滤液,得到标题化合物(0.22g,93%),其无需进一步纯化即可用于下一步。esimsm/z:c29h49n4o7[m+h]+计算值:565.35,实测值:565.60。 实施例237.(2s,4r)-5-((3s,6s,14r,15s)-14,15-双(2-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)乙酰氨基)-3-异丙基-6-甲基-2,5,8,13,16,21-十氧基-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21-二十氢-1h-苯并[b][1,4,7,10,15,20]氧杂五氮杂环二十五烷-25-基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(2s,4r)-5-(3-((s)-2-((s)-2-氨基丙酰胺基)-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯(0.150g,0.27mmol),4,4′-((((2r,3s)-2,3-双(2-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基(乙酰胺基)琥珀酰基)双(氮杂二基)-二丁酸(0.160g,0.270mmol),hatu(0.402g,1.080mmol)溶于二氯甲烷(30ml)中,然后加入tea(55μl,0.4mmol)。将反应混合物在室温搅拌过夜,减压浓缩并在硅胶柱上纯化(用乙酸乙酯/二氯甲烷,1:10至1:5洗脱),得到标题化合物(0.187g,62%)。esimsm/z:c53h73n10o17[m+h]+计算值:1121.51,实测值:1121.75。 实施例238.(2s,4r)-4-氨基-5-((3s,6s,14r,15s)-14,15-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-3-异丙基-6-甲基-2,5,8,13,16,21-十氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21-二十氢-1h-苯并[b][1,4,7,10,15,20]-氧杂五氮杂环二十五烷-25-基)-2-甲基戊酸的合成。 将(2s,4r)-5-((3s,6s,14r,15s)-14,15-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-3-异丙基-6-甲基-2,5,8,13,16,21-十氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21-二十碳氢-1h-苯并[b][1,4,7,10,15,20]-氧杂五氮杂环二十五烷-25-基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.175g,0.156mmol)溶解在二氯甲烷(6ml)中,然后加入tfa(2ml)。将反应混合物在室温搅拌2小时,用甲苯(8ml)稀释,浓缩,得到标题化合物(150mg,收率100%),其无需进一步纯化即可用于下一步。esimsm/z:c44h57n10o15[m+h]+计算值:965.39,实测值:965.70。 实施例239.1-(((2s)-1-((((1r,3r)-1-乙酰氧基-1-(4-(((2r,4s)-1-((3s,6s,14r,15s)-14,15-双(2-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)乙酰氨基)-3-异丙基-6-甲基-2,5,8,13,16,21-十氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21-二十氢-1h-苯并[b][1,4,7,10,15,20]氧杂五氮杂二十五烷-25-基)-4-羧基戊基-2-基)氨基甲酰基)噻唑-2-基)-4-甲基戊基-3-基)(甲基)氨基)-3-甲基-1-氧杂戊-2-基)氨基)-n,n,n,2-四甲基-1-氧代戊基-2-铵(b-03)的合成。 向(2s,4r)-4-氨基-5-((3s,6s,14r,15s)-14,15-双(2-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)乙酰氨基)-3-异丙基-6-甲基-2,5,8,13,16,21-七氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21-二十氢-1h-苯并[b][1,4,7,10,15,20]-氧杂五氮杂环二十五烷-25-基)-2-甲基戊酸(约50mg,0.051mmol)的dma(4ml)溶液中加入1-(((2s)-1-((((1r,3r)-1-乙酰氧基-4-甲基-1-(4-((五氟苯氧基)羰基)噻唑-2-基)戊三基)(甲基)氨基)-3-甲基-1-氧戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-铵(37mg,0.052mmol)和dipea(3.4μl,0.02mmol)。将反应混合物搅拌过夜,浓缩并用hplc纯化,用mecn/h2o梯度洗脱(c-18柱,10mm(d)x250mm(l),在45分钟内10%mecn至70%mecn,9ml/min),得到标题产物(37.1mg,收率49%)。esimsm/z:c70h99n14o20s[m]+计算值:1487.69,实测值:1487.45。 实施例240.(4r)-5-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十烷-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂七氮杂环四十六烷-46-基)-4-(2-(((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧代-2,5,8-三氮杂十一烷基-11-基)噻唑-4-甲酰胺基)-2-甲基戊酸(b-04)的合成。 向(2r)-1-(22,23-双(2,5-二氧-2-),5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-六三水-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂七氮杂环四十六烷-46-基)-4-羧基戊烷-2-铵三氟乙酸盐(60mg,0.050mmol)的dma(15ml)溶液中,加入五氟苯基活性酯(44mg,0.06mmol)和0.1mnah2po4(ph7.5,8.0ml)。将反应混合物搅拌过夜,浓缩并用hplc纯化,用mecn/h2o(c-18柱,10mm(d)x250mm(l),在45分钟内10%mecn至70%mecn,8ml/min)洗脱,得到标题产物b-4(44mg,收率52%)。esimsm/z:c79h117n14o26s[m+h]+计算值:1709.79,实测值:1709.55。 实施例241.(1r,3r)-1-(4-((((2r)-5-((2-氨基乙基)氨基)氨基)-1-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂七氮杂环四十六烷-46-基)-4-甲基-5-氧戊烷-2-基)氨基甲酰基)噻唑-2-基)-3-((2s,3s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基戊酰胺基)-4-甲基戊基乙酸酯(b-5)的合成。 向化合物b-4(22.0mg,0.0129mmol)的dma(1ml)溶液中,加入edc(15.0mg,0.078mmol),乙基-1,2-二胺盐酸盐(8.0mg,0.060mmol)和dipea(0.010ml,0.060mmol)。将混合物搅拌过夜,浓缩,并通过反相hplc纯化(250(l)mm×10(d)mm,c18柱,在40分钟内10-100%乙腈/水,流速8ml/min),得到标题化合物(14.0mg,产率62%)。esimsm/z:c81h123n16o25s[m+h]+计算值:1751.85,实测值:1751.20。 实施例242.(1r,3r)-1-(4-((((28r)-1-氨基-29-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯)-1-yl)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,28,41,44]七氧杂七氮杂环四十六烷-46-基)-26-甲基-25-氧代-3,6,9,12,15,18,21-十氧杂-24-氮杂二十八烷-28-基)氨基甲酰基)噻唑-2-基)-3-((2s,3s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基戊酰胺基)-4-甲基戊基乙酸酯(b-06)的合成。 向化合物b-4(22.0mg,0.0129mmol)的dma(1ml)溶液中加入edc(15.0mg,0.078mmol),3,6,9,12,15,18,21-七氧杂二十三烷-1,23-二胺盐酸盐(26.0mg,0.059mmol)和dipea(0.010ml,0.060mmol)。将混合物搅拌过夜,浓缩,并通过反相hplc(250(l)mmx10(d)mm,c18柱,在40分钟内10-100%乙腈/水,流速8ml/min)纯化,得到标题化合物(14.5mg,收率55%)。esimsm/z:c95h151n16o32s[m+h]+计算值:2060.03,实测值:2060.80。 实施例243.(1r,3r)-1-(4-((((28r)-29-(22,23-双(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基))-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂七氮杂环四十六烷-46-基)-1-羟基-26-甲基-25-氧代-3,6,9,12,15,18,21-十氧杂-24-氮杂二十八烷-28-基)氨基甲酰基)噻唑-2-基)-3-((2s,3s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基戊酰胺基)-4-甲基戊基乙酸酯(b-07)的合成。 向化合物b-4(22.0mg,0.0129mmol)的dma(1ml)溶液中加入edc(15.0mg,0.078mmol)和23-氨基-3,6,9,12,15,18,21-七氧杂二十三烷-1-醇(22.0mg,0.059mmol)。将混合物搅拌过夜,浓缩,并通过反相hplc(250(l)mmx10(d)mm,c18柱,在40分钟内10-100%乙腈/水,流速8ml/min)纯化,得到标题化合物(b-7)(14.1mg,收率53%)。esimsm/z:c95h150n15o33s[m+h]+计算值:2061.02,实测值:2061.74。 实施例244.(2s)-叔丁基2-((4r)-5-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3)的合成,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂七氮杂环四十六烷-46-基)-4-(2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十一烷-11-基)噻唑-4-羧酰胺基)-2-甲基戊酰胺基)-6-((叔丁氧羰基)氨基)己酯(b-08)的合成。 向化合物b-4(25.0mg,0.0146mmol)的dma(1ml)溶液中,加入edc(15.0mg,0.078mmol)和2-氨基-6-(叔丁氧基羰基)氨基)己酸叔丁酯(9.0mg,0.030mmol)。将混合物搅拌过夜,浓缩,并通过反相hplc(250(l)mmx10(d)mm,c18柱,在40分钟内10-100%乙腈/水,流速8ml/min)纯化,得到标题化合物(20.5mg,收率71%)。esimsm/z:c94h144n16o29s[m+h]+计算值:1994.00,实测值:1994.85。 实施例245.(2s)-6-氨基-2-((4r)-5-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂七氮杂环四十六烷-46-基)-4-(2-(((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十一烷-11-基)噻唑-4-羧酰胺基)-2-甲基戊酰胺基己酸(b-09)的合成。 将化合物b-8(20.0mg,0.010mmol)溶于二氯甲烷(1ml)中,然后加入tfa(1ml)。将反应混合物在室温下搅拌2小时,然后浓缩,并通过反相hplc(250(l)mm×10(d)mm,c18柱,10-100%乙腈/水,40分钟,流速8ml/min)纯化,得到标题化合物(13.5mg,收率73%)。esimsm/z:c85h129n16o27s[m+h]+计算值:1837.89,实测值:1838.20。 实施例246.(s)-叔丁基39-氨基-45-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧戊基)-2-羟基苯基)氨基)-11,21,33,40,45-五氧四,7,14,17,24,27,30-七氧十,10,20,3441-四氮杂四十五烷-1-叔丁酯的合成。 向(s)-5-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基氨基甲酰基)-3,11,23,33-四氧-1-苯基-2,14,17,20,27,30,37,40-八氧杂-4,10,24,34-四氮杂三四十三烷-43-叔丁酯(1.00g,0.742mmol)的甲醇(50ml)溶液中,加入pd/c(10wt%,20mg),然后在1atmh2压力下反应过夜。将混合物通过硅藻土(助滤剂)过滤,并将滤液浓缩,得到标题化合物(900mg,收率100%)。esimsm/z:c59h104n7o19[m+h]+计算值:1214.73,实测值:1214.90。 实施例247.(42s,50s,51r)-42-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-50,51-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,2-二甲基-4,14,24,36,4449,52-七氧代-3,7,10,17,20,27,30,33-八氧杂-13,23,37,43,48,53-六氮杂五十七烷-57-酸和38-((8s,16r,17s)-27-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)-氨基)-4-甲基-5-氧代戊基)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15,18,23-六氧基-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂五氮杂环二十六烷-8-基)-11,21,33-三氧代-4,7,14,17,24,27,30-七氧杂-10,20,34-三氮杂三十八烷-1-叔丁酯的合成。 向(s)-39-氨基-45-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-11,21,33,40,45-五氧代-4,7,14,17,24,27,30-七氧杂-10,20,34,41-四氮四十五烷-1-叔丁酯(450mg,0.370毫摩尔)和4,4′-(((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸(230mg,0.370mmol)的dma(40ml)溶液中加入edc(300mg,1.570mmol)和dipea(100mg,0.775mmol)。将反应混合物在室温搅拌过夜,减压浓缩并在硅胶柱上纯化(用乙酸乙酯/二氯甲烷,1:10至1:5洗脱),得到(42s,50s,51r)-42-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-50,51-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,2-二甲基-4,14,24,36,44,49,52-七氧代-3,7,10,17,20,27,30,33-八氧代-13,23,37,43,48,53-六氮杂五十七烷-57-酸(0.221g,收率33%)。esimsm/z:c85h134n13o30[m+h]+计算值:1816.93,实测值1817.25;和38-((8s,16r,17s)-27-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)-氨基)-4-甲基-5-氧代戊基)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15,18,23-十氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,2021,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂五氮杂环八烷-8-基)-11,21,33-三氧代-4,7,14,17,24,27,30-七氧杂-10,20,34-三氮三十八烷-1-酸酯(0.260g,收率39%)。esimsm/z:c85h132n13o29[m+h]+计算值:1797.92,实测值:1798.20。 实施例248.(39s,47r,48s,56s)-二叔丁基39,56-双((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧羰基)叔叔丁氧基)氨基)-4-甲基-5-氧代戊基)-4-氧代丁基)甲酰基)-47,48-双(3-(2,5-二氧代-2,5-二氧代-2,5-二氢-1-基吡咯-1-基)丙氨基甲酰基)11,21,33,41,46,49,54,62,74,84-十氧代-4,7,14,17,24,27,30,65,68,71,78,81,88,91-十四氧杂-10,20,34,40,45,50,55,61,75,85-十氮杂九十四烷-1,94-二酯的合成。 向(s)-39-氨基-45-(((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧戊基)-2-羟基苯基)氨基)-11,21,33,40,45-五氧-4,7,14,17,24,27,30-七氧杂-10,20,34,41-四氮四十五烷-1-叔丁酯(450mg,0.370mmol)和4,4′-((((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二烷基))二丁酸(115mg,0.185mmol)的dma(40ml)溶液中加入edc(300mg,1.570mmol)。将反应混合物在室温搅拌过夜,减压浓缩,并在硅胶柱上纯化(用1:10至1:3乙酸乙酯/二氯甲烷洗脱),得到标题化合物(0.378g,68%产率)。esimsm/z:c144h235n20o48[m+h]+计算值:3012.65,实测值:3012.95。 实施例249.(33r,34s,42s)-叔丁基42-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-33,34-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙烷胺)-27,32,35,40,48,60,70-七氧代-2,5,8,11,14,17,20,23,51,54,57,64,67,74,77-十五氧杂-26,31,36,41,47,61,71-七氮杂八十烷-80-酯的合成。 向(42s,50s,51r)-42-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-50,51-双(3-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,2-二甲基-4,14,24,36,44,49,52-七氧代-3,7,10,17,20,27,30,33-八氧杂-13,23,37,43,48,53-六氮杂五十七-57-酸(100mg,0.055mmol)的dma(30ml)溶液中加入2,5,8,11,14,17,20,23-八氧杂二十五烷-25-胺盐酸盐(30mg,0.071mmol)和edc(25mg,0.130mmol)。将反应混合物在室温搅拌过夜,减压浓缩,并在硅胶柱上纯化(用1:8至1:3乙酸乙酯/二氯甲烷洗脱),得到标题化合物(92.2mg,收率76%)。esimsm/z:c102h169n14o37[m+h]+计算值2182.17,实测值2182.95。 实施例250.(38s,46s,47r)-38-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-46,47-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基))丙烷胺)-32,40,45,48-四氧代-2,5,8,11,14,17,20,23,26,29-十氧代-33,39,44,49-四氮杂五十三烷-53-酸和(2s,4r)-5-(((8s,16r,17s)-16,17-双(3-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丙烷胺)-2,7,10,15,18,23-十氧代-8-(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十烷-35-基)-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]-氧杂五氮杂二十七烷-27-基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯的合成。 向(2s,4r)-5-(3-((s)-36-氨基-30,37-二氧代-2,5,9,12,15,18,21,24,27-九氧杂-31,38-二氮杂四十二烷酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(400mg,0.377mmol)和4,4′-(((2r,3s)-2,3-双(3-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸(234mg,0.377mmol))的dma(50ml)中溶液加入edc(300mg,1.570mmol)和dipea(100mg,0.775mmol)。将反应混合物在室温搅拌过夜,减压浓缩,并在硅胶柱上纯化(用1:10至1:5乙酸乙酯/二氯甲烷洗脱),得到(38s,46s,47r)-38-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-46,47-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-32,40,45,48-四氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-33-39,39,44,49-四氮杂五十三烷-53-酸(0.192g,31%产率)。esimsm/z:c78h124n11o28[m+h]+计算值:1662.85,实测值:1662.60;和(2s,4r)-5-(((8s,16r,17s)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15,18,23-七氧代-8-(30-氧代-2,5,9,12,15,18,21,24,27-九氧代-31-氮杂三十五烷-35-基)-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二烷-1h-苯并[b][1,4,9,12,17,22]-氧杂五氮杂环二十七烷-27-基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.260g,39%产率)。esimsm/z:c78h122n11o27[m+h]+计算值:1644.84,实测值:1645.25。 实施例251.(2s,2’s,4r,4’r)-二叔丁基5,5′-((((((7s,15r,16s,24s)-15,16-双(3-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丙酰胺)-6,9,14,17,22,25-十氧代-7,24-双(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-5,8,13,18,23,26-六氮杂三十烷-1,30-二基)双(氮杂二烯基))双(4-羟基-3,1-亚苯基)双(4-((叔丁氧基羰基)氨基)-2-甲基戊酸酯)的合成。 向(2s,4r)-5-(3-((s)-36-氨基-30,37-二氧代-2,5,9,12,15,18,21,24,27-九氧杂-31,38-二氮杂四十二烷酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(400mg,0.377mmol)和4,4′-(((2r,3s)-2,3-双(3-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸(115mg,0.185mmol)的dma(50ml)溶液中加入edc(300mg,1.570mmol)。将反应混合物在室温搅拌过夜,减压浓缩并在硅胶柱上纯化(用1:10至1:3乙酸乙酯/二氯甲烷洗脱),得到标题化合物(0.325g,收率65%)。esimsm/z:c130h215n16o44[m+h]+计算值:2704.50,实测值2704.90。 实施例252.(2s,4r)-5-(3-(((34r,35s,43s)-34,35-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-1-羟基-28,33,36,41,44-五氧代-43-(32-氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-33-氮杂三十七烷-37-基)-3,6,9,12,15,18,21,24-八氧杂-27,32,37,42,45-五氮杂四十九烷酰胺)-4-羟苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 向(38s,46s,47r)-38-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-46,47-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-32,40,45,48-四氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-33,39,44,49-四氮杂五十三烷-53-酸(100mg,0.060mmol)的dma(30ml)溶液中加入26-氨基-3,6,9,12,15,18,21,24-八氧杂二十六烷-1-醇盐酸盐(31mg,0.069mmol)和edc(35mg,0.183mmol)。将反应混合物在室温搅拌过夜,减压浓缩并在硅胶柱上纯化(用1:8至1:3乙酸乙酯/二氯甲烷洗脱),得到标题化合物(86.5mg,收率69%)。esimsm/z:c97h163n12o37[m+h]+计算值:2088.12,实测值:2088.85。 实施例253.(39s,47r,48s)-39-((4-((5-((2r,4s)-2-(2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三叠氮基十三烷基十一烷基)噻唑-4-甲酰胺)-4-羧基戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-47,48-双(3-(2,5-二氧杂-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-11,21,33,41,46,49-七氧代-4,7,14,17,24,27,30-七氧杂-10,20,34,40,45,50-六氮杂五十四烷-1,54-二酸(b-10)的合成。 将(42s,50s,51r)-42-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-50,51-双(3-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,2-二甲基-4,14,24,36,44,49,52-七氧代-3,7,10,17,20,27,30,33-八氧杂-13,23,37,43,48,53-六氮杂五十七烷-57-酸(0.120g,0.066mmol)溶解于二氯甲烷(6ml)中,然后加入tfa(2ml)。将反应混合物在室温搅拌45分钟,用甲苯(8ml)稀释,浓缩,得到(39s,47r,48s)-39-((4-((5-((5-((2r,4s)-2-氨基-4-羧基戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-47,48-双(3-(2,5-二氧杂-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-11,21,33,41,46,49-六氧代-4,7,14,17,24,27,30-七氧杂-10,20,34,40,45,50-七氧杂五十四烷-1,54-二酸三氟乙酸盐(106mg,100%产率),无需进一步纯化即可用于下一步。将化合物溶解于dma(15ml),加入2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氧杂十四-11-基)噻唑-4-羧酸五氟苯酯(46mg,0.066mmol)和dipea(10ul,0.055mmol)。将反应混合物搅拌过夜,浓缩并通过hplc纯化,用mecn/h2o梯度洗脱(c-18柱,20mm(d)x250mm(l),在45分钟内10%mecn至70%mecn,9ml/min),得到标题产物(64.1mg,收率46%)。esimsm/z:c97h150n17o33s[m+h]+计算值:2113.02,实测值:2113.80。 实施例254.38-((8s,16r,17s)-27-((2r,4s)-2-(2-((6s,9r,11r)-6-((s)-仲丁基)的合成-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧代-2,5,8-三氮杂十三烷基十一烷基)噻唑-4-羧酰胺基)-4-羧基戊基)-16,17-双(3-(2,5-二氧-2-,5-二氢-1h-吡咯-1-基)丙酰胺)-2,7,10,15,18,23-七氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂五氮杂环二十六烷-8-基)-11,21,33-三氧代-4,7,14,17,24,27,30-七氧杂-10,20,34-三氮杂三十八烷-1-酸(b-11)的合成。 将38-((8s,16r,17s)-27-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)-氨基)-4-甲基-5-氧戊基)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺)-2,7,10,15,18,23-七氧杂-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂氧杂五氮杂环二十六烷-8-基)-11,21,33-三氧代-4,7,14,17,24,27,30-七氧杂-10,20,34-三氮杂三十八烷1-叔丁酯(0.150g,0.083mmol)溶解于二氯甲烷(6ml)中,然后加入tfa(2ml)。将反应混合物在室温搅拌45分钟,用甲苯(8ml)稀释,浓缩,得到38-((8s,16r,17s)-27-((2r,4s)-2-氨基-4-羧基戊基)-16,17-双(3-(2,5-二氧-2-,5-二氢-1h-吡咯-1-基)丙酰胺)-2,7,10,15,18,23-七氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂五氮杂环二十六烷-8-基)11,21,33-三氧代-4,7,14,17,24,27,30-七氧杂-10,20,34-三氮杂三十八烷-1-酸的tfa盐(135毫克,收率101%)无需进一步纯化即可用于下一步。然后将该化合物溶解在dma(15ml)中,加入五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧代-2,5,8-三氮杂十一烷-11-基)噻唑-4-羧酸酯(60mg,0.084mmol)和dipea(10μl,0.055mmol)。将反应混合物搅拌过夜,浓缩并通过hplc纯化,用mecn/h2o梯度洗脱(c-18柱,20mm(d)x250mm(l),45分钟内10%mecn至70%mecn,9ml/min),得到标题产物(81.6mg,收率47%)。esimsm/z:c97h149n17o32s[m+h]+计算值:2095.01,实测值:2095.65。 实施例255.化合物b-12的合成。 将(39s,47r,48s,56s)-二叔丁基39,56-双((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-47,48-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-11,21,33,41,46,49,54,62,74,84-十氧代-4,7,14,17,24,27,30,65,68,71,178,81,88,91-十四氧代-10,20,34,40,45,50,55,61,75,85-十氮杂九十四烷-1,94-二酯(175mg,0.058mmol)溶于二氯甲烷(6ml),然后加入tfa(2ml)。将反应混合物在室温搅拌45分钟,用甲苯(8ml)稀释,浓缩,得到(39s,47r,48s,56s)-39,56-双((4-((5-((2r,4s)-2-氨基-4-羧基戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-47,48-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-11,21,33,41,46,49,54,62,74,84-十氧代-4,7,14,17,24,27,30,65,68,71,78,81,88,91-十四氧代-10,20,34,40,45,50,55,61,75,85-十氮杂九十四烷-1,94-二甲酸的tfa盐(151mg,收率99%)。然后将化合物溶解于dma(15ml),加入五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十一烷基十一烷基)噻唑-4-羧酸酯(85mg,0.123mmol)和dipea(18ul,0.103mmol)。将反应混合物搅拌过夜,浓缩并通过hplc纯化,用mecn/h2o梯度洗脱(c-18柱,20mm(d)x250mm(l),在45分钟内从10%mecn至70%mecn,9ml/min),得到标题产物(81.6mg,收率47%)。esimsm/z:c168h267n28o54s2[m+h]+计算值:3604.84,实测值:3604.80。 实施例256.(36s,44s,45r)-36-((4-((5-((2r,4s))-2-(2-((6s,9r,11r))-6-((s))-仲-丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十四烷-11-基)噻唑-4-甲酰胺)-4-羧基戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-44,45-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-30,38,43,46-四氧代-2,5,9,9,12,15,18,21,24,27-九氧杂-31,37,42,47-四氮杂五十一烷-51-酸(b-13)的合成。 将(2s,4r)-5-((8s,16r,17s)-16,17-双(3-(2,5-二氧基-2,5-二氢-1h-吡咯-1-基)丙酰胺)-2,7,10,15,18,23-六氧基-8-(30-氧基-2,5,9,12,15,18,21,24,27-九氧代-31-氮杂戊三氮杂环五十三烷-35-基)-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]-氧杂五氮杂环二十六烷-27-基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯(0.175g,0.152mmol)溶解在二氯甲烷(6ml)中,然后加入tfa(2ml)。将反应混合物在室温搅拌1小时,用甲苯(8ml)稀释,浓缩,得到(36s,44r,45s)-36-((4-((5-((5-((2r,4s)-2-氨基-4-羧基戊基)-2-羟基苯基)氨基)-4-氧代丁基氨基甲酰基)-44,45-双(3-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)-30,38,43,46-四氧代-2,5,9,12,15,18,21,24,27-九氧代-31,37,42,47-四氮杂五十一烷-51-酸(230mg,收率101%),无需进一步纯化即可用于下一步。然后将化合物溶解于dma(15ml),加入五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸酯(106mg,0.152mmol)和dipea(20ul,0.115mmol)。将反应混合物搅拌过夜,浓缩并通过hplc纯化,用mecn/h2o梯度洗脱(c-18柱,20mm(d)x250mm(l),45分钟内从10%mecn至70%mecn,9ml/min),得到标题产物(149.1mg,收率49%)。esimsm/z:c94h148n15o31s[m+h]+计算值:2015.01,实测值:2015.65。 实施例257.(2s,4r)-5-(3-((34r,35s,43s)-34,35-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺)-1-羟基-28,33,36,41,44-五氧代-43-(32-氧代-2,5,8,11,14,17,20,23,26,29-十氧代-33-氮杂三十七烷-37-基)-3,6,9,12,15,18,21,24-八氧杂-27,32,37,42,45-五氮杂四十九烷酰胺基)-4-羟苯基)-4-(2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧代-2,5,8-三氮杂十三烷-11-基)噻唑-4-羧酰胺基)-2-甲基戊酸(b-14)的合成。 将(2s,4r)-5-(3-((34r,35s,43s)-34,35-双(3-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丙酰胺)-1-羟基-28,33,36,41,44-五氧代-43-(32-氧代-2,5,8,11,14,17,20,23,26,29-十氧代-33-氮杂三十七烷-37-基)-3,6,9,12,15,18,21,24-八氧代-27,32,37,42,45-五氮杂四十九烷酰胺基)-4-羟苯基)4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯(0.085g,0.040mmol)溶解在二氯甲烷(6ml)中,然后加入tfa(2ml)。在室温下将反应混合物搅拌1小时,用甲苯(8ml)稀释,浓缩得到2,5,8,11,14,17,20,23,26,29-十氧杂-33-氮杂三十七烷-37-基)-3,6,9,12,15,18,21,24-八氧杂-27,32,37,42,45-五氮杂四十九烷酰胺基)-4-羟基苯基)-2-甲基戊酸的tfa盐(78mg,100%产率),用于下一步,无需进一步纯化。然后将化合物溶解于dma(15ml)中,加入五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧基-12-氧基-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸酯(40mg,0.056mmol)和dipea(7μl,0.040mmol)。将反应混合物搅拌过夜,通过高效液相色谱(hplc)纯化,用mecn/h2o梯度(c-18柱,20mm(d)x250mm(l),45分钟从10%mecn至70%mecn,9ml/min)洗脱,得到标题产物(51.3mg,收率52%)。esimsm/z:c113h187n16o40s[m+h]+计算值:2440.27,实测值:2440.90。 实施例258.(2s,4r)-5-((8s,16r,17s)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺)-2,7,10,15,18,23-七氧代-8-(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂五氮杂环二十六烷-27-基)-4-(2-(((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酰胺基)-2-甲基戊酸酸(b-15)的合成。 将(2s,4r)-5-(((8s,16r,17s)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15,18,23-七氧代8-(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-十二氢-1h-苯并[b][1,4,9,12,17,22]-氧杂五氮环二十六烷-27-基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.145g,0.0882mmol)溶于二氯甲烷(6ml),然后加入tfa(2ml)。将反应混合物在室温搅拌1小时,用甲苯(8ml)稀释,浓缩,得到(2s,4r)-4-氨基-5-((8s,16r,17s)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15,18,23-七氧代-8-(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂五氮杂环二十六烷-27-基)-2-甲基戊酸的tfa盐(133mg,101%产率),无需进一步纯化即可用于下一步。然后将化合物溶解于dma(15ml)中,加入五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧杂-12-氧代-2,5,8-三氮杂十四烷基-11-基)噻唑-4-羧酸酯(62mg,0.0885mmol)和dipea(15ul,0.086mmol)。将反应混合物搅拌过夜,浓缩并通过hplc纯化(c-18柱,20mm(d)x250mm(l),在45分钟内10%mecn至70%mecn洗脱,9ml/min),得到标题产物(83.1mg,收率47%)。esimsm/z:c94h146n15o30s[m+h]+计算值:1997.00,实测值:1997.60。 实施例259.(s,s,r,r,2s,2’s,4r,4’r)-5,5′-(((((7s,15r,16s,24s)-15,16-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-6,9,14,17,22,25-七氧代-7,24-双(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-5,8,13,18,23,26-六氮杂三十烷-1,30-二基)双(氮杂二烷基))双(4-羟基-3,1-亚苯基))双(4-(2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧杂-12-氧代-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酰胺基)-2-甲基戊酸)(b-16)的合成。 将(2s,2’s,4r,4’r)-二叔丁基5,5′-((((((7s,15r,16s,24s)-15,16-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基丙酰胺)-6,9,14,17,22,25-六氧代-7,24-双(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-5,8,13,18,23,26-六氮杂三十烷-1,30-二基)双-(氮杂二烯基))双(4-将羟基-3,1-亚苯基))双(4-((叔丁氧基羰基)氨基)-2-甲基戊酸酯)(0.175g,0.0647mmol)溶解在二氯甲烷(6ml)中,然后加入tfa(2毫升)。将反应混合物在室温搅拌1小时,用甲苯(8ml)稀释,浓缩,得到(2s,2’s,4r,4’r)-5,5′-(((((7s,15r,16s,24s)-15,16-双(3-(2,5-二氧-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)-6,9,14,17,22,25-六氧-7,24-双(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-5,8,13,18,23,26-六氮杂三十烷-1,30-二甲酰基双(氮杂二烷基)双(4-羟基-3,1-亚苯基))双(4-氨基-2-甲基戊酸)(155mg,100%产率)无需进一步纯化即可用于下一步。然后将化合物溶于dma(15ml)中,加入五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,46,0.065mmol,7,13-三氧代-12-氧代-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸酯和dipea(10μl,0.0575mmol)。将反应混合物搅拌过夜,浓缩并通过hplc纯化,用mecn/h2o梯度(c-18柱,20mm(d)x250mm(l),45分钟内从10%mecn至70%mecn,9ml/min)洗脱,得到标题产物(105.3mg,收率48%)。esimsm/z:c162h263n24o50s2[m+h]+计算值:3408.81,实测值:3408.60。 实施例260.(2s,4r)-4-羟基吡咯烷-2-羧酸甲酯盐酸盐的合成。 在0-4℃下,向反式-4-羟基-l-脯氨酸(15.0g,114.3mmol)的无水甲醇(250ml)溶液中滴加氯化亚砜(17ml,231mmol)。将所得混合物在室温搅拌过夜,浓缩,用etoh/正己烷结晶,得到标题化合物(18.0g,收率87%)。esimsm/z168.2([m+na]+)。 实施例261.(2s,4r)-1-叔丁基2-甲基4-羟基吡咯烷-1,2-二羧酸酯的合成。 向反式-4-羟基-l-脯氨酸甲酯(18.0g,107.0mmol)的甲醇(150ml)和碳酸氢钠溶液(2.0m,350ml)中,在4小时内分三批加入boc2o(30.0g,137.6),再搅拌4小时后,将反应浓缩至350ml,并用乙酸乙酯(4×80ml)萃取。合并的有机层用盐水(100ml)洗涤,用mgso4干燥,过滤,浓缩并通过硅胶柱色谱法(1∶1正己烷/乙酸乙酯)纯化,得到标题化合物(22.54g,收率86%)。esimsm/z268.2([m+na]+). 实施例262.(s)-1-叔丁基2-甲基4-氧代吡咯烷-1,2-二羧酸酯的合成。 可通过dess-martin氧化制备标题化合物,参考francomanfre等j.org.chem.1992,57,2060-2065。此外,也可用swern的氧化制备,操作步骤如下:将草酰氯(13.0ml,74.38mmol)的二氯甲烷(350ml)溶液冷却至-78℃,加入无水dmso(26.0ml)。将溶液在-78℃下搅拌15分钟,然后将(2s,4r)-1-叔丁基-2-甲基-4-羟基吡咯烷-1,2-二羧酸酯(8.0g,32.63mmol)的二氯甲烷(100ml)溶液加入。在-78℃下搅拌2小时后,滴加三乙胺(50ml,180.3mmol),将反应溶液升温至室温。将反应混合物用nah2po4溶液稀释(1.0m,400ml),分层,用二氯甲烷(2×60ml)萃取水层,合并有机层,用硫酸镁干燥,过滤,浓缩并通过硅胶柱层析(7:3正己烷/乙酸乙酯)纯化,得到标题化合物(6.73g,85%产率)。esimsm/z:266.2([m+na]+)。 实施例263.(s)-1-叔丁基2-甲基4-亚甲基吡咯烷-1,2-二羧酸酯的合成。 在0℃下,向溴化甲基三苯基鏻(19.62g,55.11mmol)的四氢呋喃(150ml)悬浮液中加入叔丁醇钾(6.20g,55.30mmol)的无水四氢呋喃(80ml)溶液。在0℃下搅拌2小时后,将得到的黄色叶立德加入到(s)-1-叔丁基-2-甲基4-氧代吡咯烷-1,2-二羧酸酯(6.70g,27.55mmol)的四氢呋喃(40ml)溶液中。在室温下搅拌1小时,浓缩反应混合物,用乙酸乙酯(200ml)稀释,用水(150ml),盐水(150ml)洗涤,经硫酸镁干燥,浓缩并在硅胶柱层析上纯化(9:1正己烷/乙酸乙酯),得到标题化合物(5.77g,87%产率)。eimsm/z:264([m+na]+)。 实施例264.(s)-甲基4-亚甲基吡咯烷-2-羧酸酯盐酸盐的合成。 在4℃下,向(s)-1-叔丁基-2-甲基-4-亚甲基吡咯烷-1,2-二羧酸酯(5.70g,23.63mmol)的乙酸乙酯(40ml)溶液中加入盐酸(12m,10ml)。将混合物搅拌1小时,用甲苯(50ml)稀释,浓缩,之后用乙醇/正己烷重结晶,得到标题化合物(3.85g,92%产率)。eimsm/z:142.2([m+h]+)。 实施例265.(s)-2-(羟甲基)-4-亚甲基吡咯烷-1-酸叔丁酯的合成。 在0℃下,向(s)-1-叔丁基2-甲基-4-亚甲基吡咯烷-1,2-二酸酯(5.20g,21.56mmol)的无水四氢呋喃(100ml)溶液中加入lialh4(15ml,2m四氢呋喃溶液)。在0℃下搅拌4小时后,通过加入甲醇(5ml)和水(20ml)淬灭反应。将反应混合物用1mhcl中和至ph7,用乙酸乙酯(80ml)稀释,通过硅藻土过滤,分离,水层用乙酸乙酯萃取。合并有机层,用硫酸钠干燥,浓缩并在硅胶柱色谱(1:5乙酸乙酯/二氯甲烷)上纯化,得到标题化合物(3.77g,82%产率)。eimsm/z:236.40([m+na]+)。 实施例266.(s)-(4-亚甲基吡咯烷-2-基)甲醇盐酸盐的合成。 在4℃下,向(s)-2-(羟甲基)-4-亚甲基吡咯烷-1-羧酸叔丁酯(3.70g,17.36mmol)的乙酸乙酯(30ml)溶液中加入hcl(12m,10ml)。将混合物搅拌1小时,用甲苯(50ml)稀释,浓缩,并用乙醇/正己烷结晶,得到标题盐酸盐(2.43g,94%产率)。eimsm/z:115.1([m+h]+)。 实施例267.4-(苄氧基)-3-甲氧基苯甲酸的合成。 向4-羟基-3-甲氧基苯甲酸(50.0g,297.5mmol)在乙醇(350ml)和氢氧化钠(2.0m,350ml)混合溶液中加入苄溴(140.0g,823.5mmol)。将混合物在65℃下搅拌8小时,浓缩,与水(2×400ml)共浓缩至约400ml,用6n盐酸酸化至ph3.0。过滤收集固体,用乙醇重结晶,在45℃下真空干燥,得到标题化合物(63.6g,83%产率)。esimsm/z:281.2([m+na]+)。 实施例268.4-(苄氧基)-5-甲氧基-2-硝基苯甲酸的合成。 向4-(苄氧基)-3-甲氧基苯甲酸(63.5g,246.0mmol)的二氯甲烷(400ml)和乙酸(100ml)溶液中加入发烟硝酸(25.0ml,528.5mmol)。将混合物搅拌6小时,浓缩,用乙醇结晶,在40℃下真空干燥,得到标题化合物(63.3g,85%产率)。esimsm/z:326.1([m+na]+)。 实施例269.(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(羟甲基)-4-亚甲基吡咯烷-1–1-基)甲酮的合成。 将催化量的dmf(30μl)加入到4-(苄氧基)-5-甲氧基-2-硝基苯甲酸(2.70g,8.91mmol)和草酰氯(2.0ml,22.50mmol)的无水二氯甲烷溶液中,将所得混合物在室温下搅拌2小时。用旋转蒸发仪除去过量的二氯甲烷和草酰氯。在n2条件下,0℃将乙酰氯重新悬浮在新鲜的二氯甲烷(70ml)中,并缓慢加入到预混合的((s)-(4-亚甲基吡咯烷-2-基)甲醇盐酸盐(1.32g,8.91mmol)和et3n(6ml)的二氯甲烷溶液中。将反应混合物升温至室温,继续搅拌8小时。除去二氯甲烷和et3n后,将残余物在水和乙酸乙酯(70/70ml)之间分配。用乙酸乙酯(2×60ml)进一步萃取水层。将合并的有机层用盐水(40ml)洗涤,干燥(硫酸镁)并浓缩。用快速硅胶柱层析(2:8正己烷/乙酸乙酯)纯化残余物,得到标题化合物(2.80g,76%产率)。eimsm/z:449.1([m+na]+)。 实施例270.(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(((叔丁基二甲基甲硅烷基)氧基)甲基)-4-亚甲基吡咯烷-1-基)甲酮的合成。 向(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(羟甲基)-4-亚甲基吡咯烷-1-基)甲酮(2.78g,8.52mmol)在二氯甲烷(10ml)和吡啶(10ml)的混合物中,加入叔丁基氯二甲基硅烷(2.50g,16.66mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:6)洗脱,得到标题化合物(3.62g,83%产率,纯度95%)。msesim/z:c27h37n2o6si[m+h]+计算值513.23,实测值513.65。 实施例271.(s)-(4-羟基-5-甲氧基-2-硝基苯基)(2-(羟甲基)-4-亚甲基吡咯烷-1-基)甲酮的合成。 向(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(羟甲基)-4-亚甲基吡咯烷-1-基)甲酮(2.80g,7.03mmol)在二氯甲烷(30ml)和甲磺酸(8ml)的混合物中,加入phsch3(2.00g,14.06mmol)。将混合物搅拌0.5小时,用二氯甲烷(40ml)稀释,小心地用0.1mna2co3溶液中和。分离混合物,用二氯甲烷(2×10ml)萃取水溶液。合并有机层,用无水硫酸钠干燥,浓缩并在硅胶柱上纯化,用甲醇/二氯甲烷(1:15至1:6)洗脱,得到标题化合物(1.84g,85%产率,约95%纯度)。msesim/z:c14h17n2o6[m+h]+计算值309.10,实测值309.30。 实施例272.(s)-((戊烷-1,5-二基双(氧基))双(5-甲氧基-2-硝基-4,1-亚苯基))双(((s)-2-(羟甲基))-4-亚甲基吡咯烷-1-基)甲酮)的合成。 向(s)-(4-羟基-5-甲氧基-2-硝基苯基)(2-(羟甲基)-4-亚甲基吡咯烷-1-基)甲酮(0.801g,2.60mmol)的丁酮(10ml)溶液中,加入碳酸铯(2.50g,7.67mmol),然后加入1,5-二碘戊烷(415mmol,1.28mmol)。将混合物搅拌26小时,浓缩并在硅胶柱上纯化,用甲醇/二氯甲烷(1:15至1:5)洗脱,得到标题化合物(0.675g,77%产率,约95%纯度)。msesim/z:c33h41n4o12[m+h]+计算值685.26,实测值685.60。 实施例273.(s)-((戊烷-1,5-二基双(氧基))双(2-氨基-5-甲氧基-4,1-亚苯基))双(((s)-2-(羟甲基))-4-亚甲基吡咯烷基-1-基)甲酮)的合成。 在(s)-((戊烷-1,5-二基二(氧基))双(5-甲氧基-2-硝基-4,1-亚苯基))二(((s)-2-(羟甲基)-4-亚甲基吡咯-1-基)甲酮)(0.670g,0.98mmol)的甲醇(10ml)溶液中,加入na2s2o4(1.01g,5.80mmol)的水(8ml)溶液。将混合物在室温下搅拌超过30小时。浓缩反应混合物,并在高真空下与dma(2×10ml)和乙醇(2×10ml)共浓缩至干,得到含有无机盐的标题化合物(总重1.63g),其无需进一步纯化,直接用于下一步反应。eimsm/z:647.32([m+na]+)。 实施例274.c-01(具有双连接子的pbd二聚体类似物)的合成。 在0℃下,向含有吡啶(0.100ml,1.24mmol)的(3s,6s,39s,42s)-6,39-双(4-((叔丁氧基羰基)氨基)丁基)-22,23-双(2,5-二氧代-2,5-)二氢-1h-吡咯-1-基)-3,42-二((4-(羟甲基)苯基)氨基甲酰基)-5,8,21,24,37,40-六氧代-11,14,17,28,31,34-六氧杂-4,7,20,25,38,41-六氮杂四十四烷-1,44-二酸二叔丁酯的四氢呋喃(8ml)溶液中,滴加三光气(0.290mg,0.977mmol)的四氢呋喃(3.0ml)溶液。将反应混合物在0℃下搅拌15分钟,然后直接用于下一步骤。 在0℃下,向含有无机盐的(s)-((戊烷-1,5-二基二(氧基))双(2-氨基-5-甲氧基-4,1-亚苯基))二(((s)-2-(羟甲基)-4-亚甲基吡咯-1-基)甲酮(0.842mg,约0.49mmol)的乙醇(10ml)悬浮液中,加入前述四氢呋喃溶液。将混合物在0℃下搅拌4小时,然后升温至室温1小时,浓缩,并通过反相hplc(c18柱,10mm×250mm)纯化,用mecn/h2o梯度洗脱(10%mecn至100%mecn,40分钟,8ml/min),得到标题化合物(561.1mg,三步产率48%)。 实施例275.c-02(具有双连接子的pbd二聚体类似物)的合成。 在0℃下,将dess-martin试剂(138.0mg,0.329mmol)加入到化合物c-1(132.0mg,0.055mmol)的二氯甲烷(5.0ml)溶液中。将反应混合物升温至室温并搅拌2小时。然后加入饱和碳酸氢钠/na2so3溶液(5.0ml/5.0ml),用二氯甲烷(3×25ml)萃取混合物。将合并的有机层用碳酸氢钠/na2so3(5.0ml/5.0ml),盐水(10ml)洗涤,用无水硫酸钠干燥,过滤,浓缩并用反相hplc(c18柱,10mm×250mm)纯化,用mecn/h2o梯度洗脱(10%mecn至100%mecn,40分钟,8ml/min),得到标题化合物(103.1mg,78%产率),为泡沫状物。esimsm/z:c117h158n16o38[m+h]+计算值2396.09,实测值2396.65。 实施例276.c-03(具有双连接子的pbd二聚体类似物)的合成。 将c-2化合物(55.0mg,0.023mmol)溶于二氯甲烷(3ml)中,然后加入tfa(3ml)。将反应混合物在室温下搅拌2小时,然后浓缩,并与二氯甲烷/甲苯共浓缩至干,得到粗产物c-3(48.0mg,100%产率,hplc纯度92%),通过反相hplc(c18柱,10mm×250mm)纯化,用mecn/h2o梯度洗脱(10%mecn至100%mecn,40分钟,8ml/min),得到c-3(42.1mg,88%产率,96%纯度),为泡沫状固体。esimsm/z:c99h126n16o34[m+h]+计算值2083.86,实测值2084.35。 实施例277.c-04(具有双连接子的pbd二聚体类似物)的合成。 将c-03化合物(35.0mg,0.017mmol)溶于四氢呋喃(3ml)和nah2po4(0.1m,ph7.5,3ml)的混合溶液中,然后在2小时内分4批加入n-琥珀酰亚胺2,5,8,11,14,17,20,23-八氧杂二十六烷-26-酸酯(43.0mg,0.084mmol)。然后将反应混合物在室温下继续搅拌4小时,并与dmf(10ml)共蒸发至干,得到粗产物c-4,将其通过反相hplc进一步纯化(250(l)mm×20(d)mm,c18色谱柱,40分钟内20-60%乙腈/水,流速8ml/min),得到纯产物c-04(39.4mg,收率81%,纯度96%),为泡沫状物。esimsm/z:c135h195n16o52[m+h]+计算值:2872.30,实测值:2871.65。 实施例278.c-05(具有连接子的pbd二聚体类似物)的合成。 向c-04化合物(35.0mg,0.012mmol)和2,5,8,11,14,17,20,23-八氧二十五烷25-胺(15.1mg,0.0394mmol)的无水dma(2ml)溶液中加入edc(30.0mg,0.156mmol)。将反应混合物在室温搅拌14小时,浓缩,通过反相hplc纯化(250(l)mmx20(d)mm,c18柱,40分钟内20-60%乙腈/水,流速8ml/min),得到纯产物c-05(31.2mg,收率77%,hplc纯度97%),为泡沫状物。esimsm/z:c161h249n18o62[m+h]+计算值:3426.68,实测值:3427.21。 实施例279.(s)-1-(4-(苄氧基)-5-甲氧基-2-硝基苯甲酰基)-4-亚甲基吡咯烷-2-羧酸甲酯的合成。 在0℃,n2下,将催化量的dmf(30μl)加入到4-(苄氧基)-5-甲氧基-2-硝基苯甲酸(2.70g,8.91mmol)和草酰氯(2.0ml,22.50mmol)的无水二氯甲烷(70ml)溶液中,并将所得混合物在室温搅拌2小时。用旋转蒸发仪除去过量的溶剂和草酰氯。将乙酰氯重新悬浮在新鲜的二氯甲烷(70ml)中,并缓慢加入到预先混合的(s)-4-亚甲基吡咯烷-2-羧酸甲酯盐酸盐(1.58g,8.91mmol)和et3n(6ml)的二氯甲烷中。使反应混合物升温至室温,继续搅拌8小时。除去二氯甲烷和et3n后,将残留物在分配在水和乙酸乙酯(70/70ml)。将水层进一步用乙酸乙酯(2×60ml)萃取。合并的有机层用盐水(40ml)洗涤,干燥(mgso4)并浓缩。用快速柱色谱(2:8正己烷/乙酸乙酯)纯化残余物,得到标题化合物(2.88g,收率76%)。eimsm/z:449.1([m+na]+)。 实施例280.(s)-1-(4-(苄氧基)-5-甲氧基-2-硝基苯甲酰基)-4-亚甲基吡咯烷-2-甲醛的合成。 在-78℃和n2中,剧烈搅拌下向(s)-1-(4-(苄氧基)-5-甲氧基-2-硝基苯甲酰基)-4-亚甲基吡咯烷-2-羧酸甲酯(2.80g,6.57mmol)的无水二氯甲烷(60ml)溶液中滴加dibal-h(1n二氯甲烷,10ml)。将混合物再搅拌90分钟后,加入2ml甲醇,之后加入5%hcl(10ml)分解过量的试剂。将所得混合物升温至0℃,分离各层,将水层进一步用二氯甲烷(3×50ml)萃取。合并的有机层用盐水洗涤,干燥(mgso4)并浓缩。用快速柱色谱(95:5chcl3/甲醇)纯化残余物,得到标题化合物(2.19g,收率84%)。eimsm/z:419.1([m+na]+)。 实施例281.(s)-8-(苄氧基)-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]-吡咯并[1,2-a]氮杂-5(11ah)-酮的合成。 将(s)-1-(4-(苄氧基)-5-甲氧基-2-硝基苯甲酰基)-4-亚甲基吡咯烷-2-甲醛(2.18g,5.50mmol)和na2s2o4(8.0g,45.97mmol)的四氢呋喃(60ml)和水(40ml)溶液在室温搅拌20小时。在高真空下除去溶剂,将残余物重悬于甲醇(60ml)中,并逐滴加入hcl(6m)直至达到ph2。将得到的混合物在室温搅拌1小时。除去大部分甲醇,然后用乙酸乙酯(100ml)稀释,用饱和碳酸氢钠,盐水洗涤乙酸乙酯溶液,干燥(mgso4),浓缩。用快速柱色谱(97:3氯仿/甲醇)纯化残余物,得到标题化合物(1.52g,80%)。eimsm/z372.1([m+na]+)。 实施例282.(s)-8-羟基-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]-吡咯并[1,2-a]氮杂-5(11ah)-酮的合成。 在0℃下,向(s)-8-(苄氧基)-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]-吡咯并[1,2-a]氮杂-5(11ah)-酮(1.50g,4.32mmol)的二氯甲烷(70ml)溶液中加入25mlch3so3h。将混合物在0℃下搅拌10分钟,然后在室温下搅拌2小时,用二氯甲烷稀释,用冷的1.0n碳酸氢钠调节ph至4,并过滤。用二氯甲烷(3×60ml)萃取水层。合并有机层,经无水硫酸钠干燥,过滤,蒸发,并用硅胶柱色谱法纯化(ch3oh/二氯甲烷1∶15),得到811mg(收率73%)的标题产物。eimsm/z281.1([m+na]+)。 实施例283.(11as,11a’s)-8,8′-(戊烷-1,5-二基双(氧))二(7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(11ah)-酮)的合成。 向搅拌的碳酸铯(0.761g,2.33mmol)的丁酮(8ml)悬浮液中加入(s)-8-羟基-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯[1,2-a]氮杂-5(11ah)-酮(401mg,1.55mmol)和1,5-二碘戊烷(240mg,0.740mmol)。将混合物在室温下搅拌过夜,浓缩,并在硅胶柱上纯化(乙酸乙酯/二氯甲烷1:10),得到337mg(78%产率)标题产物。eimsm/z:607.2([m+na]+)。 实施例284.(s)-7-甲氧基-8-((5-((s)-7-甲氧基-2-亚甲基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧基)-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,22-a][1,4]二氮杂-5(11ah)-酮的合成。 在0℃下,向(11as,11a’s)-8,8’-(戊烷-1,5-二基双(氧))双(7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯烷[1,2-a][1,4]二氮杂-5(11ah)-酮)(150mg,0.256mmol)的无水二氯甲烷(1ml)和无水乙醇(1.5ml)的溶液中,加入硼氢化钠的甲氧基乙醚溶液(0.5m,85μl,0.042mmol)。5分钟后撤去冰浴,将混合物在室温下搅拌3小时,然后冷却至0℃,用饱和氯化铵淬灭,用二氯甲烷稀释,并分层。将有机层用盐水洗涤,用无水硫酸钠干燥,通过硅藻土过滤并浓缩。通过反相hplc(c18,乙腈/水)纯化残余物。将合适的组分用二氯甲烷萃取并浓缩,得到标题化合物(64.7mg,43%),msm/z:609.2([m+na]+),625.3([m+k]+),627.2([m+na+h2o]+);和完全还原的产物(16.5mg,11%),msm/z:611.2([m+na]+),627.2([m+k]+),629.2([m+na+h2o]+);回收未反应的原料(10.2mg,7%),msm/z:607.2([m+na]+),625.2([m+na+h2o]+)。 实施例285.(s)-8-((5-(((s)-10-(3-(2-(2-叠氮基乙氧基)乙氧基)丙酰基)-7-甲氧基-2-亚甲基-5-氧代-23,5,10,11,11a六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧)-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(11ah)-酮的合成。 向(s)-7-甲氧基-8-((5-(((s)-7-甲氧基-2-亚甲基-5-氧代-2,3,5,10,11,11a-六氢)-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-8-基)氧基)戊基)氧基)-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(11ah)-酮(60.0mg,0.102mmol)和2,5-二氧代吡咯烷-1-基3-(2-(2-叠氮基乙氧基)乙氧基)丙酸酯(40.5mg,0.134mmol)的二氯甲烷(5ml)的混合物中加入edc(100.5mg,0.520mmol)。将混合物在室温下搅拌过夜,浓缩并在硅胶柱上纯化(乙酸乙酯/二氯甲烷,1:6),得到63.1mg(81%产率)标题产物。esimsm/z:c40h50n7o9[m+h]+计算值772.36,实测值772.30。 实施例286.(s)-8-((5-((s)-10-(3-(2-(2-氨基乙氧基)乙氧基)丙酰基)-7-甲氧基-2-亚甲基-5-氧代-23,5,10,11,11a六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧)-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(11ah)-酮的合成。 向(s)-8-((5-(((s)-10-(3-(2-(2-叠氮基乙氧基)乙氧基)丙酰基)-7-甲氧基-2-亚甲基-5-氧代-2,3,5,10,11,11a六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧基)-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(11ah)-酮(60mg,0.078mmol),四氢呋喃(5ml)和nah2po4缓冲溶液(ph7.5,1.0m,0.7ml)的混合物中加入pph3(70mg,0.267mmol)。将混合物在室温下搅拌过夜,浓缩后在制备hplc上纯化,用水/乙腈(35分钟,从90%水至35%水)洗脱,在高真空下干燥后得到45.1mg(79%产率)标题产物。esimsm/z:c40h52n5o9[m+h]+计算值746.37,实测值746.50。 实施例287.(s)-n-(2-((s)-8-((5-(((11s,11as)-10-((s)-15-叠氮基-5-异丙基-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十七烷-1-酰基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)-氧基)-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-10(5h)-基)-2-氧代乙基)-2-(3-(2-(2-叠氮基乙氧基)乙氧基)丙酰胺基)-3-甲基丁酰胺的合成。 向(s)-7-甲氧基-8-((5-(((s)-7-甲氧基-2-亚甲基-5-氧代2,3,5,10,11,11a六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧基)-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,2a][1,4]二氮杂-5(11ah)-酮(60.0mg,0.102mmol)和(s)-15-叠氮基-5-异丙基-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十七-1-酸(90.2mg,0.25mmol)在dma(8ml)的混合物中,加入brop(240.2mg,0.618mmol)。在室温下搅拌该混合物过夜,浓缩并在硅胶柱色谱(甲醇/二氯甲烷,1:10至1:5)上纯化,得到97.1mg(74%产率)标题产物。esimsm/z:c61h87n14o17[m+h]+,计算值1287.63,实测值1287.95。 实施例288.(s)-n-(2-((s)-8-((5-(((11s,11as)-10-((s)-15-氨基-5-异丙基-4,7-二氧代10,13-二氧杂-3,6-二氮杂十七烷-1-酰基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代2,3,5,10,11,11a六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧基)-7-甲氧基-2-亚甲基-5-氧代2,3,11,11a四氢1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-10(5h)-基)-2-氧代乙基)-2-(3-(2-(2-氨基乙氧基)乙氧基)-丙酰胺基)-3-甲基丁酰胺(c-06)合成。 向(s)-n-(2-((s)-8-((5-(((11s,11as)-10-((s)-15-叠氮基-5-异丙基-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十七烷-1-酰基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代2,3,5,10,11,11a六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)-氧基)-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a四氢-1h-苯并[e]吡咯并[1,2,2-a][1,4]二氮杂-10(5h)-基)-2-氧代乙基)-2-(3-(2-(2-叠氮基乙氧基)乙氧基)丙酰胺基)-3-甲基丁酰胺(85mg,0.066mmol)在四氢呋喃(5ml)和nah2po4缓冲溶液(ph7.5,1.0m,0.7ml)的混合物中加入pph3(100mg,0.381mmol)。将混合物在室温下搅拌过夜,经lc-ms确认形成(s)-n-(2-((s)-8-((5-(((11s,11as)-10-((s)-15-氨基-5-异丙基)-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十七烷-1-酰基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧)-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-10(5h)-基)-2-氧代乙基)-2-(3-(2-(2-氨基乙氧基)乙氧基)丙酰胺基)-3-甲基丁酰胺(esimsm/z:c61h90n10o17[m+na]+,计算值1257.66,实测值1257.90)后,加入双(2,5-二氧代吡咯烷-1-基)2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸酯(33mg,0.066mmol)。将混合物继续搅拌4小时,浓缩后在制备型hplc上纯化,用水/ch3cn(从90%水至30%水,35分钟)洗脱,在高真空下干燥后,得到40.1mg(40%产率)标题产物。esimsm/z:c73h95n12o23[m+h]+,计算值1507.66,实测值1507.90。 实施例289.4,4′-(戊烷-1,5-二基双(氧基))双(3-甲氧基苯甲酸)的合成。 在4小时内将二碘丙烷(19.0g,58.6mmol)的四氢呋喃(75ml)溶液滴加到65℃,剧烈搅拌的香草酸(20.0g,119mmol)在四氢呋喃(150ml)和naoh(340ml)水溶液中(避光,铝箔包裹烧瓶)。在暗处加热回流48小时后,将溶液冷却,真空蒸发除去四氢呋喃。残余物用乙酸乙酯萃取,分离水层,并用浓盐酸酸化至ph2。过滤收集得到的沉淀物,洗涤,干燥,并用冰醋酸重结晶,得到相应的双羧酸(14.0g,34.7mmol),为白色固体,收率60%。 实施例290.4,4′-(戊烷-1,5-二基双(氧基))双(5-甲氧基-2-硝基苯甲酸)的合成。 向悬浮在hoac(80ml,1800mmol)中的4,4′-(戊烷-1,5-二烷基双(氧基))双(3-甲氧基苯甲酸)(18.0g,66.8mmol),在室温下滴加hno3(80ml,1778mmol)。搅拌2小时后,将混合物倒入100g冰中,用乙酸乙酯萃取(2×200ml)。分离有机层,并用水(2×100ml)洗涤,然后加入4nnaoh(400ml)。用乙酸乙酯(2×100ml)萃取后,分离碱性水层,并用浓盐酸酸化至ph2。用乙酸乙酯(2×250ml)萃取混合物。合并的有机萃取物用盐水洗涤,干燥,过滤并浓缩。通过快速柱色谱纯化残余物(二氯甲烷/甲醇4:1),得到4,4′-(戊烷-1,5-二基双(氧基))双(5-甲氧基-2-硝基苯甲酸)浅黄色固体(6.1g,12.3mmol),产率为18%。rf=0.3(二氯甲烷/甲醇3:1)。 实施例291.(s)-((戊烷-1,5-二基双(氧基))双(5-甲氧基-2-硝基-4,1-亚苯基))双(((s)-2-(羟甲基))吡咯烷-1-基)甲酮)的合成。 在室温下,向4,4′-(戊烷-1,5-二烷基双(氧基))双(5-甲氧基-2-硝基苯甲酸)(5.0g,10.0mmol)和l-(+)-脯氨醇(2.25g)的dmf(100ml)溶液中加入tea(4.0g)。搅拌10分钟后,加入hatu(10.77g,28.3mmol)。将混合物在室温搅拌过夜。反应完成后,将混合物用水(100ml)稀释,并用乙酸乙酯(2×100ml)和二氯甲烷(2×50ml)萃取,将合并的有机萃取物用盐水洗涤,干燥,过滤并浓缩。残余物通过柱色谱法纯化(二氯甲烷/甲醇15:1),得到(s)-((戊烷-1,5-二基双(氧基))双(5-甲氧基-2-硝基-4,1-亚苯基)双(((s)-2-(羟甲基)吡咯烷-1-基)甲酮)(6.0g,9.1mmol),为白色泡沫状,收率91%。 实施例292.(s)-((戊烷-1,5-二基双(氧基))双(2-氨基-5-甲氧基-4,1-亚苯基))双(((s)-2-(羟甲基))的合成)吡咯烷-1-基)甲酮)的合成。 将(s)-((戊烷-1,5-二基双(氧基))双(5-甲氧基-2-硝基-4,1-亚苯基))-双((((s)-2-(羟甲基)吡咯烷-1-基)甲酮(6.0g,9.1mmol)的甲醇(100ml)溶液和10%pd/c(2.4g)混合,将混合物在氢气氛下于室温搅拌过夜。搅拌14小时后,过滤除去pd/c,并用甲醇洗涤,浓缩,并将残余物通过柱色谱法纯化(10:1二氯甲烷/甲醇),得到(s)-((戊烷-1),5-二基双(氧基))双(2-氨基-5-甲氧基-4,1-亚苯基))双((((s)-2-(羟甲基)吡咯烷-1-基)甲酮)(3.54g,5.9mmol)为白色泡沫状,收率为65%。 实施例293.双(4-((s)-2-((s)-2-((((烯丙氧基)羰基)氨基)-3-甲基丁亚酰胺基)丙酰胺基)苄基)((s)-(戊烷-1,5-二基双(氧基)双(2-((s)-2-(羟甲基)吡咯烷-1-羰基)-4-甲氧基-5,1-亚苯基))二氨基甲酸酯的合成。 在5℃下,向((s)-1-(((s)-1-((4-(羟甲基)苯基)氨基)-1-氧丙烷-2-基)氨基)-3-甲基-1-氧代丁烷-2-基)氨基甲酸烯丙基酯(8.0g,21.3mmol)的无水四氢呋喃(300ml)溶液中加入dipea(5.5g,40.3mmol)和三光气的无水四氢呋喃(50ml)溶液(3.2g,10.8mmol)。搅拌15分钟后,将溶液重新冷却至5℃,加入(s)-((戊烷-1,5-二烷基双(氧基))双(2-氨基-5-甲氧基-4,1-亚苯基)双(((s)-2-(羟甲基)-吡咯烷-1-基)甲酮)(3.2g,5.3mmol)和dipea(2.75g,21.6mmol)的无水四氢呋喃(150ml)溶液。使所得溶液升温至室温,并搅拌过夜。通过真空蒸发除去四氢呋喃。残余物通过柱色谱法纯化(20:1二氯甲烷/甲醇),得到双(4-((s)-2-((s)-2-(((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基。)-苄基)((s)-(戊烷-1,5-二基双(氧基))双(2-((s)-2-(羟甲基)吡咯烷-1-羰基)-4-甲氧基-5,1-亚苯基))二氨基甲酸酯(7.0g,4.97mmol),为黄色泡沫,收率94%。 实施例294.(11s,11as,11’s,11a’s)-双(4-((s)-2-((s)-2-((((烯丙氧基)羰基)-氨基)-3-甲基丁酰胺基)丙酰胺基)的合成苄基)8,8′-(戊烷-1,5-二基双(氧基))双(11-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 在室温下,氮气中,向双(4-((s)-2-((s)-2-((((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基)苄基)((s)-(戊烷-1),5-二基双(氧基)双(2-((s)-2-(羟基甲基)吡咯烷-1-羰基)-4-甲氧基-5,1-亚苯基))二氨基甲酸酯(300mg,0.21mmol)的无水二氯甲烷(15ml)溶液中加入dmp(280mg,0.66mmol)。反应完成后,向反应溶液中加入na2so3水溶液,然后加入碳酸氢钠水溶液,将混合物再搅拌15分钟,并用二氯甲烷(3×20ml)萃取。合并的有机萃取物用盐水洗涤,干燥,过滤并浓缩。残余物通过柱色谱法纯化(20:1二氯甲烷/甲醇),得到(11s,11as,11’s,11a’s)-双(4-((s)-2-((s)-2-(((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基)8,8′-(戊烷-1,5-二基双(氧基))双(11-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(270mg,0.19mmol),为白色泡沫状,产率92%。 实施例295.(11s,11as,11’s,11a’s)-双(4-((s)-2-((s)-2-((((烯丙氧基)羰基)-氨基)-3-甲基丁酰胺基)丙酰胺基)苄基)8,8′-(戊烷-1,5-二基双(氧基))双(11-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 向(11s,11as,11’s,11a’s)-双(4-((s)-2-((s)-2-((((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基)苄基)8,8′-(戊烷-1,5-二基双(氧基))双(11-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂10(5h)-羧酸酯(774mg,0.55mmol)与吡咯烷(196mg,2.76mmol)的无水二氯甲烷(8ml)溶液中,加入(pd(pph3)4(76mg,0.066mmol)。反应在氩气中室温下搅拌2小时,然后将反应物用二氯甲烷稀释并依次用饱和nh4cl水溶液和盐水洗涤。有机相经无水硫酸钠干燥,过滤并浓缩。残余物通过柱色谱法纯化(6:1二氯甲烷/甲醇),得到(11s,11as,11’s,11a’s)-双(4-((s)-2-((s)-2-(((烯丙氧基)羰基)氨基)-3-甲基-丁酰胺基)丙酰胺基)8,8′-(戊烷-1,5-二基双(氧基))双(11-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]-吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(420mg,0.34mmol),为白色固体,收率62%。 实施例296.(s)-2-((((烯丙氧基)羰基)氨基)-3-甲基丁酸的合成。 将氯甲酸烯丙酯(24.8g,205mmol)滴加到搅拌的l-缬氨酸(20g,171mmol)和k2co3(35.4g,257mmol)在水(250ml)和四氢呋喃(250ml)溶液中。将反应混合物在室温搅拌过夜,然后将溶剂减压浓缩,并将剩余溶液用乙醚(100ml)洗。用浓盐酸将水部分酸化至ph2,并用二氯甲烷(3×200ml)萃取。合并的有机相用盐水洗涤,经无水硫酸钠干燥,过滤并浓缩,得到产物(35g,174mmol),为白色固体,收率100%。 实施例297.(s)-2,5-二氧杂吡咯烷-1-基2-(((烯丙氧基)羰基)氨基)-3-甲基丁酸酯的合成。 在室温下,向搅拌的(s)-2-(((烯丙氧基)羰基)氨基)-3-甲基丁酸(35g,174mmol)的无水二氯甲烷(500ml)溶液中,加入edc(66.9g,348mmol)和n-羟基琥珀酰亚胺(30g,261mmol)。搅拌14小时后,将反应物用二氯甲烷稀释并用水和盐水洗涤。有机相经无水硫酸钠干燥,过滤并浓缩,得到产物(54.5g),为粘性无色油,其无需进一步纯化即可用于下一步骤。rf=0.5(2:1石油醚/乙酸乙酯) 实施例298.(s)-2-((s)-2-((((烯丙氧基)羰基)氨基)-3-甲基丁亚氨基)-丙酸的合成。 在室温下,向h-ala-oh(15.7g,176mmol)和碳酸氢钠(15.5g,185mmol)的四氢呋喃(200ml)和水(200ml)溶液中加入(s)-2,5-二氧吡咯烷-1-基2-(((烯丙氧基)-羰基)氨基)-3-甲基丁酯(50g,168mmol)的四氢呋喃(100ml)溶液。搅拌72小时后,减压蒸发四氢呋喃。用柠檬酸将残余物酸化至ph3,并用乙酸乙酯(3x350ml)萃取,将合并的萃取物用盐水洗涤,干燥,过滤并浓缩,得到白色固体。用乙醚(过量)打浆,得到纯的产物,为白色粉末(25.2g,93mmol,55%)。 实施例299.((s)-1-(((s)-1-((4-(羟甲基)苯基)氨基)-1-氧代丙烷-2-基)氨基)-3-甲基-1-氧代丁烷-2-基)氨基甲酸烯丙酯的合成。 室温下,向(s)-2-((s)-2-(((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)-丙酸(25.2g,92.6mmol)和对氨基苄醇(12.0g,97.6mmol)的四氢呋喃(300ml)溶液中加入eedq(24.0g,97.2mmol)。搅拌18小时后,减压蒸发除去溶剂,得到浅棕色固体。将固体用乙醚打浆并过滤,用过量乙醚洗涤,得到白色固体(40g,106mmol,100%)。 实施例300.4-(((苄氧基)羰基)氨基)丁酸的合成。 在5℃下,将na2co3(41.1g,387mmol)加入到4-氨基丁酸(20g,193mmol)的水溶液(300ml)中。搅拌10分钟后,滴加cbzcl(33.2ml,232mmol)的四氢呋喃(100ml)溶液。使反应升温至室温,并搅拌过夜。反应完成后,将混合物用水(100ml)稀释,并用乙酸乙酯(2×100ml)洗。用浓盐酸将水层酸化至ph2。并用乙酸乙酯(3×100ml)萃取。合并的有机物用盐水洗涤,经无水硫酸钠干燥,过滤并浓缩,得到白色固体。用石油醚(过量)打浆,得到纯的产物,为白色粉末(31.6g,70%)。 实施例301.4-((((苄氧基)羰基)氨基)丁酸叔丁酯的合成。 在5℃下,向4-((((苄氧基)羰基)氨基)丁酸(5.9g,24.9mmol)和叔丁醇(14.7g,199mmol)的无水二氯甲烷(250ml)溶液中加入dmap(0.61)和dic(4.7g,37.3mmol)。搅拌16小时后,将反应物过滤并用二氯甲烷(2×200ml)萃取,合并的有机萃取物用1nhcl,盐洗涤,用无水硫酸钠干燥,过滤并浓缩。残余物通过柱色谱法纯化(100%二氯甲烷),得到4-((((苄氧基)羰基)氨基)氨基叔丁酸叔丁酯(4.26g,14.5mmol,58%),为粘性无色油状物。 实施例302.4-氨基丁酸叔丁酯的合成。 将4-((((苄氧基)羰基)氨基)丁酸叔丁酯(1.69g,5.77mmol)的甲醇(40ml)溶液与10%pd/c(400mg)混合,在氢气下将混合物于室温下搅拌过夜,搅拌14小时后,过滤除去pd/c,并用甲醇洗涤。浓缩滤液,得到产物,其无需进一步纯化即可用于下一步(897mg,5.64mmol),无色液体,收率98%。 实施例303.(2r,3s)-2,3-双(苄基氨基)琥珀酸的合成。 向内消旋-2,3-二溴丁二酸(50g,181mmol)的乙醇(400ml)溶液中滴加苄胺(150ml),加入完成后,加热至90℃,搅拌过夜。将该混合物冷却至室温并用水稀释,加入6nhcl直至ph为4,得到白色沉淀物,将沉淀物过滤,用水洗涤并干燥,得到(2r,3s)-2,3-双(苄基氨基)琥珀酸(50g,152mmol,84%)。 实施例304.(2r,3s)-2,3-二氨基琥珀酸的合成。 将(2r,3s)-2,3-双(苄氨基)琥珀酸(18g,55mmol)的acoh(100ml)和hcl(100ml)溶液与10%pd/c(3g)混合,在氢气中于50℃搅拌过夜,搅拌48h后,过滤除去pd/c,用水洗涤。加入acoh直至ph为5,得到白色沉淀,将沉淀过滤,用水洗并干燥,得到(2r,3s)-2,3-二氨基琥珀酸(8.7g,58.8g,100%)。 实施例305.2,3-双(((苄氧基)羰基)氨基)琥珀酸的合成。 在0℃下,向(2r,3s)-2,3-二氨基琥珀酸(31.74g,214mmol)的四氢呋喃(220ml)和4nnaoh(214ml)溶液中滴加cbzcl(61ml,428mmol)。加入完成后,将混合物升温至室温并搅拌2小时,将反应混合物用水(1600ml)稀释,并用乙酸乙酯(2×15600ml)萃取。分离水层并用浓hcl酸化直至达到ph2,将所得溶液搅拌1小时并在5℃下静置以得到白色沉淀物,将沉淀物过滤,用水洗并干燥,得到2,3-双((((苄氧基)羰基)氨基)氨基)琥珀酸(52.2g,125mmol,59%)。 实施例306.((3r,4s)-2,5-二氧四氢呋喃-3,4-二基)二氨基甲酸二苄基酯的合成。 将2,3-双((((苄氧基)羰基)氨基)琥珀酸琥珀酸(5.0g,12mmol)在ac2o(37.5ml)中回流20分钟,冷却并浓缩,得到酸酐。将非对映异构体混合物与氯仿(37ml)混合,过滤收集不溶的内消旋异构体,并用石油醚洗涤,得到((3r,4s)-2,5-二氧四氢呋喃-3,4-二基)二氨基甲酸二苄酯(2.0g,5mmol,42%)。 实施例307.4,4′-((((2r,3s)-2,3-双((((苄氧基)羰基)-氨基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯的合成。 在0℃下,向((3r,4s)-2,5-二氧四氢呋喃-3,4-二基)二氨基甲酸二苄酯(2.03g,5.1mmol)和4-氨基丁酸叔丁酯(1.79g,11.3mmol)的dmf(45ml)溶液加入dipea(1.98g,15.3mmol)。搅拌5分钟后,加入hatu(4.66g,12.3mmol),将混合物升温至室温并搅拌2小时。反应完成后,将混合物用水(90ml)稀释并用乙酸乙酯(2×200ml)和二氯甲烷(2×90ml)萃取,将合并的有机萃取物用盐水洗涤,并用无水硫酸钠干燥。减压除去大部分溶剂,将白色沉淀收集并干燥,得到4,4′-((((2r,3s)-2,3-双(((苄氧基)))羰基)氨基)琥珀酰基)双(氮杂二烷基))二丁酸二叔丁酯(2.8g,4.0mmol),为白色固体,收率为80%。 实施例308.4,4′-((((2r,3s)-2,3-二氨基琥珀酰基)双-(氮杂二基))二丁酸二叔丁酯的合成。 将4,4′-((((2r,3s)-2,3-双((((苄氧基)羰基)氨基)琥珀酰基)双-(氮杂二烷基))二丁酸二叔丁酯(2.8g,4.0mmol)的甲醇(100ml)溶液与10%pd/c(1.1g)混合,在氢气下于室温搅拌过夜,搅拌18小时后,过滤除去pd/c,用甲醇洗涤。浓缩滤液,得到产物,为无色液体(940mg,2.2mmol,收率55%),其无需进一步纯化即可用于下一步。 实施例309.4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-)基)丁二酰胺)琥珀酰基)双(氮杂二基)二丁酸二叔丁酯。 在0℃下,向4,4′-(((((2r,3s)-2,3-二氨基琥珀酰)双(氮杂二烯基))-二丁酸二叔丁酯(940mg,2.19mmol)和4-(2,5-二氧代2,5-二氢-1h-吡咯-1-基)丁酸(840mg,4.59mmol)的dmf(25ml)溶液中加入dipea(1.13g,8.76mmol)。搅拌5分钟后加入hatu(1.74g,4.58mmol)。将混合物升温至室温并搅拌1小时,反应完成后,将混合物用水(50ml)稀释,并用乙酸乙酯(2×100ml)和二氯甲烷(2×50ml)萃取,合并的有机萃取物经盐水洗涤并经无水硫酸钠干燥。减压除去大部分溶剂,将白色固体收集并干燥,得到4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丁二酰亚胺基)琥珀酰基双(氮杂二基)二丁酸二叔丁酯(1.36g,1.79mmol,产率82%)。 实施例310.4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丁酰胺基)琥珀酰亚胺)琥珀酰基)双(氮杂二基)二丁酸的合成。 在0℃下,向4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丁酰胺基)琥珀酰基)双(氮杂二烷基))二丁酸二叔丁酯(1.36g,1.79mmol)的二氯甲烷(15ml)溶液中加入tfa(30ml)。搅拌18小时后,将反应浓缩,并将残余物溶于无水甲苯中。真空蒸发除去溶剂,得到白色沉淀物(1.3mg,2.0mmol,收率100%),无需进一步纯化即可用于下一步骤。 实施例311.pbd产物c-07的合成。 在0℃下,向(11s,11as,11’s,11a’s))-双(4-((s)-2-((s)-2-((((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基)苄基8,8′-(戊烷-1,5-二基双(氧基))双(11-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯[1],2-a][1,4]二氮杂-10(5h)-羧酸酯)(215mg,0.17mmol)和4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丁酰胺基)琥珀酰基)双(氮杂二基))二丁酸(115mg,0.18mmol)的dmf(18ml)溶液中加入dipea(90mg,0.70mmol)。搅拌5分钟后,加入hatu(132mg,0.35mmol),使混合物升温至室温,并搅拌过夜。反应完成后,将混合物用水(20ml)稀释,并用乙酸乙酯(2×40ml)和二氯甲烷(2×20ml)萃取,将合并的有机萃取液用盐水洗涤,干燥,过滤并浓缩。残余物通过hplc纯化,得到pbd产物c-07(10mg),为白色粉末。esimsm/z:c91h115n16o26[m+h]+,计算值:1847.81,实测值:1847.60。 实施例312.4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)琥珀酰)双(氮杂二基)二丁酸二叔丁酯。 在0℃下,向4,4′-((((2r,3s)-2,3-二氨基琥珀酰基)双(氮杂二基))-二丁酸二叔丁酯(900mg,2.09mmol)和3-(2,5-二氧代2,5-二氢-1h-吡咯-1-基)丙酸(840mg,4.97mmol)的dmf(25ml)溶液中加入dipea(0.93g,7.21mmol)。搅拌5分钟后,加入edc(1.74g,9.06mmol)。使混合物升温至室温,并搅拌1小时。反应完成后,将混合物用水(50ml)稀释,并用乙酸乙酯(2×100ml)和二氯甲烷(2×50ml)萃取,将合并的有机萃取物用盐水洗涤并用无水硫酸钠干燥。减压浓缩除去大部分溶剂,沉淀出白色固体,将其收集并干燥,得到4,4′-((((2r,3s)-2,3-双(3-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双-(氮杂二基))二丁酸二叔丁酯(1.27g,1.79mmol,产率83%)。esimsm/z:c34h49n6o12[m+h]+,计算值:733.33,实测值:733.55。 实施例313.4,4′-((((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸的合成。 在4℃下,向4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丁酰胺基)琥珀酰)双(氮杂二烷基))二丁酸二叔丁酯(502.0mg,0.685mmol)的1,4-二氧六环中加入hcl(3ml),然后将混合物在室温搅拌30分钟,用1,4-二氧六环(8ml)稀释,浓缩,与1,4-二氧六环/甲苯(1:1,2×10ml)共同蒸发至干,并用乙醇/正己烷结晶,得到标题化合物(289.0g,收率68%)。esimsm/z:c26h33n6o12[m+h]+,计算值:621.21,实测值:621.55。 实施例314.((s)-3-甲基-1-(((s)-1-((4-((((4-硝基苯氧基)羰基)-氧代)甲基)苯基)氨基)-1-氧代丙烷-2-基)氨基)-1-氧代丁-2-基)氨基甲酸烯丙酯的合成。 向((s)-1-((((s)-1-((4-(羟甲基)苯基)氨基)-1-氧丙烷-2-基)氨基)-3-甲基-1-氧代丁基-2-基)氨基甲酸烯丙酯(2.21g,5.86mmol)的无水吡啶(5ml)和二氯甲烷(20ml)的混合物中加入4-硝基苯基碳酰氯(1.82g,9.05mmol)。将混合物在室温搅拌8小时,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:12)洗脱,得到标题化合物(2.63g,收率83%)。esimsm/z:c26h31n4o9[m+h]+计算值:543.21,实测值:543.60。 实施例315.(11as,11a’s)-双(4-((s)-2-((s)-2-(((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基)苄基8,8′-(戊烷-1,5-二基双(氧基))双(7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 向(11as,11a’s)-8,8′-(戊烷-1,5-二基双(氧基))双(7-甲氧基-2-亚甲基-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂-5(10h)-酮)(288.2mg,0.490mmol)的无水乙腈(5ml)溶液中加入((s)-3-甲基-1-(((s)-1-((4-(((((4-硝基苯氧基)羰基)氧基)-甲基)苯基)氨基)-1-氧丙烷-2-氨基)-1-氧丁基-2-基)氨基甲酸烯丙酯(770.2mg,1.420mmol)和dipea(2ml)。将混合物在45℃下搅拌8小时,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶8)洗脱,得到标题化合物(492.0mg,收率72%)。msesim/z:c73h91n10o18[m+h]+计算值:1395.64,实测值:1395.95。 实施例316.(11as,11a’s)-双(4-((s)-2-((s)-2-氨基-3-甲基丁酰胺基)-丙酰胺基)苄基)8,8′-(戊烷-1,5-二基双(氧基)双(7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯)的合成。 向(11as,11a’s)-双(4-((s)-2-((s)-2-(((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基)苄基)8,8′-(戊烷-1,5-二基双(氧基))双(7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(274.2mg,0.197mmol)的二氯甲烷(5ml)溶液中加入吡咯烷(49mg,6.90mmol)和pd(pph3)4(152.0mg,0.132,mmol)。将反应在氩气下室温搅拌2小时,然后用二氯甲烷稀释,并依次用饱和氯化铵水溶液和盐水洗涤。有机相经无水硫酸钠干燥,过滤并浓缩。残余物通过柱色谱法纯化(二氯甲烷/甲醇/三乙胺=6/1/0.02),得到标题化合物(166.7mg,收率69%),为灰白色固体。msesim/z:c65h83n10o14[m+h]+计算值:1227.60,实测值:1227.93。 实施例317.pbd产物c-08的合成。 向(11as,11a’s)-双(4-((s)-2-((s)-2-氨基-3-甲基丁亚氨基)-丙酰胺基)苄基)8,8′-(戊烷-1,5-二基双(氧基)))双(7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯)(151.1mg,0.123mmol)和4,4′-((((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丙酰胺)琥珀酰基)双(氮杂二基)二丁酸(77.1mg,0.124mmol)的dma(5ml)溶液中加入edc(95.2mg,0.496mmol)。将混合物在室温下搅拌8小时,浓缩并通过c-18hplc(3μm,25×4cm)纯化,用乙腈(a)和0.1%甲酸/水(b)梯度洗脱(15%a至25%a,5分钟;35%a,15分钟;60%a至50%a,15分钟;15%a,5分钟;流速为8ml/min)。合并含有标题化合物组分,浓缩,并在干燥器中用p2o5干燥,得到c-8化合物(149.2mg,收率67%)。msesim/z:c91h111n16o24[m+h]+计算值:1811.79,实测值:1812.35。 实施例318.(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(羟基-乙基)吡咯烷基-1-基)甲酮的合成。 向4-(苄氧基)-5-甲氧基-2-硝基苯甲酸(10.20g,33.65mmol)和(s)-吡咯烷-2-基甲醇(3.85g,38.09mmol)的无水dmf(150ml)溶液中加入edc(19.50g,101.56mmol)。将混合物在室温搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶4)洗脱,得到标题化合物(11.56g,89%产率)。msesim/z:c20h23n2o6[m+h]+计算值:387.15,实测值:387.65。 实施例319.(s)-1-(4-(苄氧基)-5-甲氧基-2-硝基苯甲酰基)吡咯烷-2-甲醛的合成。 在室温下氮气中,向(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(羟甲基)-吡咯烷-1-基)甲酮(3.80g,9.84mmol)的无水二氯甲烷(15ml)溶液中加入dess-martin试剂(dmp)(5.80g,13.67mmol)。反应完成后,向反应溶液中加入na2so3水溶液,然后加入碳酸氢钠水溶液,将混合物再搅拌15分钟,并用二氯甲烷(3×20ml)萃取。合并的有机萃取物用盐水洗涤,干燥,过滤并浓缩。残余物通过硅胶柱色谱纯化(二氯甲烷/乙酸乙酯=4/1),得到标题化合物(3.13g,收率83%),为灰白色泡沫。msesim/z:c20h21n2o6[m+h]+计算值:385.13,实测值:385.60;404.75[m+h2o+h]+。 实施例320.8-羟基-7-甲氧基-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(10h)-酮的合成。 在氢化反应器中,将pd/c(10%pd,50%wet,250mg)加入到(s)-1-(4-(苄氧基)-5-甲氧基-2-硝基苯甲酰基)吡咯烷-2-甲醛(3.00g,7.80mmol)的甲醇(75ml)溶液中。抽空反应器中的空气后,充入氢气(5psi)。将反应容器振荡过夜,并通过硅藻土过滤。将滤液浓缩并通过硅胶柱色谱纯化(二氯甲烷/甲醇/三乙胺=4/1/0.05),得到标题化合物(1.66g,收率86%),为灰白色泡沫。msesim/z:c13h17n2o3[m+h]+计算值:249.12,实测值:249.50。 实施例321.4-((14s,17s)-1-叠氮基17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-((叔丁氧基羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺基)苄基8–羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 在4-8℃下,向(14s,17s)-1-叠氮基-14-(4-((叔丁氧基羰基)氨基)丁基)-17-((4-(羟甲基)苯基)氨基甲酰基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氧杂十九烷-19-叔丁酯(10.15g,13.50mmol)的无水四氢呋喃(300ml)溶液中加入dipea(3.15g,24.41mmol)和三光气的无水四氢呋喃(50ml,5.15g,17.36mmol)溶液。搅拌15分钟后,在45分钟内滴加完成8-羟基-7-甲氧基-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(10h)-酮(2.92g,11.76mmol)的四氢呋喃(100ml)溶液。使所得溶液升温至室温,并搅拌过夜。将混合物用甲苯(50ml)稀释,真空蒸发并通过硅胶柱色谱纯化(二氯甲烷/甲醇=15/1),得到标题化合物(10.02g,收率82%),为黄色泡沫。msesim/z:c50h74n9o15[m+h]+计算值:1040.52,实测值:1040.90。 实施例322.(s)-4-((14s,17s)-1-叠氮基17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-((叔丁氧基羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)苄基8-(3-碘丙氧基)-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 向4-((14s,17s)-1-叠氮基17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-((叔丁氧基羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺基)苄基8-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(2.02g,1.94mmol)的丁酮(50ml)溶液中加入cs2co3(2.50g,7.67mmol)和1,3-二碘丙烷(2.50g,8.45mmol)。将混合物在暗处于45℃搅拌36小时,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶5)洗脱,得到标题化合物(2.08g,收率90%)。msesim/z:c52h77in9o15[m+h]+计算值:1194.45,实测值:1194.95。 实施例323.(s)-2-((s)-1-叠氮基-14-甲基-12-氧代-3,6,9-三氧杂-13-氮杂十五烷酰胺基)-n-(4-(羟甲基)苯基丙酰胺的合成。 向(14s,17s)-1-叠氮基14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸(3.02g,7.75mmol)和(4-氨基苯基)甲醇(1.05g,8.53mmol)的dma溶液中加入edc(4.90g,25.52mmol)。将混合物在室温搅拌14小时,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶8至1∶3)洗脱,得到标题化合物(3.52g,收率92%)。msesim/z:c22h35in6o7[m+h]+计算值:495.25,实测值:495.60。 实施例324.(11r-11as)-4-((14s-17s)-1-叠氮-14-17-二甲基-12,15-二氧基-3,6,9-三氧基-13,16-二氮杂十八烷酰胺)苄基8-(苄氧基)-11-羟基-7-甲氧基-2-亚甲基-5-氧基-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 在室温下,将(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(羟甲基)-4-亚甲基-吡咯烷-1-基)甲酮(3.90g,9.80mmol),na2s2o4(6.0g,34.47mmol),四氢呋喃(60ml)和水(40ml)的混合物搅拌20小时,用na2co3调节ph到10,浓缩,在c-18短柱上纯化,用水/甲醇/et3n洗脱(从99.4/0.5/0.2到50/49.8/0.2)。合并含有氨基产物的组分,浓缩,用四氢呋喃(50ml)稀释,然后冷却至4-8℃。在4-8℃下,向2-(1-叠氮基-14-甲基-12-氧代-3,6,9-三氧杂-13-氮杂十五酰胺基)-n-(4-(羟甲基)苯基)-丙酰胺(6.70g,13.56mmol)的无水四氢呋喃(150ml)溶液中加入dipea(3.50g,27.12mmol)和三光气(4.10g,13.80mmol)的无水四氢呋喃(20ml)溶液。在4-8℃下搅拌15分钟后,将其在45分钟以内滴加到上述胺溶液中。将该混合物升温至室温并继续搅拌2小时,浓缩,用二氯甲烷(3×30ml)萃取,经无水硫酸钠干燥,浓缩,并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶10至1∶5)洗脱,得到标题化合物(7.23g,两步收率83%)。msesim/z:c45h57in8o12[m+h]+计算值:889.40,实测值:889.90。 实施例325.(11s,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺)苄基8-(苄氧基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 在氮气中,室温下向(11r,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺)苄基8-(苄氧基))-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(3.80g,4.27mmol)的无水二氯甲烷(40ml)溶液中加入dess-martin试剂(dmp)(2.80g,6.60mmol)。反应完成后,向反应溶液中加入na2so3水溶液,然后加入碳酸氢钠水溶液,将混合物再搅拌15分钟,并用二氯甲烷(3×20ml)萃取。合并的有机萃取物用盐水洗涤,干燥,过滤并浓缩。残余物通过硅胶柱色谱纯化(二氯甲烷/乙酸乙酯=5/1至2∶1),得到标题化合物(2.99g,收率79%),为灰白色泡沫。msesim/z:c44h55n8o12[m+h]+计算值:886.39,实测值:886.80。 实施例326.(11s,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺)苄基8,11-二羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 在0℃下,向(11s,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)苄基8-(苄氧基))-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(2.90g,3.27mmol)的二氯甲烷(40ml)溶液中加入15ml的ch3so3h。将混合物在0℃下搅拌10分钟,然后在室温下搅拌1小时,用二氯甲烷稀释,用冷的1.0n碳酸氢钠调节ph至4,并过滤。用二氯甲烷(3×60ml)萃取水层,合并有机层,经无水硫酸钠干燥,过滤,蒸发并在硅胶柱色谱上纯化(甲醇/二氯甲烷1∶15至1∶5),得到标题产物1.95g(收率75%)。msesim/z:c37h48in8o12[m+h]+计算值:797.34,实测值:797.90。 实施例327.(11s,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺)苄基8-(3-((((s)-10-)(((4-((14s,17s)-1-叠氮基17-(2-(叔丁氧基)-2-氧乙基)-14-(4-(((叔丁氧羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺基)苄基)氧)羰基)-7-甲氧基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-a][1,4]-8-基)氧基)丙氧基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 向(11s,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺基)苄基8,11-二羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(402mg,0.504mmol)和(s)-4-((14s,17s)-1-叠氮基17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-((叔-丁氧羰基)氨基)-丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)苄基8-(3-碘丙氧基)-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(650mg,0.544mmol)的丁酮(50ml)溶液中加入cs2co3(0.50g,1.53mmol)。将混合物在暗处中于45℃搅拌36小时,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:8至1:3)洗脱,得到标题化合物(809mg,收率86%)。msesim/zc89h124n17o27[m+h]+计算值:1862.89,实测值:1863.45。 实施例328.(11s,11as)-4-((14s,17s)-1-氨基-14,17-二甲基-12,15-二氧代-3,6,9-三氧代-13,16-二氮杂十八烷酰胺基)苄基8-(3-(((s)-10-(((4-((14s,17s)-1-氨基-17-(2-(叔丁氧基)-2-氧乙基)-14-(4-((叔-丁氧羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)苄基)氧)羰基)-7-甲氧基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-8-基)氧基)丙氧基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 在0-4℃,n2环境下,向(11s,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)苄基8-(3-(((s)-10-(((4-((14s,17s)-1-叠氮基17-(2-(叔丁氧基)-2-氧乙基)-14-(4-((叔-丁氧羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)-苄基)氧)羰基)-7-甲氧基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-8-基)氧基)丙氧基)-11-羟基-7-甲氧基-2-亚甲基-5–氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(750mg,0.402mmol)的四氢呋喃(8ml)溶液中加入me3p(1.0m的甲苯溶液,2.0ml,2.0mmol)。搅拌5分钟后,移去冰浴,将反应混合物在室温搅拌2小时。然后,加入水(1ml),并将混合物搅拌10分钟。将混合物用1,4-二氧六环(10ml)稀释,浓缩并与二氧六环/甲苯共浓缩至干,得到产物粗品(725mg,收率),无需进一步操作即可直接用于下一步。msesim/zc89h128n13o27[m+h]+计算值:1810.90,实测值:1811.50。 实施例329.不对称交联的pbd二聚体c-09的合成。 向上述所得的氨基化合物((11s,11as)-4-((14s,17s)-1-氨基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)苄基8-(3-(((s)-10-((((4-((14s,17s)-1-氨基-17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-(((叔丁氧基羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺基)苄基)氧基)羰基)-7-甲氧基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-8-基)氧基)丙氧基)-11-羟基-7-甲氧基-2-亚甲基-5–氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的干燥的dma(8ml)溶液中,加入4,4′-((((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基))琥珀酰基)双(氮杂二基))二丁酸(248.0mg,0.400mmol)和edc(500.0mg,2.60mmol)。将混合物搅拌24小时,浓缩并在制备型hplc(c18,250mm×50mm)上纯化,用水/乙腈洗脱(从80%水至30%水,45min,9ml/min)。在高真空下浓缩,得到488.1mg(51%收率)c-9产物。esimsm/zc115h156n19o37[m+h]+:计算值2395.08,实测值2395.90。 实施例330.不对称交联的pbd二聚体c-10的合成。 在0-4℃下,将c-9化合物(465.0mg,0.194mmol)溶于二氯甲烷(4ml),然后加入tfa(2ml)。然后将反应混合物在室温搅拌1h,用甲苯(5ml)稀释,然后浓缩,并与二氯甲烷/甲苯共蒸发至干,得到粗产物(48.0mg,100%收率,92%hplc纯)。将其通过反相hplc(250mm×20mm,c18柱,5-60%乙腈/水,40min,v=8ml/min)进一步纯化,得到泡沫状纯产品c-10(纯度96%,373.1mg,产率85%)。esimsm/zc106h140n19o35[m+h]+:计算值2238.97,实测值2239.50。 实施例331.不对称交联的pbd二聚体c-11的合成。 将c-10化合物(235.0mg,0.105mmol)溶于四氢呋喃(3ml)和0.1mph7.5的nah2po4溶液(3ml)中,在2小时内分4批加入2,5,8,111,14,17,20,23-八氧杂二十六烷-26-n-琥珀酰亚胺酯(43.0mg,0.084mmol)。然后将反应混合物继续在室温搅拌4小时,并与dmf(10ml)共同蒸发至干,得到粗产物,将其通过反相hplc进一步纯化(250mm×50mm,c18柱,20-60%乙腈/水,40min,v=8ml/min),得到泡沫状纯产物c-11(纯度95%,215.5mg,产率78%)。esimsm/zc124h174n19o44[m+h]+:计算值2633.20,实测值2633.85。 实施例332.不对称交联的pbd二聚体c-12的合成。 向c-11化合物(65.0mg,0.0246mmol)和2,5,8,11,14,17,20,23-八氧杂二十五烷25-胺(15.1mg,0.0394mmol)的无水dma(2ml)溶液中加入edc(30.0mg,0.156mmol)。将反应混合物在室温搅拌15h,浓缩,通过反相hplc(250mm×30mm,c18柱,20-60%乙腈/水,40min,v=8ml/分钟)纯化,得到产物c-12(hplc纯度95%,60.2mg,81%产率),为泡沫状固体。esimsm/zc141h209n20o51[m+h]+:计算值2998.43,实测值2999.40。 实施例333.硝基-α-鹅膏毒素的合成。 在0℃下,向α-鹅膏毒素(15.0mg,0.0163mmol,pct/ib2016/052246)的乙酸(0.5ml)和二氯甲烷(1ml)溶液中加入70%hno3(0.3ml)。将反应在0℃下搅拌1小时,然后在室温下搅拌2小时。加入水(5ml)和dma(4ml),将混合物浓缩并通过制备型hplc(h2o/mecn)纯化,得到浅黄色固体(9.8mg,62%产率)。esimsm/z:c39h54n11o16s[m+h]+计算值963.34,实测值964.95。 实施例334.硝基-β-鹅膏毒素的合成。 在0℃下,向β-鹅膏毒素(15.0mg,0.0163mmol,pct/ib2016/052246)的乙酸(0.5ml)和二氯甲烷(1ml)溶液中加入70%hno3(0.3ml)。将反应在0℃下搅拌1小时,然后在室温下搅拌2小时。加入水(5ml)和dma(4ml),将混合物浓缩并通过制备型hplc(h2o/mecn)纯化,得到浅黄色固体(9.8mg,62%产率)。esimsm/z:c39h53n10o17s[m+h]+计算值965.32,实测值965.86。 实施例335.可偶联的α-鹅膏毒素类似物d-01和d-02的合成。 向硝基-α-鹅膏毒素(9.0mg,0.0093mmol)的dma(1ml)溶液中加入pd/c(3mg,50%水),在室温下氢化(1atm)6小时。滤出催化剂,然后加入0.5ml,0.1mph7.5nah2po4和双(2,5-二氧杂吡咯烷-1-基)21,22-双(2,5-二氧杂-2,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧代-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二酸酯(11.0mg,0.0092mmol)。将混合物在室温搅拌过夜,浓缩,并在c18制备型hplc上纯化,用水/乙腈洗脱(在45分钟内从95%水至25%水)。合并组分,浓缩并在高真空下干燥,得到产物d-01(6.1mg,35%的产率),esimsm/zc81h114n19o32s[m+h]+,计算值:1896.75,实测值:1897.20;和产品d-02(4.9mg,收率27%),esimsm/zc81h116n19o33s[m+h]+,计算值:1914.76,实测值:1914.40。 实施例336.可偶联的β-鹅膏毒素类似物d-03和d-04的合成。 向硝基-β-鹅膏毒素(9.0mg,0.0093mmol)的dma(1ml)溶液中加入pd/c(3mg,50%水),然后在室温下氢化(1atm)6小时。滤出催化剂,然后加入0.5ml,0.1mph7.5的nah2po4,和双(2,5-二氧杂吡咯烷-1-基)21,22-双(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧代-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二酸酯(11.0mg,0.0092mmol)。将混合物在室温搅拌过夜,浓缩,并在c18制备型hplc上纯化,用水/乙腈洗脱(在45分钟内从95%水至25%水)。合并组分,浓缩并在高真空下干燥,得到产物d-03(7.0mg,收率40%),esimsm/zc81h113n18o33s[m+h]+,计算值:1896.74,实测值:1897.20;和产物d-04(4.7mg,收率25%),esimsm/zc81h115n18o34s[m+h]+,计算值:1915.75,实测值:1916.30。 实施例337.具有双连接子的可偶联的α-鹅膏毒素类似物d-05的合成。 向硝基-α-鹅膏毒素(9.0mg,0.0093mmol)的无水dma(1ml)溶液中加入pd/c(3mg,50%水),然后在室温下氢化(1atm)6小时。滤出催化剂,先用dma(1ml)洗涤,然后加入双(2,5-二氧杂吡咯烷-1-基)21,22-二(2,5-二氧杂-2,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧代-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二甲酸酯(40.0mg,0.033mmol)和dipea(2μl,0.011mmol)。将混合物在室温下搅拌4小时,然后加入26-氨基-3,6,9,12,15,18,21,24-八氧杂二十六烷-1-醇(30.0mg,0.072mmol)。将混合物继续搅拌过夜,通过c18制备hplc纯化,用水/乙腈洗脱(在45分钟内从95%水到30%水),在高真空下浓缩干燥后,得到标题产品d-05(14.5mg,收率69%)。esimsm/zc99h153n20o41s[m+h]+,计算值:2310.01,实测值:2310.90;和副产物2,3-双(2,5-二氧基-2,5-二氢-1h-吡咯-1-基)-n1,n4-双(1-羟基-29,32-二甲基-28,31,34-三氧基-3,6,9,12,15,18,21,24,37,40,43-十一氧杂-27,30,33-三氮杂四十五烷-45-基)丁二酰胺(24.3mg,0.013mmol),esimsm/zc78h136n10o36[m+h]+,计算值:1789.91,实测值:1790.20。 实施例338.具有双连接子的可偶联的β-鹅膏毒素类似物d-06的合成。 向硝基-β-鹅膏毒素(9.0mg,0.0093mmol)的无水dma(1ml))溶液中加入pd/c(3mg,50%水),然后在室温下氢化(1atm)6h。过滤掉催化剂,用dma(1ml)洗涤,然后加入双(2,5-二氧吡咯烷-1-基)21,22-双(2,5-二氧基-2,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧基-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二酯(40.0mg,0.033mmol)和dipea(2μl,0.011mmol)。将混合物在室温下搅拌4小时,然后加入26-氨基-3,6,9,12,15,18,21,24-八氧杂二十六烷-1-醇(30.0mg,0.072mmol)。将混合物继续搅拌过夜,在c18制备hplc上纯化,用水/乙腈洗脱(在45分钟内从95%水到30%水),在高真空下浓缩和干燥后,得到标题产物d-06(14.9mg,收率69%)。esimsm/zc99h152n19o42s[m+h]+,计算值:2311.00,实测值:2311.90;和副产物pg-04,2,3-双(2,5-二氧基-2,5-二氢-1h-吡咯-1-基)-n1,n4-双(1-羟基-29,32-二甲基-28,31,34-三氧基-3,6,9,12,15,18,21,24,37,40,43-十一氧杂-27,30,33-三氮杂四十五烷-45-基)丁二酰胺(24.8mg,0.013mmol),esimsm/zc78h136n10o36[m+h]+,计算值:1789.91,实测值:1790.20。 实施例339.制备偶联物的一般方法。 向2.0ml10mg/mlph6.0-8.0的her2抗体中分别加入0.70-2.0ml100mmnah2po4缓冲液,ph6.5-8.5缓冲液,tcep(16-20μl,20mm水溶液)和化合物a-01、a-02、a-03、a-04、b-01、b-02、b-03、b-04、b-05、b-06、b-07、b-08、b-09、b-10、b-11、b-12、b-13、b-14、b-15、b-16、c-02、c-03、c-04、c-05、c-06、c-07、c-08、c-09、c-10、c-11、c-12、d-01、d-02、d-03、d-04、d-05或d-06(28-32μl,20mmdma溶液)。将混合物在室温下温育4-18小时,然后加入dhaa(135μl,50mm)。在室温下温育过夜后,将混合物在g-25柱上纯化,用100mmnah2po4,50mmnacl,ph6.0-7.5缓冲液洗脱,得到12.8-18.1mg在14.4-15.5ml缓冲液中的偶联物化合物aa-01、aa-02、aa-03、aa-04、ba-01、ba-02、ba-03、ba-04、ba-05、ba-06、ba-07、ba-08、ba-09、ba-10、ba-11、ba-12、ba-13、ba-14、ba-15、ba-16、ca-02、ca-03、ca-04、ca-05、ca-06、ca-07、ca-08、ca-09、ca-10、ca-11、ca-12、da-01、da-02、da-03、da-04、da-05或da-06(收率75%~90%)。通过uplc-qtof质谱确定偶联物的药物/抗体比(dar),为3.1-4.2。通过sechplc(tosohbiosciences,tskgelg3000sw,7.8mm×30cm,0.5ml/min,100min)分析单体含量,为94-99%,sds-page谱图为单一谱带。偶联物结构如下所示: 其中n=2.0~4.5。 实施例340.与t-dm1对比,偶联物aa-01、aa-02、aa-03、aa-04、ba-01、ba-02、ba-03、ba-04、ba-05、ba-06、ba-07、ba-08、ba-09、ba-10、ba-11、ba-12、ba-13、ba-14、ba-15、ba-16、ca-02、ca-03、ca-04、ca-05、ca-06、ca-07、ca-08、ca-09、ca-10、ca-11、ca-12、da-01、da-02、da-03、da-04、da-05和da-06的体外细胞毒性评价。 用于细胞毒性测定的细胞系是人胃癌细胞系nci-n87,细胞在含有10%fbs的rpmi-1640中生长。测定时,将细胞(180μl,6000个细胞)加入到96孔板中的每个孔中,并在37℃,5%co2下温育24小时。接下来,在适当的细胞培养基里,用不同浓度的测试化合物(20μl)处理细胞(总体积,0.2ml)。对照孔含有细胞和培养基,但无测试化合物。将孔板在37℃和5%co2下温育120小时,然后向孔中加入mtt(5mg/ml)(20μl),并将孔板在37℃下孵育1.5小时。小心去除培养基,然后加入dmso(180μl),振荡15分钟,在490nm和570nm处测量吸光度,以620nm为参考。依照以下公式计算抑制率:抑制率%=[1-(分析值-空白对照值)/(控制值-空白对照值)]×100。 以ic50和ic90表示的细胞毒性结果: 实施例230.体内抗肿瘤活性(nci-n87异种移植肿瘤的balb/c裸鼠)。 在人胃癌n-87细胞系肿瘤异种移植模型上评估了偶联物ba-12,ba-14,ba-16,ca-03,ca-04,ca-05,ca-06,ca-07,ca-10,ca-11,ca-12,以及t-dm1的体内疗效。在五周龄的雌性balb/c裸鼠(104只动物)右肩下用在0.1ml无血清培养基中的n-87癌细胞(5×106个细胞/小鼠)进行皮下接种。肿瘤生长8天至平均大小130mm3。然后将动物随机分成13组(每组8只动物)。第一组小鼠用作对照组,注射磷酸缓冲盐水(pbs)。其它12组分别用偶联物ba-12,ba-14,ba-16,ca-03,ca-04,ca-05,ca-06,ca-07,ca-10,ca-11,ca-12和t-dm1静脉注射,剂量3mg/kg。剩余2组用偶联物c-3a和d-1a静脉注射,剂量3mg/kg。每4天测量一次肿瘤的三维尺寸,并使用公式:肿瘤体积=1/2(长×宽×高),计算肿瘤体积。同时还测量动物的体重。当满足下列任何一项标准时,处死小鼠:(1)体重减少超过处理前体重的20%,(2)肿瘤体积大于2000mm3,(3)病情严重无法进食或(4)皮肤坏死。如果肿瘤无法被感知,则认为小鼠是无肿瘤的。 试验结果绘制在图27中。所有12种偶联物都不会导致动物体重减轻。在第35天,由于肿瘤体积大于2000mm3且小鼠十分虚弱,处死对照组的动物。除了测试的ca-06以外,其余测试的12种偶联物均显示出比t-dm1更好的抗肿瘤活性。在化合物ca-04和ca-3组中的所有6/6动物在第14天至第30天完全没有可测量的肿瘤。相反,剂量为3mg/kg的t-dm1不能消除肿瘤。 权利要求书(按照条约第19条的修改) 1.一种含有2,3-二氨基琥珀酰基双连接子的偶联物,其特征在于具有(ia),(ib),(ic),(iia),(iib),(iic),(iiia),(iiib),(iiic),(iva),(ivb)和(ivc)的结构: 其中 代表单键; 代表可选为单键或可以缺省; 代表可选为单键,双键,或者可以缺省;n独立地为1到30; q是连接到r3和r4的细胞结合剂/分子,可以是目前已知的,或者即将成为已知的任何种类的分子,可与具有治疗意义或生物学修饰的细胞群的片段结合,复合或反应。优选地,细胞结合剂/分子是免疫治疗蛋白,抗体,单链抗体;与靶细胞结合的抗体片段;单克隆抗体;单链单克隆抗体;或结合靶细胞的单克隆抗体片段;嵌合抗体;与靶细胞结合的嵌合抗体片段;域抗体;与靶细胞结合的域抗体片段;模拟抗体的adnectins;darpins;淋巴因子;激素;维生素;增长因子;集落刺激因子;或营养转运分子(转铁蛋白);含超过四个氨基酸的结合肽,或蛋白质,或抗体,或附着在白蛋白,聚合物,树枝状大分子,脂质体,纳米颗粒,囊泡或(病毒)衣壳上的小的细胞结合分子或配体; drug1或/和drug2是细胞毒性分子/药剂是治疗药物/分子/试剂,或免疫治疗蛋白质/分子,或用于增强细胞结合或稳定细胞结合剂的功能分子,或细胞表面受体结合配体,或抑制细胞增殖分子;或用于监测,检测或研究细胞结合作用的分子。它也可以是免疫治疗化合物、化学治疗化合物的类似物或前药,或药学上可接受的盐,水合物或水合盐,或晶体,或光学异构体,外消旋体,非对映异构体或对映异构体,抗体(probody)或抗体(probody)片段,或sirna、dna分子,或细胞表面结合配体; x1和x2相同或不同,独立地选自nh、nhnh、n(r1)、n(r1)n(r2)、o、s、s-s、o-nh、o-n(r1)、ch2-nh、ch2-n(r1)、ch=nh、ch=n(r1)、s(o)、s(o2)、p(o)(oh)、s(o)nh、s(o2)nh、p(o)(oh)nh、nhs(o)nh、nhs(o2)nh、nhp(o)(oh)nh、n(r1)s(o)n(r2)、n(r1)s(o2)n(r2)、n(r1)p(o)(oh)n(r2)、os(o)nh、os(o2)nh、op(o)(oh)nh、c(o)、c(nh)、c(nr1)、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)nh、oc(nh)nh、oc(nr1)nh、nhc(o)nh、nhc(nh)nh、nhc(nr1)nh、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)n(r1)、oc(nh)n(r1)、oc(nr1)n(r1)、nhc(o)n(r1)、nhc(nh)n(r1)、nhc(nr1)n(r1)、n(r1)c(o)n(r1)、n(r1)c(nh)n(r1)、n(r1)c(nr1)n(r1);或c1-c6烷基;c2-c8烯基、杂烷基、烷基环烷基或杂环烷基;c3-c8芳基、芳烷基、杂环、碳环、环烷基、杂烷基环烷基、烷基羰基或杂芳基; y1、y2、z1和z2是相同或不同的官能团,独立地通过二硫化物,硫醚,硫酯,肽,腙,醚,酯,氨基甲酸酯,碳酸酯,胺(二级,三级或四级),亚胺,环杂烷基,杂芳基,烷氧基或酰胺键,连接至细胞结合分子q;y1、y2、z1和z2独立地具有以下结构:c(o)ch、c(o)c、c(o)ch2、arch2、c(o)、nh、nhnh、n(r1)、n(r1)n(r2)、o、s、s-s、o-nh、o-n(r1)、ch2-nh.ch2-n(r1)、ch=nh、ch=n(r1)、s(o)、s(o2)、p(o)(oh)、s(o)nh、s(o2)nh、p(o)(oh)nh、nhs(o)nh、nhs(o2)nh、nhp(o)(oh)nh、n(r1)s(o)n(r2)、n(r1)s(o2)n(r2)、n(r1)p(o)(oh)n(r2)、os(o)nh、os(o2)nh、op(o)(oh)nh、c(o)、c(nh)、c(nr1)、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)nh、oc(nh)nh、oc(nr1)nh、nhc(o)nh、nhc(nh)nh、nhc(nr1)nh、c(o)nh、c(nr1)nh、oc(o)n(r1)、oc(nh)n(r1)、oc(nr1)n(r1)、nhc(o)n(r1)、nhc(nh)n(r1)、nhc(nr1)n(r1)、n(r1)c(o)n(r1)、n(r1)c(nh)n(r1)、n(r1)c(nr1)n(r1);或c1-c8烷基、c2-c8杂烷基、烷基环烷基、杂环烷基;c3-c8芳基、芳烷基、杂环、碳环、环烷基、杂环烷基、烷基羰基、杂芳基; r1、r2、r3和r4中的各个原子以所有可能的化学方式结合,比如形成亚烷基,亚烯基和亚炔基,醚,聚氧化烯,酯,胺,亚胺,多胺,肼,腙,酰胺,脲,氨基脲,卡巴肼,烷氧胺,氨基甲酸酯,氨基酸,肽,酰氧基胺,异羟肟酸,或上述组合。优选地,r1、r2、r3和r4相同或不同,独立地选自o、nh、s、nhnh、n(r5)、n(r3)n(r3’)、如式(och2ch2)por5、(och2ch-(ch3))por5、nh(ch2ch2o)pr5、nh(ch2ch(ch3)o)pr5、n[(ch2ch2o)pr5]-[(ch2ch2o)p’r5’]、(och2ch2)pcoor5、ch2ch2(och2ch2)pcoor5的聚乙烯氧基单,其中p和p’独立地是选自0至约1000的整数,或上述的组合;c1-c8烷基;c2-c8杂烷基、烷基环烷基、杂环烷基、酯、醚或酰胺;c3-c8芳基,芳烷基,杂环,碳环,环烷基,杂烷基环烷基,烷基羰基或杂芳基;或1~24氨基酸;其中r5和r5’独立地为h;c1-c8烷基;c2-c8杂烷基、烷基环烷基或杂环烷基;c3-c8芳基,芳烷基,杂环;c2-c8酯、醚或酰胺;或1~24氨基酸; 或r1、r2、r3和r4可任选地由下列一个或多个连接子组分构成:6-马来酰亚胺基己酰基(“mc”)、马来酰亚胺丙酰基(“mp”)、缬氨酸-瓜氨酸(“val-cit”或“vc”)、丙氨酸-苯丙氨酸(“ala-phe”或“af”)、对氨基芐氧基-羰基(“pab”)、4-硫代戊酰基(“spp”)、4-(n-马来酰亚胺甲基)环己烷-1酰基(“mcc”)、(4-乙酰基)氨基苯酰基(“siab”)、4-硫丁酰基(spdb)、4-硫-2-羟基磺酰基-丁酰基(2-sulfo-spdb),或含有1-8个天然或非天然氨基酸单的天然或非天然肽。天然氨基酸最优选自天冬氨酸、谷氨酸、精氨酸、组氨酸、赖氨酸、丝氨酸、苏氨酸、天冬酰胺、谷氨酰胺、半胱氨酸、硒代半胱氨酸、酪氨酸、苯丙氨酸、甘氨酸、脯氨酸、色氨酸和丙氨酸; 或r1、r2、r3和r4独立地可包含以下亲水结构之一: 其中是连接位点;x3、x4、x5、x6和x7独立地选自nh、nhnh、n(r5)、n(r5)n(r5’)、o、s、c1-c6烷基、c2-c6杂烷基、烷基环烷基或杂环烷基、c3-c8芳基、芳烷基、杂环、碳环、环烷基、杂环烷基、烷基羰基、杂芳基、或1~8个氨基酸;其中r5和r5’独立地为h、c1-c8烷基、c2-c8杂烷基、烷基环烷基或杂环烷基、c3-c8芳基、芳烷基、杂环、碳环、杂环烷基、烷基羰基或杂芳基、c1-c8酯、醚或酰胺;或具有式(och2ch2)p或(och2ch(ch3))p的聚乙烯氧基,其中p是0到约5000的整数,或其组合; 或r1、r2、r3、r4、y1、y2、z1和z2独立地含有自我毁灭或非自我毁灭的组分,肽单、腙键、二硫化物、酯、肟、酰胺或硫醚键。自我毁灭单包括,与对氨基芐基氨甲酰基(pab)电子结构相似的芳香化合物,例如2-氨基咪唑-5-甲醇的衍生物、杂环pab类似物、β-葡糖苷酸、以及邻或对氨基芐基缩醛; 自我毁灭型连接子组分具有以下结构之一: 其中(*)标记的原子是另外的间隔体或可断裂连接子单、或细胞毒性剂和/或结合分子(cba)的连接点;x1、y1、z2和z3独立地为nh、o或s;z1独立地为h、nhr5、or1、sr5、cox1r5,其中x1和r5如前文所定义;v为0或1;u1独立地为h、oh、c1-c6烷基,(och2ch2)n、f、cl、br、i、or5、sr5、nr5r5’、n=nr5、n=nr5、n=r5、nr5r5’、no2、sor5r5’、so2r5、so3r5、so3r5、oso3r5、oso3r5、pr5r5’、po5r5’、po2r5r5’、opo(or5)(or5′)或och2po(or5(or5(or5′)、其中,其中,r5和r5’独立选自h、c1-c8烷基、c2-c8烷基,烯基、杂烷基或氨基酸;c3-c8芳基、烷基、烷基、烷基、或氨基酸;c3-c8芳基、杂环、碳环、环烷基、杂环烷基、杂芳烷基、烷基羰基或糖苷;或药用阳离子盐; 非自我毁灭型连接子组分具有以下结构之一:*(ch2ch2o)r*; 其中(*)标记的原子是另外的间隔体或可释放的连接子单、或细胞毒性剂和/或结合分子的连接点;x1、y1、u1、r5、r5’如前文所定义;r为0~100;m和n独立地为0~20; 或r1、r2、r3和r4独立地包含可释放的连接子组分,其包含至少一个可在生理条件下被破坏的键,例如ph、酸、碱、氧化作用、代谢、生化或酶不稳定的键,包含以下结构: -(cr5r6)m(aa)r(cr7r8)n(och2ch2)t-、(cr5r6)m(cr7r8)n(aa)r(och2ch2)t-、(aa)r-(cr5r6)m(cr7r8)n(och2ch2)t-、(cr5r6)m(cr7r8)n(och2ch2)r(aa)t-、-(cr5r6)m-(cr7=cr8)(cr9r10)n(aa)t(och2ch2)r-、-(cr5r6)m(nr11co)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m(aa)t(nr11co)(cr9r10)n(och2ch2)r-、-(cr5r6)m(oco)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、-(cr5r6)m(co)(aa)t-(cr9r10)n(och2ch2)r-、-(cr5r6)m(nr11co)(aa)t(cr9r10)n(och2ch2)r-、-(cr5r6)m-(oco)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、-(cr5r6)m(co)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m-苯基co(aa)t(cr7r8)n-、-(cr5r6)m-呋喃co(aa)t(cr7r8)n-、-(cr5r6)m-恶唑co(aa)t(cr7r8)n-、-(cr5r6)m-噻唑基co(aa)t(ccr7r8)n-、-(cr5r6)t-噻吩co(cr7r8)n-、-(cr5r6)t-咪唑co-(cr7r8)n-、-(cr5r6)t-吗啉co(aa)t-(cr7r8)n-、-(cr5r6)t哌嗪-co(aa)t-(cr7r8)n-、-(cr5r6)t-n甲基co(aa)t-(cr7r8)n-、-(cr5r)m-(aa)t苯基-、-(cr5r6)m-(aa)t呋喃、-(cr5r6)m-恶唑(aa)t、-(cr5r6)m-噻唑基(aa)t、-(cr5r6)m-噻吩-(aa)t-、-(cr5r6)m-咪唑(aa)t-、-(cr5r6)m-吗啉(aa)t-、-(cr5r6)m-哌嗪(aa)t-、-(cr5r6)m-n甲基哌嗪(aa)t-、k(cr5r6)m(aa)r(cr7r8)n(och2ch2)t-、k(cr5r6)m(cr7r8)n(aa)r(och2ch2)t-、k(aa)r-(cr5r6)m(cr7r8)n(och2ch2)t-、k(cr5r6)m(cr7r8)n(och2ch2)r(aa)t-、k(cr5r6)m-(cr7=cr8)(cr9r10)n(aa)t(och2ch2)r-、k(cr5r6)m(nr11co)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m(aa)t(nr11co)(cr9r10)n(och2ch2)r-、k(cr5r6)m(oco)(aa)t(cr9r10)n-(och2ch2)r-、k(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m(co)(aa)t-(cr9r10)n(och2ch2)r-、k(cr5r6)m(nr11co)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m-(oco)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、k-(cr5r6)m(co)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m-苯基co(aa)t(cr7r8)n-、k-(cr5r6)m-呋喃co(aa)t-(cr7r8)n-、k(cr5r6)m-恶唑co(aa)t(cr7r8)n-、k(cr5r6)m-噻唑基co(aa)t-(cr7r8)n-、k(cr5r6)t-噻吩co(cr7r8)n-、k(cr5r6)t咪唑-co-(cr7r8)n-、k(cr5r6)t吗啉co(aa)t(cr7r8)n-、k(cr5r6)t哌嗪-co(aa)t-(cr7r8)n-、k(cr5r6)t-n甲基co(aa)t(cr7r8)n-、k(cr5r)m(aa)t苯基、k-(cr5r6)m-(aa)t呋喃-、-k(cr5r6)m-恶唑(aa)t-、k(cr5r6)m-噻唑基(aa)t-、k(cr5r6)m-噻吩-(aa)t-、k(cr5r6)m-咪唑(aa)t-、k(cr5r6)m-吗啉(aa)t-、k(cr5r6)m-哌嗪(aa)t-、k(cr5r6)mn甲基哌嗪(aa)t-;其中aa、m和n定义如前文所描述;t和r独立地为0-100;r3、r4、r5、r6、r7和r8独立地选自h、卤化物、c1-c8烷基、c2-c8芳基、烯基、炔基、醚、酯、胺或酰胺,这些基团均可以被以下基团所取代:一个或多个卤素、cn、nr1r2、cf3、or1、芳基、杂环、s(o)r1、so2r1、-co2h、-so3h、-or1、-co2r1、-conr1、-po2r1r2、-po3h或p(o)r1r2r3;k是nr1、-ss-、-c(=o)-、-c(=o)nh-、-c(=o)o-、-c=nh-o-、-c=n-nh-、-c(=o)nh-nh-、o、s、se、b、het(c3-c8杂环或杂芳环),或含有1-20个相同或不同氨基酸的肽。 或者r1、r2、r3和r4独立地为具有1-18个碳原子的直链烷基,或具有式(och2ch2)p的聚乙烯氧基单,p=1~5000,或含有1~20个氨基酸单(l或d形式)的肽,或上述组合。 此外,y1、y2、r1、r2、r3、r4、z1或z2可独立地由以下一个或多个组分构成: 6-马来酰亚胺己酰胺基(mc)、马来酰亚胺基丙酰胺基(mp)、硫代马来酰胺基、硫代氨基氧代丁酸、硫代氨基氧代丁烯酸、缬氨酸瓜氨酸(val-cit)、丙氨酸苯丙氨酸(ala-phe)、赖氨酸苯丙氨酸(lys-phe)、赖氨酸丙氨酸(lys-ala),p-对氨基苄氧羰基(pab)、4-硫代戊酰基(spp)、4-硫代丁酰基(spdb),4-(n-马来酰亚胺甲基)环已烷基-1-酰基(mcc)、马来酰亚胺乙胺基(me)、4-硫代-2-羟基磺酰基丁酰基(2-磺酰-spdb)、芳基硫基(pys),(4-乙酰基)氨基苯甲酰基(siab)、氧基苄基硫基、氨基苄基硫基、二氧基苄硫基、二氨基苄硫基、氨基氧基苄硫基、烷氧基氨基(aoa)、亚乙基氧基(eo)、4-甲基-4-二硫代戊酰基(mpdp)三唑、二硫代、烷基磺酰基、烷基磺酰胺基、磺胺双酰胺基、磷酸二酰胺基、烷基膦酰胺酸基、次膦酸基、n-甲基烷基膦酰胺酸基、n,n’-二甲基膦酰胺酸基、烷基二膦酰胺基,肼、乙酰亚胺;肟、乙酰乙酰肼、氨基乙胺、氨基乙基-氨基乙基胺,和l-或d-,或含有1-20个氨基酸的天然或非天然肽;其中原子中间的连接键意味着它可以连接相邻的碳原子键;其中波浪线指另外键连接的位点; 或者,y1、y2、r1、r2、r3、r4、z1或z2可以独立地缺省,但是y1、y2、r1、r2、r3、r4、z1和z2不可以同时缺省。 2.如权利要求1中所述的偶联物,其特征在于具有式(i-01)、(i-02)、(i-03)、(i-04)、(i-05)、(i-06)、(i-07)、(i-08)、(i-09)、(i-10)、(i-11)、(i-12)、(i-13)、(i-14)、(i-15)、(i-16)、(i-17)、(i-18)、(i-19)、(i-20)、(i-21)、(i-22)、(i-23)、(ii-01)、(ii-02)、(ii-03)、(ii-04)、(ii-05)、(ii-06)、(ii-07)、(ii-08)、(ii-09)、(ii-10)、(ii-11)、(ii-12)、(ii-13)、(ii-14)、(ii-15)、(ii-16)、(ii-17)、(ii-18)、(iii-01)、(iii-02)、(iii-03)、(iii-04)、(iii-05)、(iii-06)、(iii-07)、(iii-08)、(iii-09)、(iii-10)、(iii-11)、(iii-12)、(iii-13)、(iii-14)、(iii-15)、(iii-16)、(iii-17)、(iii-18)、(iii-19)、(iii-20)、(iv-01)、(iv-02)、(iv-03)、(iv-04)、(iv-05)、(iv-06)、(iv-07)、(iv-08)、(iv-09)、(iv-10)、(iv-11)、(iv-12)、(iv-13)、(iv-14)、(iv-15)、(iv-16)、(iv-17)、(iv-18)、(iv-19)和(iv-20)的结构: 其中:drug1、drug2、n、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、drug1和drug2如前文所定义;此外,drug1和drug2其中之一独立地,可以缺省,但是不能同时缺省。 3.如权利要求2中所述的偶联物,由式(va)、(vb)、(vc)、(via)、(vib)、(vic)、(viia)、(viib)、(viic)、(viiia)、(viiib)和(viiic)所示的具有有高反应活性的立体异构体制备,其特征在于细胞毒性分子的两个或多个官能团可以同时或依次与化合物的lv1和/或lv2反应: 其中: 任选地是单键或双键或三键,或者可以缺省;当代表三键时,lv1和lv2同时缺省; drug1、drug2、n、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1和z2的定义与权利要求1中定义相同; lv1和lv2为相同或不同的反应官能团,这些官能团可以与细胞结合分子上的硫基、胺、羧酸、硒醇、酚或羟基发生反应。lv1和lv2独立地选自羟基(oh)、氟(f)、氯(cl)、溴(br)、碘(i)、硝基苯氧基、n-羟基琥珀酰亚胺(nhs)基、苯氧基、二硝基苯氧基、五氟苯氧基、四氟苯氧基、三氟苯氧基、二氟苯氧基、一氟苯氧基、五氯苯氧基、三氟甲磺酰基、咪唑基、二氯苯氧基、三氯苯氧基、四氯苯氧基、1-羟基苯并三唑基、甲苯磺酰基、甲磺酰基、2-乙基-5-苯基异恶唑-3’-磺酰基、酸酐或与其它酸酐作用形成的酸酐,例如乙酸酐、甲酸酐,或与多肽缩合试剂、mitsunobu反应试剂作用生成的中间体。缩合剂选自:1-乙基-(3-二甲基氨基丙基)碳二亚胺(edc)、二环己基碳二亚胺(dcc)、n,n’-二异丙基碳二亚胺(dic)、n-环己基-n’-(2-吗啉代-乙基)碳二亚胺甲基对甲苯磺酸盐(cmc或cme-cdi)、1,1′-羰基二咪唑(cdi)、氧-(苯并三唑-1-)基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tbtu)、n,n,n’,n’-四甲基-氧-(1h-苯并三唑-1-基)-六氟磷酸铵(hbtu)、(苯并三唑-1-基氧基)三(二甲基氨基)-六氟磷酸盐(bop)、(苯并三唑-1-基氧基)三吡咯烷基六氟磷酸盐(pybop)、氰基膦酸二乙酯(depc)、氯-n,n,n’,n’-四甲基甲脒六氟磷酸盐、1-[双(二甲基氨基)亚甲基]-1h-1,2,3-三唑并[4,5-b]吡啶3-氧六氟磷酸盐(hatu)、1-[(二甲氨基)(吗啉代)亚甲基]-1h-[1,2,3]三唑并[4,5-b]吡啶-1-鎓3-氧六氟磷酸盐(hdma)、2-氯-1,3-二甲基-咪唑六氟磷酸盐(cip)、六氟磷酸氯代吡咯烷酮鎓(pyclop)、氟-n,n,n’,n’-双(四亚甲基)甲脒六氟磷酸盐(btffh)、n,n,n’,n’-四甲基-s-(1-氧代-2-吡啶基)硫脲六氟磷酸盐、氧-(2-氧代-1(2h)吡啶基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tptu)、s-(1-氧代-2-吡啶基)n,n,n’,n’-四甲基硫脲四氟硼酸盐、氧-[(乙氧基羰基)-氰基甲基氨基]-n,n,n’,n’-六氟磷酸四甲基脲(hotu)、(1-氰基-2-乙氧基-2-氧代乙基氨基氧基)二甲氨基-吗啉代-六氟磷酸盐(comu)、氧-(苯并三唑-1-基)-n,n,n’,n’-双(四亚甲基)六氟磷酸盐(hbpyu)、n-芐基-n’-环己基-碳二亚胺(有或没有聚合物结合)、二吡咯烷基(n-琥珀酰亚胺基氧基)碳鎓六氟磷酸盐(hspyu)、氯二吡咯烷基六氟磷酸盐(pyclu)、2-氯-1,3-二甲基咪唑四氟硼酸盐(cib)、(苯并三唑-1-基氧基)二呱啶碳六氟磷酸盐(hbpipu)、氧-(6-氯苯并三唑-1-基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tctu)、溴代(二甲基氨基)-六氟磷酸盐(brop)、丙基膦酸酐(ppaca、)、2-吗啉代乙基异氰化物(mei)、n,n,n’,n’-四甲基-氧-(n-琥珀酰亚胺基)六氟磷酸盐(hstu)、2-溴-1-乙基-吡啶鎓四氟硼酸盐(bep)、氧-[(乙氧基羰基)氰基-亚甲基氨基]-n,n,n’,n’-四甲基脲四氟硼酸盐(totu)、4-(4,6-二甲氧基-1,3,5-三嗪-2-基)-4-甲基吗啉氯化物(mmtm、dmtmm)、n,n,n’,n’-四甲基-氧-(n-琥珀酰亚胺基)脲四氟硼酸(tstu)、o-(3,4-二氢-4-氧代-1,2,3-苯并三嗪-3-基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tdbtu)、1,1′-(偶氮二羰基)-二呱啶(add)、二-(4-氯芐基)偶氮二羧酸酯(dcad)、偶氮二羧酸二叔丁酯(dbad)、偶氮二羧酸二异丙酯(diad)、偶氮二羧酸二乙酯(dead)。另外,lv1和lv2可以是酸酐,或与其它c1-c8酸酐作用形成的酸酐; 或lv1和lv2独立地选自卤化物(氟化物、氯化物、溴化物和碘化物)、甲磺酰基(甲磺酰基)、甲苯磺酰基(甲苯磺酰基)、三氟甲基磺酰基(三氟甲磺酸酯)、三氟甲基磺酸酯、硝基苯氧基、n-琥珀酰亚胺基氧基(nhs)、苯氧基;二硝基苯氧基;五氟苯氧基、四氟苯氧基、三氟苯氧基、二氟苯氧基、单氟苯氧基、五氯苯氧基、1h-咪唑-1-基、氯苯氧基、二氯苯氧基、三氯苯氧基、四氯苯氧基、n-(苯并三唑基)氧基、2-乙基-5-苯基异恶唑-3′-磺酰基、苯基恶二唑磺酰基(-砜-oda)、2-乙基-5-苯基异恶唑鎓-基、苯基恶二唑基(oda)、恶二唑基、不饱和碳(碳-碳、碳-氮、碳-硫、碳-磷、硫-氮、磷-氮、氧-氮或碳-氧之间的双键或三键)、或以下结构之一:二硫化物;卤代乙酰基;酰卤化物;n-羟基丁二酰亚胺酯基;马来酰亚胺基;单取代马来酰亚胺基;单取代丁二酰亚胺基;二取代丁二酰亚胺基;二取代丁二酰亚胺基;-cho醛基;乙烯磺酰基;丙烯酰基;2-(对甲氧基)乙酰基;2-(甲氧基)乙酰基;2-(硝基苯氧基)乙酰基;2-(二硝基苯酚氧基)乙酰基;2-(氟苯氧基)-乙酰基;2-(二氟苯氧基)-乙酰基;2-((三氟甲基)-磺酰氧基)乙酰基;酮或醛基;2-(五氟苯氧基)乙酰基;甲基砜麻黄二唑基(oda);酸酐、烷氧基氨基;叠氮基、炔基、或酰肼,其中x1’为f,cl,br,i或lv3;x2’是o,nh,n(r1)或ch2;r3独立地为h,芳基,杂芳基或芳香基团,其中一个或几个氢原子独立地被-r1,-卤素,-or1,-sr1,-nr1r2,-no2,-s(o)r1,-s(o)2r1或-coor1取代;lv3是离去基团,选自f、cl、br、i;硝基苯氧基;n-羟基琥珀酰亚胺基(nhs);苯氧基;二硝基苯氧基;五氟苯氧基;四氟苯氧基;二氟苯氧基;单氟苯氧基;五氯苯氧基;三氟甲磺酰基;咪唑基;二氯酚基;四氯苯氧基;1-羟基苯并三唑基;甲苯甲磺酰基;甲磺酰基;2-乙基-5-苯基异恶唑-3′-磺酰基,r1和r2如前文所定义。 4.如权利要求3所述的偶联物,其特征在于具有式(v-01)、(v-02)、(v-03)、(v-04)、(v-05)、(v-06)、(v-07)、(v-08)、(v-09)、(v-10)、(v-11)、(v-12)、(v-13)、(v-14)、(v-15)、(v-16)、(v-17)、(v-18)、(v-19)、(v-20)、(v-21)、(v-22)、(v-23)、(vi-01)、(vi-02)、(vi-03)、(vi-04)、(vi-05)、(vi-06)、(vi-07)、(vi-08)、(vi-09)、(vi-10)、(vi-11)、(vi-12)、(vi-13)、(vi-14)、(vi-15)、(vi-16)、(vi-17)、(vi-18)、(vii-01)、(vii-02)、(vii-03)、(vii-04)、(vii-05)、(vii-06)、(vii-07)、(vii-08)、(vii-09)、(vii-10)、(vii-11)、(vii-12)、(vii-13)、(vii-14)、(vii-15)、(vii-16)、(vii-17)、(vii-18)、(vii-19)、(vii-20)、(viii-01)、(viii-02)、(viii-03)、(viii-04)、(viii-05)、(viii-06)、(viii-07)、(viii-08)、(viii-09)、(viii-10)、(viii-11)、(viii-12)、(viii-13)、(viii-14)、(viii-15)、(viii-16)、(viii-17)、(viii-18)、(viii-19)、和(viii-20)所示的结构: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、drug1和drug2如前文所定义;x1和x1’独立地为h、f、cl、br、i、ots、oms、otf、n3、cho、-c=ch、-c≡c-、arc(=o)r1、c(=o)nhnh2、-o-nh2、硝基苯氧基、n-羟基琥珀酰亚胺(nhs)、苯氧基、二硝基苯氧基、五氟苯氧基、四氟苯氧基、二氟苯氧基、单氟苯氧基、五氯苯氧基、三氟甲磺酰基、咪唑基、二氯酚基、四氯苯氧基、1-羟基苯并三唑基、甲苯甲磺酰基、甲磺酰基,2-乙基-5-苯基异恶唑-3′-,酸酐或与其它酸酐作用形成的酸酐、例如乙酸酐、甲酸酐,o-nhs(on-氢琥珀酰亚胺)、o-咪唑、o-三唑、o-四唑、o-ar、o-arno2、o-ar(no2)2、o-arf4、o-arf3、o-arf5、o-arf2、o-arf、o-arcl4、o-arcl3、o-arcl5、o-arcl2、o-arcl、o-arso3h、o-aropo3h2、o-ar(no2)cooh、s-ar(no2)2cooh、o-吡啶、o-硝基苯氧基、o-二硝基苯氧基、o-五氟苯氧基、o-四氟苯氧基、o-三氟苯氧基、o-二氟苯氧基、o-氟苯氧基、o-五氯苯氧基、o-四氯苯氧基、o-三氯苯氧基、o-二氯苯氧基、o-氯苯氧基、o-吡啶、o-硝基吡啶、o-二硝基吡啶、o-c1-c8烷基、o-三氟甲磺酸盐、o-苯并三唑、s-ar、s-arno2、s-ar(no2)2、s-arf4、s-arf3、s-arf5、s-arf2、s-arf、s-arcl4、s-arcl3、s-arcl5、s-arcl2、s-arcl、s-arso3h、s-aropo3h2、s-ar(no2)cooh、s-ar(no2)2cooh、s-吡啶、ss-吡啶、s-硝基吡啶、s-二硝基吡啶、s-c1-c8烷基、ss-c1-c8烷基、s-三氟甲磺酸酯、s-苯并三唑、其中ar是c3-c8芳环;或与多肽缩合试剂生成的,或与mitsunobu反应偶联试剂生成的中间体分子。 5.如权利要求1所述的偶联物,由式(ix-01)、(ix-02)、(ix-03)、(ix-04)、(ix-05)、(ix-06)、(ix-07)、(ix-08)、(ix-09)、(ix-10)、(ix-11)、(ix-12)、(ix-13)、(ix-14)、(ix-15)、(ix-16)、(ix-17)、(ix-18)、(ix-19)、(ix-20)、(ix-21)、(ix-22)、(ix-23)、(x-01)、(x-02)、(x-03)、(x-04)、(x-05)、(x-06)、(x-07)、(x-08)、(x-09)、(x-10)、(x-11)、(x-12)、(x-13)、(x-14)、(x-15)、(x-16)、(x-17)、(x-18)、(x-19)、和(x-20)所示的高反应活性的化合物制得,其特征在于其特征在于细胞毒性分子的两个或多个官能团可以同时或依次与化合物的lv1和/或lv2反应: 其中:q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、lv1、lv2、lv1’、和lv2’如前文所定义;此外,drug1和drug2其中之一独立地,可以缺省,但是不能同时缺省。 6.如权利要求1所述的偶联物,由式(xi-01)、(xi-02)、(xi-03)、(xi-04)、(xi-05)、(xi-06)、(xi-07)、(xi-08)、(xi-09)、(xi-10)、(xi-11)、(xi-12)、(xi-13)、(xi-14)、(xi-15)、(xi-16)、(xi-17)、(xi-18)、(xii-01)、(xii-02)、(xii-03)、(xii-04)、(xii-05)、(xii-06)、(xii-07)、(xii-08)、(xii-09)、(xii-10)、(xii-11)、(xii-12)、(xii-13)、(xii-14)、(xii-15)、(xii-16)、(xii-17)、(xii-18)、(xii-19)、(xii-20)、(xii-21)、(xii-22)、(xii-23)和(xii-24)所示的高反应活性的化合物制得,其特征在于细胞毒性分子和细胞连接分子可以独立地,同时或依次与化合物反应: 其中q,x1,x2,y1,y2,r1,r2,r3,r4,r5,r5’,z1,z2,lv1,lv2,lv1’,lv2’,x1和x1’的定义同前文。 7.如权利要求1所述的偶联物,其中y1,y2,z1和z2与细胞结合剂/分子中一对巯基连接,将细胞结合剂的链间二硫键还原为巯基对的还原剂选自:二硫苏糖醇(dtt)、二硫赤藓糖醇(dte)、l-谷胱甘肽(gsh)、三(2-羧乙基)膦(tcep)、2-巯基乙胺(β-mea)或/和β-巯基乙醇(β-me、2-me)。 8.如权利要求1所述的偶联物,其中drug1或drug2选自: (1).化疗剂,选自于:a)烷基化剂,选自氮芥:氯苯那普,氯普那嗪,环磷酰胺,达喀尔巴嗪,雌二醇氮芥,异环磷酰胺,氮芥,盐酸二甲氧胺,氧化二氮芥,盐酸氨氯地平,麦考酚酸,卫矛醇,呱泊溴烷,新氮芥,苯芥胆甾醇,松龙苯芥,噻替呱,曲磷胺对,尿嘧啶;cc-1065和阿多来新、卡折来新、比折来新或其合成类似物;多卡霉素及其合成类似物,kw-2189或cbi-tmi、;苯并二氮二聚体或吡咯并苯二氮(pbd)二聚体,托美霉素二聚体,吲哚并苯并二氮杂二聚体,咪唑并苯并噻二氮杂二聚体,或恶唑烷并苯并二氮杂的二聚体;亚硝基脲:包括卡莫司汀,洛莫司汀,氯化梭菌素,福莫司汀,尼莫司汀,拉莫司汀;烷基磺酸盐:包括白苏芬、树苏芬、磺胺异丙磺胺和皮苏芬;三氮烯或达喀尔巴嗪;含铂化合物:包括卡铂,顺铂,奥沙利铂;吖丙啶类,苯并二氢吡喃酮,卡洛酮,美妥替派和乌雷多巴;乙烯亚胺和甲基三聚氰胺,包括六甲蜜胺,三亚乙基三胺,三乙基磷酰胺,三亚乙基硫代磷酰胺和三羟甲基甲基胺; b).植物生物碱:选自长春花生物碱,包括长春新碱,长春碱,长春地辛,长春瑞滨,去甲长春碱;紫杉醇类:包括紫杉醇,多西紫杉醇及其类似物;美登素类包括dm1、dm2、dm3、dm4、dm5、dm6、dm7、美登素、安沙霉素及其类似物);cryptophycin(包括cryptophycin1和cryptophycin8);埃博霉素,软珊瑚醇,迪莫利德,草苔虫内酯,海兔毒素,澳瑞斯汀,tubulysins,cephalostatin;pancratistatin;erbulins;sarcodictyin;海绵抑制素; c)dna拓扑异构酶抑制剂:选自依托泊苷替尼,包括9-氨基喜树碱、喜树碱、克立那托、多拉霉素、依托泊苷、磷酸依托泊苷、伊立替康、米托蒽醌、诺消灵、视黄酸(视黄醇)、替尼泊苷、拓扑替康、9-硝基喜树碱或rfs2000、丝裂霉素及其类似物; d)抗代谢物:选自抗叶酸剂(dhfr抑制剂,包括甲氨蝶呤、曲麦克特、二甲叶酸、蝶罗呤、氨喋呤(4-氨基苯甲酸)或其他叶酸类似物);imp脱氢酶抑制剂(包括麦考酚酸、噻唑呋林、利巴韦林、eicar);核糖核苷酸还原酶抑制剂(包括羟基脲、去铁胺);嘧啶类似物:尿嘧啶类似物(包括安西他滨、阿扎胞苷、6-氮尿嘧啶、卡培他滨(希罗达)、卡莫氟、阿糖胞苷、双脱氧尿苷、脱氧氟尿苷、依诺他滨、5-氟尿嘧啶、氟尿苷、ratitrexed(tomudex))和胞嘧啶类似物(包括阿糖胞苷,胞嘧啶阿拉伯糖苷,氟达拉滨);嘌呤类似物(包括硫唑嘌呤,氟达拉滨,巯嘌呤,硫胺素,硫鸟嘌呤);叶酸补充剂,弗洛林酸;和烟酰胺磷酸核糖基转移酶(nampt)的抑制剂; e)激素疗法剂:选自受体拮抗剂:抗雌激素(包括甲地孕酮,雷洛昔芬,他莫昔芬),lhrh兴奋剂(包括戈斯他林,醋酸亮丙瑞林);抗雄激素药(包括比卡鲁胺,氟他胺,卡鲁司酮,丙酸倍他雄酮,表雄甾醇,戈舍瑞林,亮丙瑞林,美替利定,尼鲁米特,睾内酯,曲洛司坦及其他雄激素抑制剂);维甲类化合物:维生素d3类似物(包括cb1093,eb1089,kh1060,胆钙化醇,麦角钙化甾醇);光动力疗法剂(包括维替泊芬,酞菁,光敏剂pc4,去甲氧基-竹红菌素a);细胞因子(干扰素-α,干扰素-γ,肿瘤坏死因子(tnf),含tnf的人蛋白); f)激酶抑制剂,选自bibw2992(抗-egfr/erb2),伊马替尼,吉非替尼,呱加他尼,索拉非尼,达沙替尼,舒尼替尼,厄洛替尼,尼洛替尼,拉帕替尼,阿西替尼,帕唑帕尼,凡德他尼,e7080(抗vegfr2),mubritinib,普纳替尼(ap24534),bafetinib(inno-406),bosutinib(ski-606),卡博替尼,维莫德吉,iniparib,鲁索利替尼,cyt387,阿西替尼,tivozanib,索拉非尼,贝伐单抗,西妥昔单抗,曲妥珠单抗,雷珠单抗,帕尼单抗,伊斯平斯; g)聚(adp-核糖)聚合酶(parp)抑制剂,选自奥拉帕里、尼拉帕里、依尼帕里、塔拉佐帕里、维利帕里、维利帕里、cep9722(cephalon)、e7016(eisai)、bgb-290(beigene)、3-氨基苯甲酰酰胺; h)抗生素:选自烯二炔类抗生素(选自加利车霉素、加利车霉素γ1、δ1、α1和β1,达因霉素,包括达因霉素a和脱氧米霉素,埃斯培拉霉素,卡塔尔霉素,c-1027,maduropeptin,或新卡嗪奥斯汀和相关色蛋白烯二炔抗生素),aclacinomysins,放线菌素,安曲霉素,重氮丝氨酸,博来霉素,卡诺霉素,卡拉霉素,洋红霉素,嗜癌素,色霉素,达金霉素,柔红霉素,去柔红霉素,6-重氮-5-氧代-l-去甲亮氨酸,阿霉素,吗啉-阿霉素,氰基吗啉-阿霉素,2-吡咯啉阿霉素和脱氧柔红霉素,表柔比星,阿柔比星,伊达比星,马可霉素,nitomycin,霉酚酸,诺加霉素,橄榄霉素,peplomycin,potfiromycin,嘌呤霉素,奎拉霉素,罗道霉素,链黑霉素,链脲霉素,杀结核菌素,乌苯美司,净司他丁,佐柔比星; i)聚酮化合物(番荔素),bullatacin和bullatacinone;吉西他滨,环氧酶素和卡菲偌米布,硼替佐米,沙利度胺,来那度胺,pomalidomide,tosedostat,zybrestat,plx4032,sta-9090,stimuvax,allovectin-7,xegeva,provenge,yervoy,异戊二烯化抑制剂和洛伐他汀,多巴胺能神经毒素(选自星形孢菌素),放线菌素(包含放线菌素d,更生霉素),鹅膏毒素,博莱霉素(包括博来霉素a2,博莱霉素b2,培洛霉素),蒽环类抗生素,包括柔红霉素,阿霉素(亚德里亚霉素),伊达比星,表柔比星,佐柔比星,米托蒽醌,mdr抑制剂(或维拉帕米),ca2+atp酶抑制剂(或毒胡萝卜素),组蛋白去乙酰酶抑制剂(伏立诺他,罗米地辛,帕比司他,丙戊酸,mocetinostat(mgcd0103),belinostat,pci-24781,恩替诺特,sb939,resminostat,givinostat,ar-42,cudc-101,萝卜硫素,曲古抑菌素a);塞来昔布,格列酮类,表没食子儿茶素没食子酸酯,双硫仑,salinosporamidea;抗肾上腺药物,选自:氨鲁米特,米托坦,曲洛司坦,醋葡醛内酯,醛磷酰胺,氨基乙酰丙酸,安吖啶,阿拉伯糖苷,bestrabucil,比生群,edatraxate,defofamine,美可辛,地吖醌,依氟鸟氨酸(dfmo),elfomithine,依利醋铵,依托格鲁,硝酸镓,胞嘧啶,羟基脲,伊班膦酸盐,香菇多糖,氯尼达明,米托胍腙,米托蒽醌,莫呱达醇,二胺硝吖啶,喷司他丁,蛋氨氮芥,吡柔比星,鬼臼酸,2-乙肼,甲基苄肼;呱嗪二酮丙烷;根霉素;西佐;螺环锗;细格孢氮杂酸;三亚胺醌;三氯三乙胺;单端孢霉烯(包括t-2毒素,疣孢菌素a,杆孢菌素a和anguidine),聚氨酯,sirna,反义药物; 2)自身免疫疾病药物:环孢菌素,环孢菌素a,氨基己酸,硫唑嘌呤,溴隐亭,苯丁酸氮芥,氯喹,环磷酰胺,皮质类固醇(包括安西奈德,倍他米松,布地奈德,氢化可的松,氟尼缩松,丙酸氟替卡松,氟可龙达那唑,地塞米松,曲安奈德,二丙酸倍氯米松),dhea,依那西普,羟基氯喹,英夫利昔单抗,美洛昔康,甲氨蝶呤,麦考酚酸酯,泼尼松,西罗莫司,他克莫司; 3)抗感染性疾病药物,包括: a)氨基糖苷类:阿米卡星,阿司米星,庆大霉素(奈替米星,西索米星,异帕米星),潮霉素b,卡那霉素(阿米卡星,阿贝卡星,氨基脱氧卡那霉素,地贝卡星,妥布霉素),新霉素(framycetin,巴龙霉素,核糖霉素),奈替米星,壮观霉素,链霉素,妥布霉素,甲基姿苏霉素; b)酰胺醇类:迭氮氯霉素,氯霉素,氟苯尼考,甲砜霉素; c)安沙霉素:格尔德霉素,除莠霉素; d)碳青霉烯类:比阿培南,多利培南,厄他培南,亚胺培南/西司他丁,美罗培南,帕尼培南; e)头孢烯:碳头孢烯(洛拉卡比),头孢乙腈,氯氨苄青霉素,头孢拉定,头孢羟氨,头孢洛宁,头孢噻啶,头孢噻吩或头孢金素,头孢氨苄,头孢来星,头孢孟多,头孢匹林,羟胺唑头孢菌素,氟唑头孢菌素,孢西酮,唑啉头孢菌素,头孢拉宗,头孢卡品,头孢达肟,头孢吡,头孢克肟,头孢西丁,头孢罗齐,头孢甲氧环烯胺,头孢替唑,头孢呋辛,头孢克肟,头孢地尼,头孢托仑,头孢吡,头孢他美,头孢甲肟,头孢地嗪,头孢尼西,头孢呱酮,头孢雷特,头孢噻肟,噻乙胺唑头孢菌素,头孢唑兰,头孢氨苄,头孢咪唑,头孢匹胺,头孢匹罗,头孢泊肟,头孢罗齐,头孢喹诺,头孢磺啶,头孢他啶,头孢特仑,头孢布腾,头孢噻林,头孢唑肟,头孢吡普,头孢曲松,头孢呋辛,头孢唑南,头霉素(头孢西丁,头孢替坦,头孢氰唑),氧(碳)头孢烯(氟氧头孢,拉氧头孢); f)糖肽:博来霉素,万古霉素(奥利万星,特拉万星),替考拉宁(达巴万星),雷莫拉宁; g)甘氨酰环素:如替加环素; h)β-内酰胺酶抑制剂:青霉烷(舒巴坦,他唑巴坦),氧青霉烷(克拉维酸); i)林可酰胺:克林霉素,林可霉素; j)脂肽:达托霉素,a54145,钙依赖性抗生素(cda); k)大环内酯类:阿奇霉素,克霉素,克拉霉素,地红霉素,红霉素,氟雷霉素,交沙霉素,酮内酯(泰利霉素,塞红霉素),麦迪霉素,米卡霉素,竹桃霉素,利福霉素(异烟肼、利福平,利福布丁,利福喷汀),罗匹霉素,罗红霉素,大观霉素,螺旋霉素,他克莫司(fk506),醋竹桃霉素,泰利霉素; l)单环胺:氨曲南,替吉莫南; m)恶唑烷酮类:利奈唑胺; n)青霉素类:阿莫西林,氨苄青霉素(匹氨西林,海洛西林,巴氨西林,氨苄青霉素,阿霉素),阿替代西林,阿洛西林,苄青霉素,苄星青霉素苄青霉素,苄星青霉素苯氧甲基青霉素,克洛西林,普鲁卡因青霉素(美替西林),美洛西林,甲氧西林,萘夫西林,苯唑西林,醋甲西林,青霉素,非奈西林,苯氧基甲基青霉素,呱拉西林,氨苄西林,磺苯西林,替莫西林,替卡西林; o)多肽:杆菌肽,粘菌素,多粘菌素b; p)喹诺酮类:阿拉曲沙星,巴洛沙星,环丙沙星,克林沙,达氟沙星,二氟沙星,依诺沙星,恩诺沙星,加雷沙星,加替沙星,吉米沙星,格帕沙星,卡诺曲伐沙星,左氧氟沙星,洛美沙星,麻保沙星,莫西沙星,那氟沙星,诺氟沙星,奥比沙星,氧氟沙星,培氟沙星,曲伐沙星,格帕沙星,西他沙星,司帕沙星,替马沙星,托沙星,曲伐沙星; q)链阳性菌素:普那霉素,奎奴普丁/达福普汀; r)磺胺类:氨芐磺胺,偶氮磺胺,磺胺嘧啶,磺胺甲异唑、磺胺酰亚胺、磺胺吡啶、磺胺异恶唑、甲氧苄啶、磺胺甲恶唑(复方磺胺甲恶唑); s)类固醇抗菌药物:如夫西地酸; t)四环素类:强力霉素,金霉素,氯米西环素,地美环素,雷莫昔林,美西环素,美他环素,米诺环素,土霉素,潘美环素,吡咯烷甲基四环素,四环素,甘氨酰环素(如替加环素); u)其他类型的抗生素:番荔枝素,胂凡纳明,细菌萜醇抑制剂(杆菌肽),danal/ar抑制剂(环丝氨酸),dictyostatin,圆皮海绵内酯,软珊瑚醇,埃博霉素,乙胺丁醇,依托泊苷,法罗培南,夫西地酸,呋喃唑酮,异烟肼,laulimalide,甲硝唑,莫匹罗星,nam合成抑制剂(例如磷霉素),呋喃妥因,紫杉醇,普兰西霉素,吡嗪酰胺,奎奴普丁/达福普汀,利福平,他唑巴坦替硝唑,乌菊花素; 4)抗病毒药物: a)侵入/融合抑制剂:阿帕韦洛,马拉韦罗,vicriviroc,gp41(恩夫韦肽),pro140,cd4(艾巴利珠单抗); b)整合酶抑制剂:雷特格韦,elvite-gravir,globoidnana; c)成熟抑制剂:bevirimat,vivecon; d)神经氨酸酶抑制剂:奥司他韦,扎那米韦,帕拉米韦; e)核苷和核苷酸:阿巴卡韦,阿昔单韦,阿德福韦,阿莫西韦,阿昔单抗,溴夫定,西多福韦,克拉夫定,地塞米松,去羟肌苷(ddi),elvucitabine,恩曲他滨(ftc),恩替卡韦,泛昔洛韦,氟拉西林(5-fu),3’-氟取代的2’,3’-脱氧核苷类似物,包括3’-氟-2’,3’-双脱氧胸苷(flt)和3’-氟-2’,3’-双脱氧鸟苷(flg),福米韦生,9-鸟嘌呤,碘苷,拉米夫定(3tc),1-核苷(包括β-1-胸苷和β-1-2′-脱氧胞苷),喷昔洛韦,racivir,利巴韦林,迪替丁,司他夫定(d4t),塔利巴韦林(viramidine),替比夫定,替诺福韦,三氟尿苷伐昔洛韦,缬更昔洛韦,扎西他滨(ddc),齐多夫定(azt); f)非核苷类:金刚烷胺,阿替吡啶,卡普韦林,二芳基嘧啶(依曲韦林,rilpivirine),地拉夫定,二十二烷醇,乙米韦林,依法韦仑,膦甲酸(磷酰基甲酸),咪喹莫特,聚乙二醇干扰素,洛韦胺,洛德腺苷,甲吲噻腙,奈韦拉平,nov-205,长效干扰素α,鬼臼毒素,利福平,金刚乙胺,瑞喹莫德(r-848),醋胺金刚烷; g)蛋白酶抑制剂:安普那韦,阿扎那韦,boceprevir,darunavir,福萨那韦,印地那韦,洛匹那韦,奈非那韦,普来可那立,利托那韦,沙奎那韦,telaprevir(vx-950),替拉那韦; h)其它类型的抗病毒药物:抗体酶,阿比朵尔,calanolidea,ceragenin,氰维林-n,二芳基嘧啶,表没食子儿茶素没食子酸酯(egcg),膦甲酸,格里菲辛,taribavirin(viramidine),羟基脲,kp-1461,米替福新,普来可那立,混成抑制剂,利巴韦林,seliciclib; (5).放射性同位素,可以选自(放射性核素)3h、11c、14c、18f、32p、35s、64cu、68ga、86y、99tc、111in、123i、124i、125i、131i、133xe、177lu、211at、或213bi。 (6).发色团分子,能够吸收紫外线、荧光、红外光、近红外光、可见光;黄色素、红细胞、虹彩色素、白细胞、黑色素和蓝绿色素的一类或一个亚类、荧光分子吸收光后再发光的荧光化学物质。视觉光转导分子、荧光团分子、发光分子、萤光素化合物。非蛋白质有机荧光团,选自:氧杂蒽衍生物(包括荧光素、罗丹明、俄勒冈绿、伊红和德克萨斯红);花青衍生物(包括花青、吲哚羰花青、氧杂花青、硫代花青和部花青);方酸衍生物和环取代的方酸、包括seta、setau和square染料;萘衍生物(包括丹酰和氟硅酸钠衍生物);香豆素衍生物;恶二唑衍生物(包括吡啶基恶唑、硝基苯并恶唑和苯并恶二唑);蒽衍生物(包括蒽醌类、包括draq5、 draq7和cytrak橙);芘衍生物(包括级联蓝等);恶嗪衍生物(包括尼罗红、尼罗蓝、甲酚紫、恶嗪170等);吖啶衍生物(包括黄醇黄素、吖啶橙、吖啶黄等);芳基甲胺衍生物(包括金胺、结晶紫、孔雀石绿)和四吡咯衍生物(卟吩、酞菁、胆红素)。生色分子选自以下荧光化合物的任何类似物和衍生物:cf染料、draq和cytrak探针、bodipy、alexafluor、dylightfluor、atto和tracy、fluoprobes、abberiordyes、dy和megastokesdyes、sulfocy染料、hilytefluor、seta、setau和squaredyes、quasar和calfluordyes、surelightdyes(apc、rpepercp、phycobilisomes)、apc、apcxl、rpe、bpe、别藻蓝蛋白(apc)、氨基胭脂蛋白、apc-cy7偶联物、bodipy-fl、cascadeblue、cy2、cy3、cy3.5、cy3b、cy5、cy5.5、cy7、f荧光素、fluorx、羟基香豆素、丽丝胺罗丹明b、萤光黄、me-甲氧基香豆素、nbd、pacificblue、pacificorange、pe-cy5偶联物、pe-cy7偶联物、percp、r-藻红蛋白(pe)、red613、seta-555-叠氮化物、seta-555-dbco、seta-555-nhs、seta-580-nhs、seta-680-nhs、seta-780-nhs、seta-apc-780、seta-percp-680、seta-r-pe-670、setau-380-nhs、setau-405-马来酰亚胺、setau-405-nhs、setau-425-nhs、setau-647-nhs、texasred、tritc、trured、x-rhodamine、7-aad(7-氨基放线菌素d、cg-选择性的)、吖啶橙、色霉素a3、cytrak橙(redexcitationdark)、dapi、draq5、draq7、溴化乙锭、hoechst33258、hoechst33342、lds751、光辉霉素、碘化丙啶(pi)、sytox蓝、sytox绿、sytox橙、噻唑橙、to-pro:菁染料单体、toto-1、to-pro-1、toto-3、to-pro-3、yoseta-1、yoyo-1;荧光化合物:包括dcfh(2’、7′-二氯二氢荧光素、氧化形式)、dhr(二氢罗丹明123、氧化形式、光催化氧化)、fluo-3(am酯,ph>6)、fluo-4(am酯,ph7.2)、indo-1(am酯,低/高钙(ca2+))、snarf(ph6/9)、别藻蓝蛋白(apc)、amcyan1(四聚体、clontech)、asred2(四聚体、clontech)、azamigreen(单体)、azurite、b-藻红蛋白(bpe)、cerulean、cypet、dsred单体(clontech)、dsred2(“rfp”)、ebfp、ebfp2、ecfp、egfp(弱二聚体)、emerald(弱二聚体)、eyfp(弱二聚体)、gfp(s65a突变)、gfp(s65c突变)、gfp(s65l突变)、gfp(s65t突变)、gfp(y66f突变)、gfp(y66h突变)、gfp(y66w突变)、gfpuv、hcred1、j-red、katusha、kusabiraorange(单体、mbl)、mcfp、mcherry、mcitrine、midoriishicyan(二聚体、mbl)、mkate(tagfp635、单体)、mkeima-red(单体)、mko、morange、mplum、mraspberry、mrfp1(单体)、mstrawberry、mtfp1、mturquoise2、p3(藻胆体复合物)、多甲藻黄素-叶绿素-蛋白质复合物(percp)、r-phycoerythrin(rpe)、t-sapphire、tagcfp(二聚体)、taggfp(二聚体)、tagrfp(二聚体)、tagyfp(二聚体)、tdtomato(tandem二聚体)、topaz、turbofp602(二聚体)、turbofp635(二聚体)、turbogfp(二聚体)、turborfp(二聚体)、turboyfp(二聚体)、venus、wildtypegfp、ypet、zsgreen1(四聚体)、zsyellow1(四聚体)及其衍生物。 (7).细胞结合配体或受体激动剂,可以选自:叶酸衍生物、谷氨酸尿素衍生物、生长抑素及其类似物(选自奥曲肽(sandostatin)和兰瑞肽(somatuline))、芳香磺酰胺、aromaticsulfonamides、垂体腺苷酸环化酶激活肽(pacap)(pac1)、血管活性肠肽(vip/pacap)(vpac1,vpac2)、α-黑素细胞刺激激素(α-msh)、胆囊收缩素(cck)/胃泌素受体激动剂、蛙皮素(选自pyr-gln-arg-leu-gly-asn-gln-trp-ala-val-gly-his-leu-met-nh2)/胃泌素释放肽(grp)、神经降压素受体及其受体亚型(ntr1,ntr2,ntr3)、物质p(nk1受体)配体、神经肽y(y1–y6)、归巢肽包括rgd(arg-gly-asp),ngr(asn-gly-arg),二聚和多聚环状rgd肽(选自crgdfv),taasgvrsmh和ltlrwvglms(硫酸软骨素蛋白多糖ng2受体)和f3肽、细胞穿透肽(cpps)、肽激素,选自促黄体激素释放激素(lhrh)激动剂和拮抗剂,和促性腺激素释放激素(gnrh)激动剂,通过靶向卵泡刺激素(fsh)和黄体生成素(lh)起作用,以及睾酮产物,选自布舍瑞林(pyr-his-trp-ser-tyr-d-ser(otbu)-leu-arg-pro-nhet)、戈那瑞林(pyr-his-trp-ser-tyr-gly-leu-arg-pro-gly-nh2)、戈舍瑞林(pyr-his-trp-ser-tyr-d-ser(otbu)-leu-arg-pro-azgly-nh2)、组氨瑞林(pyr-his-trp-ser-tyr-d-his(n-苯基)-leu-arg-pro-nhet)、醋酸亮丙瑞林(pyr-his-trp-ser-tyr-d-leu-leu-arg-pro-nhet)、那法瑞林(pyr-his-trp-ser-tyr-2nal-leu-arg-pro-gly-nh2)、曲普瑞林(pyr-his-trp-ser-tyr-d-trp-leu-arg-pro-gly-nh2)、德舍瑞林、阿巴瑞克(ac-d-2nal-d-4-氯-d-3-(3-吡啶基)ala-ser-(n-me)tyr-d-asn-leu-异丙基-lys-pro-d-ala-nh2)、西曲瑞克(ac-d-2nal-d-4-chloro-phe-d-3-(3-pyridyl)ala-ser-tyr-d-cit-leu-arg-pro-d-ala-nh2)、地加瑞克(ac-d-2nal-d-4-chlorophe-d-3-(3-吡啶基)ala-ser-4-氨基phe(l-hydroorotyl)-d-4-氨基phe(氨基甲酰基)-leu-异丙基lys-pro-d-ala-nh2)和加尼瑞克(ac-d-2nal-d-4-chlorophe-d-3-(3-吡啶基)ala-ser-tyr-d-(n9,n10-二乙基)-homoarg-leu-(n9,n10-二乙基)-homoarg-pro-d-ala-nh2),模式识别受体(prrs),选自toll受体(tlrs)、c型凝集素和nodlike受体(nlrs)、降钙素受体激动剂、整合素受体及其受体亚型(选自αvβ1、αvβ3、αvβ5、αvβ6、α6β4、α7β1、αlβ2、αiibβ3)激动剂(选自grgdspk,环(rgdfv)(l1)及其衍生物[环(-n(me)r-gdfv)、环(r-sar-dfv)、环(rg-n(me)d-fv)、环(rgd-n(me)f-v)、环(rgdf-n(me)v-)(cilengitide)]、纳米抗体(vhh的衍生物(骆驼ig))、域抗体(dab、vh或vl域的衍生物)、双特异性t细胞engager(bite、双特异性双抗体)、双亲和重新定位(dart,双特异性双抗体)、四价串联抗体(tandab,二聚双特异双抗体)、anticalin(lipocalins的衍生物)、adnectins(10thfn3(fibronectin))、设计的锚蛋白重复蛋白(darpins)、avimers、egf受体和vegf受体激动剂。(8).药学上可接受的盐,酸或其衍生物,水合物或水合盐、或晶体结构、或任何上述药物的旋光异构体,外消旋物,非对映异构体或对映异构体。 9.如权利要求1所述的偶联物,其中drug1或drug2是发色团分子,用于检测,监测或研究细胞结合分子的相互作用和/或功能,和/或偶联物与靶细胞的相互作用。 10.如权利要求1所述的偶联物,其中drug1或drug2是聚亚烷基二醇[包含聚(乙二醇),聚(丙二醇),环氧乙烷或环氧丙烷的共聚物或其类似物],用于延长细胞结合分子在哺乳动物中的半衰期。 11.如权利要求1所述的偶联物,其中drug1或drug2是细胞结合配体,细胞受体激动剂或细胞受体结合分子,用作靶向导体/导向器以将偶联物递送至恶性细胞,或用于调节或共刺激期望的免疫应答或改变信号传导途径。 12.如权利要求1或2中任一项所述的偶联物,其中drug1或drug2选自tu-bulysin、美登素、紫杉烷类、cc-1065类似物、柔红霉素和多柔比星化合物、毒伞肽(包括鹅膏毒素)、indolecarboxamide、苯并二氮卓二聚体(例如吡咯并苯二氮杂卓(pbd)、托美霉素、氨茴霉素、吲哚并苯并二氮、咪唑并苯并噻二氮杂卓或恶唑烷并苯并二氮杂卓的二聚体)、加利车霉素类和烯二炔类抗生素、放线菌素、氮丝菌素、博来霉素、表柔比星、他莫昔芬、伊达比星、多拉司汀、澳瑞斯汀(例如mmae、mmaf、澳瑞斯汀pye、澳瑞斯汀tp、澳瑞斯汀2-aq、6-aq、eb(aeb)、efp(aefp)和它们的同系物)、多卡霉素、甲氨蝶呤,thiotepa,长春碱,长春新碱,hemasterins,nazumamides,microginins,radiumumins,altobactins,microsclerodermins,theonellamides,esperamicins,艾日布林,烟酰胺磷酸核糖基转移酶(nampt),rna,sirna,sirna抑制因子及其类似物和衍生物、药学上可接受的盐、酸、衍生物、水合物或水合盐、或晶体结构;或任何上述药物的旋光异构体、外消旋物、非对映异构体或对映异构体。 13.如权利要求1、2、8、9、10、11、或12中所述的偶联物,其中细胞结合剂/分子选自抗体、蛋白质、抗体、纳米抗体、维生素(包括叶酸)、肽、高分子胶束、脂质体、脂蛋白基药物载体、纳米颗粒药物载体、树枝状聚合物,以及涂附在细胞结合配体上的上述分子或颗粒,或上述物质的组合。 14.如权利要求1、2、8、9、10、11、12或13中任一项所述的偶联物,其中细胞结合剂/分子选自抗体,抗体样蛋白,完整抗体(多克隆抗体、单克隆抗体、抗体二聚体、抗体多聚体)或多特异性抗体(选自双特异性抗体、三特异性抗体或四特异性抗体),单链抗体,与靶细胞、单克隆抗体、单链单克隆抗体结合的抗体片段,与靶细胞结合的单克隆抗体片段,嵌合抗体,与靶细胞结合的嵌合抗体片段,域抗体,与靶细胞结合的域抗体片段,表面修饰抗体,单链表面修饰抗体,或与靶细胞结合的表面修饰抗体片段,人源化抗体或表面修饰抗体,人源化单链抗体,或与靶细胞结合的人源化抗体片段,抗独特型(抗-id)抗体,cdr,双抗体,三抗体,四抗体,微抗体,前抗体,前抗体片段,小免疫蛋白(sip),淋巴因子,激素,维生素,生长因子,菌落刺激因子,营养转运分子,大分子量蛋白,经抗体或大分子量蛋白质修饰的纳米颗粒或聚合物分子。 15.如权利要求1、2、8、9、10、11、12、13或14中任一项所述的偶联物,其中细胞结合剂/分子是能够抗肿瘤细胞、病毒感染细胞、微生物感染细胞、寄生虫感染细胞、自身免疫细胞、活化细胞、骨髓细胞、活化t细胞、b细胞或黑素细胞或者任何表达以下一种抗原或受体的细胞:cd2、cd2r、cd3、cd3gd、cd3e、cd4、cd5、cd6、cd7、cd8、cd8a、cd8b、cd9、cd10、cd11a、cd11b、cd11c、cd12、cd12w、cd13、cd14、cd15、cd15s、cd15u、cd16、cd16a、cd16b、cd17、cdw17、cd18、cd19、cd20、cd21、cd22、cd23、cd24、cd25、cd26、cd27、cd28、cd29、cd30、cd31、cd32、cd33、cd34、cd35、cd36、cd37、cd38、cd39、cd40、cd41、cd42、cd42a、cd42b、cd42c、cd42d、cd43、cd44、cd44r、cd45、cd45ra、cd45rb、cd45ro、cd46、cd47、cd47r、cd48、cd49a、cd49b、cd49c、cd49e、cd49f、cd50、cd51、cd52、cd53、cd54、cd55、cd56、cd57、cd58、cd59、cd60、cd60a、cd60b、cd60c、cd61、cd62e、cd62l、cd62p、cd63、cd64、cd65、cd65s、cd66、cd66a、cd66b、cd66c、cd66d、cd66e、cd66f、cd67、cd68、cd69、cd70、cd71、cd72、cd73、cd74、cd74、cd75、cd75s、cd76、cd77、cd78、cd79、cd79a、cd79b、cd80、cd81、cd82、cd83、cd84、cdw84、cd85、cd86、cd87、cd88、cd89、cd90、cd91、cd92、cdw92、cd93、cd94、cd95、cd96、cd97、cd98、cd99、cd99r、cd100、cd101、cd102、cd103、cd104、cd105、cd106、cd107、cd107a、cd107b、cd108、cd109、cd110、cd111、cd112、cd113、cdw113、cd114、cd115、cd116、cd117、cd118、cd119、cdw119、cd120a、cd120b、cd121a、cd121b、cdw121b、cd122、cd123、cdw123、cd124、cd125、cdw125、cd126、cd127、cd128、cdw128、cd129、cd130、cd131、cdw131、cd132、cd133、cd134、cd135、cd136、cdw136、cd137、cdw137、cd138、cd139、cd140a、cd140b、cd141、cd142、cd143、cd144、cd145、cdw145、cd146、cd147、cd148、cd149、cd150、cd151、cd152、cd153、cd154、cd155、cd156a、cd156b、cdw156c、cd157、cd158a、cd158b、cd159a、cd159b、cd159c、cd160、cd161、cd162、cd162r、cd163、cd164、cd165、cd166、cd167、cd167a、cd168、cd169、cd170、cd171、cd172a、cd172b、cd172g、cd173、cd174、cd175、cd175s、cd176、cd177、cd178、cd179、cd180、cd181、cd182、cd183、cd184、cd185、cd186、cdw186、cd187、cd188、cd189、cd190、cd191、cd192、cd193、cd194、cd195、cd196、cd197、cd198、cdw198、cd199、cdw199、cd200、cd200a、cd200b、cd201、cd202、cd202b、cd203、cd203c、cd204、cd205、cd206、cd207、cd208、cd209、cd210、cdw210、cd211、cd212、cd213a1、cd213a2、cd214、cd215、cd216、cdw217、cdw218a、cdw218b、cd219、cd220、cd221、cd222、cd223、cd224、cd225、cd226、cd227、cd228、cd229、cd230、cd231、cd232、cd233、cd234、cd235a、cd235ab、cd235b、cd236、cd236r、cd237、cd238、cd239、cd240、cd240ce、cd240d、cd241、cd242、cd243、cd244、cd245、cd246、cd247、cd248、cd249、cd250、cd251、cd252、cd253、cd254、cd256、cd257、cd258、cd259、cd260、cd261、cd262、cd263、cd264、cd265、cd266、cd267、cd268、cd269、cd270、cd271、cd272、cd273、cd274、cd275、cd276(b7-h3)、cd277、cd278、cd279、cd280、cd281、cd282、cd283、cd284、cd285、cd286、cd287、cd288、cd289、cd290、cd291、cd292、cdw293、cd294、cd295、cd296、cd297、cd298、cd299、cd300a、cd300c、cd300e、cd301、cd302、cd303、cd304、cd305、cd306、cd307、cd308、cd309、cd310、cd311、cd312、cd314、cd315、cd316、cd317、cd318、cd319、cd320、cd321、cd322、cd323、cd324、cdw325、cd326、cdw327、cdw328、cdw329、cd330、cd331、cd332、cd333、cd334、cd335、cd336、cd337、cdw338、cd339、4-1bb、5ac、5t4(滋养层糖蛋白、tpbg、5t4、wnt激活的抑制因子1或waif1)、腺癌抗原、ags-5、ags-22m6、激活素受体样激酶1、afp、akap-4、alk、α-整合素、αvβ6、氨基肽酶n、淀粉样蛋白β、雄激素受体、血管生成素2、血管生成素3、膜联蛋白a1、炭疽毒素保护性抗原、抗转铁蛋白受体、aoc3(vap-1)、b7-h3、炭疽芽孢杆菌、baff(b细胞活化因子)、b淋巴瘤细胞、bcr-abl、bombesin、boris、c5、c242抗原、ca125(碳水化合物抗原125、muc16)、ca-ix(或caix、碳酸酐酶9)、calla、canag、canislupusfamiliarisil31、碳酸酐酶ix、心肌肌球蛋白、ccl11(c-c基序趋化因子11)、ccr4(c-c趋化因子受体4型、cd194)、ccr5、cd3e(ε)、cea(癌胚抗原)、ceacam3、ceacam5(癌胚抗原)、cfd(因子d)、ch4d5、胆囊收缩素2(cck2r)、cldn18(claudin-18)、结块因子a、cripto、fcsf1r(集落刺激因子1受体、cd115)、csf2(集落刺激因子2、粒细胞-巨噬细胞集落刺激因子(gm-csf))、ctla4(细胞毒性t淋巴细胞相关蛋白4)、ctaa16.88肿瘤抗原、cxcr4(cd184)、c-x-c趋化因子受体4型、环状adp核糖水解酶、细胞周期蛋白b1、cyp1b1、巨细胞病毒、巨细胞病毒糖蛋白b、达比加群、dll3(δ样配体3)、dll4(δ样配体4)、dpp4(二肽基肽酶4)、dr5(死亡受体5)、大肠杆菌志贺毒素型pe-1、大肠杆菌志贺毒素型pe-2、ed-b、egfl7(含egf样结构域的蛋白质7)、egfr、egfrii、egfrviii、内皮糖蛋白(cd105)、内皮素b受体、内毒素、epcam(上皮细胞粘附分子)、epha2、episialin、erbb2(表皮生长因子受体2)、erbb3、erg(tmprss2ets融合基因)、大肠杆菌、etv6-aml、fap(成纤维细胞活化蛋白α)、fcgr1、甲胎蛋白、纤维蛋白ii、β链、纤连蛋白额外结构域-b、folr(叶酸受体)、叶酸受体α、叶酸水解酶、fos相关抗原1、呼吸道合胞病毒f蛋白、卷曲受体、岩藻糖基gm1、gd2神经节苷脂、g-28(细胞表面抗原glyvolipid)、gd3独特型、globoh、磷脂酰肌醇蛋白聚糖3、n-羟乙酰神经氨酸、gm3、gmcsf受体α链、生长分化因子8、gp100、gpnmb(跨膜糖蛋白nmb)、gucy2c(鸟苷酸环化酶2c、鸟苷酸环化酶c(gc-c)、肠鸟苷酸环化酶、鸟苷酸环化酶c受体、热稳定肠毒素受体)、热休克蛋白、血凝素、乙型肝炎表面抗原、乙型肝炎病毒、her1(人表皮生长因子受体1)、her2、her2/neu、her3(erbb-3)、igg4、hgf/sf(肝细胞生长因子/散射因子)、hhgfr、hiv-1、组蛋白复合物、hla-dr(人类白细胞抗原)、hla-dr10、hla-drb、hmwmaa、人绒毛膜促性腺激素、hngf、人分散因子受体激酶、hpve6/e7、hsp90、htert、icam-1(细胞间粘附分子1)、独特型、igf1r(igf-1、胰岛素样生长因子1受体)、ighe、ifn-g、influezahemag-glutinin、ige、igefc区、ighe、白细胞介素(il-1、il-2、il-3、il-4、il-5、il-5、il-6、il-6r、il-7、il-8、il-9、il-9、il-10、il-11、il-12、il-13、il-13、il-15、il-17、il-17、il-17a、il-18、il-19、il-20、il-20、il-21、il-22、il-23、il-27、il-27、或il-28)、il31ra、ilgf2(胰岛素样生长因子2)、整合素(α4、αiibβ3、αvβ3、αvβ3、α4β7、α7、α5β1、α5β7、α5β1、α5β7、α5β8、il-α6β4、α7β7、αllβ3、α5β5、αvβ5)、干扰素γ诱导蛋白、itga2、itgb2、kir2d、lck、le、legumain、lewis-y抗原、lfa-1(淋巴细胞功能相关抗原1、cd11a)、lhrh、lingo-1、脂磷壁酸、liv1a、lmp2、lta、mad-ct-1、mad-ct-2、mage-1、mage-2、mage-3、magea1、magea3、mage4、mart1、mcp-1、mif(巨噬细胞移动抑制因子或糖基化抑制因子(gif))、ms4a1(跨膜4域亚家族a成员1)、msln(间皮素)、muc1(粘蛋白1、细胞表面相关(muc1)或多形上皮粘蛋白(pem))、muc1-klh、muc16(ca125)、mcp1(单核细胞趋化蛋白1)、melana/mart1、ml-iap、mpg、ms4a1(跨膜4域亚家族a)、mycn、髓鞘相关糖蛋白、肌肉生长抑制素、na17、narp-1、nca-90(粒细胞抗原)、nectin-4(asg-22me)、ngf、神经凋亡调节蛋白酶1、nogo-a、notch受体、nucleolin、neu癌基因产物、ny-br-1、ny-eso-1、ox-40、oxldl(氧化低密度脂蛋白)、oy-tes1、p21、p53非突变体、p97、page4、pap、抗-(n-羟乙酰神经氨酸)的互补位、pax3、pax5、pcsk9、pdcd1(pd-1、程序性细胞死亡蛋白1、cd279)、pdgf-rα(α型血小板衍生生长因子受体)、pdgfr-β、pdl-1、plac1、plap样睾丸碱性磷酸酶、血小板衍生生长因子受体β、磷酸钠共转运蛋白、pmel17、聚唾液酸、蛋白酶3(pr1)、前列腺癌、ps(磷脂酰丝氨酸)、前列腺癌细胞、铜绿假单胞菌、psma、psa、psca、狂犬病病毒糖蛋白、rhd(rh多肽1(rhpi)、cd240)、恒河猴因子、rankl、rantes受体(ccr1、ccr3、ccr5)、rhoc、ras突变体、rgs5、robo4、呼吸道合胞病毒、ron、肉瘤易位断点、sart3、硬骨素、slamf7(slamfamilymember7)、selectinp、sdc1(syndecan1)、sle(a)、somatomedinc、sip(鞘氨醇-1-磷酸)、生长抑素、精子蛋白17、ssx2、steap1(前列腺的六种跨膜上皮抗原1)、steap2、stn、tag-72(肿瘤相关糖蛋白72)、survivin、t-cellreceptor、tcell跨膜蛋白、tem1(肿瘤内皮标志物1)、tenb2、腱生蛋白c(tn-c)、tgf-α、tgf-β(转化生长因子β)、tgf-β1、tgf-β2(转化生长因子β2)、tie(cd202b)、tie2、tim-1(cdx-014)、tn、tnf、tnf-α、tnfrsf8、tnfrsf10b(肿瘤坏死因子受体超家族成员10b)、tnfrsf13b(肿瘤坏死因子受体超家族成员13b)、tpbg(滋养层糖蛋白)、trail-r1(肿瘤坏死凋亡诱导配体受体1)、trailr2(死亡受体5(dr5))、肿瘤相关钙信号转导2、肿瘤特异性糖基化muc1、tweak受体、tyrp1(糖蛋白75)、trop-2、trp-2、酪氨酸酶、vcam-1(cd106)、vegf、vegf-a、vegf-2(cd309)、vegfr-1、vegfr2或波形蛋白、wt1、xage1或表达任何胰岛素生长因子受体或任何表皮生长因子受体的细胞。 16.如权利要求15所述的肿瘤细胞,选自淋巴瘤细胞、骨髓瘤细胞、肾细胞、乳腺癌细胞、前列腺癌细胞、卵巢癌细胞、结直肠癌细胞、胃癌细胞、鳞状癌细胞、小细胞肺癌细胞、非小细胞肺癌细胞、睾丸癌细胞、恶性细胞或任何因不受控制的、快速生长和分裂而引起癌症的细胞。 17.如权利要求1所述的偶联物,其中drug1或drug2是发色分子,选自于以下结构ac01、ac02、ac03、ac04、ac05、ac06、andac07、ac08、ac09、ac010、和ac11: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、n的定义与前文相同;r12和r12’独立地为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、o(ch2ch2o)pch2ch2nhso3h、nh(ch2ch2o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh-ar-cooh、nh-ar-nh2,其中p=0-5000,aa是氨基酸,(aa)n包含了相同或不同的天然或非天然氨基酸,n=1-30。 18.如权利要求1所述的偶联物,其中drug1或drug2是tubulysin类似物,选自于以下结构t01、t02、t03、t04、t05、t06、t07、t08、t09、t10、t11、t12、t13、t14、t15、t16、t017、t18、t19、t20、t21、t22和t23: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、和n的定义如前文所述;y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;mab为抗体,优选地为单克隆抗体;r12为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、nhoh、nhor1、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nhso3h、nh(ch2ch2o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh(ch2ch2nh)pch2ch2nh2、nh(ch2ch2s)pch2ch2nh2、nh(ch2ch2nh)pch2ch2oh、nh(ch2ch2s)pch2ch2oh、nh-r1-nh2、或nh(ch2ch2o)pch2ch2nhpo3h2、其中aa为1-8个氨基酸;n为1-20;p为1-5000;r1、r1’、r2、r3、r4和r5独立地为h、c1-c8直链或支链烷基、酰胺或胺;c2-c8芳基、烯基、炔基、杂芳基、杂烷基、烷基环烷基、酯、醚、杂环烷基或酰氧基胺;或含有1-8个氨基酸的肽或(och2ch2)p或(och2ch(ch3))p、其中p是1到约5000的整数;两个r:r1r2、r2r3、r1r3或r3r4可以形成烷基、芳基、杂芳基、杂烷基或烷基环烷基的3~8环状;x3是h、ch3、ch2ch3、c3h7或x1’r1’,其中x1’是nh、n(ch3)、nhnhnh、o或s;r1’为h或c1-c8直链或支链烷基、芳基、杂芳基、杂烷基、烷基环烷基或酰氧基胺;r3’为h或c1-c6直链或支链烷基;z3为h、coor1、nh2、nhr1、or1、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1、o-糖苷(葡萄糖苷、半乳糖苷、甘露糖苷、葡萄糖醛酸苷/葡糖苷酸、阿洛糖苷、果糖苷等)、nh糖苷、s-糖苷或ch2糖苷;m1和m2独立地是h、na、k、ca、mg、nh4或nr1r2r3。 19.如权利要求1所述的偶联物,其中drug1或drug2是加利车霉素类似物,选自于以下结构c01和c02: 其中q、x1x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1。 20.如权利要求1所述的偶联物,其中drug1或drug2是美登素生物碱类似物,选自于以下结构my01、my02、my03、my04、my05、my06、my07和my08: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文;优选地x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1。 21.如权利要求1,其中drug1或drug2紫杉烷类似物,选自于以下结构tx01,tx02和tx03: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义同前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o) nhnhc(o)和c(o)nr1。 22.如权利要求1,其中drug1或drug2是cc-1065类似物和/或多卡霉素类似物,选自于以下结构cc01、cc02、cc03、cc04、cc05、cc06和cc07: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;q优选地为单克隆抗体;z3是h、po(om1)(om2)、so3m1、ch2po(om1)(om2)、ch3n(ch2ch2)2nc(o)-、o(ch2ch2)2nc(o)-、r1或糖苷。 23.如权利要求1所述偶联物,其中drug1或drug2是柔红霉素或多柔比星同系物,选自于以下结构da01、da02、da03、da04、da05、da06、da07、da08、da09、da10和da11: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义如前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;r12为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、nhoh、nhor1、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nh-so3h、nh(ch2ch2o)pch2ch2nh-so3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2-ch2nhpo3h2、nh(ch2ch2o)pch2-ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh(ch2ch2nh)pch2-ch2nh2、nh(ch2ch2s)pch2ch2nh2、nh(ch2ch2nh)pch2ch2oh、nh(ch2ch2s)pch2-ch2oh、nh-r1-nh2、或nh(ch2ch2o)pch2ch2nhpo3h2。 24.如权利要求1所述的偶联物,其中drug1或drug2是澳瑞斯汀或多拉司汀类似物,选自于以下结构au01、au02、au03、au04、au05、au06、au07、au08、au09、au10、au11、au12、au13、au14、au15、au16、au17、au18、au19、au20、au21、au22、au23、au24、au25、au26、和au27: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义同前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;r12是oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、nhoh、nhor1、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nh-so3h、nh(ch2ch2o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2-ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh(ch2ch2nh)pch2-ch2nh2、nh(ch2ch2s)pch2ch2nh2、nh(ch2ch2nh)pch2ch2oh、nh(ch2ch2s)pch2-ch2oh、nh-r1-nh2或nh(ch2ch2o)pch2ch2nhpo3h2,其中aa为1-8个氨基酸;p为1-5000;q优选为单克隆抗体;r1、r2、r3、r4和r5独立地为h,c1-c8直链或支链烷基,芳基,杂芳基,杂烷基,烷基环烷基,酯,醚,酰胺,胺,杂环烷基或酰氧基胺;或含有1-8个氨基酸的肽,或具有式(och2ch2)p或(och2ch(ch3))p的聚乙烯基氧单,其中p是1至约5000的整数。两个r:r1r2,r2r3,r1r3或r3r4可形成烷基,芳基,杂芳基,杂烷基或烷基环烷基的3~8个成员环;x3为h,ch3或x1’r1’,其中x1’为nh,n(ch3),nhnh,o或s,r1’是h或c1-c8直链或支链烷基,芳基,杂芳基,杂烷基,烷基环烷基,酰氧基胺;r3’是h或c1-c6直链或支链烷基;z3’是h、coor1、nh2、nhr1、or1、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1、或o-糖苷(葡糖苷、半乳糖苷、甘露糖苷、葡糖苷酸/葡糖苷酸、阿洛糖苷、果糖苷等)、nh糖苷、s-糖苷或ch2糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 25.如权利要求1所述的偶联物,其中drug1或drug2是苯并二氮卓二聚体,选自以下结构pb01、pb02、pb03、pb04、pb05、pb06、pb07、pb08、pb09、pb10、pb11、pb12、pb13、pb14、pb15、pb16、pb17、pb18、pb19、pb20、pb21、pb22、pb23、pb24、pb25、pb26、pb27、pb28、pb29、pb30、pb31和pb32: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;r1、r2、r3、r1’、r2’和r3’独立地为h、f、cl、=o、=s、oh、sh、c1-c8直链或支链烷基、芳基、烯基、杂芳基、杂烷基、烷基环烷基、酯(coor5or–oc(o)r5)、醚(or5)、酰胺(conr5)、氨基甲酸酯(oconr5)、胺(nhr5、nr5r5′)、杂环烷基或酰氧基胺(-c(o)nhoh、-onhc(o)r5),含20种天然或非天然氨基酸的多肽,或如式(och2ch2)p或(och2ch(ch3))p的聚乙烯氧基单,其中p是1至约5000的整数。两个r:r1r2、r2r3、r1r3、r1’r2’、r2’r3’或r1’r3’可独立形成烷基、芳基、杂芳基、杂烷基或烷基环烷基的3~8个环;x3和y3独立地为n、nh、ch2或cr5、其中r5、r6、r12和r12’独立地为h、oh、nh2、nh(ch3)、nhnh2、cooh、sh、oz3、sz3、f、cl、或c1-c8直链或支链烷基、芳基、杂芳基、杂烷基、烷基环烷基、酰氧基胺;z3为h、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1或o-糖苷(葡萄糖苷、半乳糖苷、甘露糖苷、葡糖苷酸/葡糖苷酸、阿洛糖苷、果糖等)、nh-糖苷、s-糖苷或ch2-糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 26.如权利要求1所述的偶联物,其中drug1或drug2是鹅膏毒肽及其类似物,选自于以下结构am01、am02、am03、am04、am05、am06、am07、am08和am09: 其中x1、x2、q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh,nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、chc(o)nh-nhc(o)、c(o)nr1或缺省;r7、r8和r9独立地为h、oh、or1、nh2、nhr1、c1-c6烷基或缺省;y2为o、o2、nr1、nh或缺省;r10是ch2、o、nh、nr1,nhc(o)、nhc(o)nh、nhc(o)o、oc(o)o、c(o)、oc(o)、oc(o)(nr1)、(nr1)c(o)(nr1)、c(o)r1或缺省;r11为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2-ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nhso3h、nh(ch2ch2-o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2c-h2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、或nh(ch2ch2o)pch2ch2nhpo3h2其中aa为1-20个氨基酸;n和m1独立地为1-30;p为1-5000;z3为h、oh、coor1、nh2、nhr1、or1、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1或o-糖苷(葡萄糖苷,半乳糖苷,甘露糖苷,葡糖苷/葡糖苷酸,阿洛糖苷,果糖苷等)nh糖苷、s-糖苷或ch2-糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 27.如权利要求1所述的偶联物,其中drug1或drug2是喜树碱及其衍生物,选自以下结构cp01、cp02、cp03、cp04、cp05和cp06: 其中q、x1,x2,y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)、c(o)nr1或缺省;z3为h、oh、coor1、nh2、nhr1、or1、ch3、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1、或o-糖苷(葡萄糖苷、半乳糖苷、甘露糖苷、葡糖醛酸苷/葡糖醛酸苷、阿洛糖苷、果糖苷等)、nh-糖苷、s-糖苷或ch2-糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 28.如权利要求1所述的偶联物,其中drug1或drug2是艾日布林及其衍生物,选自于以下结构eb01,和eb02: 其中q、x1、x2、y1、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)、c(o)nr1或缺省。 29.如权利要求1所述的偶联物,其中drug1或drug2是烟酰胺磷酸核糖基转移酶抑制剂,选自于以下结构np01,np02,np03,np04,np05,np06,np07,np08和np09: 其中q、x1、x2、y1、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;x5为f、cl、br、i、oh、or1、r1、opo3h2、oso3h、nhr1、ocor1、nhcor1;优选地,x1、x2、y1和y2为独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)、c(o)nr1或缺省。 30.如权利要求1或10所述的偶联物,其中drug1或drug2是聚亚烷基二醇类似物,选自以下结构pg01、pg02和pg03: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义与前文相同;优选地y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;p为1-5000;r1和r3与上述r1定义相同,且优选地r1和r3为独立地h、oh、och3、ch3、或oc2h5。 31.如权利要求1所述的偶联物,其中drug1或drug2是细胞结合配体或细胞受体激动剂及其类似物,选自以下结构:lb01(叶酸偶联物)、lb02(pmsa配体偶联物)、lb03(pmsa配体偶联物)、lb04(pmsa配体偶联物)、lb05(生长抑素偶联物)、lb06(生长抑素偶联物)、lb07(奥曲肽、生长抑素类似物偶联物)、lb08(兰瑞肽、生长抑素类似物偶联物)、lb09(伐普肽(sanvar)、生长抑素类似物偶联物)、lb10(caix配体偶联物)、lb11(caix配体偶联物)、lb12(胃泌素释放肽受体(grpr)、mba偶联物)、lb13(促黄体激素释放激素(lh-rh)配体和gnrh偶联物)、lb14(促黄体激素释放激素(lh-rh)和gnrh配体偶联物)、lb15(gnrh拮抗剂、abarelix偶联物)、lb16(钴胺素、维生素b12类似物偶联物)、lb17(钴胺素、维生素b12类似物偶联物)、lb18(αvβ3整联蛋白受体、环状rgd五肽偶联物)、lb19(vegf受体的异二价肽配体偶联物)、lb20(神经髓质素b偶联物)、lb21(g蛋白偶联受体蛙皮素偶联物)、lb22(类toll受体tlr2偶联物)、lb23(雄激素受体偶联物)、lb24(αv整合素受体西仑吉肽/环(-rgdfv-)偶联物)、lb25(利福布汀类似物偶联物)、lb26(利福布汀类似物偶联物)、lb27(利福布汀类似物偶联物)、lb28(氟氢可的松偶联物)、lb29(地塞米松偶联物)、lb30(丙酸氟替卡松偶联物)、lb31(丙酸倍氯米松偶联物)、lb32(曲安奈德偶联物)、lb33(泼尼松偶联物)、lb34(泼尼松龙偶联物)、lb35(甲基强的松龙偶联物)、lb36(倍他米松偶联物)、lb37(伊立替康类似物偶联物)、lb38(克唑替尼类似物偶联物)、lb39(硼替佐米类似物偶联物)、lb40(卡菲佐米类似物偶联物)、lb41(卡菲佐米类似物偶联物)、lb42(亮丙瑞林类似物偶联物)、lb43(曲普瑞林类似物偶联物)、lb44(克林霉素偶联物)、lb45(利拉鲁肽类似物偶联物)、lb46(索马鲁肽类似物偶联物)、lb47(瑞他帕林类似物偶联物)、lb48(indibulin类似物偶联物)、lb49(长春碱类似物偶联物)、lb50(利西那肽类似物偶联物)、lb51(奥希替尼类似物偶联物)、lb52(核苷类似物偶联物)、lb53(厄洛替尼类似物偶联物)和lb54(拉帕替尼类似物偶联物): 其中y5、是n、ch、c(cl)、c(ch3)、或c(coor1);r1是h、c1-c6烷基、c3-c8芳基; 其中x1、x2、q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;x3为ch2、o、nh、nhc(o)、nhc(o)nh、c(o)、oc(o)、oc(o)(nr3)、r1、nhr1、nr1、c(o)r1或缺省;x4为h、ch2、oh、o、c(o)、c(o)nh、c(o)n(r1)、r1、nhr1、nr1、c(o)r1或c(o)o;x5为h、ch3、f、或cl;m1和m2为独立的h、na、k、ca、mg、nh4、nr1r2r3;r6为5′-脱氧腺苷、me、oh、或cn。 32.如权利要求1所述的偶联物,其中细胞毒性分子是dna,rna,mrna,小干扰rna(sirna),微rna(mirna),或与piwi相互作用rnas(pirna),偶联物选自以下结构si-1: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)和c(o)nr1;是单链或双链的dna、rna、mrna、sirna、mirna或pirna。 33.权利要求1、5、6、12、13、14、15、16、17、18、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35或36中任一项所述的偶联物,其中细胞连接分子/剂选自于igg抗体,单克隆抗体,或igg类抗体蛋白质,具有st1、st2、st3、st4、st5、或st6的结构,其通过轻重链之间的二硫键,或重链之间上部二硫键,或重链之间下部二硫键被还原产生的一对巯基,特异性偶联: 其中y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选的x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)和c(o)nr1;m1、m2、m3和m4独立地为1-30。 34.如权利要求33所述的偶联物,当含有相同或不同本发明中的双键连接子的细胞毒性分子,依次地,逐步地与细胞结合分子偶联时,在细胞结合分子的不同偶联位点上连接的药物(或细胞毒性分子)和m1可以是不同的。 35.如权利要求33或34中任一项所述的偶联物,其中drug选自tubulysin、美登素、紫杉烷类、cc-1065类似物、柔红霉素和多柔比星化合物、毒伞肽(包括鹅膏毒素)、indolecarboxamide、苯并二氮卓二聚体、吡咯并苯二氮杂卓(pbd)二聚体、托美霉素二聚体、氨茴霉素二聚体、吲哚并苯并二氮二聚体、咪唑并苯并噻二氮杂卓、恶唑烷并苯并二氮杂卓的二聚体、加利车霉素类和烯二炔类抗生素、放线菌素、氮丝菌素、博来霉素、表柔比星、他莫昔芬、伊达比星、多拉司汀、澳瑞斯汀(包括甲基澳瑞斯汀、mmae、mmaf、澳瑞斯汀pye、澳瑞斯汀tp、澳瑞斯汀2-aq、6-aq、eb(aeb)、efp(aefp)和它们的同系物)、多卡霉素、格尔德霉素、hsp90抑制剂、烟酰胺磷酸核糖基转移酶抑制剂、centanacycin、甲氨喋呤、噻替派、长春地辛、长春新碱、erbulins,、半米塔林、nazumamides、微晶蛋白、放射敏素、streptonigtin、sn38或其它喜树碱类似物或降解物、alterobactin、microsclerodermins、theonellamides、esperamicin、pnu-及其类似物和衍生物、药学上可接受的盐、酸、衍生物、水合物或水合盐;或晶体结构;或任何上述药物的旋光异构体、外消旋物、非对映异构体或对映异构体;或权利要求8所述的细胞毒性分子/化合物。 36.如权利要求3所述的化合物,具有如a-01、a-02、a-03、a-04、b-01、b-02、b-03、b-04、b-05、b-06、b-07、b-08、b-09、b-10、b-11、b-12、b-13、b-14、b-15、b-16、c-01、c-02、c-03、c-04、c-05、c-06、c-07、c-08、c-09、c-10、c-11、c-12、d-01、d-02、d-03、d-04、d-05、d-06、pg-04、97、98、116、125、129、133、135、157a、157b、157c、157d、157e、157f、162、163、235a、235b、235c、236a、236b、236c、238a、238b、238c、255、256、258a、258b、258c、260、262、267、271、272、274、276、278、282、284、286、287、306、309、314、318和325的结构: 37.如权利要求1所述的偶联物,具有如aa-01、aa-02、aa-03、aa-04、ba-01、ba-02、ba-03、ba-04、ba-05、ba-06、ba-07、ba-08、ba-09、ba-10、ba-11、ba-12、ba-13、ba-14、ba-15、ba-16、ca-02、ca-03、ca-04、ca-05、ca-06、ca-07、ca-08、ca-09、ca-10、ca-11、ca-12、da-01、da-02、da-03、da-04、da-05或da-06、99、117、126、130、136、158a、158b、158c、158d、158e、158f、164、237a、237b、237c、239a、239b、239c、257、259、261、263、268、273、275、277、279、283、285、288、307、310、315、319和326的结构: 其中m1,和n与权利要求1中的定义相同;mab是抗体;交叉键表示它可以连接两个原子中的任何一个。 38.一种药物组合物,其包含治疗有效量的,权利要求1、2、8、9、10、11、12、13、14、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、或37、中的任一偶联物,和药学上可接受的盐,载体,稀释剂或辅料,或偶联物的组合物,以治疗癌症、感染或自身免疫性疾病。 39.如权利要求38所述的药物组合物,其以液体制剂形式或以冻干制剂形式存在,包括以重量计的,0.01%-99%的权利要求1、2、8、9、10、11、12、13、14、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、或37、中一种或多种偶联物,0.0%-20.0%的一种或多种多醇;0.0%-2.0%的一种或多种表面活性剂;0.0%-5.0%的一种或多种防腐剂;0.0%-30%的一种或多种氨基酸;0.0%-5.0%一种或多种抗氧化剂;0.0%-0.3%的一种或多种金属螯合剂;0.0%-30.0%的一种或多种缓冲盐,用于将制剂的ph调节至4.5至8.5;以及0.0%-30.0%的一种或多种等渗剂,用于在复溶后施用于患者时,将渗透压调节在250至350mosm之间。 其中多醇选自果糖、甘露糖、麦芽糖、乳糖、阿拉伯糖、木糖、核糖、鼠李糖、半乳糖、葡萄糖、蔗糖、海藻糖、山梨糖、松三糖、棉子糖、甘露醇、木糖醇、赤藓糖醇、麦芽糖醇、乳糖醇、赤藓糖醇、苏糖醇、山梨糖醇、甘油或l-葡萄糖酸盐及其金属盐; 其中表面活性剂选自聚山梨酸酯20、聚山梨酸酯40、聚山梨酸酯65、聚山梨酸酯80、聚山梨酸酯81或聚山梨酸酯85、泊洛沙姆、聚(环氧乙烷)-聚(环氧丙烷)、聚乙烯-聚丙烯、triton;十二烷基硫酸钠(sds))、月桂基硫酸钠;辛基钠糖苷;十二烷基、肉豆蔻酰基、亚油基或硬脂基磺基甜菜碱;十二烷基、肉豆蔻酰基、亚油基或硬脂基肌氨酸;亚油酸、肉豆蔻基或十六烷基甜菜碱;月桂酰胺基丙基、椰油酰胺基丙基-、亚油酰胺基丙基-、豆蔻酰氨基丙基-、棕榈酰丙基-丙基或异硬脂酰胺基丙基-甜菜碱(月桂酰胺基丙基);肉豆蔻酰丙基-、棕榈酰胺基丙基或-异硬脂酰胺基丙基-二甲基胺;甲基椰油酰基-钠或甲基油基-甲基十二烷基磺酸钠;十二烷基甜菜碱-、椰油酰胺基丙基甜菜碱和椰油两性甘氨酸酯;或异硬脂基乙基亚胺基乙醇硫酸盐;聚乙二醇、聚丙二醇,以及乙烯和丙二醇的共聚物; 其中的防腐剂选自苯甲醇、十八烷基二甲基苄基氯化铵、六甲基氯化铵、苯扎氯铵、苄索氯铵、苯酚、丁基和芐基醇、对羟基苯甲酸烷基酯、对羟基苯甲酸甲酯或对羟基苯甲酸丙酯、邻苯二酚、间苯二酚、环己醇、3-戊醇或间甲酚 其中氨基酸选自精氨酸、胱氨酸、甘氨酸、赖氨酸、组氨酸、鸟氨酸、异亮氨酸、亮氨酸、丙氨酸、甘氨酸谷氨酸或天冬氨酸; 其中抗氧化剂选自抗坏血酸、谷胱甘肽、胱氨酸或甲硫氨酸; 其中螯合剂选自edta或egta; 其中缓冲盐选自柠檬酸、抗坏血酸、葡萄糖酸、碳酸、酒石酸、琥珀酸、乙酸或邻苯二甲酸的钠、钾、铵或三羟基乙基氨基盐;tris或氨丁三醇的盐酸、磷酸或硫酸盐;精氨酸、甘氨酸、甘氨酰甘氨酸或组氨酸的乙酸盐、氯化物、磷酸盐、硫酸盐或琥珀酸盐; 其中等渗剂选自甘露醇、山梨醇、乙酸钠、氯化钾、磷酸钠、磷酸钾、柠檬酸三钠或氯化钠。 40.如权利要求38或39所述的药物组合物,其特征在于以液体或冻干制剂的形式保存在西林瓶,瓶,预填充注射器或预填充自动注射器中。 41.如权利要求1、2、8、9、10、11、12、13、14、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、或37、所述的偶联物,或权利要求38或39所述的药物组合物,具有体外,体内或离体细胞杀伤活性。 42.如权利要求38或39所述的药物组合物,其与化疗剂,放射治疗,免疫治疗剂,自身免疫失调剂,抗感染剂或其他偶联物同时给药,以协同治疗或预防癌症、自身免疫性疾病或传染性疾病。 43.如权利要求42所述的协同剂,选自以下一种或几种药物:阿巴西普、abemaciclib、乙酸阿比特龙、abraxane、阿杜卡奴单抗、对乙酰氨基酚/氢可酮、阿卡替尼、阿杜卡奴单抗、阿达木单抗、adxs31-142、adxs-her2、阿法替尼二马来酸盐、阿地白介素、阿乐替尼、阿伦单抗、艾力替尼、alitretinoin、ado-trastuzumabemtansine、安非他明/右旋安非他明、阿那曲唑、apatinib、阿立哌唑、蒽环类药物、阿立哌唑、atazanavir、阿特朱单抗、阿托伐他汀、avelumab、avxs-101、axicabtageneciloleucel、阿西替尼、贝利司他、bcg-live、贝伐单抗、贝沙罗汀、blinatumomab、硼替佐米、波舒替尼、本妥昔单抗、布格替尼、布地奈德、布地奈德/福莫特罗、丁丙诺啡、byl719(α特异性pi3k抑制剂)、卡巴他赛、卡博替尼、卡马替尼、卡培他滨、卡非佐米、嵌合抗原受体工程t(car-t)细胞、塞来昔布、色瑞替尼、西妥昔单抗、西奥罗尼、西达本胺、环孢素、cinacalcet、克唑替尼、考比替尼、cosentyx、克唑替尼、tisagenlecleucel、达比加群、达拉菲尼、达卡巴嗪、达利珠单抗、达科替尼、达托霉素、达拉木单抗、darbepoetinalfa、darunavir、达沙替尼、denileukindiftitox、地诺单抗、depakote、dexlansoprazole、dexmethylphenidate、地塞米松、l-3、4-二羟基苯基丙氨酸、dinutuximab、阿法链道酶、强力霉素、度洛西汀、德卫利昔、度伐鲁单抗、依托珠单抗、emicizumab、emtricibine/利匹韦林/替诺福韦、地索普西富马酸、恩曲他滨/替诺福韦/依非韦伦、依诺肝素、恩沙替尼、恩杂鲁胺、易吡替尼、阿法依伯汀、厄洛替尼、埃索美拉唑、eszopiclone、依那西普、依维莫司、依西美坦、依维莫司、艾塞那肽er、依泽替米贝、依泽替米贝/辛伐他汀、法米替尼、非诺贝特、非戈替尼、非格司亭、芬戈莫德、氟马替尼、丙酸氟替卡松、氟替卡松/沙美特罗、呋喹替尼、氟维司群、gazyva、吉非替尼、醋酸格拉替雷、醋酸戈舍瑞林、gsk(bcma-adc)、henatinib、埃克替尼、伊马替尼、替伊莫单抗、依鲁替尼、埃克替尼、艾代拉里斯、异环磷酰胺、英夫利昔单抗、咪喹莫特、immunocyst、immunobcg、iniparib、门冬胰岛素、地特胰岛素、甘精胰岛素、赖脯胰岛素、干扰素α、干扰素α-1b、干扰素α-2a、干扰素α-2b、干扰素β、干扰素β1a、干扰素β1b、干扰素γ-1a、拉帕替尼、易普利姆玛、异丙托溴铵/沙丁胺醇、伊沙唑米、卡努玛、莱地鲁单伉、醋酸兰瑞肽、来那度胺、来那度胺、甲磺酸乐伐替尼、来曲唑、左旋甲状腺素、左旋甲状腺素、利多卡因、利奈唑胺、利拉鲁肽、lisdexamfetamine、ln-144(肿瘤浸润淋巴细胞)、lorlatinib、德立替尼/delitinib、美金刚、甲氧基聚乙二醇epoetin-beta、哌醋甲酯、美托洛尔、曲美替尼、美西他滨/利匹韦林/替诺福韦、莫达非尼、莫米松、mycidac-c、霉酚酸、耐昔妥珠单抗、诺拉替尼、尼罗替尼、尼拉帕尼、尼沃鲁单抗、奥法木单抗、奥比曲妥珠单抗、奥瑞珠单抗、奥拉帕尼、奥美沙坦、奥美沙坦/氢氯苯噻哒嗪、奥马珠单抗、omega-3脂肪酸乙酯、oncorine、奥司他韦、奥希替尼、羟考酮、奥扎莫德、帕波克利、帕利珠单抗、帕尼单抗、帕比司他、帕唑帕尼、派姆单抗、pd-1抗体、pd-l1抗体、培美曲塞、帕妥珠单抗、吡非尼酮、肺炎球菌结合疫苗、泊马度胺、普瑞巴林、proscavax、普萘洛尔、普喹替尼、吡咯替尼、喹硫平、雷贝拉唑、氯化镭223、雷洛昔芬、raltegravir、雷莫芦单抗、雷珠单抗、瑞戈非尼、瑞博西尼、瑞莎珠单抗、利妥昔单抗、利伐沙班、罗米地辛、罗苏伐他汀、磷酸鲁索替尼、沙丁胺醇、索凡替尼、索马鲁肽、sevelamer、西地那非、司妥昔单抗、西莫替尼、西帕替尼/cipatinib、辛波莫德、sipuleucel-t、西他列汀、西他列汀/二甲双胍、solifenacin、索兰珠单抗、索尼吉布、索拉非尼、磺胺替尼、舒尼替尼、他克莫司、tacrimus、他达那非、他莫昔芬、甲磺酸达拉非尼、talimogenela-herparepvec、talazoparib、特拉瑞韦、talazoparib、替莫唑胺、替西罗莫司、替奈普酶、替诺福韦/恩曲他滨、富马酸替诺福韦酯、睾酮凝胶、替加卡托/依伐卡托、沙利度胺、theliatinib、ticebcg、噻托溴铵、tisagenlecleucel、托珠单抗、托瑞米芬、曲美替尼、曲妥珠单抗、曲贝替定(海鞘素743)、曲美替尼、替西木单抗、trifluridine/tipiracil、维甲酸、乌帕替尼、uro-bcg、优特克单抗、valoctocogeneroxaparvovec、缬沙坦、veliparib、凡德他尼、威罗菲尼、维特克拉、维莫德吉、索凡替尼、伏立诺他、阿柏西普、zostavax及其类似物、衍生物、药学上可接受的盐、载体、稀释剂或其辅料,或以上的组合。
本发明申请涉及以2,3-二氨基琥珀酰基双连接子(双链连接子)链接细胞毒性药物/分子与细胞结合分子的偶联物。本发明还涉及具有所述连接子的细胞毒性药物/分子与细胞结合分子偶联物的制备,尤其是药物具有氨基,羟基,二氨基,氨基羟基,二羟基,羧基,肼,醛和巯基时,可以以特定方式与双连接子结合,以及相应偶联物的治疗用途。 发明背景 抗体药物偶联物(adc),是通过一个有条件稳定的连接子链接的小分子化疗药物与抗体(mabs)的协同组合,可通过受体介导的内吞作用使小分子药物在肿瘤内优先蓄积,而不进入健康的组织,已经成为了一类非常有效的抗癌药物,adc药物目前具有庞大且增长迅速的临床管线。adc的三个组分,单克隆抗体,连接子和细胞毒性药物,均会影响偶联物的功效和毒性。优化每个组分,同时增强adc整体的功能,这一直是adc设计和开发的主要考虑。我们相信,能获得定点释放,有效荷载,最优化学计量和大分子的均质性的连接子技术,对于获得药物良好的药代动力学,功效和耐受性至关重要(lambert,j.和chari,r.,j.med.chem.2014,57,6949-64;ponte,j.等,bioconj.chem.,2016,27(7),1588-98;dovgan,i.等,sci.rep.2016,6,30835;ross,p.l.和wolfe,j.l.j.pharm.sci.105(2),391-7;chen,t.等j.pharm.biomed.anal.,2016,117,304-10;zhao,r.y.等,2011,j.med.chem.54,3606-23)。 先前对抗体药物偶联物(adc)稳定性的研究,由于连接子的相对稳定,主要集中在由于相对稳定的有效负载量(例如美登素)的去偶联而导致的药物释放(piwkoc.等,clin.druginvestig.2015,35(8),487-93;lambert,j.和chari,r.j.med.chem.2014,57,6949-64)。但是上市药物t-dm1(抗体-美登素偶联物)作为her2阳性的、无法切除的局部晚期或转移性乳腺癌的一线治疗方案,和作为her2阳性晚期胃癌的二线治疗方案,在临床试验中均失败,因为相比于其副作用,它对患者的益处有限(ellis,p.a.等,j.clin.oncol.2015,33(2015asco年会附录摘要507);shen,k.等,sci.rep.2016;6:23262;degoeij,b.e.和lambert,j.m.curropinimmunol2016,40,14-23;barrios,c.h.等,j.clin.oncol.2016,34(2016asco年会附录摘要593))。 为解决脱靶毒性问题,研究者在adc分子设计时,试图在单一有效荷载的基础上,扩大连接子-有效载荷和偶联化学的范围,尤其是解决靶向adc上连接子-有效荷载的效能问题(lambert,j.m.ther.deliv.2016,7,279-82;zhao,r.y.等,2011,j.med.chem.54,3606-23)。如今,许多药物开发者和学术机构都非常注重开发新型的可靠的特异性连接子和定点偶联方法,这些adc具有更长的循环半衰期,更高的疗效,可能更低的脱靶毒性,更好的体内药代动力学(pk)特性,以及生产时有更好的批次间一致性(hamblett,k.j.等,clin.cancerres.2004,10,7063-70;adem,y.t.等,bioconjugatechem.2014,25,656-664;boylan,n.j.bioconjugatechem.2013,24,1008–1016;strop,p.等,2013chem.biol.20,161-67;wakankar,a.mabs,2011,3,161–172)。迄今报道的这些特异性偶联方法包括在抗体基因工程改造,引入半胱氨酸(junutula,j.r.等,nat.biotechnol.2008,26,925–32;junutula,j.r.等,2010clin.cancerres.16,4769;美国专利8,309,300;7,855,275;7,521,541;7,723,485;wo2008/),引入硒代半胱氨酸(hofer,t.等,biochemistry2009,48,12047–57;li,x.等,methods2014,65,133–8;美国专利8,916,159),引入含有五氟芳香试剂标签的半胱氨酸(zhang,c.等,nat.chem.2015,8,1–9),引入巯基岩藻糖(okeley,n.m.等,2013bioconjugatechem.24,1650),或引入非天然氨基酸(axup,j.y.等,proc.nat.acad.sci.usa.2012,109,16101-6;zimmerman,e.s.等,2014,bioconjug.chem.25,351–361;wu,p.等,2009proc.natl.acad.sci.106,3000-5;rabuka,d.等,nat.protoc.2012,7,1052-67;美国专利8,778,631;美国专利申请;wo2010/081110,wo2006/069246,wo2007/059312;美国专利7,332,571;7,696,312和7,638,299;wo2007/;美国专利7,632,492和7,829,659),通过二溴马来酰胺(jones,m.w.等j.am.chem.soc.2012,134,1847–52),双砜试剂(badescu,g.等bioconjug.chem.2014,25,1124–36;wo2013/,wo2014/064424),二溴哒嗪二酮(maruani,a.等nat.commun.2015,6,6645)重新桥接还原的分子间二硫化物,通过半乳糖基和唾液酸转移酶(zhou,q.等bioconjug.chem.2014,25,510–520;美国专利申请),甲酰甘氨酸生成酶(fge)(drake,p.m.等bioconj.chem.2014,25,1331–41;carrico,i.s.等,美国专利7,985,783;8,097,701;8,349,910,和美国专利申请,),磷酸泛酰巯基乙胺基转移酶(pptases)(grünewald,j.等bioconjug.chem.2015,26,2554–62),转肽酶a(beerli,r.r.等plosone2015,10,e0)等而偶联,可与streptoverticilliummobaraense转谷氨酰胺酶(mtg)(strop,p.bioconj.chem.2014,25,855–62;strop,p.等,chem.biol.2013,20,161–7;美国专利8,871,908)或与微生物转谷氨酰胺酶(mtgase)(dennler,p.等,2014,bioconjug.chem.25,569–78;siegmund,v.等angew.chemie-int.ed.2015,54,13420–4;美国专利申请;美国专利7,893,019)作用导入谷氨酰胺标签,或通过酶/细菌在蛋白质主链外部形成异肽键-肽键(kang,h.j.等science2007,318,1625–8;zakeri,b.等proc.natl.acad.sci.usa2012,109,e690–7;zakeri,b.&howarth,m.j.am.chem.chem.soc.2010,132,4526–7)而偶联。 我们已经公开了几种桥连天然抗体的链间二硫键被还原产生的一对巯基的偶联方法,例如使用溴代马来酰亚胺和二溴代马来酰亚胺连接子(wo2014/009774),2,3-二取代的琥珀酸/2-单取代的/2,3-二取代的富马酸或马来酸连接子(wo2015/,wo),乙炔二羧酸连接子(wo2015/,wo)或肼连接子(wo2015/)。与通过抗体上的半胱氨酸或赖氨酸残基偶联的传统的、非选择性偶联物相比,用这些连接子和方法制备的adc具有更好的治疗窗口。在本专利申请,我们公开了含2,3-二氨基琥珀酰基的新型双连接子,和它们与细胞毒性分子的偶联方法,特别是细胞毒性分子中含有二氨基,氨基-羟基,二羟基,羧基,醛,肼和巯基等基团时的方法。用双连接子制备的免疫偶联物靶向递送的半衰期延长,并且在血液循环中对非靶细胞,组织或器官的暴露最小,具有更小的脱靶毒性。 技术实现要素: 本发明描述了抗体与细胞毒性分子通过双连接子偶联,特别是当细胞毒性分子具有氨基,羟基,二氨基,氨基-羟基,二羟基,羧基,肼或巯基等两个官能团时。它还提供了双连接子,以特定方式将细胞结合分子与细胞毒性分子偶联的方法。 本发明的一个方面,含有2,3-二氨基琥珀酰基双连接子的偶联物由式(i)、(ii)、(iii)或(iv)表示: 其中: 表示单键; 任选为单键,或可缺省; 任选为单键、双键,或可缺省; n独立地为1-30; q是与r3和r4连接的细胞结合剂/分子,可以是目前已知的,或者即将变为已知的任何种类的分子,可与具有治疗意义或被生物修饰的细胞的片段结合,复合或反应。优选地,细胞结合剂/分子是免疫治疗蛋白,抗体,抗体片段或具有超过四个氨基酸的肽; drug1或/和drug2是细胞毒性分子/剂,是治疗药物,或免疫治疗蛋白质/分子,或用于增强细胞结合剂的结合或稳定细胞结合剂的功能分子,或细胞表面受体结合配体,或抑制细胞增殖的分子; x1和x2相同或不同,独立地选自nh、nhnh、n(r1)、n(r1)n(r2)、o、s、s-s、o-nh.o-n(r1)、ch2-nh、ch2-n(r1)、ch=nh、ch=n(r1)、s(o)、s(o2)、p(o)(oh)、s(o)nh、s(o2)nh、p(o)(oh)nh、nhs(o)nh、nhs(o2)nh、nhp(o)(oh)nh、n(r1)s(o)n(r2)、n(r1)s(o2)n(r2)、n(r1)p(o)(oh)n(r2)、os(o)nh、os(o2)nh、op(o)(oh)nh、c(o)、c(nh)、c(nr1)、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)nh、oc(nh)nh、oc(nr1)nh、nhc(o)nh、nhc(nh)nh、nhc(nr1)nh、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)n(r1)、oc(nh)n(r1)、oc(nr1)n(r1)、nhc(o)n(r1)、nhc(nh)n(r1)、nhc(nr1)n(r1)、n(r1)c(o)n(r1)、n(r1)c(nh)n(r1)、n(r1)c(nr1)n(r1)、或c1-c6烷基、c2-c8烯基,杂烷基、烷基环烷基或杂环烷基、c3-c8芳基、ar-烷基、杂环、碳环、环烷基、杂烷基环烷基、烷基羰基或杂芳基; y1、y2、z1和z2可以相同或不同,独立地连接细胞结合分子q或drug1或drug2的官能团、与之形成二硫化物、醚、酯、硫醚、硫酯、肽、腙、氨基甲酸酯、碳酸酯、胺(仲、叔或季胺)、亚胺、环杂烷基、杂芳族、烷基肟或酰胺键;优选地,y1、y2、z1和z2独立地具有以下结构:c(o)ch、c(o)c、c(o)ch2、arch2、c(o)、nh、nhnh、n(r1)、n(r1)n(r2)、o、s、s-s、o-nh、o-n(r1)、ch2-nh.ch2-n(r1)、ch=nh、ch=n(r1)、s(o)、s(o2)、p(o)(oh)、s(o)nh、s(o2)nh、p(o)(oh)nh、nhs(o)nh、nhs(o2)nh、nhp(o)(oh)nh、n(r1)s(o)n(r2)、n(r1)s(o2)n(r2)、n(r1)p(o)(oh)n(r2)、os(o)nh、os(o2)nh、op(o)(oh)nh、c(o)、c(nh)、c(nr1)、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)nh、oc(nh)nh、oc(nr1)nh、nhc(o)nh、nhc(nh)nh、nhc(nr1)nh、c(o)nh、c(nr1)nh、oc(o)n(r1)、oc(nh)n(r1)、oc(nr1)n(r1)、nhc(o)n(r1)、nhc(nh)n(r1)、nhc(nr1)n(r1)、n(r1)c(o)n(r1)、n(r1)c(nh)n(r1)、n(r1)c(nr1)n(r1);或c1-c8烷基,c2-c8杂烷基,烷基环烷基,杂环烷基;c3-c8芳基、ar-烷基、杂环、碳环、环烷基、杂烷基环烷基、烷基羰基、杂芳基; 优选地,y1、y2、z1和z2与细胞结合剂/分子上的巯基对相连接。巯基优选为通过还原剂将细胞结合剂的链间二硫键还原而产生,还原剂包括二硫苏糖醇(dtt),二硫赤藓糖醇(dte),l-谷胱甘肽(gsh),三(2-羧乙基)膦(tcep),2-巯基乙胺(β-mea),或/和β巯基乙醇(β-me,2-me); r1、r2、r3和r4是包含c,n,o,s,si和p原子的链状结构,最优含0-500个原子,共价连接x和z1,y和z2。r1、r2、r3和r4的各个原子以所有可能的化学方式结合,比如形成亚烷基,亚烯基和亚炔基,醚,聚氧化烯,酯,胺,亚胺,多胺,肼,腙,酰胺,脲,氨基脲,卡巴肼,烷氧胺,氨基甲酸酯,氨基酸,肽,酰氧基胺,异羟肟酸,或上述组合。优选地,r1、r2、r3和r4相同或不同,独立选自o、nh、s、nhnh、n(r5)、n(r3)n(r3’)、如式(och2ch2)por5或(och2ch-(ch3))por5或nh(ch2ch2o)pr5或nh(ch2ch(ch3)o)pr5或n[(ch2ch2o)pr5]-[(ch2ch2o)p’r5’]或(och2ch2)pcoor5或ch2ch2(och2ch2)pcoor5的聚乙烯氧基单,其中p和p’独立地是选自0至约1000的整数,或上述的组合;c1-c8烷基;c2-c8杂烷基,烷基环烷基,杂环烷基;c3-c8芳基,芳烷基,杂环,碳环,环烷基,杂烷基环烷基,烷基羰基或杂芳基; 更优选地,r1、r2、r3、r4、r5和r5’独立地是h,c1-c8烷基,c2-c8杂烷基、烷基环烷基或杂环烷基,c3-c8芳基、ar-烷基、杂环、碳环、杂烷基环烷基、烷基羰基或杂芳基;或c1-c8碳原子酯、醚或酰胺;或1~24个氨基酸;或具有式(och2ch2)p或(och2ch(ch3))p的聚乙烯氧基,其中p是0-约5000的整数,或上述的组合; r1、r2、r3和r4可以任选地包含6-马来酰亚胺基己酰基(“mc”)、马来酰亚胺基丙酰基(“mp”)、缬氨酸-瓜氨酸(“val-cit”或“vc”)、丙氨酸-苯丙氨酸(“ala-phe”或“af”)、对氨基苄氧基羰基(“pab”)、4-硫戊酸酯(“spp”)、4-(n-马来酰亚胺甲基)环己烷-1羧酸酯(“mcc”)、(4-乙酰基)氨基-苯甲酸酯(“siab”)、4-硫代丁酸酯(spdb)、4-硫代-2-羟基磺酰基丁酸酯(2-磺基-spdb)或具有1-8个天然或非天然氨基酸的肽,天然氨基酸优选自天冬氨酸、谷氨酸、精氨酸、组氨酸、赖氨酸、丝氨酸、苏氨酸、天冬酰胺、谷氨酰胺、半胱氨酸、硒代半胱氨酸、酪氨酸、苯丙氨酸、甘氨酸、脯氨酸、色氨酸和丙氨酸; 另外,r1、r2、r3、r4、y1、y2、z1和z2独立地可缺省。 另一方面,本发明提供了含有2,3-二氨基琥珀酰基团的高反应活性的双连接子,如式(v)、(vi)、(vii)和(viii),细胞结合分子的两个或多个基团可以同时或依次与它们反应,形成前文式(i)、(ii)、(iii)和(iv)中的结构: 其中: 任选地是单键或双键或三键,或者可以缺省;当代表三键时,lv1和lv2同时缺省; drug1、drug2、n、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1和z2的定义与式(i)-(iv)中相同; lv1和lv2代表相同或不同的离去基团,可以与细胞结合分子上的巯基、胺、羧酸、硒醇、苯酚或羟基反应。此类离去基团包括但不限于,卤化物(例如氟化物,氯化物,溴化物和碘化物)、甲磺酰基、甲苯磺酰基、三氟甲基磺酰基、三氟甲基磺酸酯、硝基苯氧基、n-琥珀酰亚胺基(nhs)、苯氧基、二硝基苯氧基、五氟苯氧基、四氟苯氧基、三氟苯氧基、二氟苯氧基、一氟苯氧基、五氯苯氧基、1h-咪唑-1-基、一氯苯氧基、二氯苯氧基、三氯苯氧基、四氯苯氧基、n-(苯并三唑基)氧基、2-乙基-5-苯基异恶唑-3′-磺酰基、苯基恶二唑-磺酰基、2-乙基-5-苯基异恶唑基、苯基恶二唑基(oda)、恶二唑基、不饱和键(碳-碳、碳-氮、碳-硫、碳-磷、硫-氮、磷-氮、氧-氮或碳-氧之间的双键或三键),或者与mitsunobu反应的缩合试剂作用产生的中间体分子。 另一方面,本发明提供了如下列式(ix)和(x)的高反应活性的双连接子,其中细胞毒性分子的两个或多个官能团可以同时或依次与之反应形成式(i)、(ii)、(iii)或(iv)中的结构。 其中: q、n、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1和z2的定义和式(i)-(iv)中相同;lv1、lv2、lv1’以及lv2’的定义与lv1与lv2在式(v)-(viii)中的定义相同; 另一方面,本发明提供了如下式(xi)和(xii)的高反应活性的双连接子,细胞毒性分子和细胞结合分子可以独立地、同时或依次与之反应形成式(i)-(iv)中的结构: 其中x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1和z2的定义与式(i)-(iv)中相同;lv1、lv2、lv1’及lv2’的定义与lv1与lv2在式(v)-(viii)中的定义相同; 本发明还涉及制备式(i),(ii),(iii)和(iv)的细胞结合分子-药物偶联物的方法。 附图说明 图1显示了酪氨酸(tyr)和tubutyrosine(tut)类似物的合成,其在苯环上具有氨基或硝基,可与细胞结合分子双链连接。 图2显示了tubulysin类似物片段的合成。 图3显示了tubulysin类似物片段的合成。 图4显示了含有2,3-二氨基琥珀酰基的双连接子和含有具有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成。 图5显示了含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图6显示了含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图7显示了具有含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图8显示了含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联 图9显示了具有含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图10显示了具有含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图11显示了具有含有2,3-二氨基琥珀酰基双连接子的tubulysin类似物的合成及其通过抗体的一对巯基与抗体的偶联,以及澳瑞斯汀片段的合成。 图12显示了含有双连接子的澳瑞斯汀片段的合成。 图13显示了含有双连接子的澳瑞斯汀f的合成及其与抗体的偶联,以及amanitin片段和连接子的合成。 图14显示了含有双连接子的澳瑞斯汀f的合成及其与抗体的偶联。 图15显示了含有双连接子的amanitin类似物的合成。 图16显示了通过抗体上的一对巯基将含有双连接子的amanitin类似物与抗体的偶联。 图17显示了通过抗体上的一对巯基将含有双连接子的amanitin类似物与抗体的偶联。 图18显示了通过抗体的一对巯基和双连接子将tubulysin类似物和cbi二聚体类似物与抗体偶联。 图19显示了含有双连接子的cbi二聚体类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图20显示了含有双连接子的cbi二聚体类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图21显示了含有双连接子的cbi二聚体类似物的合成及其通过抗体的一对巯基与抗体的偶联。 图22显示了含有双连接子的cbi二聚体类似物的合成及其通过抗体的一对巯基与抗体的偶联,以及pbd二聚体片段的合成。 图23显示了含有双连接子的pbd二聚体的合成及其通过抗体的一对巯基与抗体的偶联。 图24显示了含有双连接子的pbd二聚体的合成及其通过抗体的一对巯基与抗体的偶联。 图25显示了含有双连接子的pbd二聚体的合成及其通过抗体的一对巯基与抗体的偶联。 图26显示了含有双连接子的pbd二聚体的合成及其通过抗体的一对巯基与抗体的偶联。 图27比较了偶联物ba-12,ba-14,ba-16,ca-03,ca-04,ca-05,ca-06,ca-07,ca-10,ca-11,ca-12和t-dm1在人胃肿瘤n87细胞模型上的抗肿瘤作用,采用pbs对照,静脉注射,一次给药3mg/kg。除了ca-06以外,所有12种偶联物均显示出抗肿瘤活性。 发明内容 定义 “烷基”是指在烷烃上除去一个或两个氢原子而产生的脂肪烃基团或单价基团。它可以是直链或是支链的,在链中含有c1-c8(1-8个碳原子)。“支链”是指直链烷基上连接有一个或多个低碳数的烷基,如甲基、乙基或丙基。示例性的烷基包括甲基、乙基、正丙基、异丙基、正丁基、叔丁基、正戊基、3-戊基、辛基、壬基、癸基、环戊基、环己基、2,2-二甲基丁基、2,3-二甲基丁基、2,2-二甲基戊基、2,3-二甲基戊基、3,3-二甲基戊基、2,3,4-三甲基戊基、3-甲基-己基、2,2-二甲基己基、2,4-二甲基己基、2,5-二甲基己基、3,5-二甲基己基、2,4-二甲基戊基、2-甲基庚基、3-甲基庚基、正庚基、异庚基、正辛基和异辛基。c1-c8烷基可以是未被取代的或被一个或多个下列基团取代,包括但不限于c1-c8烷基、-o-(c1-c8烷基)、-芳基、-c(o)r’、-oc(o)r’、-c(o)or’、-c(o)nh2,-c(o)nhr’、-c(o)n(r’)2、-nhc(o)r’、-sr’、-s(o)2r’、-s(o)r’、-oh、-卤素、-n3、-nh2、-nh(r’)、-n(r’)2和-cn;其中每个r’独立地选自于c1-c8烷基和芳基。 “卤素”指氟、氯、溴或碘原子;优选氟和氯原子。 “杂烷基”指其中1至4个碳原子独立地被选自o、s和n的杂原子所取代的c2-c8烷基。 “碳环”指含有3到8个碳原子的饱和或不饱和单环,或含有7到13个碳原子的饱和或不饱和双环。单环碳环有3到6个环原子,典型的有5或6个环原子。双环碳环有7到12个环原子,构成[4,5]、[5,5]、[5,6]或[6,6]的双环系统,或有9个或10个环原子,构成[5、6]或[6,6]的双环系统。具有代表性的c3-c8的碳环包括但不限于:-环丙基、-环丁基、-环戊基、-环戊二烯基、-环己基、-环己烯基、-1,3-环己二烯基、-1,4-环己二烯基、-环庚基、-1,3-环庚二烯基、-1,3,5-环庚三烯基、-环辛基和-环辛二烯基。 “c3-c8碳环”可以是未被取代的或被一个或多个下列基团取代,包括但不限于c1-c8烷基、-o-(c1-c8烷基)、-芳基、-c(o)r’、-oc(o)r’、-c(o)or’、-c(o)nh2、-c(o)nhr’、-c(o)n(r’)2、-nhc(o)r’、-sr’、-s(o)r’、-s(o)2r’、-oh、-卤素、-n3、-nh2、-nh(r’)、-n(r’)2及-cn;其中每个r’独立地选自c1-c8烷基和芳基。 “烯基”指含有碳-碳双键的直链或支链脂肪烃基团,链内含有2-8个碳原子。示例性的烯基包括乙烯基、丙烯基、正丁烯基、异丁烯基、3-甲基丁-2-烯基、正戊烯基、己烯基、庚烯基、辛烯基。 “炔基”指含有碳-碳三键的直链或支链脂肪烃基团,链内含有2-8个碳原子。示例性的炔基包括乙炔基、丙炔基、正丁炔基、2-丁炔基、3-甲基丁炔基、5-戊炔基、正戊炔基、己炔基、庚炔基和辛炔基。 “亚烷基”是指含1-18个碳原子的饱和的、支炼或直链或环状烃基,并带有两个通过从母体烷烃的相同或两个不同碳原子上除去两个氢原子而产生的一价自由基。典型的亚烷基包括但不限于:亚甲基(-ch2-)、1,2-乙基(-ch2ch2-)、1,3-丙基(-ch2ch2ch2-)、1,4-丁基(-ch2ch2ch2ch2-)等。 “亚烯基”指含2-18个碳原子的不饱和的、支链或直链或环状烃基,并带有通过从母体烯烃的相同或两个不同碳原子上除去两个氢原子而产生的两个一价自由基。典型的亚烯基包括但不限于:1,2-亚乙基(-ch=ch-)。 “亚炔基”指含2-18个碳原子的不饱和的、支链或直链或环状烃基,并带有通过从母体炔的相同或两个不同碳原子上除去两个氢原子而产生的两个一价自由基。典型的亚炔基包括但不限于:乙炔、炔丙基和4-戊炔基。 “芳基”或“芳香基”指由一个或多个环组成的芳香或杂芳香基团,包含三至十四个碳原子,优选六至十个碳原子。术语“杂芳香基”是指芳香基上的一个或几个碳,最优是一个、两个、三个或四个碳原子,被氧(o)、氮(n)、硅(si)、硒(se)、磷(p)或(s)所取代,优选被氧、硫和氮所取代而产生的基团。术语“芳基”或“芳香基”也指其中一个或几个氢原子独立地被-r’、卤素、-or’、-sr’、-nr’r”、-n=nr’、-n=r’、-nr’r”、-no2、-s(o)r’、-s(o)2r’、-s(o)2or’、-os(o)2or’、-pr’r”、-p(o)r’r”、-p(or’)(or”)、-p(o)(or’)(or”)或-op(o)(or’)(or”)所取代而产生的芳香基团。其中r’和r”独立地为氢、烷基、烯基、炔基、杂烷基、芳基、芳烷基、羰基或其药用盐。 “杂环”指一个环结构,其中一到四个环碳原子独立地被o、n、s、se、b、si或p等杂原子所取代。优选的杂原子是o、n和s。在《化学与物理手册》第78版的225-226页(thehandbookofchemistryandphysics,78thedition,crcpress,inc.,1997-1998,第225页至226页)上也有杂环化合物的相关描述,在此引作参考。优选的非芳基杂环包括环氧基、氮丙啶基、硫杂丙基、吡咯烷基、吡唑烷基、咪唑烷基、环氧乙烷基、四氢呋喃基、二氧戊环基、四氢吡喃基、二噁烷基、二氧戊环基、呱啶基、呱嗪基、吗啉基、吡喃基、咪唑啉基、吡咯啉基、吡唑啉基、噻唑烷基、四氢噻喃基、二噻烷基、硫代吗啉基、二氢吡喃基、四氢吡喃基、二氢吡喃基、四氢吡啶基、二氢吡啶基、四氢嘧啶基、二氢噻喃基、氮杂环庚烷基,以及上述基团与苯基缩合得到的稠环。 术语“杂芳基”或“芳基杂环”是指含3到14,优选5至10个原子的芳香性杂环、包含单环、双环或多环。示例包括吡咯基、吡啶基、吡唑基、噻吩基、嘧啶基、吡嗪基、四唑基、吲哚基、喹啉基、嘌呤基、咪唑基、噻吩基、噻唑基、苯并噻唑基、呋喃基、苯并呋喃基、1,2,4-噻二唑基、异噻唑基、三唑基、四唑基、异喹啉基、苯并噻吩基、异苯并呋喃基、吡唑基、咔唑基、苯并咪唑基、异恶唑基、吡啶基-n-氧化物,以及上述基团与苯基缩合得到的稠环。 “烷基”、“环烷基”、“烯基”、“炔基”、“芳基”、“杂芳基”、“杂环”等也指相应的去除两个氢原子而形成的“亚烷基”、“环亚烷基”、“亚烯基”、“亚炔基”等。 “芳烷基”指烷基上一个与碳原子(通常为末端或sp3碳原子)连接的氢原子被芳基取代而得到的一类非环烷基。典型的芳烷基包括芐基、2-苯基乙-1-基、2-苯基乙烯-1-基、萘基甲基、2-萘基乙-1-基、2-萘基乙-1-基、萘并芐基、2-萘基苯基-1-基等。 “杂芳烷基”指烷基上一个与碳原子(通常为末端或sp3碳原子)连接的氢原子被杂芳基取代而得到的一类非环烷基。杂芳烷基的实例有2-苯并咪唑基甲基、2-呋喃基乙基。 “羟基保护基”的实例包括甲氧基甲基醚、2-甲氧基乙氧基甲基醚、四氢吡喃基醚、芐基醚、对甲氧基芐基醚、三甲基甲硅醚、三乙基硅醚、三异丙基硅醚、叔丁基二甲基硅醚、三苯基甲基硅醚、乙酸酯、取代乙酸酯、特戊酸酯、苯甲酸酯、甲磺酸酯和对甲苯磺酸酯。 “离去基团”指可以被另一个官能团取代的官能团。这些离去基团是本领域公知的,实例包括卤化物(如氯化物、溴化物和碘化物)、甲磺酰基、对甲苯磺酰基和三氟甲磺酰基。优选的离去基团选自硝基苯氧基、n-羟基琥珀酰亚胺基(nhs)、苯氧基、二硝基苯氧基、五氟苯氧基、四氟苯氧基、二氟苯氧基、一氟苯氧基、五氯苯氧基、三氟甲磺酰基、咪唑基、氯酚基、四氯苯氧基、1-羟基苯并三唑基、甲苯磺酰基、甲磺酰基、2-乙基-5-苯基异恶唑-3′-磺酰基,酸酐或与其它酸酐作用形成的酸酐,例如乙酸酐、甲酸酐、或与多肽缩合试剂、mitsunobu反应试剂作用生成的中间体。 以下缩写为本发明所采用,其定义为:boc,叔丁氧基羰基、brop,溴代十四烷基鏻六氟磷酸盐;cdi,1,1′-羰基二咪唑;dcc,二环己基碳二亚胺;dce,二氯乙烷;dcm,二氯甲烷;dead为偶氮二甲酸二乙酯;diad,偶氮二甲酸二异丙基酯;dibal-h,二异丁基氢化铝;dipea或dea,二异丙基乙胺;depc,二乙基氰基磷酸酯;dma,n,n-二甲基乙酰胺;dmap,4-(n,n-二甲基氨基)吡啶;dmf,n,n-二甲基甲酰胺;dmso,二甲基亚砜;dtpa为二亚乙基三胺五乙酸;dtt,二硫苏糖醇;edc,1-(3-二甲基氨基丙基)-3-乙基碳二亚胺盐酸盐;esi-ms,电喷雾质谱;乙酸乙酯,etoac为乙酸乙酯;fmoc,n-(9-芴基甲氧基羰基);hatu,o-(7-氮杂苯并三唑-1-基)-n,n,n’,n’-四甲基脲六氟磷酸盐;hobt,1-羟基苯并三唑;hplc,高效液相色谱;nhs,n-羟基琥珀酰亚胺;mecn为乙腈;meoh为甲醇;mmp,4-甲基吗啉;pab,对氨基苯甲酸;pbs,磷酸盐缓冲液(ph7.0-7.5);ph,为苯基;phe为l-苯丙氨酸;pybrop为溴-三-吡咯烷-鏻六氟磷酸盐;peg,聚乙二醇;sec,尺寸排阻色谱;tcep,三(2-羧乙基)膦;tfa,三氟乙酸;thf,四氢呋喃;val,缬氨酸;tl为薄层色谱;uv为紫外线。 “氨基酸”可以是天然或非天然的,优选α-氨基酸。天然氨基酸由基因所编码,包括丙氨酸、精氨酸、天冬酰胺、天冬氨酸、半胱氨酸、谷氨酸、谷氨酰胺、甘氨酸、组氨酸、异亮氨酸、亮氨酸、赖氨酸、蛋氨酸、苯丙氨酸、脯氨酸、丝氨酸、苏氨酸、酪氨酸、色氨酸和缬氨酸。非天然氨基酸是蛋白质氨基酸的衍生物,包括羟脯氨酸、羊毛硫氨酸、2-氨基异丁酸、脱氢丙氨酸、γ-氨基丁酸(神经递质)、鸟氨酸、瓜氨酸、β-丙氨酸(3-氨基丙酸)、γ-羧基谷氨酸、硒代半胱氨酸(存在于许多非真核以及大多数真核细胞中、但不是由dna直接进行编码)、吡咯赖氨酸(仅在一些古细菌和一种细菌中发现)、n-甲酰基甲硫氨酸(通常是细菌、线粒体和叶绿体中蛋白质中最初的氨基酸)、5-羟色氨酸、l-二羟基苯丙氨酸、三碘甲腺原氨酸、l-3,4-二羟基苯丙氨酸(dopa)和o-磷酸丝氨酸。术语“氨基酸”还包括氨基酸类似物和模拟物。类似物是具有与天然氨基酸相同结构通式h2n(r)chco2h的化合物,其中r在天然氨基酸里未能发现。类似物的实例包括高丝氨酸、正亮氨酸、甲硫氨酸-亚砜和甲硫氨酸甲基锍。更优的是氨基酸模拟物,它是具有与α-氨基酸的化学结构不同、但是功能类似的化合物。天然氨基酸多为“l”立体化学构型,“非天然氨基酸”为“d”构型的氨基酸。在本专利申请中使用1至8个氨基酸时、其序列优选为蛋白水解酶可识别的序列。许多水解酶可识别序列是本领域已知的,可以参见:matayoshi等,science247:954(1990);dunn等,meth.enzymol.241:254(1994);seidah等,meth.enzymol.244:175(1994);thornberry,meth.enzymol.244:615(1994);weber等,meth.enzymol.244:595(1994);smith等,meth.enzymol.244:412(1994)及bouvier等,meth.enzymol.248:614(1995);此处引作参考。特别是选自以下序列:val-cit、ala-val、ala-ala、val-val、val-ala-val、lys-lys、ala-asn-val、val-leu-lys、cit-cit、val-lys、ala-ala-asn、asp-lys、asp-glu、glu-lys、lys、cit、ser及glu。 “糖苷”是糖通过糖苷键在其异头碳上与另一基团键合得到的分子。糖苷可以通过o-、n-、s-或c-糖苷键连接,分别产生o-糖苷、糖基胺、硫代糖苷和c-糖苷。其结构式为cm(h2o)n(其中m可以不同于n,m、n<36)。本发明中的糖苷包括葡萄糖(右旋糖)、果糖(左旋糖)、阿洛糖、阿卓糖、甘露糖、古洛糖、艾杜糖、半乳糖、塔罗糖、半乳糖胺、氨基葡萄糖、唾液酸、n-乙酰氨基葡萄糖、磺基奎诺糖(6-脱氧-6-磺基-d-吡喃葡萄糖)、核糖、阿拉伯糖、木糖、来苏糖、山梨糖醇、甘露醇、蔗糖、乳糖、麦芽糖、海藻糖、麦芽糖糊精、棉子糖、葡萄糖醛酸(葡糖苷酸)和水苏糖。它可以是d或l的构型、5原子环状呋喃糖的形式、6原子环状吡喃糖的形式,或是非环形式、α-异构体(异头碳的-oh在haworth投影碳原子平面之下)、或β-异构体(异头碳的-oh在haworth投影碳原子平面之上),包括单糖、二糖、多醇或含3-6个糖单的低聚糖。 本发明申请中的“抗体”指全长免疫球蛋白分子或全长免疫球蛋白分子的免疫活性部分,如含有抗原结合位点的分子,该结合位点免疫特异性地与靶标抗原或部分靶标抗原结合,靶标包括但不限于,癌细胞或产生与自身免疫疾病相关的自免疫抗体的细胞。本发明中的免疫球蛋白可以是免疫球蛋白的任何类型(例如igg、ige、igm、igd、iga和igy)、类别(例如igg1、igg2、igg3、igg4、iga1和iga2)或子类。免疫球蛋白可以来自任何物种,但优选的免疫球蛋白来源于人、鼠或兔。本发明的抗体优选是单克隆抗体,包括但不限于多克隆、单克隆、双特异性、人、人源化或嵌合抗体,单链抗体,fv、fab片段、f(ab’)片段、f(ab’)2片段、由fab表达库产生的片段,抗独特型(抗id)抗体,cdr和任何能免疫特异性地结合癌细胞抗原、病毒抗原或微生物抗原的上述结构的表位结合片段。 “对映异构体”,也称为“光学异构体”,是两个立体异构体中的一个,它们是彼此的镜像,不可重迭(不等同),就像人的左右手,除非沿着某一平面被翻转,它们是不可重迭的(仅通过改变方向不能让双手重迭)。化合物中的单个手性原子或类似的结构特征使得该化合物具有两种可能的结构,它们不可重迭,是彼此的镜像。在某一化合物中存在的多个手性特征增加了可能存在的构型的数目,其中可能会有一些互为镜像。对映体纯的化合物是指在检测方法的能力范围内,仅具有同一种手性的样品。在对称的环境中,两个对映体可以使平面偏振光(+/-)在相反的方向上等量旋转(偏振光可以被认为是不对称的介质),除此之外,它们具有相同的化学性质和物理性质。由于这个原因,它们有时也被称为光学异构体。光学异构体及其等量的对映体的混合物被称为外消旋体,它对平面偏振光无净旋转,因为每个正旋转(+)都被负旋转(-)完全抵消。通常两个对映异构体与其他的对映异构体物质发生不同的化学反应。由于许多生物分子是对映体,因此有时两种对映体对生物有机体的影响存在显著差异。例如,在药物中,通常只有一种对映体可以发生想要的生理作用,而另一种对映体或是活性较低、或无活性,有时甚至产生不良反应。基于这样的发现,可以开发仅由一种对映体(“对映体纯”)组成的药物以增强药理学效力,有时还可以消除一些副作用。 同位素是特定化学素的质子数相同,中子数不同的不同核素。同一素的所有同位素具有相同数量的质子。一个原子序数指定一个特定的素,但非同位素;特定素原子可以有不同的中子数。核子(质子和中子)的数量是原子的质量数,特定素的每个同位素具有不同的质量数。例如、碳-12、碳-13和碳-14是碳素的三种同位素,质量数分别为12,13和14。碳的原子序数为6,意味着每个碳原子都有6个质子,因此这些同位素的中子数分别为6、7和8。氢原子有三种同位素:氕(1h)、氘(2h)和氚(3h),氘的质量是氕的两倍,氚的质量是氕的三倍。通过动力学同位素效应,同位素替代实验可用于确定化学反应的机理。同位素替代实验还可用于研究外源化合物通过吸收和分布机制进入体内后,身体如何对它产生作用,体内物质的代谢变化(例如通过细胞色素p450或葡萄糖醛酸转移酶等代谢酶的作用),以及药物代谢产物的排泄途径,是为药代动力学(pk)研究。同位素替代实验可用于研究药物的生化和生理作用,包括在动物(包括人类)、微生物或生物组合上所显现出来的作用(例如感染),是为药效学(pd)研究。两者(pk和pd)一起决定药物的剂量、益处及副作用。同位素可以采用一种稳定的(非放射性的)或非稳定的素。药物的同位素取代物还可能具有与原始药物不同的治疗功效。 “药学上”或“药学上可接受的”是指当分子实体和组合物酌情施用于动物或人时,不会产生不利、过敏或其他不良反应。 “药学上可接受的溶剂化物”或“溶剂化物”是指一种或多种溶剂分子与本发明公开的化合物的结合物。形成药学上可接受的溶剂合物的溶剂的实例,包括但不限于水、异丙醇、乙醇、甲醇、dmso、乙酸乙酯、乙酸和乙醇胺。 “药学上可接受的辅料”包括任何载体、稀释剂、佐剂或其它介质,例如防腐剂或抗氧化剂、填充剂、崩解剂、润湿剂、乳化剂、悬浮剂、溶剂、分散介质、包衣剂、抗细菌剂和抗真菌剂、等渗剂和吸收延迟剂等。这些介质和药剂与药物活性物质一起使用在本领域内是熟知的。任何传统介质或药剂,除非与活性成分不兼容,也可以考虑将其用于治疗组合物中。补充活性成分也可以加入组合物中,成为合适的治疗组合。 本发明中,“药用盐”是指此处公开化合物的衍生物,是母体化合物的酸盐或碱盐。药学上可接受的盐包括由无毒无机酸或有机酸与母体化合物形成的常规无毒盐或季铵盐。例如,所述常规无毒盐包括衍生自无机酸(例如盐酸、氢溴酸、硫酸、氨基磺酸、磷酸、硝酸等)的盐;以及由有机酸,例如乙酸、丙酸、琥珀酸、酒石酸、柠檬酸、甲磺酸、苯磺酸、葡萄糖醛酸、谷氨酸、苯甲酸、水杨酸、甲苯磺酸、草酸、富马酸、马来酸及乳酸等制备的盐。另外的盐包括铵盐,如三甲胺、葡甲胺、丙三醇等的盐、金属盐、如钠、钾、钙、锌或镁盐。 本发明中的药用盐可以从包含酸性或碱性片段的母体化合物,用常规的化学方法制成。一般地说,这些盐可以通过在本发明化合物的游离酸或碱的水溶液或有机溶液或两者的混合溶液中,加入其它适当的等当量的碱或酸而形成。非水相的反应介质一般为乙醚,乙酸乙酯,乙醇,异丙醇或者乙腈。可以适用盐的列表可参见《remington’spharmaceuticalsciences》,第17版,mackpublishingcompany,easton,pa,1985,第1418页。 “施用”或“给药”是指以任何方式向受试者转移、递送、引入或运输药物或其他药剂。这些方式包括口服用药、局部接触、静脉内、腹膜内、肌肉内、病灶内、鼻内、皮下或鞘内给药。本发明还考虑使用装置或器械来施用药剂。这种装置可以使用主动或被动型传输,而且可以是缓释或快速释放递送装置。 “治疗有效量”是指有效预防或治疗本文提及的病理状况的,本发明化合物/药物的量。 术语“患者”或“受试者”指受到或可能受到本文所述病理状况影响的动物或人。优选地,患者是人类。 就癌症而言,术语“治疗”包括以下任何一项或全部:阻止肿瘤细胞或癌细胞生长、复制,减轻整体肿瘤量,以及改善与该疾病相关的一个或多个症状。 就自身免疫性疾病而言,术语“治疗”包括以下任一项或全部:阻止与自身免疫性疾病相关的细胞的复制,包括但不限于能够产生自身免疫性抗体的细胞,减轻自身免疫性抗体量和改善自身免疫性疾病的一个或多个症状。 就传染病而言、术语“治疗”包括以下任何一项或全部:阻止引起传染病的病原体的生长、增殖或复制、以及改善传染病的一个或多个症状。 “哺乳动物”或“动物”的实例包括但不限于人、鼠、家鼠、豚鼠、猴、猪、山羊、牛、马、狗、猫、鸟和家禽。 术语“化合物”,“细胞毒剂”,“细胞毒性化合物”,“细胞毒性二聚体”和“细胞毒性二聚体化合物”可互换使用,包括本发明中或参考文献中公开的结构、结构式代表的结构或其衍生物。该术语还包括本发明中公开的化合物的立体异构体、几何异构体、互变异构体、溶剂化物、代谢产物、盐(例如药学上可接受的盐)和前药以及它们的盐。还包括任何上述结构的溶剂化物、水合物和多晶型物。本发明中在某些方面具体列举“立体异构体”、“几何异构体”、“互变异构体”、“溶剂化物”、“代谢物”、“盐”、“前药”、“前药盐”、“偶联物”、“偶联物的盐”、“溶剂化物”、“水合物”或“多晶型物”,不应据此认为,若在本发明的其他方面仅仅使用术语“化合物”,而未列举上述术语时,是有意省略这些形式。 术语“亚胺反应性试剂”是指能够与亚胺基反应的试剂。亚胺反应性试剂的实例包括但不限于亚硫酸盐(h2so3,h2so2或hso3-,so32-,hso2-与阳离子形成的盐),焦亚硫酸盐(h2s2o5或s2o52-与阳离子形成的盐),单,二,三和四硫代磷酸酯(po3sh3、po2s2h3、pos3h3、ps4h3或po3s3-、po2s23-、pos33-、ps43-与阳离子形成的盐),硫代磷酸酯((r5o)2ps(or5)、r5sh、r5soh、r5so2h、r5so3h),各种胺(羟胺(nh2oh)、肼(nh2nh2)、nh2or5、r5nhr5’、nh2r5),nh2-co-nh2、nh2-c(=s)-nh2、硫代硫酸盐(h2s2o3或s2o32-与阳离子形成的盐)、连二亚硫酸盐(h2s2o4或s2o42-与阳离子形成的盐)、二硫代磷酸酯(p(=s)(or5)(sh)(oh)或与阳离子形成的盐)、异羟肟酸(r5c(=o)nhoh或与阳离子形成的盐)、酰肼(r5conhnh2)、甲醛次硫酸盐(hoch2so2h或hoch2so2-与阳离子形成的盐,例如hoch2so2-na+)、糖化核苷酸(例如gdp-甘露糖)、fludarabine或它们的混合物,其中r5和r5’都独立地为具有1至8个碳原子的直链或支链烷基、并被至少一个选自-–n(r5)(r5’)、-co2h、-so3h、和-po3h的取代基取代;r5和r5’可以进一步可选地被本文所述烷基取代基取代;优选地,阳离子是单价阳离子,例如na+或k+。优选地,亚胺反应性试剂选自亚硫酸盐、羟胺、尿素和肼。更优选地,亚胺反应性试剂是nahso3或khso3. “细胞结合剂”或“细胞结合分子”可以是目前已知的或将成为已知的分子,包括肽和非肽。通常,它们可以是抗体(尤其是单克隆抗体)或包含至少一个结合位点的抗体片段、淋巴因子、激素、生长因子、营养转运分子(例如转铁蛋白),或任何其他细胞结合分子或物质(例如维生素)。 可以使用的细胞结合剂的更具体的例子包括:单克隆抗体、单链抗体、抗体的片段,例如fab、fab’、f(ab’)2、fv(parham,j.immunol.131,2895-2902(1983);spring等,j.immunol.,113,470-478(1974);nisonoff等,arch.biochem.biophys.,89,230-244(1960))、fab表达文库产生的片段、抗独特型(anti-id)抗体、cdr、以上任一项的可以其免疫特异性结合癌细胞抗原、病毒抗原或微生物抗原的表位结合片段;干扰素;肽;淋巴因子如il-2、il-3、il-4、il-6;激素,例如胰岛素、trh(促甲状腺激素释放激素)、msh(促黑素细胞刺激激素)、类固醇激素,例如雄激素和雌激素;生长因子和集落刺激因子,例如egf、tgfα、胰岛素样生长因子(igf-i、igf-ii)、g-csf、m-csf和gm-csf(burgess,immunologytoday,5,155-158(1984));维生素,例如叶酸;转铁蛋白(o’keefe等,j.biol.chem.,260,932-937(1985))。 利用单克隆抗体技术可以生产极具选择性的细胞结合剂,特异性的单克隆抗体。在本领域中众所周知的产生单克隆抗体技术是,通过用感兴趣的抗原,例如完整的靶细胞,从靶细胞,全病毒,灭火全病毒,病毒蛋白,如病毒外壳蛋白等分离的抗原,来免疫小鼠,大鼠,仓鼠或任何其他哺乳动物而产生。合适的细胞结合剂的选择是取决于待靶向的特定细胞群,但是通常,如果可以获得合适的单克隆抗体,则优选单克隆抗体。 本专利公开了新型双连接子偶联物,其中的连接子及其合成实例如图1至26和实施例所示。 一种含2,3-二氨基琥珀酰基双链接的细胞结合剂和细胞毒性分子的偶联物 双链接偶联物如结构式(i),(ii),(iii)或(iv)所示: 或其光学异构体、外消旋体、非对映体或对映体; 其中 代表单键; 代表可选为单键或可以缺省; 代表可选为单键,双键,或者可以缺省;n独立地为1到30; q是连接到r3和r4的细胞结合剂/分子,可以是目前已知的,或者即将成为已知的任何种类的分子,可与具有治疗意义或生物学修饰的细胞群的片段结合,复合或反应。优选地,细胞结合剂/分子是免疫治疗蛋白,抗体,单链抗体;与靶细胞结合的抗体片段;单克隆抗体;单链单克隆抗体;或结合靶细胞的单克隆抗体片段;嵌合抗体;与靶细胞结合的嵌合抗体片段;域抗体;与靶细胞结合的域抗体片段;模拟抗体的adnectins;darpins;淋巴因子;激素;维生素;增长因子;集落刺激因子;或营养转运分子(转铁蛋白);含超过四个氨基酸的结合肽,或蛋白质,或抗体,或附着在白蛋白,聚合物,树枝状大分子,脂质体,纳米颗粒,囊泡或(病毒)衣壳上的小的细胞结合分子或配体; drug1或/和drug2是细胞毒性分子/药剂是治疗药物/分子/试剂,或免疫治疗蛋白质/分子,或用于增强细胞结合或稳定细胞结合剂的功能分子,或细胞表面受体结合配体,或抑制细胞增殖分子;或用于监测,检测或研究细胞结合作用的分子。它也可以是免疫治疗化合物、化学治疗化合物的类似物或前药,或药学上可接受的盐,水合物或水合盐,或晶体,或光学异构体,外消旋体,非对映异构体或对映异构体,抗体(probody)或抗体(probody)片段,或sirna、dna分子,或细胞表面结合配体; 优选地,细胞毒性分子是许多小分子药物中的任何一种,包括但不限于tubulysins、卡奇霉素、澳瑞斯汀、美登素、cc-1065类似物、吗啉代多柔比星、紫杉烷、cryptophycins、鹅膏毒素(例如amanitins)、埃坡霉素、艾日布林、格尔德霉素、喜树碱(例如sn-38)、多卡霉素、道诺霉素、甲氨蝶呤、长春地辛、长春新碱和苯并二氮杂卓二聚体(例如吡咯并苯并二氮杂卓(pbd)、托马霉素、吲哚啉并苯并二氮杂卓、咪唑并噻二氮杂卓或恶唑烷并苯并二氮杂卓的二聚体); x1和x2相同或不同,独立地选自nh、nhnh、n(r1)、n(r1)n(r2)、o、s、s-s、o-nh、o-n(r1)、ch2-nh、ch2-n(r1)、ch=nh、ch=n(r1)、s(o)、s(o2)、p(o)(oh)、s(o)nh、s(o2)nh、p(o)(oh)nh、nhs(o)nh、nhs(o2)nh、nhp(o)(oh)nh、n(r1)s(o)n(r2)、n(r1)s(o2)n(r2)、n(r1)p(o)(oh)n(r2)、os(o)nh、os(o2)nh、op(o)(oh)nh、c(o)、c(nh)、c(nr1)、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)nh、oc(nh)nh、oc(nr1)nh、nhc(o)nh、nhc(nh)nh、nhc(nr1)nh、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)n(r1)、oc(nh)n(r1)、oc(nr1)n(r1)、nhc(o)n(r1)、nhc(nh)n(r1)、nhc(nr1)n(r1)、n(r1)c(o)n(r1)、n(r1)c(nh)n(r1)、n(r1)c(nr1)n(r1);或c1-c6烷基;c2-c8烯基、杂烷基、烷基环烷基或杂环烷基;c3-c8芳基、芳烷基、杂环、碳环、环烷基、杂烷基环烷基、烷基羰基或杂芳基; y1、y2、z1和z2是相同或不同的官能团,独立地通过二硫化物,硫醚,硫酯,肽,腙,醚,酯,氨基甲酸酯,碳酸酯,胺(二级,三级或四级),亚胺,环杂烷基,杂芳基,烷氧基或酰胺键,连接至细胞结合分子q;优选地,y1、y2、z1和z2独立地具有以下结构:c(o)ch、c(o)c、c(o)ch2、arch2、c(o)、nh、nhnh、n(r1)、n(r1)n(r2)、o、s、s-s、o-nh、o-n(r1)、ch2-nh.ch2-n(r1)、ch=nh、ch=n(r1)、s(o)、s(o2)、p(o)(oh)、s(o)nh、s(o2)nh、p(o)(oh)nh、nhs(o)nh、nhs(o2)nh、nhp(o)(oh)nh、n(r1)s(o)n(r2)、n(r1)s(o2)n(r2)、n(r1)p(o)(oh)n(r2)、os(o)nh、os(o2)nh、op(o)(oh)nh、c(o)、c(nh)、c(nr1)、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)nh、oc(nh)nh;oc(nr1)nh、nhc(o)nh、nhc(nh)nh、nhc(nr1)nh、c(o)nh、c(nr1)nh、oc(o)n(r1)、oc(nh)n(r1)、oc(nr1)n(r1)、nhc(o)n(r1)、nhc(nh)n(r1)、nhc(nr1)n(r1)、n(r1)c(o)n(r1)、n(r1)c(nh)n(r1)、n(r1)c(nr1)n(r1);或c1-c8烷基、c2-c8杂烷基、烷基环烷基、杂环烷基;c3-c8芳基、芳烷基、杂环、碳环、环烷基、杂环烷基、烷基羰基、杂芳基; 优选地,y1、y2、z1和z2连接到细胞结合剂/分子的巯基对上。巯基优选地是通过选自二硫苏糖醇(dtt)、二硫代三甘醇(dte)、l-谷胱甘肽(gsh)、三(2-羧乙基)磷化氢(tcep)、2-巯基乙胺(β-mea)或/和β-巯基乙醇(β-me,2-me)的还原剂将细胞结合剂的链间二硫键还原而生成的成对硫原子; r1、r2、r3和r4是包含c,n,o,s,si和p原子的链状结构,最优含0-500个原子,共价连接x和z1,y和z2。r1、r2、r3和r4中的各个原子以所有可能的化学方式结合,比如形成亚烷基,亚烯基和亚炔基,醚,聚氧化烯,酯,胺,亚胺,多胺,肼,腙,酰胺,脲,氨基脲,卡巴肼,烷氧胺,氨基甲酸酯,氨基酸,肽,酰氧基胺,异羟肟酸,或上述组合。优选地,r1、r2、r3和r4相同或不同,独立地选自o、nh、s、nhnh、n(r5)、n(r3)n(r3’)、如式(och2ch2)por5、(och2ch-(ch3))por5、nh(ch2ch2o)pr5、nh(ch2ch(ch3)o)pr5、n[(ch2ch2o)pr5]-[(ch2ch2o)p’r5’]、(och2ch2)pcoor5、ch2ch2(och2ch2)pcoor5的聚乙烯氧基单,其中p和p’独立地是选自0至约1000的整数,或上述的组合;c1-c8烷基;c2-c8杂烷基,烷基环烷基,杂环烷基;c3-c8芳基,芳烷基,杂环,碳环,环烷基,杂烷基环烷基,烷基羰基或杂芳基; 更优选的r1、r2、r3、r4、r5和r5’独立地为h、c1-c8烷基、c2-c8杂烷基、烷基环烷基或杂环烷基、c3-c8芳基、芳烷基、杂环、碳环、杂烷基环烷基、烷基羰基或杂芳基;或c2-c8酯、醚或酰胺;或1~24氨基酸;或结构式为(och2ch2)p或(och2ch(ch3))p的聚乙烯氧基单,其中p是0到约5000的整数,或上述组合; r1、r2、r3和r4可任选地由下列一个或多个连接子组分构成:6-马来酰亚胺基己酰基(“mc”)、马来酰亚胺丙酰基(“mp”)、缬氨酸-瓜氨酸(“val-cit”或“vc”)、丙氨酸-苯丙氨酸(“ala-phe”或“af”)、对氨基芐氧基-羰基(“pab”)、4-硫代戊酰基(“spp”)、4-(n-马来酰亚胺甲基)环己烷-1酰基(“mcc”)、(4-乙酰基)氨基苯酰基(“siab”)、4-硫丁酰基(spdb)、4-硫-2-羟基磺酰基-丁酰基(2-sulfo-spdb),或含有1-8个天然或非天然氨基酸单的天然或非天然肽。天然氨基酸最优选自天冬氨酸、谷氨酸、精氨酸、组氨酸、赖氨酸、丝氨酸、苏氨酸、天冬酰胺、谷氨酰胺、半胱氨酸、硒代半胱氨酸、酪氨酸、苯丙氨酸、甘氨酸、脯氨酸、色氨酸和丙氨酸; 此外,r1、r2、r3和r4独立地可包含以下亲水结构之一: 其中是连接位点;x3、x4、x5、x6和x7独立地选自nh、nhnh、n(r5)、n(r5)n(r5’)、o、s、c1-c6烷基、c2-c6杂烷基、烷基环烷基或杂环烷基、c3-c8芳基、芳烷基、杂环、碳环、环烷基、杂环烷基、烷基羰基、杂芳基、或1~8个氨基酸;其中r5和r5’独立地为h、c1-c8烷基、c2-c8杂烷基、烷基环烷基或杂环烷基、c3-c8芳基、芳烷基、杂环、碳环、杂环烷基、烷基羰基或杂芳基、c1-c8酯、醚或酰胺;或具有式(och2ch2)p或(och2ch(ch3))p的聚乙烯氧基,其中p是0到约5000的整数,或其组合; r1、r2、r3、r4、y1、y2、z1和z2独立地可以含有自我毁灭或非自我毁灭的组分,肽单、腙键、二硫化物、酯、肟、酰胺或硫醚键。自我毁灭单包括但不限于,与对氨基芐基氨甲酰基(pab)电子结构相似的芳香化合物,例如2-氨基咪唑-5-甲醇的衍生物、杂环pab类似物、β-葡糖苷酸、以及邻或对氨基芐基缩醛; 优选地,自我毁灭型连接子组分具有以下结构之一: 其中(*)标记的原子是另外的间隔体或可断裂连接子单、或细胞毒性剂和/或结合分子(cba)的连接点;x1、y1、z2和z3独立地为nh、o或s;z1独立地为h、nhr5、or1、sr5、cox1r5,其中x1和r5如前文所定义;v为0或1;u1独立地为h、oh、c1-c6烷基,(och2ch2)n、f、cl、br、i、or5、sr5、nr5r5’、n=nr5、n=nr5、n=r5、nr5r5’、no2、sor5r5’、so2r5、so3r5、so3r5、oso3r5、oso3r5、pr5r5’、po5r5’、po2r5r5’、opo(or5)(or5′)或och2po(or5(or5(or5′)、其中,其中,r5和r5’独立选自h、c1-c8烷基、c2-c8烷基,烯基、杂烷基或氨基酸;c3-c8芳基、烷基、烷基、烷基、或氨基酸;c3-c8芳基、杂环、碳环、环烷基、杂环烷基、杂芳烷基、烷基羰基或糖苷;或药用阳离子盐;; 非自我毁灭型连接子组分具有以下结构之一: 其中(*)标记的原子是另外的间隔体或可释放的连接子单、或细胞毒性剂和/或结合分子的连接点;x1、y1、u1、r5、r5’如前文所定义;r为0~100;m和n独立地为0~6; 进一步优选地,r1、r2、r3和r4独立地包含可释放的连接子组分。术语“可释放的”是指连接子上包含至少一个可在生理条件下被破坏的键,例如ph、酸、碱、氧化作用、代谢、生化或酶不稳定的键。应当理解,导致键断裂不一定是生物或代谢过程、而可能是一个标准化学反应、例如水解或取代反应,这种生理条件的例子有:ph值比细胞浆内ph低的内涵体,恶性细胞内存在的毫摩尔浓度的大量谷胱甘肽(与细胞内巯基发生二硫键交换反应); 可释放连接子组分r1、r2、r3和r4的实例包括但不限于: -(cr5r6)m(aa)r(cr7r8)n(och2ch2)t-、(cr5r6)m(cr7r8)n(aa)r(och2ch2)t-、(aa)r-(cr5r6)m(cr7r8)n(och2ch2)t-、(cr5r6)m(cr7r8)n(och2ch2)r(aa)t-、-(cr5r6)m-(cr7=cr8)(cr9r10)n(aa)t(och2ch2)r-、-(cr5r6)m(nr11co)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m(aa)t(nr11co)(cr9r10)n(och2ch2)r-、-(cr5r6)m(oco)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、-(cr5r6)m(co)(aa)t-(cr9r10)n(och2ch2)r-、-(cr5r6)m(nr11co)(aa)t(cr9r10)n(och2ch2)r-、-(cr5r6)m-(oco)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、-(cr5r6)m(co)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m-苯基co(aa)t(cr7r8)n-、-(cr5r6)m-呋喃co(aa)t(cr7r8)n-、-(cr5r6)m-恶唑co(aa)t(cr7r8)n-、-(cr5r6)m-噻唑基co(aa)t(ccr7r8)n-、-(cr5r6)t-噻吩co(cr7r8)n-、-(cr5r6)t-咪唑co-(cr7r8)n-、-(cr5r6)t-吗啉co(aa)t-(cr7r8)n-、-(cr5r6)t哌嗪-co(aa)t-(cr7r8)n-、-(cr5r6)t-n甲基co(aa)t-(cr7r8)n-、-(cr5r)m-(aa)t苯基-、-(cr5r6)m-(aa)t呋喃、-(cr5r6)m-恶唑(aa)t、-(cr5r6)m-噻唑基(aa)t、-(cr5r6)m-噻吩-(aa)t-、-(cr5r6)m-咪唑(aa)t-、-(cr5r6)m-吗啉(aa)t-、-(cr5r6)m-哌嗪(aa)t-、-(cr5r6)m-n甲基哌嗪(aa)t-、k(cr5r6)m(aa)r(cr7r8)n(och2ch2)t-、k(cr5r6)m(cr7r8)n(aa)r(och2ch2)t-、k(aa)r-(cr5r6)m(cr7r8)n(och2ch2)t-、k(cr5r6)m(cr7r8)n(och2ch2)r(aa)t-、k(cr5r6)m-(cr7=cr8)(cr9r10)n(aa)t(och2ch2)r-、k(cr5r6)m(nr11co)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m(aa)t(nr11co)(cr9r10)n(och2ch2)r-、k(cr5r6)m(oco)(aa)t(cr9r10)n-(och2ch2)r-、k(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m(co)(aa)t-(cr9r10)n(och2ch2)r-、k(cr5r6)m(nr11co)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m-(oco)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、k-(cr5r6)m(co)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m-苯基co(aa)t(cr7r8)n-、k-(cr5r6)m-呋喃co(aa)t-(cr7r8)n-、k(cr5r6)m-恶唑co(aa)t(cr7r8)n-、k(cr5r6)m-噻唑基co(aa)t-(cr7r8)n-、k(cr5r6)t-噻吩co(cr7r8)n-、k(cr5r6)t咪唑-co-(cr7r8)n-、k(cr5r6)t吗啉co(aa)t(cr7r8)n-、k(cr5r6)t哌嗪-co(aa)t-(cr7r8)n-、k(cr5r6)t-n甲基co(aa)t(cr7r8)n-、k(cr5r)m(aa)t苯基、k-(cr5r6)m-(aa)t呋喃-、-k(cr5r6)m-恶唑(aa)t-、k(cr5r6)m-噻唑基(aa)t-、k(cr5r6)m-噻吩-(aa)t-、k(cr5r6)m-咪唑(aa)t-、k(cr5r6)m-吗啉(aa)t-、k(cr5r6)m-哌嗪(aa)t-、k(cr5r6)mn甲基哌嗪(aa)t-;其中aa、m和n定义如前文所描述;t和r独立地为0-100;r3、r4、r5、r6、r7和r8独立地选自h、卤化物、c1-c8烷基、c2-c8芳基、烯基、炔基、醚、酯、胺或酰胺,这些基团均可以被以下基团所取代:一个或多个卤素、cn、nr1r2、cf3、or1、芳基、杂环、s(o)r1、so2r1、-co2h、-so3h、-or1、-co2r1、-conr1、-po2r1r2、-po3h或p(o)r1r2r3;k是nr1、-ss-、-c(=o)-、-c(=o)nh-、-c(=o)o-、-c=nh-o-、-c=n-nh-、-c(=o)nh-nh-、o、s、se、b、het(c3-c8杂环或杂芳环),或含有1-20个相同或不同氨基酸的肽。 更优选地,r1、r2、r3和r4独立地为具有1-18个碳原子的直链烷基,或具有式(och2ch2)p的聚乙烯氧基单,p=1~5000,或含有1~20个氨基酸单(l或d形式)的肽,或上述组合。 此外,y1、y2、r1、r2、r3、r4、z1或z2可独立地由以下一个或多个组分构成: 6-马来酰亚胺己酰胺基(mc)、马来酰亚胺基丙酰胺基(mp)、硫代马来酰胺基、硫代氨基氧代丁酸、硫代氨基氧代丁烯酸、缬氨酸瓜氨酸(val-cit)、丙氨酸苯丙氨酸(ala-phe)、赖氨酸苯丙氨酸(lys-phe)、赖氨酸丙氨酸(lys-ala),p-对氨基苄氧羰基(pab)、4-硫代戊酰基(spp)、4-硫代丁酰基(spdb),4-(n-马来酰亚胺甲基)环已烷基-1-酰基(mcc)、马来酰亚胺乙胺基(me)、4-硫代-2-羟基磺酰基丁酰基(2-磺酰-spdb)、芳基硫基(pys),(4-乙酰基)氨基苯甲酰基(siab)、氧基苄基硫基、氨基苄基硫基、二氧基苄硫基、二氨基苄硫基、氨基氧基苄硫基、烷氧基氨基(aoa)、亚乙基氧基(eo)、4-甲基-4-二硫代戊酰基(mpdp)三唑、二硫代、烷基磺酰基、烷基磺酰胺基、磺胺双酰胺基、磷酸二酰胺基、烷基膦酰胺酸基、次膦酸基、n-甲基烷基膦酰胺酸基、n,n’-二甲基膦酰胺酸基、烷基二膦酰胺基,肼、乙酰亚胺;肟、乙酰乙酰肼、氨基乙胺、氨基乙基-氨基乙基胺,和l-或d-,或含有1-20个氨基酸的天然或非天然肽;其中原子中间的连接键意味着它可以连接相邻的碳原子键;其中波浪线指另外键连接的位点; 或者,y1、y2、r1、r2、r3、r4、z1或z2可以独立地缺省,但是y1、y2、r1、r2、r3、r4、z1和z2不可以同时缺省。 优选地,式(i)、(ii)、(iii)和(iv)的立体异构体可由下列式(ia)、(ib)、(ic)、(iia)、(iib)、(iic)、(iva)、(ivb)和(ivc)表示: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、drug1和drug2与前文定义相同。 优选地,双连接偶联物用以下式(i-01)、(i-02)、(i-03)、(i-04)、(i-05)、(i-06)、(i-07)、(i-08)、(i-09)、(i-10)、(i-11)、(i-12)、(i-13)、(i-14)、(i-15)、(i-16)、(i-17)、(i-18)、(i-19)、(i-20)、(i-21)、(i-22)、(i-23)、(ii-01)、(ii-02)、(ii-03)、(ii-04)、(ii-05)、(ii-06)、(ii-07)、(ii-08)、(ii-09)、(ii-10)、(ii-11)、(ii-12)、(ii-13)、(ii-14)、(ii-15)、(ii-16)、(ii-17)、(ii-18)、(iii-01)、(iii-02)、(iii-03)、(iii-04)、(iii-05)、(iii-06)、(iii-07)、(iii-08)、(iii-09)、(iii-10)、(iii-11)、(iii-12)、(iii-13)、(iii-14)、(iii-15)、(iii-16)、(iii-17)、(iii-18)、(iii-19)、(iii-20)、(iv-01)、(iv-02)、(iv-03)、(iv-04)、(iv-05)、(iv-06)、(iv-07)、(iv-08)、(iv-09)、(iv-10)、(iv-11)、(iv-12)、(iv-13)、(iv-14)、(iv-15)、(iv-16)、(iv-17)、(iv-18)、(iv-19)、和(iv-20)所表示: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、drug1和drug2的定义如前文所述。此外,drug1和drug2中的一个独立地可以缺省,但不能同时缺省。 以含有2,3-二氨基琥珀酰基的连接子双链接的药物和细胞结合分子偶联物的制备 以双链连接药物和细胞结合分子的偶联物的制备途径,示于图1-46和实施例中。 另一方面,本发明提供了含有以下2,3-二氨基琥珀酰基的式(v),(vi),(vii)和(viii)的易于反应的双连接子,其中细胞结合的两个或更多个残基分子可以同时或顺序反应形成上述式(i),(ii),(iii)和(iv): 另一方面,本发明提供了如式v),(vi),(vii)和(viii)所示的,高反应活性的,含有2,3-二氨基琥珀酰基的双连接子,细胞结合分子的两个或多个基团可以同时或依次与之反应,形成式(i),(ii),(iii)和(iv)中的结构: 其中: 任选地可以是单键、双键或三键,或者可以缺省;当代表三键时,lv1和lv2缺省; drug1、drug2、n、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1以及z2与式(i)-(iv)中的定义相同; lv1和lv2为相同或不同的反应官能团,这些官能团可以与细胞结合分子上的硫基、胺、羧酸、硒醇、酚或羟基发生反应。lv1和lv2独立地选自羟基(oh)、氟(f)、氯(cl)、溴(br)、碘(i)、硝基苯氧基、n-羟基琥珀酰亚胺(nhs)基、苯氧基、二硝基苯氧基、五氟苯氧基、四氟苯氧基、三氟苯氧基、二氟苯氧基、一氟苯氧基、五氯苯氧基、三氟甲磺酰基、咪唑基、二氯苯氧基、三氯苯氧基、四氯苯氧基、1-羟基苯并三唑基、甲苯磺酰基、甲磺酰基、2-乙基-5-苯基异恶唑-3’-磺酰基、酸酐或与其它酸酐作用形成的酸酐,例如乙酸酐、甲酸酐,或与多肽缩合试剂、mitsunobu反应试剂作用生成的中间体。缩合剂的例子如下:1-乙基-(3-二甲基氨基丙基)碳二亚胺(edc)、二环己基碳二亚胺(dcc)、n,n’-二异丙基碳二亚胺(dic)、n-环己基-n’-(2-吗啉代-乙基)碳二亚胺甲基对甲苯磺酸盐(cmc或cme-cdi)、1,1′-羰基二咪唑(cdi)、氧-(苯并三唑-1-)基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tbtu)、n,n,n’,n’-四甲基-氧-(1h-苯并三唑-1-基)-六氟磷酸铵(hbtu)、(苯并三唑-1-基氧基)三(二甲基氨基)-六氟磷酸盐(bop)、(苯并三唑-1-基氧基)三吡咯烷基六氟磷酸盐(pybop)、氰基膦酸二乙酯(depc)、氯-n,n,n’,n’-四甲基甲脒六氟磷酸盐、1-[双(二甲基氨基)亚甲基]-1h-1,2,3-三唑并[4,5-b]吡啶3-氧六氟磷酸盐(hatu)、1-[(二甲氨基)(吗啉代)亚甲基]-1h-[1,2,3]三唑并[4,5-b]吡啶-1-鎓3-氧六氟磷酸盐(hdma)、2-氯-1,3-二甲基-咪唑六氟磷酸盐(cip)、六氟磷酸氯代吡咯烷酮鎓(pyclop)、氟-n,n,n’,n’-双(四亚甲基)甲脒六氟磷酸盐(btffh)、n,n,n’,n’-四甲基-s-(1-氧代-2-吡啶基)硫脲六氟磷酸盐、氧-(2-氧代-1(2h)吡啶基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tptu)、s-(1-氧代-2-吡啶基)n,n,n’,n’-四甲基硫脲四氟硼酸盐、氧-[(乙氧基羰基)-氰基甲基氨基]-n,n,n’,n’-六氟磷酸四甲基脲(hotu)、(1-氰基-2-乙氧基-2-氧代乙基氨基氧基)二甲氨基-吗啉代-六氟磷酸盐(comu)、氧-(苯并三唑-1-基)-n,n,n’,n’-双(四亚甲基)六氟磷酸盐(hbpyu)、n-芐基-n’-环己基-碳二亚胺(有或没有聚合物结合)、二吡咯烷基(n-琥珀酰亚胺基氧基)碳鎓六氟磷酸盐(hspyu)、氯二吡咯烷基六氟磷酸盐(pyclu)、2-氯-1,3-二甲基咪唑四氟硼酸盐(cib)、(苯并三唑-1-基氧基)二呱啶碳六氟磷酸盐(hbpipu)、氧-(6-氯苯并三唑-1-基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tctu)、溴代(二甲基氨基)-六氟磷酸盐(brop)、丙基膦酸酐(ppaca、)、2-吗啉代乙基异氰化物(mei)、n,n,n’,n’-四甲基-氧-(n-琥珀酰亚胺基)六氟磷酸盐(hstu)、2-溴-1-乙基-吡啶鎓四氟硼酸盐(bep)、氧-[(乙氧基羰基)氰基-亚甲基氨基]-n,n,n’,n’-四甲基脲四氟硼酸盐(totu)、4-(4,6-二甲氧基-1,3,5-三嗪-2-基)-4-甲基吗啉氯化物(mmtm、dmtmm)、n,n,n’,n’-四甲基-氧-(n-琥珀酰亚胺基)脲四氟硼酸(tstu)、o-(3,4-二氢-4-氧代-1,2,3-苯并三嗪-3-基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tdbtu)、1,1′-(偶氮二羰基)-二呱啶(add)、二-(4-氯芐基)偶氮二羧酸酯(dcad)、偶氮二羧酸二叔丁酯(dbad)、偶氮二羧酸二异丙酯(diad)、偶氮二羧酸二乙酯(dead)。另外,lv1和lv2可以是酸酐,或与其它c1-c8酸酐作用形成的酸酐; 优选的lv1和lv2独立地选自卤化物(例如氟化物、氯化物、溴化物和碘化物)、甲磺酰基(甲磺酰基)、甲苯磺酰基(甲苯磺酰基)、三氟甲基磺酰基(三氟甲磺酸酯)、三氟甲基磺酸酯、硝基苯氧基、n-琥珀酰亚胺基氧基(nhs)、苯氧基;二硝基苯氧基;五氟苯氧基、四氟苯氧基、三氟苯氧基、二氟苯氧基、单氟苯氧基、五氯苯氧基、1h-咪唑-1-基、氯苯氧基、二氯苯氧基、三氯苯氧基、四氯苯氧基、n-(苯并三唑基)氧基、2-乙基-5-苯基异恶唑-3′-磺酰基、苯基恶二唑磺酰基(-砜-oda)、2-乙基-5-苯基异恶唑鎓-基、苯基恶二唑基(oda)、恶二唑基、不饱和碳(碳-碳、碳-氮、碳-硫、碳-磷、硫-氮、磷-氮、氧-氮或碳-氧之间的双键或三键)、或以下结构之一: 二硫化物;卤代乙酰基;酰卤化物;n-羟基丁二酰亚胺酯基;马来酰亚胺基;单取代马来酰亚胺基;单取代丁二酰亚胺基;二取代丁二酰亚胺基;二取代丁二酰亚胺基;-cho醛基;乙烯磺酰基;丙烯酰基;2-(对甲氧基)乙酰基;2-(甲氧基)乙酰基;2-(硝基苯氧基)乙酰基;2-(二硝基苯酚氧基)乙酰基;2-(氟苯氧基)-乙酰基;2-(二氟苯氧基)-乙酰基;2-((三氟甲基)-磺酰氧基)乙酰基;酮或醛基;2-(五氟苯氧基)乙酰基;甲基砜麻黄二唑基(oda);酸酐、烷氧基氨基;叠氮基、炔基、或酰肼,其中x1’为f,cl,br,i或lv3;x2’是o,nh,n(r1)或ch2;r3独立地为h,芳基,杂芳基或芳香基团,其中一个或几个氢原子独立地被-r1,-卤素,-or1,-sr1,-nr1r2,-no2,-s(o)r1,-s(o)2r1或-coor1取代;lv3是离去基团,选自f、cl、br、i;硝基苯氧基;n-羟基琥珀酰亚胺基(nhs);苯氧基;二硝基苯氧基;五氟苯氧基;四氟苯氧基;二氟苯氧基;单氟苯氧基;五氯苯氧基;三氟甲磺酰基;咪唑基;二氯酚基;四氯苯氧基;1-羟基苯并三唑基;甲苯甲磺酰基;甲磺酰基;2-乙基-5-苯基异恶唑-3′-磺酰基,酸酐或与其它酸酐作用形成的酸酐,例如乙酸酐、甲酸酐;或与多肽缩合试剂、mitsunobu反应试剂作用生成的中间体。 式(i)中结构的优选立体异构体由式(va)、(vb)、(vc)、(via)、(vib)、(vic)、(viia)、(viib)、(viic)、(viiia)、(viiib)和(viiic)所示: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、lv1、lv2、drug1和drug2如前文所定义。 优选地,含双链连接子的偶联物如结构式(v-01)、(v-02)、(v-03)、(v-04)、(v-05)、(v-06)、(v-07)、(v-08)、(v-09)、(v-10)、(v-11)、(v-12)、(v-13)、(v-14)、(v-15)、(v-16)、(v-17)、(v-18)、(v-19)、(v-20)、(v-21)、(v-22)、(v-23)、(vi-01)、(vi-02)、(vi-03)、(vi-04)、(vi-05)、(vi-06)、(vi-07)、(vi-08)、(vi-09)、(vi-10)、(vi-11)、(vi-12)、(vi-13)、(vi-14)、(vi-15)、(vi-16)、(vi-17)、(vi-18)、(vii-01)、(vii-02)、(vii-03)、(vii-04)、(vii-05)、(vii-06)、(vii-07)、(vii-08)、(vii-09)、(vii-10)、(vii-11)、(vii-12)、(vii-13)、(vii-14)、(vii-15)、(vii-16)、(vii-17)、(vii-18)、(vii-19)、(vii-20)、(viii-01)、(viii-02)、(viii-03)、(viii-04)、(viii-05)、(viii-06)、(viii-07)、(viii-08)、(viii-09)、(viii-10)、(viii-11)、(viii-12)、(viii-13)、(viii-14)、(viii-15)、(viii-16)、(viii-17)、(viii-18)、(viii-19)、和(viii-20)所示: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、drug1和drug2如前文所定义;x1和x1’独立为h、f、cl、br、i、ots、oms、otf、n3、cho、-c=ch、-c≡c-、arc(=o)r1、c(=o)nhnh2、-o-nh2、硝基苯氧基、n-羟基琥珀酰亚胺(nhs)、苯氧基、二硝基苯氧基、五氟苯氧基、四氟苯氧基、二氟苯氧基、单氟苯氧基、五氯苯氧基、三氟甲磺酰基、咪唑基、二氯酚基、四氯苯氧基、1-羟基苯并三唑基、甲苯甲磺酰基、甲磺酰基,2-乙基-5-苯基异恶唑-3′-,酸酐或与其它酸酐作用形成的酸酐、例如乙酸酐、甲酸酐,o-nhs(on-氢琥珀酰亚胺)、o-咪唑、o-三唑、o-四唑、o-ar、o-arno2、o-ar(no2)2、o-arf4、o-arf3、o-arf5、o-arf2、o-arf、o-arcl4、o-arcl3、o-arcl5、o-arcl2、o-arcl、o-arso3h、o-aropo3h2、o-ar(no2)cooh、s-ar(no2)2cooh、o-吡啶、o-硝基苯氧基、o-二硝基苯氧基、o-五氟苯氧基、o-四氟苯氧基、o-三氟苯氧基、o-二氟苯氧基、o-氟苯氧基、o-五氯苯氧基、o-四氯苯氧基、o-三氯苯氧基、o-二氯苯氧基、o-氯苯氧基、o-吡啶、o-硝基吡啶、o-二硝基吡啶、o-c1-c8烷基、o-三氟甲磺酸盐、o-苯并三唑、s-ar、s-arno2、s-ar(no2)2、s-arf4、s-arf3、s-arf5、s-arf2、s-arf、s-arcl4、s-arcl3、s-arcl5、s-arcl2、s-arcl、s-arso3h、s-aropo3h2、s-ar(no2)cooh、s-ar(no2)2cooh、s-吡啶、ss-吡啶、s-硝基吡啶、s-二硝基吡啶、s-c1-c8烷基、ss-c1-c8烷基、s-三氟甲磺酸酯、s-苯并三唑、其中ar是c3-c8芳环;或与多肽缩合试剂生成的,或与mitsunobu反应偶联试剂生成的中间体分子。 另一方面,本发明提供了如结构式(ix)和(x)的高反应活性双链连接子,细胞毒性分子的两个或多个官能团可以同时或依次与之反应形成如式(i)的结构: 其中: q、n、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、和z2定义如式(i)-(iv);lv1、lv2、lv1’和lv2’的定义如lv1和lv2在式(v)-(viii)中的定义; lv1、lv2、lv1’和lv2’独立地,可以同时或依次与细胞毒性药物的官能团反应分别形成如式(i)、(ii)、(iii)和(iv)的结构; 此外,优选地,lv1、lv2、lv1’和lv2’独立地为二硫化物、马来酰亚胺基、卤代乙酰基、烷氧基胺、叠氮基、酮、醛、肼、氨基、羟基、羧酸盐、咪唑、硫醇或炔烃;或n-羟基琥珀酰亚胺酯、对硝基苯基酯、二硝基苯基酯、五氟苯基酯、五氯苯基酯;四氟苯基酯;二氟苯基酯;单氟苯基酯;或五氯苯基酯、二氯苯基酯、四氯苯基酯或1-羟基苯并三唑酯;三氟甲磺酸酯、甲磺酸酯或甲苯磺酸酯;2-乙基-5-苯基异恶唑-3′-磺酸酯;吡啶基二硫化物或硝基吡啶基二硫化物;马来酰亚胺、卤代乙酸酯、乙炔二羧基或酰卤(氟化物、氯化物、溴化物或碘化物)。优选地,x和y具有以下结构之一:n-羟基琥珀酰亚胺酯;马来酰亚胺;二硫化物;卤代乙酰基;酰卤;乙烯磺酰基;丙烯酰基;2-(甲苯氧基)乙酰基;2-(甲氧基)乙酰基;2-(硝基苯氧基)乙酰基;2-(二硝基苯氧基)乙酰基;2-(氟苯氧基)-乙酰基;2-2-(二氟苯氧基)-乙酰基;2-((三氟甲基)-磺酰基)氧基)乙酰基;酮或醛、2-(五氟苯氧基)乙酰基;甲基砜苯基恶二唑(oda);酸酐、氨基氧烷基;叠氮基、炔基或酰肼。其中x1’是f、cl、br、i或lv3;x2’是o、nh、n(r1)或ch2;r3和r5是h、r1、芳基、杂芳基或其中一个或几个h原子独立地被-r1、-卤素、-or1、-sr1、-nr1r2、-no2、-s(o)r1、-s(o)2r1或-coor1取代的芳基;lv3是选自甲磺酰基(ms)、甲苯磺酰基(ts)、三氟甲基磺酰基、三氟甲基磺酸酯、硝基苯氧基、n-琥珀酰亚胺基氧基(nhs)、苯氧基;二硝基苯氧基;五氟苯氧基、四氟苯氧基、三氟苯氧基、二氟苯氧基、单氟苯氧基、五氯苯氧基、1h-咪唑-1-基、氯苯氧基、二氯苯氧基、三氯苯氧基、四氯苯氧基、n-(苯并三唑基)氧基、2-乙基-5-苯基异恶唑鎓基、苯基恶二唑基(oda)、恶二唑基或与mitsunobu反应缩合试剂反应产生的中间分子,其中r1和r2如前文所定义; 优选地,用于制备偶联物的双链连接子化合物由式(ix-01)、(ix-02)、(ix-03)、(ix-04)、(ix-05)、(ix-06)、(ix-07)、(ix-08)、(ix-09)、(ix-10)、(ix-11)、(ix-12)、(ix-13)、(ix-14)、(ix-15)、(ix-16)、(ix-17)、(ix-18)、(ix-19)、(ix-20)、(ix-21)、(ix-22)、(ix-23)、(x-01)、(x-02)、(x-03)、(x-04)、(x-05)、(x-06)、(x-07)、(x-08)、(x-09)、(x-10)、(x-11)、(x-12)、(x-13)、(x-14)、(x-15)、(x-16)、(x-17)、(x-18)、(x-19)和(x-20)表示: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、lv1、lv2、lv1’和lv2’定义如前文所述。此外,drug1和drug2相互独立,其一可以缺省,但不可同时缺省。 能与药物/细胞毒性剂的末端胺或羟基反应的官能团lv1、lv2、lv1’和lv2’包括但不限于:n-羟基琥珀酰亚胺酯、对硝基苯基酯,二硝基苯基酯,五氟苯基酯,酰氯或羧酸酐;能和细胞毒性剂的末端巯基反应的官能团可以是吡啶二硫化物,硝基吡啶二硫化物,马来酰亚胺基,卤代乙酸酯,甲基砜基苯基恶二唑(oda),酰氯或羧酸酐;能和末端酮或醛反应的官能团可以是,但也不限于胺,烷氧基胺,肼,酰氧基胺或酰肼;和末端叠氮基反应的官能可以是,也不限于炔基。 另一方面,本发明提供了如式(xi)和(xii)的高反应活性的双连接子,细胞毒性分子和细胞结合分子独立地,可以或同时或依序与之反应生成式(i)-(iv)的结构。 其中x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1和z2定义如式(i)-(iv);lv1、lv2、lv1’和lv2’的定义和lv1与lv2在式(v)-(viii)中的定义; 优选地,用于制备偶联物的双连接子化合物进一步由下式表示: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、lv1、lv2、lv1’、lv2’、x1和x1’定义如前文所述; 部分结构式(i),(ii),(iii)和(iv)中分子的制备如图1-26所示或在实施例中描述。为了合成式(i),(ii),(iii)和(iv)中的偶联物,通常药物上或细胞毒性分子上的两个官能团,依次或同时与结构式为(xi)和(xii)的连接子上的lv1’,lv2’,lv1和lv2基团反应,反应在有机溶剂中或含有0.1%-99.5%有机溶剂的水性介质中或完全水性介质中进行,形成结构式如(v),(vi),(vii),或(viii)的化合物。可分离相应的化合物,或者使其立即同时或依次与细胞结合分子上的两个或更多个基团反应,优选的基团为还原细胞结合分子的二硫键而产生的一对游离巯基,形成结构式为(i),(ii),(iii)或(iv)的偶联化合物。反应在0-60℃,ph5-9的水性介质中进行,可添加或不添加0-30%的可与水混溶的有机溶剂,例如dma,dmf,乙醇,甲醇,丙酮,乙腈,thf,异丙醇,二恶烷,丙二醇或乙二醇。 或者,式(i)、(ii)、(iii)或(iv)中的偶联物也可以通过首先使式(xi)或(xii)中的连接子与两个或更多个细胞结合分子上的基团反应,优选在0-60℃,ph5~9水溶液中或者加入0~30%与水混溶的有机溶剂,与细胞结合分子中还原二硫键而产生的一对游离巯基反应,形成如式(ix)或(x)的经修饰的细胞结合分子。巯基对优选是通过选自以下的还原剂将细胞结合剂的链间二硫键还原:二硫苏糖醇(dtt)、二硫赤藓糖醇(dte)、l-谷胱甘肽(gsh)、三(2-羧乙基)膦(tcep)、2-巯基乙胺(β-mea)或/和β-巯基乙醇(β-me、2-me),反应在ph4~9水性介质中进行,可加入或不加入0~30%的与水混溶有机溶剂。式(xi)和(xii)上的反应基团lv1’、lv2’、lv1和lv2各自独立地为二硫化物、硫醇、硫酯、马来酰亚胺基、卤代乙酰基、叠氮化物、1-炔、酮、醛、烷氧基氨基、三氟甲磺酸酯、羰基咪唑、甲苯磺酸酯、甲磺酸酯、2-乙基-5-苯基异恶唑-3′-磺酸酯,或硝基苯酚酯、n-羟基琥珀酰亚胺(nhs)酯、苯酚酯、二硝基苯酚酯、五氟苯酚酯、四氟苯酚酯、二氟苯酚酯、一氟苯酚酯、五氯苯酚酯、二氯苯酚酯、四氯苯酚酯、1-羟基苯并三唑的酯、酸酐或酰肼,或其他酸酯衍生物。然后与药物/细胞毒剂上的一个或两个基团同时或依次,在0-60℃,ph4-9.5的水性介质中加入或不加入0-30%的与水混溶的有机溶剂中反应,经柱纯化或透析后,得到式(i)、(ii)、(iii)或(iv)中的化合物。药物/细胞毒性剂的反应基团以不同方式与式(ix)或(x)中修饰的细胞结合分子反应。例如,若式(i)、(ii)、(iii)或(iv)的细胞结合剂-药物偶联物中含有二硫键,它的形成通过修饰的细胞结合剂(ix)或(x)中的二硫键和具有游离巯基的药物之间的二硫键交换来实现;若式(i)、(ii)、(iii)或(iv)的细胞结合剂-药物偶联物中含有硫醚键,它的形成通过修饰的细胞结合剂(ix)或(x)中的马来酰亚胺基或卤代乙酰基或乙基磺酰基和具有游离巯基的药物反应来实现;若在偶联物中含有酸不稳定腙键,它的形成可以通过药物或式(ix)或(x)化合物上的羰基与式(ix)或(x)化合物或者药物分子上的酰肼反应来实现,该方法为本领域所熟知(例如p.hamann等,cancerres.53,3336-34,1993;b.laguzza等,j.med.chem.32;548-55,1959;p.trail等,cancerres.,57,100-5,1997);若在偶联物中含有三唑键,它的形成可以通过药物或式(ix)或(x)中化合物的1-炔基与另一对应物上的叠氮基通过化学反应来实现(huisgen环加成)(lutz,j-f.等,2008,adv.drugdel.rev.60,958–70;sletten,e.m.等,2011,accchem.research44,666-76)。通过在式(ix)或(x)中修饰的细胞结合剂或药物上的酮或醛与另一对应物上的氧胺反应,实现细胞结合剂-药物偶联物中肟的连接。含巯基的药物可与式(ix)或(x)中带有马来酰亚胺基,卤代乙酰基或乙基磺酰基取代基的修饰的细胞结合分子连接子在水性缓冲液,ph5.5~9.0下反应,得到含硫醚键的如式(i)、(ii)、(iii)或(iv)所示的细胞结合分子-药物偶联物。含巯基的药物可以与带有吡啶基二硫代官能团的式(ix)或(x)中的修饰的连接子进行二硫键交换,得到二硫键连接的偶联物。带有羟基或巯基的药物可以在温和碱,例如ph8.0-9.5环境下,与带有卤素,特别是羧酸酯的α卤化物的如式(ix)或(x)中的修饰的连接子反应,得到醚或硫醚链接的偶联药物。在脱水剂如edc或dcc存在下,药物上的羟基可以与带有羧基的如式(xi)或(xii)所示的连接子缩合,产生酯键,得到的如式(ix)或(x)所示的经药物修饰的桥连接子可以与细胞结合分子偶联。含有氨基的药物可以与如式((ix)或(x)所示的细胞结合分子连接子上的nhs、咪唑、硝基苯酚、n-羟基琥珀酰亚胺(nhs)、苯酚、二硝基苯酚、五氟苯酚、四氟苯酚、二氟苯酚、单氟苯酚、五氯苯酚、三氟甲磺酸酯、咪唑、二氯苯酚、四氯苯酚、1-羟基苯并三唑的酯,甲苯磺酸酯,甲磺酸酯,2-乙基-5-苯基异恶唑-3′-磺酸酯缩合,得到酰胺链接的偶联物。 合成的偶联物可以通过标准生物化学方法纯化,例如在sephadexg25或sephacryls300柱上进行凝胶过滤,吸附色谱,离子交换,或透析。在一些情况下,细胞结合剂为小分子化合物(例如叶酸、黑素细胞刺激激素、egf等),与小分子药物偶联后,可以通过色谱法纯化,例如hplc、中压柱层析法或离子交换色谱法。 为了使结构式(v),(vi),(vii)或(viii)中的细胞毒性分子-双链连接子与细胞结合分子,优选抗体,上的一对游离巯基的偶联反应有更高产率,可能需要在反应混合物中加入少量水溶性有机溶剂或相转移剂。可将式(v),(vi),(vii)或(viii)中的交联剂(连接子),以高浓度如1-500mm溶解于可与水混溶的极性有机溶剂中,例如不同的醇(如甲醇、乙醇和丙醇)、丙酮、乙腈、四氢呋喃(thf)、1,4-二恶烷、二甲基甲酰胺(dmf)、二甲基乙酰胺(dma)或二甲基亚砜(dmso)。同时,将细胞结合分子,如抗体以1~50mg/ml浓度溶解在ph4~9.5,最优ph6~8.5的缓冲液中,再用0.5~20eq.的tcep或dtt处理20分钟至48小时。还原后,dtt可通过sec色谱纯化去除。tcep也可以通过sec色谱法或离子交换色谱法去除,或者留在反应混合物中,无需进一步纯化。此外,以tcep还原抗体或其他细胞结合剂,可以在如式(v),(vi),(vii)或(viii)所示的药物-连接子分子共存时进行,此时药物与细胞结合分子的偶联,可以与tcep还原抗体同时实现。 进行细胞结合剂的修饰的水溶液为ph4至9之间缓冲液,优选在6.0至7.5之间,可以含有适合用于这个ph范围的任何非亲核性缓冲盐。典型的缓冲液包括磷酸盐、乙酸盐、三乙醇胺盐酸盐、hepes和mops缓冲液,也可含有其它组分,例如环糊精、羟丙基-β-环糊精、聚乙二醇、蔗糖和其它盐,如nacl和kcl。在将式(v),(vi),(vii)或(viii)中的药物-连接子加入到已经被还原的细胞结合分子的溶液中后,将反应混合物在4℃至45℃,优选15℃的温度下保温。对反应进程的监测,可以通过测量在某一特定紫外线波长(例如254nm)吸光度的减少,或某一特定紫外线波长(例如280nm)吸光度的增加,或选择其它适当波长。反应完成后,被修饰的细胞结合剂可以以常规方式被分离,例如使用凝胶过滤色谱、离子(阳离子或阴离子)交换色谱、吸附色谱,硅胶或氧化铝柱层析色谱,结晶、制备薄层色谱或hplc方法。 可以通过测量反应生成的硝基吡啶硫酮、二硝基吡啶二硫酮、吡啶硫酮、羧基酰胺基吡啶二硫酮和二羧基酰胺基吡啶二硫酮基团的紫外吸光度,对修饰的程度进行评估。对于没有发色基团分子的偶联反应、修饰或偶联反应可以通过lc-ms监测、优选uplc-qtof质谱或毛细管电泳质谱法(ce-ms)监测。本发明所述的连接子含有多种官能团,可与细胞结合分子,尤其是具有合适取代基的修饰的细胞结合分子反应。例如,带有氨基或羟基的修饰的细胞结合分子,可以与带有n-羟基琥珀酰亚胺(nhs)酯的药物反应,带有巯基的修饰的细胞结合分子,可以与带有马来酰亚胺基或卤代乙酰基的药物反应。另外,带有羰基(酮或醛)基团的细胞结合分子,可以与带有酰肼或烷氧基胺的药物反应。基于连接子上官能团的反应活性,本领域技术人员可以很容易地确定使用哪种连接子分子。 细胞结合剂 本发明的偶联物中的细胞结合分子cb或q,和被修饰的细胞结合分子,是目前已知的或将成为已知的,可与具有治疗学意义或能在生物学意思上被修饰的细胞的片段结合,复合或反应的分子。 细胞结合剂包括但不限于大分子量蛋白质,例如抗体、抗体样蛋白质、全长抗体、多克隆抗体、单克隆抗体、二聚体、多聚体、多特异性抗体(例如双特异性抗体、三特异性抗体或四特异性抗体);单链抗体;抗体片段、例如fab、fab’、f(ab’)2、fv、(parham,j.immunol.-902(1983)),由fab表达文库产生的片段,抗独特型(抗id)抗体、cdr’s、双抗体、三抗体、四抗体、微抗体、前抗体、前抗体片段、小免疫蛋白(sip),和上述任何一种的表位结合片段,能免疫特异性结合癌细胞抗原、病毒抗原、微生物抗原或免疫系统产生的能够识别,结合特定抗原或表现出所需生物活性的蛋白质(miller等,j.immunology,2003,170:4854-61);干扰素(如i型、ii、iii);肽;淋巴因子如il-2、il-3、il-4、il-5、il-6、il-7、il-8、il-9、il-10、il-11、il-12、il-13、il-14、il-5、il-16、il-17、il-18、il-19、il-20、il-21、il-22、il-23、il-24、il-25、gm-csf、干扰素γ(ifn-γ);激素如胰岛素、trh(促甲状腺激素释放激素)、msh(促黑素细胞激素)、类固醇激素如雄激素和雌激素;生长因子和集落刺激因子如表皮生长因子(egf)、粒细胞巨噬细胞集落刺激因子(gm-csf)、转化生长因子(tgf)如tgfα、tgfβ、胰岛素和胰岛素样生长因子(igf-i、igf-ii)、g-csf、m-csf和gm-csf(burgess,immunologytoday5155-8(1984));牛痘生长因子(vgf);成纤维细胞生长因子(fgf);小分子量的蛋白质、多肽、肽和肽激素、如铃蟾肽、胃泌素、胃泌素释放肽;血小板衍生生长因子;白细胞介素和细胞因子、如白细胞介素-2(il-2)、白细胞介素-6(il-6)、白血病抑制因子、粒细胞-巨噬细胞集落刺激因子(gm-csf);维生素、如叶酸;载脂蛋白和糖蛋白、如转铁蛋白(o’keefe等,j.biol.chem.260,932-937(1985));糖结合蛋白或脂蛋白,如凝集素;细胞营养转运分子;和小分子抑制剂,如前列腺特异性膜抗原(psma)抑制剂和小分子酪氨酸激酶抑制剂(tki)、非肽或任何其他细胞结合分子或物质,如生物活性聚合物(dhar等,proc.natl.acad.sci.2008,105,17356-61);生物活性树枝状大分子(lee,等,nat.biotechnol.2005,23,1517-26;almutairi等,proc.natl.acad.sci.2009,106,685-90);纳米颗粒(liong等,acsnano,2008,2,1309-12;medarova等,nat.med.2007,13,372-7;javier等,bioconjugatechem.2008,19,1309-12);脂质体(medinai等,curr.phar.des.2004,10,2981-9);病毒衣壳(flenniken等,virusesnanotechnol.2009,327,71-93)。 通常,如果可获得合适的单克隆抗体,则优选单克隆抗体作为细胞表面结合剂。并且抗体可以是鼠、人、人源化、嵌合或衍生自其他物种。 本发明中使用的抗体的生产涉及体内或体外方法或其组合。用于产生多克隆抗受体肽抗体的方法在本领域中是众所周知的,例如美国专利no.4,493,795(nestor等)。单克隆抗体通常通过将骨髓瘤细胞与已经用所需抗原免疫的小鼠的脾细胞融合来制备(g.和milstein,c.1975,nature256:495-7)。详细方法在《antibodies-alaboratorymanual》,harlow和lane编辑,冷泉港实验室出版社,纽约(1988)中描述,引用并入本文。特别地,可通过用感兴趣的抗原如完整的靶细胞,从靶细胞,全病毒,灭活的全病毒和病毒蛋白中分离的抗原,来免疫小鼠,大鼠,仓鼠或任何其他哺乳动物,来制备单克隆抗体。通常使用聚乙二醇(peg)6000将脾细胞与骨髓瘤细胞融合。通过它们对hat(次黄嘌呤-氨基蝶呤-胸腺嘧啶)的敏感性来选择融合杂种。通过其对特定受体的免疫反应或抑制靶细胞上受体活性的能力,可鉴定适于制备产本发明的单克隆抗体的杂交瘤。 本发明中使用的单克隆抗体可以通过单克隆杂交瘤培养来生产,培养基中含有分泌具有特定抗原特异性的抗体分子的杂交瘤。将培养物保持在特定的条件,保持足够的时间以使杂交瘤将抗体分子分泌到培养基中。然后收集含有抗体的培养基,通过众所周知的技术进一步分离抗体分子,例如使用蛋白a亲和层析,阴离子,阳离子,疏水或尺寸排阻色谱法(尤其是通过蛋白a亲和层析和尺寸排阻色谱法),离心,差别溶解度法或任何其他蛋白质纯化的标准技术。 用于制备抗体的培养基在本领域都是众所周知的,包括合成培养基,市售可得。示例性的合成培养基为:dulbecco的基本必需培养基(dmem;dulbecco等,virol.8,396(1959))中加入4.5mg/l葡萄糖,0~20mm谷氨酰胺,0~20%胎牛血清,若干ppm的重金属盐,如cu、mn、fe或zn等,或/和其他重金属盐,并加入消泡剂,如聚氧乙烯-聚氧乙烯嵌段共聚物。 另外,生产抗体的细胞株也可以通过细胞融合之外的方法得到,比如说用癌基因dna直接转化b淋巴细胞,或者致癌病毒如eb病毒(ebv,也称人疱疹病毒4(hhv-4))或者肉瘤相关疱疹病毒(kshv)转染b淋巴细胞(可参考美国专利4,341,761;4,399,121;4,427,783;4,444,887;4,451,570;4,466,917;4,472,500;4,491,632;4,493,890)。单克隆抗体也可以通过抗-受体多肽或含末端羧基的多肽而得到。具体可见文献:niman等,proc.natl.acad.sci.,1983,80,4949-4953;geysen等,proc.natl.acad.sci.,1985,82,178-182;lei等,biochemistry,1995,34(20),6675-6688等。通常,抗-受体多肽或多肽类似物可以单独或与免疫原载体连接,作为免疫原生产抗-受体多肽单克隆抗体。 还有其他已知的各种技术,可以用来生产本发明里作为结合分子的单克隆抗体。特别有用的是生产全人源抗体的方法。其中一个方法是噬菌体展示技术,此方法通过亲和富集,从大量的人抗体中筛选出特异性结合抗原的抗体。噬菌体展示技术,包括构建和筛选噬菌体展示库是一种非常成熟的技术,具体可以参考:dente等,gene.148(1):7-13(1994);little等,biotechnoladv.12(3):539-55(1994);clackson等,nature352:264-8(1991);huse等,science246:1275-81(1989)。 通过非人源的如老鼠的杂交瘤技术获得的抗体,可以通过人源化以避免注射入人体时产生抗抗体。最常见的人源化抗体的方法是互补决定区嫁接和表面修饰,这些方法在大量文献中都有描述,如美国专利5,859,205;6,797,492;liu等,immunolrev.,2008,222,9-27;almagro等,frontbiosci.,2008,1(13),1619-33;lazar等,molimmunol.,2007,44(8),1986-98;li等,proc.natl.acad.sci.,2006,103(10),3557-62。全人源抗体也可以通过将带有人免疫球蛋白重链、轻链的抗原免疫转基因小鼠、兔子、猴子以及其他转基因哺乳动物而得到。这样的转基因小鼠例子有xenomouse(abgenix/amgen.),humab-mouse(medarex/bms),velocimouse(regeneron),参见美国专利6,596,541;6,207,418;6,150,584;6,111,166;6,075,181;5,922,545;5,661,016;5,545,806;5,436,149和5,569,825。在人体治疗中,通过将鼠源的可变区与人的非可变区融合为“嵌合抗体”,这类抗体比鼠抗在人体中具有更小的免疫原性(kipriyanov等,molbiotechnol.,2004,26,39-60;houdebine,curropinbiotechnol.,2002,13,625-629)。另外,通过可变区的点突变可以使抗体结合抗原的亲和力和特异性提高(brannigan等,nat.rev.mol.cellbiol.,2002,3,964-70;adams等,j.immunol.methods.,1999,231,249-60)。非可变区的替换可以改进抗体介导的结合功能和其细胞毒性。 对恶性细胞抗原免疫特异性的抗体也可以商业获得,或通过本领域技术人员公知的任何方法,如化学合成或重组表达技术生产。对恶性细胞抗原免疫特异性的抗体的核苷酸序列可以商业获得,例如从genbank数据库或类似数据库,文献出版物或通过常规克隆和测序获得。 除抗体外,结合/阻断/靶或以某种其他方式与靶细胞上的表位或相应受体相互作用的肽或蛋白质均可用作结合分子。这些肽或蛋白质可以是对表位或相应受体具有亲和力的任何随机肽或蛋白质,并且它们不一定是免疫球蛋白家族。这些肽可以通过与噬菌体展示抗体类似的技术分离(szardenings,jreceptsignaltransductres.2003,23(4):307-49)。对来自这种随机肽文库的肽的使用可以类似于抗体和抗体片段。肽或蛋白质的结合分子可以与大分子或其它材料偶联或连接,例如,但不限于白蛋白,聚合物,脂质体,纳米颗粒,树枝状大分子,只要这样的附着允许肽或蛋白质保持其抗原结合特异性。 在优选的实施例中,本发明的细胞结合分子是单克隆抗体。用于与本发明的与细胞毒剂偶联的抗体的例子包括,但不限于3f8(抗gd2)、阿巴单抗(抗ca-125)、阿昔单抗(抗cd41(整联蛋白α-iib)、阿达木单抗(抗tnf-α)、adecatumumab(抗epcam、cd326)、阿非莫单抗(抗tnf-α)、afutuzumab(抗cd20)、alacizumab单抗(抗vegfr2)、ald518(抗il-6)、alemtuzumab(campath、mabcampath、抗cd52)、altumomab(抗cea)、anatumomab(抗tag-72)、anrukinzumab(ima-638、抗-il-13)、apolizumab(抗-hla-dr)、阿奇单抗(抗-cea)、阿塞珠单抗(抗-l-选择蛋白cd62l)、atlizumab(tocilizumab、actemra、roactemra、抗-il-6受体)、atorolimumab(抗-rhesus因子)、bapineuzumab(抗-β淀粉样蛋白)、basiliximab(simulect、抗cd25(il-2受体的α链))、bavituximab(抗磷脂酰丝氨酸)、bectumomab(lymphoscan、抗-cd22)、贝利单抗(benlysta、lymphostat-b、抗baff)、benralizumab(抗cd125)、bertilimumab(抗ccl11(eotaxin-1))、besilesomab(scintimun、抗cea相关抗原)、贝伐单抗(avastin、抗vegf-a)、biciromab(fibriscint、抗纤维蛋白iiβ链)、bivatuzumab(抗-cd44v6)、blinatumomab(bite、抗cd19)、brentuximab(cac10、抗-cd30tnrsf8)、briakinumab(抗il-12、il-23)、canakinumab(ilaris、抗il-1)、cantuzumab(c242、抗canag)、capromab、catumaxomab(removab、抗epcam、抗cd3)、cc49(抗tag-72)、cedelizumab(抗cd4)、certolizumab单抗(cimzia抗tnf-α)、西妥昔单抗(爱必妥、imc-c225、抗egfr)、citatuzumabbogatox(抗epcam)、cixutumumab(抗igf-1)、clenoliximab(抗cd4)、clivatuzu-mab(抗muc1)、conatumumab(抗trail-r2)、cr6261(抗流感a血凝素)、dacetuzumab(抗cd40)、daclizumab(zenapax、抗cd25(il-2受体α链))、daratumumab(抗cd38(环adp核糖水解酶)、denosumab(prolia、抗rankl)、detumomab(抗b淋巴瘤细胞)、dorlimomab、dorlixizumab、ecromeximab(抗gd3神经节苷脂)、eculizumab(soliris、抗-c5)、edobacomab(抗内毒素)、edrecolomab(panorex、mab17-1a、抗-epcam)、efalizumab(raptiva、抗lfa-1(cd11a))、efungumab(mycograb、抗hsp90)、elotuzumab(抗slamf7)、elsilimomab(抗il-6)、enlimomab单抗(抗icam-1(cd54))、epitumomab(抗episialin)、依他珠单抗(抗-cd22)、erlizumab(抗-itgb2(cd18))、ertumaxomab(rexomun、抗her2/neu、cd3)、依他拉单抗(abegrin、抗整联蛋白αvβ3)、exbivirumab(抗乙肝表面抗原)、fanolesomab(neutrospec、抗cd15)、faralimomab(抗干扰素受体)、farletuzumab(抗叶酸受体1)、felvizumab(抗呼吸道合胞病毒)、fezakinumab(抗-il-22)、figitumumab(抗-igf-1受体)、fontolizumab(抗-ifn-γ)、foravirumab(抗狂犬病病毒糖蛋白)、fresolimumab(抗tgf-β)、galiximab(抗cd80)、gantenerumab(抗β淀粉样蛋白)、gavilimomab(抗cd147(basigin))、gemtuzumab(抗cd33)、girentuximab(抗碳酸酐酶9)、glembatumumab(cr011、抗gpnmb)、golimumab(simponi、抗-tnf-α)、gomiliximab(抗-cd23(ige受体))、ibalizumab(抗-cd4)、ibritumomab(抗cd20)、igovomab(indimacis-125、抗ca-125)、imciromab(myoscint、抗心肌肌凝蛋白)、infliximab(remicade、抗tnf-α)、intetumumab(抗cd51)、inolimomab(抗cd25(il-2受体α链)、伊珠单抗(抗-cd22)、ipilimumab(抗cd152)、iratumumab(抗cd30(tnfrsf8))、keliximab(抗-cd4)、labetuzumab(cea-cide、抗cea)、lebrikizumab(抗il-13)、lemalesomab(抗nca-90(粒细胞抗原))、lerdelimumab(抗tgfβ2)、lexatumumab(抗trail-r2)、libivirumab(抗乙肝表面抗原)、lintuzumab(抗cd33)、鲁米木单抗(抗cd40)、鲁米单抗(抗cd23(ige受体)、mapatumumab(抗trail-r1)、马西莫单抗(抗t-细胞受体)、马妥珠单抗(抗egfr)、mepolizumab(bosatria、抗il-5)、metelimumab(抗tgfβ1)、milatuzumab(抗cd74)、minretumomab(抗tag-72)、mitumomab(bec-2、抗gd3神经节苷脂)、morolimumab(抗恒河猴因子)、motavizumab(numax、抗呼吸道合胞病毒)、muromonab-cd3(orthocloneokt3、抗cd3)、nacolomab(抗c242)、naptumomab(抗5t4)、那他珠单抗(tysabri、抗整联蛋白α4)、奈巴单抗(抗内毒素)、necitumumab(抗egfr)、nerelimomab(抗-tnf-α)、nimotuzumab(theracim、theraloc、抗-egfr)、nofetumomab、ocrelizumab(抗cd20)、奥利木单抗(afolimomab、抗lfa-1(cd11a))、ofatumumab(arzerra、抗cd20)、olaratumab(抗pdgf-rα)、omalizumab(xolair、抗igefc区)oportuzumab(抗epcam)、oregovomab(ovarex、抗ca-125)、otelixizumab(抗cd3)、pagibaximab(抗脂磷壁酸)、palivizumab(synagis、abbosynagis、抗呼吸道合胞病毒)、帕尼单抗(vectibix、abx-egf、抗egfr)、panobacumab(抗铜绿假单胞菌(pseudomonasaeruginosa))、帕考珠单抗(抗il-4)、pemtumomab(theragyn、抗muc1)、pertuzumab(omnitarg、2c4、抗her2/neu)、pexelizumab(抗c5)、pintumomab(抗腺癌抗原)、priliximab(抗-cd4)、pritumumab(抗波形蛋白)、pro140(抗-ccr5)racotumomab(1e10、抗-n-羟乙酰神经氨酸(neugc、ngna)-神经节苷脂gm3))、rafivirumab(抗狂犬病病毒糖蛋白)、ramucirumab(抗vegfr2)、ranibizumab(lucentis、抗vegf-a)、raxibacumab(抗炭疽毒素、保护性抗原)、regavirumab(抗巨细胞病毒糖蛋白b)、reslizumab(抗-il-5)、rilotumumab(抗-hgf)、rituximab(mabthera、rituxanmab、抗-cd20)、robatumumab(抗-igf-1受体)、rontalizumab(抗ifn-α)、rovelizumab(leukar-rest、抗cd11、cd18)、ruplizumab(antova、抗cd154(cd40l))、satumomab(抗tag-72)、sevirumab(抗巨细胞病毒)、sibrotuzumab(抗fap)、西法木单抗(抗ifn-α)、siltuximab(抗il-6)、siplizumab(抗cd2)、smartmi95(抗cd33)、solanezumab(抗β淀粉状蛋白)、sonepcizumab(抗鞘氨醇-1-磷酸)、sontuzumab(抗-episialin)、stamulumab(抗-myostatin)、sulesomab(leukoscan、抗nca-90(粒细胞抗原))、tacatuzumab(抗α甲胎蛋白)、tadocizumab(抗整联蛋白αiibβ3)、talizumab(抗ige)、tanezumab(anti-ngf)、taplitumomab(抗cd19)、tefibazumab(aurexis、(抗凝聚因子a))、telimomab、tenatumomab(抗腱生蛋白c)、teneliximab(抗cd40)、teplizumab(抗cd3)、tgn1412(抗cd28)、ticilimumab(tremelimumab、抗-ctla-4)、tigatuzumab(抗trail-r2)、tnx-650(抗il-13)、tocilizumab(atlizumab、actemra、roactemra、il-6受体)、toralizumab(抗cd154(cd40l))、tositumomab(抗cd20)、曲妥珠单抗(赫赛汀、抗her2/neu)、tremelimumab(抗ctla-4)、tucotuzumabcelmoleukin(抗epcam)、tuvirumab(抗乙型肝炎病毒)、urtoxazumab(抗大肠杆菌)、ustekinumab(stelara、抗-il-12、il-23)、vapaliximab(抗-aoc3(vap-1))、维多珠单抗(抗整联蛋白α4β7)、维妥珠单抗(抗cd20)、vepalimomab(抗aoc3(vap-1))、visilizumab(nuvion、抗cd3)、vitaxin(抗血管整合素avb3)、volociximab(抗整联蛋白α5β1)、votumumab(humaspect、抗肿瘤抗原ctaa16.88)、zalutumumab(humax-egfr、zanolimumab(humax-cd4、抗-cd4)、ziralimumab(抗-cd147(basigin))、zolimomab(抗-cd5)、依那西普alefaceptabataceptrilonacept(arcalyst)、14f7(抗irp-2(铁调节蛋白2))、14g2a(抗gd2神经节苷脂、源于nat.cancerinst.、治疗黑素瘤和实体瘤)、j591(抗-psma、源于weillcornell医学院、治疗前列腺癌)、225.28s(抗hmw-maa(高分子量黑素瘤相关抗原)、sorinradiofarmacisrl(源于意大利米兰、治疗黑色素瘤)、col-1(抗ceacam3、cgm1、源于natcancerinst.、治疗结肠直肠癌和胃癌)、cyt-356(治疗前列腺癌)、hnk20(oravaxinc.治疗呼吸道合胞病毒感染)、immurait(源于immunomedics、治疗nhl)、lym-1(抗hla-dr10、peregrinepharm)、mak-195f(抗tnf(肿瘤坏死因子、tnfa、tnf-α、tnfsf2、源于abbott/knoll、治疗脓毒症中毒性休克)、medi-500(t10b9、抗cd3、trαβ(t细胞受体α/β)、源于medimmuneinc、用于移植物抗宿主疾病病)、ringscan(抗tag72(肿瘤相关糖蛋白72)、源于neoprobecorp.、用于乳腺癌、结肠癌和直肠癌)、avicidin(抗epcam(上皮细胞粘附分子))、抗-tacstd1(肿瘤相关钙信号转导1)、抗ga733-2(胃肠肿瘤相关蛋白2)、抗egp-2(上皮糖蛋白2)、抗ksa、ks1/4抗原、m4s、肿瘤抗原17-1a、cd326(源于neorx公司、治疗结肠癌、卵巢癌、前列腺癌和nhl)、lymphocide(源于immunomedics,nj)、smartid10(源于proteindesignlabs)、oncolym(源于technicloneinc,ca)、allomune(源于biotransplant,ca)、anti-vegf(源于genentech,ca)、ceacide(源于immunomedics,nj)、imc-1c11(源于imclone,nj)和cetuximab(源于imclone,nj)。 用于结合抗原的其它抗体,包括但不限于抗以下抗原的抗体:氨肽酶n(cd13)、膜联蛋白a1、b7-h3(cd276、各种癌症)、ca125(卵巢癌)、ca15-3(各种癌)、ca19-9(各种癌)、l6(各种癌)、lewisy(各种癌)、lewisx(各种癌)、甲胎蛋白(各种癌)、ca242、胎盘碱性磷酸酶(各种癌)、前列腺特异性抗原(前列腺癌)、前列腺酸性磷酸酶(前列腺癌)、表皮生长因子(各种癌)、cd2(霍奇金病、非霍奇金淋巴瘤的淋巴瘤、多发性骨髓瘤)、cd3的ε(t细胞淋巴瘤、肺癌、乳腺癌、胃癌、卵巢癌、自身免疫性疾病、恶性腹水)、cd19(b细胞恶性肿瘤)、cd20(非霍奇金淋巴瘤)、cd22(白血病、淋巴瘤、多发性骨髓瘤、系统性红斑狼疮)、cd30、cd33、cd37、cd38(多发性骨髓瘤)、cd40(淋巴瘤、多发性骨髓瘤、白血病)、cd51(转移性黑素瘤、肉瘤)、cd52、cd56(小细胞肺癌癌、卵巢癌、merkel细胞癌、以及液体肿瘤、多发性骨髓瘤)、cd66e(癌症)、cd70(转移性肾细胞癌和非霍奇金淋巴瘤)、cd74(多发性骨髓瘤)、cd80(淋巴瘤)、cd98(癌症),粘蛋白(癌)、cd221(实体瘤)、cd227(乳腺癌、卵巢癌)、cd262(非小细胞肺癌和其他癌)、cd309(卵巢癌)、cd326(实体瘤)、ceacam3(大肠癌、胃癌)、ceacam5(癌胚抗原;cea、cd66e)(乳腺癌、结肠直肠癌和肺癌)、dll3(δ状-3)、dll4(δ状-4)、egfr(表皮生长因子受体、各种癌症)、ctla4(黑色素瘤)、cxcr4(cd184、血红素肿瘤、实体肿瘤)、内皮糖蛋白(cd105、实体瘤)、epcam(上皮细胞粘附分子、膀胱癌、头、颈、结肠、前列腺非霍奇金淋巴瘤、和卵巢癌)、erbb2(表皮生长因子受体2;肺癌、乳腺癌、前列腺癌)、fcgr1(自身免疫性疾病)、folr(叶酸受体、卵巢癌)、gd2神经节苷脂(癌症)、g-28(一种细胞表面抗原glyvolipid、黑素瘤)、独特型gd3(癌症)、热休克蛋白(癌症)、her1(肺、胃癌)、her2(乳腺癌、肺癌和卵巢癌)、hla-dr10(nhl)、hla-drb(非霍奇金淋巴瘤、b细胞白血病)、人绒毛膜促性腺激素(癌)、igf1r(胰岛素样生长因子1受体、实体瘤、血液癌症)、il-2受体(白细胞介素2受体、t-细胞白血病和淋巴瘤)、il-6r(白细胞介素6受体、多发性骨髓瘤、类风湿性关节炎、castleman病、il6依赖性肿瘤)、整合素(素αvβ3、α5β1、α6β4、αllβ3、α5β5、αvβ5细胞附着因子、各种癌症)、mage-1(各种癌)、mage-2(各种癌)、mage-3(各种癌)、mage4(各种癌)、抗转铁蛋白受体(各种癌)、p97(黑色素瘤)、ms4a1(跨膜域4亚科a成员1、非霍奇金b细胞淋巴瘤、白血病)、muc1或muc1-klh(乳腺癌、卵巢癌、子宫颈癌、支气管和胃肠道癌症)、muc16(ca125)(卵巢癌)、cea(大肠癌)、gp100(黑色素瘤)、mart1(黑色素瘤)、mpg(黑色素瘤)、ms4a1(跨膜域4蛋白a、小细胞肺癌、非霍奇金淋巴瘤)、核仁、神经癌基因产物(癌)、p21(癌)、抗(n-羟乙酰神经氨酸)抗体结合位(乳腺癌、黑色素瘤)、plap样睾丸碱性磷酸酶(卵巢癌、睾丸癌)、psma(前列腺肿瘤)、psa(前列腺癌)、robo4、tag72(肿瘤相关糖蛋白72、白血病、胃癌、结肠直肠癌、卵巢癌)、t细胞的跨膜蛋白(各种癌症)、tie(cd202b)、tnfrsf10b(肿瘤坏死因子受体超家族成员10b、各种癌症)、tnfrsf13b(肿瘤坏死因子受体超家族成员13b、多发性骨髓瘤、非霍奇金淋巴瘤、以及其他癌症、类风湿性关节炎和系统性红斑狼疮)、tpbg(滋养层糖蛋白、肾细胞癌)、trail-r1(肿瘤坏死凋亡诱导配体受体1、淋巴瘤、非霍奇金淋巴瘤、大肠癌、肺癌)、vcam-1(cd106、黑色素瘤)、血管内皮生长因子、血管内皮生长因子-a、vegf-2(cd309、各种癌症)。抗体识别的一些其他的肿瘤相关抗原可见于各种综述(gerber等,mabs1:3,247-253(2009);novellino等,cancerimmunolimmunother.54(3),187-207(2005);franke等,cancerbiotherradiopharm.2000,15,459-76)。 细胞结合剂,更优选为抗体,是能够抗肿瘤细胞、病毒感染细胞、微生物感染细胞、寄生虫感染细胞、自身免疫细胞、活化细胞、骨髓细胞、活化t细胞、b细胞或黑素细胞的任何试剂。更具体地说,细胞结合剂可以是能够抗以下任何一种抗原或受体的任何试剂/分子:cd2、cd2r、cd3、cd3gd、cd3e、cd4、cd5、cd6、cd7、cd8、cd8a、cd8b、cd9、cd10、cd11a、cd11b、cd11c、cd12、cd12w、cd13、cd14、cd15、cd15s、cd15u、cd16、cd16a、cd16b、cd17、cdw17、cd18、cd19、cd20、cd21、cd22、cd23、cd24、cd25、cd26、cd27、cd28、cd29、cd30、cd31、cd32、cd33、cd34、cd35、cd36、cd37、cd38、cd39、cd40、cd41、cd42、cd42a、cd42b、cd42c、cd42d、cd43、cd44、cd44r、cd45、cd45ra、cd45rb、cd45ro、cd46、cd47、cd47r、cd48、cd49a、cd49b、cd49c、cd49e、cd49f、cd50、cd51、cd52、cd53、cd54、cd55、cd56、cd57、cd58、cd59、cd60、cd60a、cd60b、cd60c、cd61、cd62e、cd62l、cd62p、cd63、cd64、cd65、cd65s、cd66、cd66a、cd66b、cd66c、cd66d、cd66e、cd66f、cd67、cd68、cd69、cd70、cd71、cd72、cd73、cd74、cd74、cd75、cd75s、cd76、cd77、cd78、cd79、cd79a、cd79b、cd80、cd81、cd82、cd83、cd84、cdw84、cd85、cd86、cd87、cd88、cd89、cd90、cd91、cd92、cdw92、cd93、cd94、cd95、cd96、cd97、cd98、cd99、cd99r、cd100、cd101、cd102、cd103、cd104、cd105、cd106、cd107、cd107a、cd107b、cd108、cd109、cd110、cd111、cd112、cd113、cdw113、cd114、cd115、cd116、cd117、cd118、cd119、cdw119、cd120a、cd120b、cd121a、cd121b、cdw121b、cd122、cd123、cdw123、cd124、cd125、cdw125、cd126、cd127、cd128、cdw128、cd129、cd130、cd131、cdw131、cd132、cd133、cd134、cd135、cd136、cdw136、cd137、cdw137、cd138、cd139、cd140a、cd140b、cd141、cd142、cd143、cd144、cd145、cdw145、cd146、cd147、cd148、cd149、cd150、cd151、cd152、cd153、cd154、cd155、cd156a、cd156b、cdw156c、cd157、cd158a、cd158b、cd159a、cd159b、cd159c、cd160、cd161、cd162、cd162r、cd163、cd164、cd165、cd166、cd167、cd167a、cd168、cd169、cd170、cd171、cd172a、cd172b、cd172g、cd173、cd174、cd175、cd175s、cd176、cd177、cd178、cd179、cd180、cd181、cd182、cd183、cd184、cd185、cd186、cdw186、cd187、cd188、cd189、cd190、cd191、cd192、cd193、cd194、cd195、cd196、cd197、cd198、cdw198、cd199、cdw199、cd200、cd200a、cd200b、cd201、cd202、cd202b、cd203、cd203c、cd204、cd205、cd206、cd207、cd208、cd209、cd210、cdw210、cd211、cd212、cd213a1、cd213a2、cd214、cd215、cd216、cdw217、cdw218a、cdw218b、cd219、cd220、cd221、cd222、cd223、cd224、cd225、cd226、cd227、cd228、cd229、cd230、cd231、cd232、cd233、cd234、cd235a、cd235ab、cd235b、cd236、cd236r、cd237、cd238、cd239、cd240、cd240ce、cd240d、cd241、cd242、cd243、cd244、cd245、cd246、cd247、cd248、cd249、cd250、cd251、cd252、cd253、cd254、cd256、cd257、cd258、cd259、cd260、cd261、cd262、cd263、cd264、cd265、cd266、cd267、cd268、cd269、、cd270、cd271、cd272、cd273、cd274、cd275、cd276(b7-h3)、cd277、cd278、cd279、cd280、cd281、cd282、cd283、cd284、cd285、cd286、cd287、cd288、cd289、cd290、cd291、cd292、cdw293、cd294、cd295、cd296、cd297、cd298、cd299、cd300a、cd300c、cd300e、cd301、cd302、cd303、cd304、cd305、cd306、cd307、cd308、cd309、cd310、cd311、cd312、cd314、cd315、cd316、cd317、cd318、cd319、cd320、cd321、cd322、cd323、cd324、cdw325、cd326、cdw327、cdw328、cdw329、cd330、cd331、cd332、cd333、cd334、cd335、cd336、cd337、cdw338、cd339、4-1bb、5ac、5t4(滋养层糖蛋白、tpbg、5t4、wnt激活的抑制因子1或waif1)、腺癌抗原、ags-5、ags-22m6、激活素受体样激酶1、afp、akap-4、alk、α-整合素、αvβ6、氨基肽酶n、淀粉样蛋白β、雄激素受体、血管生成素2、血管生成素3、膜联蛋白a1、炭疽毒素保护性抗原、抗转铁蛋白受体、aoc3(vap-1)、b7-h3、炭疽芽孢杆菌、baff(b细胞活化因子)、b淋巴瘤细胞、bcr-abl、bombesin、boris、c5、c242抗原、ca125(碳水化合物抗原125、muc16)、ca-ix(或caix、碳酸酐酶9)、calla、canag、canislupusfamiliarisil31、碳酸酐酶ix、心肌肌球蛋白、ccl11(c-c基序趋化因子11)、ccr4(c-c趋化因子受体4型、cd194)、ccr5、cd3e(ε)、cea(癌胚抗原)、ceacam3、ceacam5(癌胚抗原)、cfd(因子d)、ch4d5、胆囊收缩素2(cck2r)、cldn18(claudin-18)、结块因子a、cripto、fcsf1r(集落刺激因子1受体、cd115)、csf2(集落刺激因子2、粒细胞-巨噬细胞集落刺激因子(gm-csf))、ctla4(细胞毒性t淋巴细胞相关蛋白4)、ctaa16.88肿瘤抗原、cxcr4(cd184)、c-x-c趋化因子受体4型、环状adp核糖水解酶、细胞周期蛋白b1、cyp1b1、巨细胞病毒、巨细胞病毒糖蛋白b、达比加群、dll3(δ样配体3)、dll4(δ样配体4)、dpp4(二肽基肽酶4)、dr5(死亡受体5)、大肠杆菌志贺毒素型pe-1、大肠杆菌志贺毒素型pe-2、ed-b、egfl7(含egf样结构域的蛋白质7)、egfr、egfrii、egfrviii、内皮糖蛋白(cd105)、内皮素b受体、内毒素、epcam(上皮细胞粘附分子)、epha2、episialin、erbb2(表皮生长因子受体2)、erbb3、erg(tmprss2ets融合基因)、大肠杆菌、etv6-aml、fap(成纤维细胞活化蛋白α)、fcgr1、甲胎蛋白、纤维蛋白ii、β链、纤连蛋白额外结构域-b、folr(叶酸受体)、叶酸受体α、叶酸水解酶、fos相关抗原1、呼吸道合胞病毒f蛋白、卷曲受体、岩藻糖基gm1、gd2神经节苷脂、g-28(细胞表面抗原glyvolipid)、gd3独特型、globoh、磷脂酰肌醇蛋白聚糖3、n-羟乙酰神经氨酸、gm3、gmcsf受体α链、生长分化因子8、gp100、gpnmb(跨膜糖蛋白nmb)、gucy2c(鸟苷酸环化酶2c、鸟苷酸环化酶c(gc-c)、肠鸟苷酸环化酶、鸟苷酸环化酶c受体、热稳定肠毒素受体)、热休克蛋白、血凝素、乙型肝炎表面抗原、乙型肝炎病毒、her1(人表皮生长因子受体1)、her2、her2/neu、her3(erbb-3)、igg4、hgf/sf(肝细胞生长因子/散射因子)、hhgfr、hiv-1、组蛋白复合物、hla-dr(人类白细胞抗原)、hla-dr10、hla-drb、hmwmaa、人绒毛膜促性腺激素、hngf、人分散因子受体激酶、hpve6/e7、hsp90、htert、icam-1(细胞间粘附分子1)、独特型、igf1r(igf-1、胰岛素样生长因子1受体)、ighe、ifn-g、influezahemag-glutinin、ige、igefc区、ighe、白细胞介素(例如il-1、il-2、il-3、il-4、il-5、il-5、il-6、il-6r、il-7、il-8、il-9、il-9、il-10、il-11、il-12、il-13、il-13、il-15、il-17、il-17、il-17a、il-18、il-19、il-20、il-20、il-21、il-22、il-23、il-27、il-27、或il-28)、il31ra、ilgf2(胰岛素样生长因子2)、整合素(α4、αiibβ3、αvβ3、αvβ3、α4β7、α7、α5β1、α5β7、α5β1、α5β7、α5β8、il-α6β4、α7β7、αllβ3、α5β5、αvβ5)、干扰素γ诱导蛋白、itga2、itgb2、kir2d、lck、le、legumain、lewis-y抗原、lfa-1(淋巴细胞功能相关抗原1、cd11a)、lhrh、lingo-1、脂磷壁酸、liv1a、lmp2、lta、mad-ct-1、mad-ct-2、mage-1、mage-2、mage-3、magea1、magea3、mage4、mart1、mcp-1、mif(巨噬细胞移动抑制因子或糖基化抑制因子(gif))、ms4a1(跨膜4域亚家族a成员1)、msln(间皮素)、muc1(粘蛋白1、细胞表面相关(muc1)或多形上皮粘蛋白(pem))、muc1-klh、muc16(ca125)、mcp1(单核细胞趋化蛋白1)、melana/mart1、ml-iap、mpg、ms4a1(跨膜4域亚家族a)、mycn、髓鞘相关糖蛋白、肌肉生长抑制素、na17、narp-1、nca-90(粒细胞抗原)、nectin-4(asg-22me)、ngf、神经凋亡调节蛋白酶1、nogo-a、notch受体、nucleolin、neu癌基因产物、ny-br-1、ny-eso-1、ox-40、oxldl(氧化低密度脂蛋白)、oy-tes1、p21、p53非突变体、p97、page4、pap、抗-(n-羟乙酰神经氨酸)的互补位、pax3、pax5、pcsk9、pdcd1(pd-1、程序性细胞死亡蛋白1、cd279)、pdgf-rα(α型血小板衍生生长因子受体)、pdgfr-β、pdl-1、plac1、plap样睾丸碱性磷酸酶、血小板衍生生长因子受体β、磷酸钠共转运蛋白、pmel17、聚唾液酸、蛋白酶3(pr1)、前列腺癌、ps(磷脂酰丝氨酸)、前列腺癌细胞、铜绿假单胞菌、psma、psa、psca、狂犬病病毒糖蛋白、rhd(rh多肽1(rhpi)、cd240)、恒河猴因子、rankl、rantes受体(ccr1、ccr3、ccr5)、rhoc、ras突变体、rgs5、robo4、呼吸道合胞病毒、ron、肉瘤易位断点、sart3、硬骨素、slamf7(slamfamilymember7)、selectinp、sdc1(syndecan1)、sle(a)、somatomedinc、sip(鞘氨醇-1-磷酸)、生长抑素,精子蛋白17、ssx2、steap1(前列腺的六种跨膜上皮抗原1)、steap2、stn、tag-72(肿瘤相关糖蛋白72)、survivin、t-cellreceptor、tcell跨膜蛋白、tem1(肿瘤内皮标志物1)、tenb2、腱生蛋白c(tn-c)、tgf-α、tgf-β(转化生长因子β)、tgf-β1、tgf-β2(转化生长因子β2)、tie(cd202b)、tie2、tim-1(cdx-014)、tn、tnf、tnf-α、tnfrsf8、tnfrsf10b(肿瘤坏死因子受体超家族成员10b)、tnfrsf13b(肿瘤坏死因子受体超家族成员13b)、tpbg(滋养层糖蛋白)、trail-r1(肿瘤坏死凋亡诱导配体受体1)、trailr2(死亡受体5(dr5))、肿瘤相关钙信号转导2、肿瘤特异性糖基化muc1、tweak受体、tyrp1(糖蛋白75)、trop-2、trp-2、酪氨酸酶、vcam-1(cd106)、vegf、vegf-a、vegf-2(cd309)、vegfr-1、vegfr2或波形蛋白、wt1、xage1或表达任何胰岛素生长因子受体或任何表皮生长因子受体的细胞。 在具体的实施例中,本发明的双链接的偶联物可用于治疗癌症。目标癌症包括但不限于,肾上腺皮质癌、肛门癌、膀胱癌、大脑肿瘤(脑干神经胶质瘤、小脑星形细胞瘤、脑星形细胞瘤、室管膜瘤、成神经管细胞瘤、幕上原始神经外胚层和松果体肿瘤、视觉通路和下丘脑胶质瘤)、乳腺癌、类癌肿瘤、胃肠道癌症、未知小细胞癌、宫颈癌、结肠癌、子宫内膜癌、食道癌、肝外胆管癌、尤因家族肿瘤(pnet)、颅内生殖细胞肿瘤、眼癌、眼内黑色素瘤、胆囊癌、胃癌(胃癌)、性腺外生殖细胞瘤、孕周滋养细胞瘤、头颈癌、下咽癌、胰岛细胞癌、肾癌(肾细胞癌)、喉癌、白血病(急性淋巴细胞,急性髓系,慢性淋巴细胞,慢性粒细胞,毛细胞)、嘴唇和口腔癌症、肝癌、肺癌(非小细胞,小细胞)、淋巴瘤(艾滋病相关,中枢神经系统的,皮肤t细胞的,霍奇金病,非霍奇金病)、恶性间皮瘤、黑色素瘤、梅克尔细胞癌、转移性鳞状颈癌与隐匿性原发性癌、多发性骨髓瘤和其他浆细胞肿瘤、蕈样肉芽肿、骨髓增生异常综合征、骨髓增生异常、鼻咽癌、神经母细胞瘤、口腔癌、口咽癌、骨肉瘤、卵巢癌(上皮、生殖细胞瘤、低恶性肿瘤)、胰腺癌(外分泌,胰岛细胞癌)、副鼻窦和鼻腔癌、甲状旁腺癌、阴茎癌、嗜铬细胞瘤、垂体肿瘤、浆细胞肿瘤、前列腺癌横纹肌肉瘤、直肠癌、肾细胞癌(肾癌)、肾盂和输尿管(移行细胞)、唾腺癌、赛塞里综合症、皮肤癌(皮肤t细胞淋巴瘤,卡波西氏肉瘤,黑色素瘤)、小肠肿瘤、软组织肉瘤、胃癌、睾丸癌、胸腺瘤(恶性)、甲状腺癌、尿道癌症、子宫癌、不寻常的少年的癌症、阴道肿瘤、外阴肿瘤和维尔姆斯瘤。 在另一个具体的实施例中,本发明的偶联物、相应的组合物和方法可以用于治疗或预防自身免疫疾病。自身免疫性疾病包括但不限于,achlorhydra自身免疫性活动性慢性肝炎、急性播散性脑脊髓炎、急性出血性脑白质炎、艾迪生病、无精症、斑秃、肌萎缩侧索硬化症、强直性脊柱炎、抗gbm/tbm肾炎、抗磷脂综合征、抗异常酶综合征、关节炎、特应性过敏、特应性皮炎、自身免疫性再生障碍性贫血、自身免疫性心肌病、自身免疫性溶血性贫血、自身免疫性肝炎、自身免疫性内耳疾病、自身免疫性淋巴组织增生综合征、自身免疫性周围神经病、自身免疫性胰腺炎、自身免疫性多内分泌综合征i、ii和iii型、自身免疫性黄体酮皮炎、自身免疫性血小板减少性紫癜、自身免疫性葡萄膜炎、balo病/balo同心硬化症、bechets综合征、berger氏病、bickerstaff脑炎、blau综合征、大疱性类天疱疮、castleman病、chagas病、慢性疲劳免疫功能障碍综合征、慢性炎性脱髓鞘性多发性神经病、慢性复发性多灶性骨髓炎、慢性莱姆病、慢性阻塞性肺病、churg-strauss综合征、瘢痕性类天疱疮、乳糜泄、cogan综合征、冷凝集素病、补体成分2缺乏症、颅骨动脉炎、crest综合征、crohns病(特发性炎症性肠病)、库欣综合征、皮肤白细胞增多性血管炎、德戈氏病、dercum氏病、疱疹样皮炎、皮肌炎、1型糖尿病、弥漫性皮肤系统性硬化症、dressler综合征、盘状红斑狼疮、湿疹、子宫内膜异位症、附着点炎相关的关节炎、eosinophilic筋膜炎、大疱性表皮松解症、结节性红斑、特发性混合性冷球蛋白血症、伊文氏综合征、纤维发育不良性骨化症、纤维肌痛、纤维化性肌炎、纤维性肺泡炎、胃炎、胃肠类天疱疮、巨细胞动脉炎、肾小球肾炎、古德帕斯丘尔综合征、格雷夫斯病、格林-巴利综合征、桥本氏脑炎、桥本氏甲状腺炎、溶血性贫血、过敏性紫癜、妊娠性肝炎、化脓性汗腺炎、休斯综合征(抗磷脂综合征)、低丙球蛋白血症、特发性炎性脱髓鞘疾病、特发性肺纤维化、特发性血小板减少性紫癜(自身免疫性血小板减少性紫癜)、iga肾病(伯杰氏病)、包涵体肌炎、炎性脱髓鞘性多神经炎、间质性膀胱炎、过敏性肠综合征、少年特发性关节炎、青少年类风湿性关节炎、川崎氏病、朗伯-伊顿重症肌无力综合征、白细胞碎屑性血管炎、扁平苔癣、硬化性硬化症、线状iga疾病(lad)、lougehrig病(也称肌萎缩侧索硬化症)、狼疮性肝炎、红斑狼疮、majeed综合征、美尼尔氏病、显微镜下多动脉炎、米勒-费希尔综合征、混合性结缔组织病、硬斑病、穆罕默德-哈贝曼病、麦考利综合征、多发性骨髓瘤、多发性硬化症、重症肌无力、肌炎、嗜睡症、视神经脊髓炎(devic病)、神经性肌强直、眼睑瘢痕性类天疱疮、opsoclonusmyoclonus综合征、ord甲状腺炎、回文风湿病、pandas(与链球菌相关的小儿自身免疫性神经精神病)、paraneoplastic小脑变性、阵发性睡眠性血红蛋白尿症、parryromberg综合征、parsonnage-turner综合征、睫状体平部炎、天疱疮、寻常型天疱疮、贫血、周围脑脊髓炎、poems综合征、结节性多动脉炎、风湿性多肌痛、多发性肌炎、原发性胆汁性肝硬化、原发性硬化性胆管炎、进行性炎症性神经病变、牛皮癣、牛皮癣性关节炎、坏疽性皮肤炎、纯红细胞再生障碍、rasmussen脑炎、雷诺现象、复发性多软骨炎、赖特综合征、不宁腿综合症、后神经纤维化、类风湿性关节炎、类风湿热、结节病、精神分裂症、施密特综合征、schnitzler综合征、施尼茨勒综合征、巩膜炎、硬皮病、干燥综合征、脊椎关节病、粘稠血症、still病、僵人综合征、亚急性细菌性心内膜炎、苏萨克综合征、sweet综合征、小舞蹈病、交感神经性贫血、takayasu动脉炎、颞动脉炎(巨细胞动脉炎)、tolosa-hunt综合征、横贯性脊髓炎、溃疡性结肠炎(特发性炎性肠病)、未分化结缔组织病、未分化脊柱关节病、血管炎、白癜风、韦格纳肉芽肿病、威尔逊氏综合征、威斯科特-奥尔德里奇综合征。 在另一个具体的实施例中,本发明中双链接偶联物上的结合分子,可用于治疗或预防自身免疫疾病,包括但不限于,抗弹性蛋白抗体、abys抗上皮细胞抗体、抗地下室膜iv型胶原蛋白抗体、抗核抗体、抗dsdna、抗ssdna、抗心磷脂抗体igm、igg、抗乳糜泻抗体、抗磷脂抗体igk、igg、抗sm抗体、抗线粒体抗体、甲状腺抗体、微粒体抗体、t细胞抗体、甲状腺球蛋白抗体、抗scl-70、抗jo、抗u.sub.1rnp、抗la/ssb、抗ssa、抗ssb、抗壁细胞抗体、抗组蛋白、抗rnp、c-anca、p-anca、抗着丝粒、抗纤维蛋白原、抗gbm抗体、抗神经节苷脂抗体、抗desmogein3抗体、抗p62抗体、抗sp100抗体、抗线粒体(m2)抗体、类风湿因子抗体、抗mcv抗体、抗拓扑异构酶抗体、抗中性粒细胞胞质(canca)抗体。 在某些优选的实施例中,本专利申请中偶联物上的结合分子,可以与自身免疫性疾病相关的激活淋巴细胞上表达的受体或受体复合物相结合。受体或受体复合物包含,免疫球蛋白基因超家族成员(例如cd2、cd3、cd4、cd8、cd19、cd20、cd22、cd25、cd27、cd28、cd30、cd33、cd37、cd38、cd56、cd70、cd79、cd79b、cd90、cd152/ctla-4、pd-1、pd-l1或icos)、tnf受体超家族成员(例如cd27、cd40、cd95/fas、cd134/ox40、cd137/4-1bb、inf-r1、tnfr-2、rank、taci、bcma、骨保护素、apo2/trail-r1、trail-r2、trail-r3、trail-r4和apo-3)、整合蛋白、细胞因子受体、趋化因子受体、主要组织相容性蛋白、凝集素(c型、s型或i型)或补体控制蛋白。 在另一个具体实施例中,可用的对病毒或微生物抗原具有免疫特异性的细胞结合配体是人源化或人单克隆抗体。“病毒抗原”包括但不限于,任何能够引发免疫应答的病毒肽,多肽蛋白(例如hivgp120、hivnef、rsvf糖蛋白、流感病毒神经氨酸苷酶、流感病毒血凝素、htlvtax、疱疹单纯疱疹病毒糖蛋白(例如gb、gc、gd和ge)和乙型肝炎表面抗原)。“微生物抗原”包括但不限于,任何能够引发免疫应答的微生物肽、多肽、蛋白质、糖、多糖或脂质分子(例如细菌、真菌、致病原生动物或酵母多肽、包括如lps和荚膜多糖5/8)。可用于治疗病毒或微生物感染的抗体的实例,包括但不限于:帕利珠单抗,它是用于治疗rsv感染的,人源化抗呼吸道合胞病毒单克隆抗体;pro542,是一种cd4融合抗体,用于治疗hiv感染;奥斯他韦,是一种用于治疗乙型肝炎病毒的人抗体;protvir,是一种人源化igg1抗体,用于治疗巨细胞病毒,和抗lps抗体。 以双连接子链接的本发明中的细胞结合分子-药物偶联物可用于治疗感染性疾病。这些感染性疾病包括但不限于,不动杆菌属感染、放线菌病、非洲昏睡病(非洲锥虫病)、艾滋病(获得性免疫缺陷综合症)、阿米巴病、无形体病、炭疽、溶血性耶尔森菌感染、阿根廷出血热、蛔虫病、曲霉病、星状病毒感染、巴贝斯虫病、蜡状芽孢杆菌感染、细菌性肺炎、细菌性阴道炎、类杆菌感染、小袋虫病、蛔虫感染、bk病毒感染、黑色发结节病、人芽囊原虫感染、芽生菌病、玻利维亚出血热、疏螺旋体感染、肉毒中毒(和婴儿肉毒中毒)、巴西出血热、布鲁氏杆菌病、伯克霍尔德氏菌感染、布鲁里溃疡、杯状病毒感染(诺如病毒和沙波病毒)、弯曲杆菌病、念珠菌病(念珠菌病、鹅口疮)、猫抓病、蜂窝组织炎、chagas病(美洲锥虫病)、子囊、水痘、衣原体、肺炎衣原体感染、霍乱、色素母细胞瘤、华支睾吸虫、艰难梭状芽孢杆菌感染、球孢子菌病、科罗拉多蜱热病、普通感冒(急性病毒性鼻咽炎、急性鼻炎)、克雅氏病、克里米亚-刚果出血热、隐球菌病、隐孢子虫病、皮肤幼虫迁徙、环孢子虫病、肠杆菌感染、肠道病毒感染、流行性斑疹伤寒、传染性红斑(第五种疾病)、急疹、姜片虫病、肝片吸虫病、致命性家族性失眠、丝虫病、产气荚膜梭菌食物中毒、自由活体阿米巴感染、梭杆菌感染、气性坏疽(梭菌性肌坏死)、地丝菌病、格斯特曼-斯特拉斯勒-谢克尔病综合征、贾第鞭毛虫病、马鼻疽、淋病、肉芽肿性腹泻(第五性病)、a群链球菌感染、b群链球菌感染、流感嗜血杆菌感染、手足口病(hfmd)、汉坦病毒肺综合征、幽门螺杆菌感染、溶血性尿毒综合征、肾综合征出血热、甲型肝炎、乙型肝炎、丙型肝炎、丁型肝炎、戊型肝炎、单纯性疱疹、组织胞浆菌病、钩虫感染、人类博卡病毒感染、人类ewingii埃里希体病、人类粒细胞无形体病、人类偏肺病毒感染、人类单核细胞埃里希体病、人乳头瘤病毒感染、人副流感病毒感染、膜壳绦虫病、艾巴氏病毒传染性单核细胞增多症(单)、流行性感冒、等孢子虫病、川崎病、角膜炎、金格杆菌感染、库鲁病、拉沙热、军团病(退伍军人症)、军团病(庞蒂亚克热)、利什曼病、莱姆病、淋巴丝虫病(象皮病)、淋巴细胞性脉络丛脑膜炎、疟疾、马尔堡出血热、麻疹、类鼻疽病(惠氏病)、脑膜炎、脑膜炎球菌病、后殖吸虫病、微孢子虫病、传染性软疣、腮腺炎、小鼠斑疹伤寒(地方性斑疹伤寒)、支原体肺炎、足菌肿、蝇蛆病、新生儿结膜炎(新生儿眼病)、变异型克雅氏病(vcjd、nvcjd)、诺卡氏菌病、盘尾丝虫病(河盲症)、副球孢子菌病(南美芽生菌病)、肺吸虫病、巴斯德氏菌病、头虱、体虱、阴虱、盆腔炎、百日咳、鼠疫、肺炎球菌感染、肺孢子虫肺炎、肺炎、脊髓灰质炎、普氏菌感染、原发性阿米巴脑膜脑炎、进行性多灶性白质脑病、鹦鹉热、q热、狂犬病、鼠咬热、呼吸道合胞病毒感染、鼻孢子虫病、鼻病毒感染、立克次体感染、立克次体痘、裂谷热、落基山斑疹热、轮状病毒感染、风疹、沙门氏菌病、sars(严重急性呼吸综合征)、疥疮、血吸虫病、败血症、志贺氏菌病(bacillary痢疾)、带状疱疹(带状疱疹)、天花(天花)、孢子丝菌、葡萄球菌食物中毒、感染金黄色葡萄球菌、粪类圆线虫病、梅毒、绦虫病、破伤风、须癣(barber痒)、头皮癣、体癣、股癣、手癣、掌黑癣、足癣(香港脚)、甲癣(灰指甲)、花斑癣、弓蛔虫病(眼幼虫移行症)、弓蛔虫病(内脏幼虫移行症)、弓形体病、旋毛虫病、滴虫病、鞭虫病(鞭虫感染)、肺结核、兔热病、解脲脲原体感染、委内瑞拉马脑炎、委内瑞拉出血热、病毒性肺炎、西尼罗河热、白毛结节病(白癣)、假结核耶尔森氏菌、耶尔森氏鼠疫杆菌肠道病、黄热病、接合菌病。 本发明的细胞结合剂,更优选为抗体,抗病原菌株包括但不限于,鲍氏不动杆菌、以色列放线菌、放线菌和丙酸杆菌、布氏锥虫、hiv(人免疫缺陷病毒病毒)、溶组织内阿米巴、无形体属、炭疽芽孢杆菌、溶血弧菌、胡宁病毒、蛔虫属、曲霉属、星状病毒科、巴贝虫属、蜡状芽孢杆菌、多种细菌、拟杆菌属、大肠杆菌、蛔虫属、bk病毒、结节菌、人芽囊原虫、皮炎芽生菌、马丘波病毒、疏螺旋体属、肉毒梭菌、清风藤属、布鲁氏菌属、通常为洋葱伯克霍尔德菌和其他伯克霍尔德氏菌种、溃疡分枝杆菌、杯状病毒科、弯曲杆菌属、通常为白色假丝酵母和其他假丝酵母属、汉赛巴尔通体、a群链球菌和葡萄球菌、克氏锥虫、杜克雷嗜血杆菌、vzv、沙眼衣原体、科罗拉多蜱热病毒、鼻病毒、冠状病毒、cjd朊病毒、克里米亚-刚果出血热病毒、新型隐球菌、隐孢子虫属、巴西钩虫、多种寄生虫、环孢子虫、带状绦虫、巨细胞病毒、登革热病毒(den-1、den-2、den-3和den-4)-黄病毒、脆弱双歧杆菌、白喉棒状杆菌、裂头绦虫、麦地那龙线虫、埃博拉病毒、棘球绦虫属、埃立克体肠球菌属、肠道病毒属、普氏立克次体、细小病毒b19、人疱疹病毒6和人疱疹病毒7、布氏姜片虫、肝片吸虫和巨大片吸虫、ffi朊病毒、丝虫目超家族、产气荚膜梭菌、梭杆菌属、其他梭状芽孢杆菌、白地霉、gss朊病毒、肠道贾第虫、伯克霍尔德氏菌、刺孢小芽孢杆菌和革兰氏假丝酵母、淋球菌、肉芽肿克雷伯氏菌、化脓性链球菌、无乳链球菌、流感嗜血杆菌、肠道病毒、主要是柯萨奇a病毒和肠道病毒71、无名病毒、幽门螺旋杆菌、大肠杆菌o157:h7、布尼亚病毒科、甲型肝炎病毒、乙型肝炎病毒、丙型肝炎病毒、丁型肝炎病毒、戊型肝炎病毒、单纯疱疹病毒1、单纯疱疹病毒2、荚膜组织胞浆菌、十二指肠腺瘤和壶腹癌流感嗜血杆菌、人博卡病毒、埃里希体、嗜吞噬细胞无嗜血杆菌、人偏肺病毒、查菲埃里希体、人乳头瘤病毒、人副流感病毒、微小膜壳绦虫和缩小膜壳绦虫、艾巴氏病毒、正粘病毒科家族、贝氏等孢球虫、金格杆菌、肺炎克雷伯菌、克雷伯氏菌、嗜肺军团菌、嗜肺军团菌、嗜肺军团菌、利什曼原虫属、麻风分枝杆菌和结核分枝杆菌、钩端螺旋体属、单核细胞增多性李斯特氏菌、伯氏疏螺旋体和其他疏螺旋体属物种、班氏旋毛虫和马来丝虫、淋巴细胞脉络丛脑膜炎病毒(lcmv)疟原虫属、马尔堡病毒、麻疹病毒、类鼻疽伯克霍尔德氏菌、脑膜炎奈瑟氏球菌、横川后殖吸虫、小孢子虫目门、传染性软疣病毒(mcv)、腮腺炎病毒、伤寒立克次氏体、肺炎支原体、多种细菌和真菌寄生双翅蝇幼虫、沙眼衣原体和淋病奈瑟菌、vcjd朊病毒、诺卡氏菌和其他诺卡氏菌属、盘尾丝虫属、盘鲍拟亚科、副龙属西马尼和其他副属、巴斯德氏菌属、头虱、人体虱、百日咳博德特氏菌鼠疫耶尔森氏菌、肺炎链球菌、肺炎球菌、脊髓灰质炎病毒、普雷沃氏菌属、奈氏格氏杆菌、jc病毒、鹦鹉热衣原体、伯氏考克斯体、狂犬病病毒、单链球菌和螺旋菌、呼吸道合胞病毒、鼻孢子菌、鼻病毒、立克次体属、由小株立克次体、裂谷热病毒、立克次体立克次体、轮状病毒、风疹、沙门氏菌属、sars冠状病毒、人疥螨、血吸虫属、体细胞属、志贺菌属、水痘带状疱疹病毒、天花少校或天花小、申克孢子丝菌、金黄色葡萄球菌属、金黄色葡萄球菌、链球菌化脓、圆线虫、梅毒螺旋体、绦虫属、破伤风、癣属癣音铀、癣属、絮状表皮癣菌、红色毛癣菌、须毛癣菌、红色毛癣菌、威尼克外瓶黴、毛癣菌属属、细胞死亡属、弓箭毒或弓箭毒、刚地弓形虫、旋毛虫、阴道毛滴虫、三丘里三种、结核分枝杆菌、弗朗西拉图拉菌、尿素和马脑炎病毒、委内瑞拉马脑炎病毒、霍乱弧菌、瓜纳里托病毒、西尼罗河病毒、beigelii丝孢、假结核耶尔森氏菌、小肠结肠炎耶尔森氏菌、黄热病病毒、毛霉菌目阶(毛霉菌病)和虫霉目阶(虫霉属真菌病)、毛霉菌目绿脓杆菌、弯曲杆菌(弧菌)、气单胞菌、艾氏菌、耶尔森氏菌、志贺痢疾杆菌、志贺氏杆菌、志贺氏菌、沙门氏菌、伤寒沙门氏菌、雅司螺旋体、奋森氏螺旋体、伯氏疏螺旋体、细螺旋体、卡氏肺孢子虫、流产布鲁氏菌、布鲁杆菌、布鲁氏菌、支原体属、普氏立克次体、恙虫病立克次氏体、衣原体属、致病性真菌(烟曲霉、白色念珠菌、荚膜组织胞浆菌)、原生动物(溶组织内阿米巴、tenas毛滴虫、hominis毛滴虫、冈比亚锥虫、罗得西亚锥虫、罗氏利什曼原虫、热带利什曼原虫、巴西利什曼原虫、肺孢子虫肺炎、间日疟原虫、恶性疟原虫、疟原虫疟疾)或helminiths(日本血吸虫、曼氏血吸虫、埃及血吸虫和钩虫)。 其他用作本发明的细胞结合剂,治疗病毒性疾病的抗体,包括但不限于,抗下列致病性病毒抗原的抗体:痘病毒、疱疹病毒、腺病毒、小黄病毒、肠病毒、小核糖核酸病毒、细小病毒、呼肠病毒、逆转录病毒、流感病毒、副流感病毒、腮腺炎、麻疹、呼吸道合胞病毒、风疹、虫媒病毒、弹状病毒、沙门氏菌、非a/非b型肝炎病毒、鼻病毒、冠状病毒、罗托病毒、致癌病毒、如hbv(肝细胞癌)、人乳头状瘤病毒(宫颈癌、肛门癌)、卡波济氏肉瘤相关的疱疹病毒(卡波济氏肉瘤肉瘤)、人类疱疹病毒第四型(鼻咽癌、伯基特淋巴瘤、原发性中枢神经系统淋巴瘤)、瘤病毒(默克尔细胞癌)、sv40(猿猴病毒40)、hcv(肝细胞癌)、htlv-1(成人t细胞白血病/淋巴瘤);免疫紊乱导致病毒,如人类免疫缺陷病毒(艾滋病)、中枢神经系统病毒,如jcv(进行性多灶性脑白质病)、丙型肝炎病毒(亚急性硬化性全脑炎)、lcv(淋巴细胞性脉络丛脑膜炎)、亚博病毒脑炎、正粘病毒(脑炎性脑炎)、rv(狂犬病)、长鼻病毒、疱疹病毒脑膜炎、拉姆齐亨特综合征ii型、脊髓灰质炎病毒(脊髓灰质炎病毒、后脊髓灰质炎综合征)、htlv-1(热带麻痹性麻痹))、巨细胞病毒(巨细胞病毒视网膜炎、hsv(疱疹性角膜炎)、心血管病毒,如cbv(心包炎、心肌炎)、呼吸系统/急性病毒性鼻内炎/病毒性肺炎,如爱泼斯坦-巴尔病毒(ebv感染/传染性单核病)、巨细胞病毒、非典冠状病毒(严重急性呼吸综合征)或正黏液病毒、流感病毒a/b/c(流感/禽流感)、副粘病毒、人类副流感病毒、rsv(人类呼吸道合胞病毒)、hmpv、消化系统病毒(腮腺炎病毒、巨细胞病毒(巨细胞病毒食管炎)、腺病毒(腺病毒感染)、轮状病毒、诺瓦克病毒、星状病毒、冠状病毒、乙型肝炎病毒、cbv、甲型肝炎病毒、丙型肝炎病毒、丁型肝炎病毒、戊型肝炎病毒、hgv)、泌尿生殖病毒,如bk病毒、muv(腮腺炎)。 更进一步,本发明也包括用本发明中偶联物和可接受的载体,稀释剂或辅料构成的组合物,以治疗癌症、感染或自身免疫性疾病。治疗癌症、感染和自身免疫性疾病的方法可以在体外,体内或离体实施。体外用途的实例包括用它处理细胞培养物,以杀死除了不表达靶抗原的变体以外的所有细胞;或者杀死表达不需要的抗原的变体。离体使用的例子包括在进行移植(hsct)之前对造血干细胞(hsc)进行处理,以杀死患病或恶性肿瘤细胞。例如,在癌症治疗中的自体移植之前或在自身免疫性疾病的治疗中从骨髓中去除肿瘤细胞或淋巴细胞,或在移植之前为了防止移植物抗宿主疾病从同种异体骨髓或组织中除去t细胞和其他淋巴细胞。这样的临床离体治疗可以按如下步骤进行:从患者或其他个体收获骨髓,然后在含有血清的培养基中约37℃下孵育约30分钟至约48小时,在该培养基中加入本发明的偶联物,浓度范围从约1pm至0.1mm。具体的药物浓度和孵育时间应当由专业临床医师决定。孵育后,用含血清的培养基洗涤骨髓细胞,并按照已知的方法通过静脉注射给患者。若患者在骨髓采集和再输注治疗细胞之间,还接受其它治疗(例如消融化疗或全身辐射疗程)的情况下,应使用标准医疗设备将处理后的骨髓细胞在液氮中冷冻储存。 用于偶联的药物/细胞毒性剂 在本发明中,可与细胞结合分子偶联的药物是包括细胞毒性剂在内的小分子药物。本发明中的“小分子药物”泛指分子量为100至4000,更优200至3000的有机、无机或金属有机化合物。这些小分子药物在本领域文献中已被充分描述,如wo0a2和美国专利4,956,303。小分子药物包括已知的药物和即将成为已知的药物。 已知的药物包括但不限于, 1)化疗药物:a)烷基化剂,如氮芥:氯苯那普,氯普那嗪,环磷酰胺,达喀尔巴嗪,雌二醇氮芥,异环磷酰胺,氮芥,盐酸二甲氧胺,氧化二氮芥,盐酸氨氯地平,麦考酚酸,卫矛醇,呱泊溴烷,新氮芥,苯芥胆甾醇,松龙苯芥,噻替呱,曲磷胺对,尿嘧啶;cc-1065(包括其阿多来新、卡折来新、比折来新及其合成类似物);多卡霉素(包括kw-2189和cbi-tmi、及其合成类似物);苯并二氮二聚体(例如吡咯并苯二氮(pbd)或托美霉素,吲哚并苯并二氮杂,咪唑并苯并噻二氮杂或恶唑烷并苯并二氮杂的二聚体);亚硝基脲(卡莫司汀,洛莫司汀,氯化梭菌素,福莫司汀,尼莫司汀,拉莫司汀);烷基磺酸盐(白苏芬、树苏芬、磺胺异丙磺胺和皮苏芬);三氮烯(达喀尔巴嗪);含铂化合物(卡铂,顺铂,奥沙利铂);吖丙啶类,如苯并二氢吡喃酮,卡洛酮,美妥替派和乌雷多巴;乙烯亚胺和甲基三聚氰胺,包括六甲蜜胺,三亚乙基三胺,三乙基磷酰胺,三亚乙基硫代磷酰胺和三羟甲基甲基胺; b)植物生物碱:如长春花生物碱(长春新碱,长春碱,长春地辛,长春瑞滨,去甲长春碱);紫杉醇类(紫杉醇,多西紫杉醇及其类似物);美登素类(dm1、dm2、dm3、dm4、美登素、安沙霉素及其类似物);cryptophycin(特别是cryptophycin1和cryptophycin8);埃博霉素,软珊瑚醇,迪莫利德,草苔虫内酯,海兔毒素,澳瑞斯汀,tubulysins,cephalostatin;pancratistatin;erbulins;sarcodictyin;海绵抑制素; c)dna拓扑异构酶抑制剂,例如依托泊苷替尼(9-氨基喜树碱,喜树碱,克立那托,多拉霉素,依托泊苷,磷酸依托泊苷,伊立替康,米托蒽醌,诺消灵,视黄酸(视黄醇),替尼泊苷,拓扑替康,9-硝基喜树碱(rfs2000));丝裂霉素(丝裂霉素c); d)抗代谢物,例如抗叶酸剂,dhfr抑制剂(甲氨蝶呤,曲麦克特,二甲叶酸,蝶罗呤,氨喋呤(4-氨基苯甲酸)或其他叶酸类似物);imp脱氢酶抑制剂(麦考酚酸,噻唑呋林,利巴韦林,eicar);核糖核苷酸还原酶抑制剂(羟基脲,去铁胺);嘧啶类似物,尿嘧啶类似物(安西他滨,阿扎胞苷,6-氮尿嘧啶,卡培他滨(希罗达),卡莫氟,阿糖胞苷,双脱氧尿苷,脱氧氟尿苷,依诺他滨,5-氟尿嘧啶,氟尿苷,ratitrexed(tomudex);胞嘧啶类似物(阿糖胞苷,胞嘧啶阿拉伯糖苷,氟达拉滨);嘌呤类似物(硫唑嘌呤,氟达拉滨,巯嘌呤,硫胺素,硫鸟嘌呤);叶酸补充剂,如弗洛林酸;和烟酰胺磷酸核糖基转移酶(nampt)的抑制剂; e)激素疗法剂,如受体拮抗剂,抗雌激素(甲地孕酮,雷洛昔芬,他莫昔芬),lhrh兴奋剂(戈斯他林,醋酸亮丙瑞林);抗雄激素药(比卡鲁胺,氟他胺,卡鲁司酮,丙酸倍他雄酮,表雄甾醇,戈舍瑞林,亮丙瑞林,美替利定,尼鲁米特,睾内酯,曲洛司坦及其他雄激素抑制剂);维甲类化合物,维生素d3类似物(cb1093,eb1089,kh1060,胆钙化醇,麦角钙化甾醇);光动力疗法剂(维替泊芬,酞菁,光敏剂pc4,去甲氧基-竹红菌素a);细胞因子(干扰素-α,干扰素-γ,肿瘤坏死因子(tnf),含tnf的人蛋白); f)激酶抑制剂,如bibw2992(抗-egfr/erb2),伊马替尼,吉非替尼,呱加他尼,索拉非尼,达沙替尼,舒尼替尼,厄洛替尼,尼洛替尼,拉帕替尼,阿西替尼,帕唑帕尼,凡德他尼,e7080(抗vegfr2),mubritinib,普纳替尼(ap24534),bafetinib(inno-406),bosutinib(ski-606),卡博替尼,维莫德吉,iniparib,鲁索利替尼,cyt387,阿西替尼,tivozanib,索拉非尼,贝伐单抗,西妥昔单抗,曲妥珠单抗,雷珠单抗,帕尼单抗,伊斯平斯;g)聚(adp-核糖)聚合酶(parp)抑制剂,如奥拉帕里、尼拉帕里、依尼帕里、塔拉佐帕里、维利帕里、维利帕里、cep9722(cephalon)、e7016(eisai)、bgb-290(beigene)、3-氨基苯甲酰酰胺; h)抗生素,如烯二炔类抗生素(加利车霉素,特别是加利车霉素γ1,δ1,α1和β1(参考j.med.chem.1996,39(11),2103-2117;angewchemintl.ed.engl.1994,33:183-186),达因霉素,包括达因霉素a和脱氧米霉素,埃斯培拉霉素,卡塔尔霉素,c-1027,maduropeptin,新卡嗪奥斯汀和相关色蛋白烯二炔抗生素),aclacinomysins,放线菌素,安曲霉素,重氮丝氨酸,博来霉素,卡诺霉素,卡拉霉素,洋红霉素,嗜癌素,色霉素,达金霉素,柔红霉素,去柔红霉素,6-重氮-5-氧代-l-去甲亮氨酸,阿霉素,吗啉-阿霉素,氰基吗啉-阿霉素,2-吡咯啉阿霉素和脱氧柔红霉素,表柔比星,阿柔比星,伊达比星,马可霉素,nitomycin,霉酚酸,诺加霉素,橄榄霉素,peplomycin,potfiromycin,嘌呤霉素,奎拉霉素,罗道霉素,链黑霉素,链脲霉素,杀结核菌素,乌苯美司,净司他丁,佐柔比星; i)其他,如聚酮化合物(番荔素),特别是bullatacin和bullatacinone;吉西他滨,环氧酶素(如卡菲偌米布),硼替佐米,沙利度胺,来那度胺,pomalidomide,tosedostat,zybrestat,plx4032,sta-9090,stimuvax,allovectin-7,xegeva,provenge,yervoy,异戊二烯化抑制剂(如洛伐他汀),多巴胺能神经毒素(如星形孢菌素),放线菌素(如放线菌素d,更生霉素),博莱霉素(如博来霉素a2,博莱霉素b2,培洛霉素),蒽环类抗生素(如柔红霉素),鹅膏毒素,阿霉素(亚德里亚霉素),伊达比星,表柔比星,吡柔比星,佐柔比星,米托蒽醌,mdr抑制剂(如维拉帕米),ca2+atp酶抑制剂(如毒胡萝卜素),组蛋白去乙酰酶抑制剂(伏立诺他,罗米地辛,帕比司他,丙戊酸,mocetinostat(mgcd0103),belinostat,pci-24781,恩替诺特,sb939,resminostat,givinostat,ar-42,cudc-101,萝卜硫素,曲古抑菌素a);塞来昔布,格列酮类,表没食子儿茶素没食子酸酯,双硫仑,salinosporamidea;抗肾上腺药物,如氨鲁米特,米托坦,曲洛司坦,醋葡醛内酯,醛磷酰胺,氨基乙酰丙酸,安吖啶,阿拉伯糖苷,bestrabucil,比生群,edatraxate,defofamine,美可辛,地吖醌,依氟鸟氨酸(dfmo),elfomithine,依利醋铵,依托格鲁,硝酸镓,胞嘧啶,羟基脲,伊班膦酸盐,香菇多糖,氯尼达明,米托胍腙,米托蒽醌,莫呱达醇,二胺硝吖啶,喷司他丁,蛋氨氮芥,吡柔比星,鬼臼酸,2-乙肼,甲基苄肼;呱嗪二酮丙烷;根霉素;西佐;螺环锗;细格孢氮杂酸;三亚胺醌;三氯三乙胺;单端孢霉烯(特别是t-2毒素,疣孢菌素a,杆孢菌素a和anguidine),聚氨酯,sirna,反义药物和核酸分解酶。 2)自身免疫疾病药物,包括但不限于,环孢菌素,环孢菌素a,氨基己酸,硫唑嘌呤,溴隐亭,苯丁酸氮芥,氯喹,环磷酰胺,皮质类固醇(例如安西奈德,倍他米松,布地奈德,氢化可的松,氟尼缩松,丙酸氟替卡松,氟可龙达那唑,地塞米松,曲安奈德,二丙酸倍氯米松),dhea,依那西普,羟基氯喹,英夫利昔单抗,美洛昔康,甲氨蝶呤,麦考酚酸酯,泼尼松,西罗莫司,他克莫司。 3)抗感染性疾病药物,包括但不限于a)氨基糖苷类:阿米卡星,阿司米星,庆大霉素(奈替米星,西索米星,异帕米星),潮霉素b,卡那霉素(阿米卡星,阿贝卡星,氨基脱氧卡那霉素,地贝卡星,妥布霉素),新霉素(framycetin,巴龙霉素,核糖霉素),奈替米星,壮观霉素,链霉素,妥布霉素,甲基姿苏霉素;b)酰胺醇类:迭氮氯霉素,氯霉素,氟苯尼考,甲砜霉素;c)安沙霉素:格尔德霉素,除莠霉素;d)碳青霉烯类:比阿培南,多利培南,厄他培南,亚胺培南/西司他丁,美罗培南,帕尼培南;e)头孢烯:碳头孢烯(洛拉卡比),头孢乙腈,氯氨苄青霉素,头孢拉定,头孢羟氨,头孢洛宁,头孢噻啶,头孢噻吩或头孢金素,头孢氨苄,头孢来星,头孢孟多,头孢匹林,羟胺唑头孢菌素,氟唑头孢菌素,孢西酮,唑啉头孢菌素,头孢拉宗,头孢卡品,头孢达肟,头孢吡,头孢克肟,头孢西丁,头孢罗齐,头孢甲氧环烯胺,头孢替唑,头孢呋辛,头孢克肟,头孢地尼,头孢托仑,头孢吡,头孢他美,头孢甲肟,头孢地嗪,头孢尼西,头孢呱酮,头孢雷特,头孢噻肟,噻乙胺唑头孢菌素,头孢唑兰,头孢氨苄,头孢咪唑,头孢匹胺,头孢匹罗,头孢泊肟,头孢罗齐,头孢喹诺,头孢磺啶,头孢他啶,头孢特仑,头孢布腾,头孢噻林,头孢唑肟,头孢吡普,头孢曲松,头孢呋辛,头孢唑南,头霉素(头孢西丁,头孢替坦,头孢氰唑),氧(碳)头孢烯(氟氧头孢,拉氧头孢);f)糖肽:博来霉素,万古霉素(奥利万星,特拉万星),替考拉宁(达巴万星),雷莫拉宁;g)甘氨酰环素:如替加环素;h)β-内酰胺酶抑制剂:青霉烷(舒巴坦,他唑巴坦),氧青霉烷(克拉维酸);i)林可酰胺:克林霉素,林可霉素;j)脂肽:达托霉素,a54145,钙依赖性抗生素(cda);k)大环内酯类:阿奇霉素,克霉素,克拉霉素,地红霉素,红霉素,氟雷霉素,交沙霉素,酮内酯(泰利霉素,塞红霉素),麦迪霉素,米卡霉素,竹桃霉素,利福霉素(异烟肼、利福平,利福布丁,利福喷汀),罗匹霉素,罗红霉素,大观霉素,螺旋霉素,他克莫司(fk506),醋竹桃霉素,泰利霉素;l)单环胺:氨曲南,替吉莫南;m)恶唑烷酮类:利奈唑胺;n)青霉素类:阿莫西林,氨苄青霉素(匹氨西林,海洛西林,巴氨西林,氨苄青霉素,阿霉素),阿替代西林,阿洛西林,苄青霉素,苄星青霉素苄青霉素,苄星青霉素苯氧甲基青霉素,克洛西林,普鲁卡因青霉素(美替西林),美洛西林,甲氧西林,萘夫西林,苯唑西林,醋甲西林,青霉素,非奈西林,苯氧基甲基青霉素,呱拉西林,氨苄西林,磺苯西林,替莫西林,替卡西林;o)多肽:杆菌肽,粘菌素,多粘菌素b;p)喹诺酮类:阿拉曲沙星,巴洛沙星,环丙沙星,克林沙,达氟沙星,二氟沙星,依诺沙星,恩诺沙星,加雷沙星,加替沙星,吉米沙星,格帕沙星,卡诺曲伐沙星,左氧氟沙星,洛美沙星,麻保沙星,莫西沙星,那氟沙星,诺氟沙星,奥比沙星,氧氟沙星,培氟沙星,曲伐沙星,格帕沙星,西他沙星,司帕沙星,替马沙星,托沙星,曲伐沙星;q)链阳性菌素:普那霉素,奎奴普丁/达福普汀;r)磺胺类:氨芐磺胺,偶氮磺胺,磺胺嘧啶,磺胺甲异唑、磺胺酰亚胺、磺胺吡啶、磺胺异恶唑、甲氧苄啶、磺胺甲恶唑(复方磺胺甲恶唑);s)类固醇抗菌药物:如夫西地酸;t)四环素类:强力霉素,金霉素,氯米西环素,地美环素,雷莫昔林,美西环素,美他环素,米诺环素,土霉素,潘美环素,吡咯烷甲基四环素,四环素,甘氨酰环素(如替加环素);u)其他类型的抗生素:番荔枝素,胂凡纳明,细菌萜醇抑制剂(杆菌肽),danal/ar抑制剂(环丝氨酸),dictyostatin,圆皮海绵内酯,软珊瑚醇,埃博霉素,乙胺丁醇,依托泊苷,法罗培南,夫西地酸,呋喃唑酮,异烟肼,laulimalide,甲硝唑,莫匹罗星,nam合成抑制剂(例如磷霉素),呋喃妥因,紫杉醇,普兰西霉素,吡嗪酰胺,奎奴普丁/达福普汀,利福平,他唑巴坦替硝唑,乌菊花素; 4)抗病毒药物:a)侵入/融合抑制剂:阿帕韦洛,马拉韦罗,vicriviroc,gp41(恩夫韦肽),pro140,cd4(艾巴利珠单抗);b)整合酶抑制剂:雷特格韦,elvite-gravir,globoidnana;c)成熟抑制剂:bevirimat,vivecon;d)神经氨酸酶抑制剂:奥司他韦,扎那米韦,帕拉米韦;e)核苷和核苷酸:阿巴卡韦,阿昔单韦,阿德福韦,阿莫西韦,阿昔单抗,溴夫定,西多福韦,克拉夫定,地塞米松,去羟肌苷(ddi),elvucitabine,恩曲他滨(ftc),恩替卡韦,泛昔洛韦,氟拉西林(5-fu),3’-氟取代的2’,3’-脱氧核苷类似物,如3’-氟-2’,3’-双脱氧胸苷(flt)和3’-氟-2’,3’-双脱氧鸟苷(flg),福米韦生,9-鸟嘌呤,碘苷,拉米夫定(3tc),1-核苷(例如β-1-胸苷和β-1-2′-脱氧胞苷),喷昔洛韦,racivir,利巴韦林,迪替丁,司他夫定(d4t),塔利巴韦林(viramidine),替比夫定,替诺福韦,三氟尿苷伐昔洛韦,缬更昔洛韦,扎西他滨(ddc),齐多夫定(azt);f)非核苷类:金刚烷胺,阿替吡啶,卡普韦林,二芳基嘧啶(依曲韦林,rilpivirine),地拉夫定,二十二烷醇,乙米韦林,依法韦仑,膦甲酸(磷酰基甲酸),咪喹莫特,聚乙二醇干扰素,洛韦胺,洛德腺苷,甲吲噻腙,奈韦拉平,nov-205,长效干扰素α,鬼臼毒素,利福平,金刚乙胺,瑞喹莫德(r-848),醋胺金刚烷;g)蛋白酶抑制剂:安普那韦,阿扎那韦,boceprevir,darunavir,福萨那韦,印地那韦,洛匹那韦,奈非那韦,普来可那立,利托那韦,沙奎那韦,telaprevir(vx-950),替拉那韦;h)其它类型的抗病毒药物:抗体酶,阿比朵尔,calanolidea,ceragenin,氰维林-n,二芳基嘧啶,表没食子儿茶素没食子酸酯(egcg),膦甲酸,格里菲辛,taribavirin(viramidine),羟基脲,kp-1461,米替福新,普来可那立,混成抑制剂,利巴韦林,seliciclib; 5)双链接连接子偶联的药物还包括放射性同位素。放射性同位素(放射性核素)的实例有3h,11c,14c,18f,32p,35s,64cu,68ga,86y,99tc,111in,123i,124i,125i,131i,133xe,177lu,211at或213bi。放射性同位素标记的抗体可用于受体靶向成像实验,或者可用于如本发明的抗体-药物偶联物的靶向治疗(wuetalnaturebiotechnology2005,23(9)1137-1146)。细胞结合分子,例如抗体可以通过本专利的连接子连结配体试剂,进行标记。配体可以用文献(currentprotocolsinimmunology,volumes1和2,coligenetal,ed.wiley-interscience,newyork,n.y.pubs.(1991))所述的方法与放射性金属结合、螯合或生成复合物。可以络合金属离子的螯合配体包括dota,dotp,dotma,dtpa和teta(macrocyclics,dallas,tx)等 6)上述任何药物的药学上可接受的盐,酸或其衍生物,水合物或水合盐;或晶体结构;或任何上述药物的旋光异构体,外消旋物,非对映异构体或对映异构体。 在另一个实施例中,结构式(i)和(ii)中的药物/细胞毒性剂可以是发色分子,得到的偶联物可用于检测,监测或研究细胞结合分子与靶细胞的相互作用。发色分子可以吸收一种光,如紫外光,荧光,红外光,近红外光或可见光;发色分子包括黄色素,红细胞,虹彩色素,白细胞,黑色素和蓝绿色素的一类或一个亚类,荧光分子(吸收光后再发光的荧光化学物质)的一类或一个亚类,视觉光转导分子的一类或一个亚类,光子分子的一类或一个亚类,冷光分子的一类或一个亚类和荧光素化合物的一类或一个亚类。 发色分子可选自,但不限于,非蛋白质有机荧光团,例如氧杂蒽衍生物(荧光素,罗丹明,俄勒冈绿,伊红和德克萨斯红);花青衍生物(花青,吲哚羰花青,氧杂花青,硫代花青和部花青);方酸衍生物和环取代的方酸,包括seta,setau和square染料;萘衍生物(丹酰和氟硅酸钠衍生物);香豆素衍生物;恶二唑衍生物(吡啶基恶唑,硝基苯并恶唑和苯并恶二唑);蒽衍生物(蒽醌类,包括draq5,draq7和cytrak橙);芘衍生物(级联蓝等);恶嗪衍生物(尼罗红,尼罗蓝,甲酚紫,恶嗪170等);吖啶衍生物(黄醇黄素,吖啶橙,吖啶黄等);芳基甲胺衍生物(金胺,结晶紫,孔雀石绿)和四吡咯衍生物(卟吩,酞菁,胆红素)。 生色分子选自以下荧光化合物的任何类似物和衍生物:cf染料(biotium),draq和cytrak探针(bios-tatus),bodipy(invitrogen),alexafluor(invitrogen),dylightfluor(thermoscientific,pierce),atto和tracy(sigmaaldrich),fluoprobes(interchim),abberior染料(abberior),dy和megastokes染料(dyomics),sulfocy染料(cyandye),hilytefluor(anaspec),seta,setau和square染料(biosearchtechnologies),surelight染料(apc,rpepercp,phycobilisomes)(columbiabiosciences),apc,apcxl,rpe,bpe(phyco-biotech)。 广泛使用的可与本发明连接子反应或偶联的荧光化合物的实例有:别藻蓝蛋白(apc),氨基胭脂蛋白,apc-cy7偶联物,bodipy-fl,cascadeblue,cy2,cy3,cy3.5,cy3b,cy5,cy5.5,cy7,荧光素,fluorx,羟基香豆素,丽丝胺罗丹明b,萤光黄,me-甲氧基香豆素,nbd,pacificblue,pacificorange,pe-cy5偶联物,pe-r-藻红蛋白(pe),red613,seta-555-叠氮化物,seta-555-dbco,seta-555-nhs,seta-580-nhs,seta-680-nhs,seta-apc-780,seta-percp-680,seta-r-pe-670,setau-380-nhs,setau-405-马来酰亚胺,setau-405-nhs,setau-425-nhs,setau-647-nhs,texasred,tritc,trured,x-rhodamine。 可以与本发明的连接子相连,用于研究核酸或蛋白质的荧光化合物,选自下列化合物或其衍生物:7-aad(7-氨基放线菌素d,cg-选择性的),吖啶橙,色霉素a3,cytrak橙(biostatus),dapi,draq5,draq7,溴化乙锭,hoechst33258,hoechst33342,lds751,光辉霉素,碘化丙啶(pi),sytox蓝,sytox绿,sytox橙,噻唑橙,to-pro,菁染料单体,toto-1,to-pro-1,toto-3,to-pro-3,yoseta-1,yoyo-1。可以与本发明的连接子相连,用于研究细胞的荧光化合物,选自下列化合物或其衍生物:dcfh(2’,7′-二氯二氢荧光素,氧化形式),dhr(二氢罗丹明123,氧化形式,光催化氧化),fluo-3(am酯,ph>6),fluo-4(am酯,ph7.2),indo-1(am酯,低/高钙(ca2+)),snarf(ph6/9)。优选的荧光化合物选自:别藻蓝蛋白(apc),amcyan1(四聚体,clontech),asred2(四聚体,clontech),蓟绿(单体,mbl),azurite,b-藻红蛋白(bpe),cerulean,cypet,dsred单体(clontech),dsred2(“rfp”,clontech),ebfp,ebfp2,ecfp,egfp(弱二聚体,clontech),emerald(弱二聚体,invitrogen),eyfp(弱二聚体,clontech),gfp(s65a突变),gfp(s65c突变),gfp(s65l突变),gfp(y66h突变),gfp(y66w突变),gfpuv,hcred1,j-red,katusha,kusabiraorange(单聚体,mbl),mcfp,mcherry(单体,mbl),mkate(tagfp635,单体,evrogen),mkeima-red(单体,mbl),mko,morange,mplum,mraspberry,mrfp1(单体,tsien实验室),mstrawberry,mtfp1,mturquoise2,p3(藻胆体复合物),多甲藻黄素-叶绿素-蛋白质复合物(percp),r-phycoerythrin(rpe),t-sapphire,tagcfp(二聚体,evrogen),taggfp(二聚体,evrogen),tagrfp(二聚体,evrogen),tagyfp(二聚体,evrogen),tdtomato(串联二聚体),topaz,turbofp602(二聚体,evrogen),turbofpp635(二聚体,evrogen),turbogfp(二聚体,evrogen),turborfp(二聚体,evrogen),turboyfp(二聚体,evrogen),venus,野生型gfp型,ypet,zsgreen1(四聚体,clontech),zsyellow1(四聚体,clontech)。 通过双链连接子连接的抗体-发色团分子的偶联物的结构的实例如下:ac01,ac02,ac03,ac04,ac05,ac06和ac07,ac08,ac09,ac010和ac11: ac10(ir800cw偶联物)、 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、n的定义与前文相同;r12和r12’独立地为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、o(ch2ch2o)pch2ch2nhso3h、nh(ch2ch2o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh-ar-cooh、nh-ar-nh2,其中p=0-5000,aa是氨基酸,(aa)n包含了相同或不同的天然或非天然氨基酸,n=1-30。 在另一个实施方案中,结构式(i),(ii),(iii)和(iv)中的药物可以是聚亚烷基二醇,哺乳动物给药时,用于延长细胞结合分子的半衰期。聚亚烷基二醇包括但不限于聚乙二醇(peg),聚丙二醇以及环氧乙烷和环氧丙烷的共聚物;优选的是peg,更优选的是单官能活化的羟基peg(例如,单个末端活化的羟基peg,包括羟基peg-活性酯,羟基peg-单醛,羟基peg-单胺,羟基peg-单酰肼,羟基peg-单肼基甲酸酯,羟基peg-单碘乙酰胺,羟基peg-单马来酰亚胺,羟基peg-邻二硫吡啶,羟基peg-单肟,羟基peg-单苯基碳酸酯,羟基peg-单苯基乙二醛,羟基peg-单噻唑烷-2-硫酮,羟基peg-单硫代酯,羟基peg-单巯基,羟基peg-单三嗪和羟基peg-单乙烯基砜)。 在某些实施例中,聚亚烷基二醇分子量为约10da至约200kda,优选约88da至约40kda的分子量;具有两个分支,每个分支分子量为约88da至约50kda;更优选的具有两个分支,每个分支约88da至约20kda。在一个具体实施例中,聚亚烷基二醇是聚乙二醇,分子量为约10kda,20kda,或40kda。在具体的实施例中,peg是直链或支链10kdapeg,直链或支链20kdapeg或直链或支链40kdapeg。许多美国专利公开了直链或支链“非抗原性”peg聚合物及其衍生物或偶联物的制备,见美国专利号;;;;;;;;;;;;;;;;;;;;;;;;和。通过桥连接子连接的抗体-聚亚烷基二醇偶联物的结构如pg01,pg02和pg03: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义与前文相同;优选地y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;p为1-5000;r1和r3与上述r1定义相同,且优选地r1和r3为独立地h、oh、och3、ch3、或oc2h5。 在另一个实施方案中,优选的通过本专利的连接子连接至细胞结合分子的细胞毒剂是tubulysin,美登素,紫杉烷类,cc-1065类似物,柔红霉素和多柔比星化合物,毒伞肽(包括鹅膏毒素),indolecarboxamide,苯并二氮卓二聚体(例如吡咯并苯二氮杂卓(pbd),托美霉素,氨茴霉素,吲哚并苯并二氮,咪唑并苯并噻二氮杂卓或恶唑烷并苯并二氮杂卓的二聚体),加利车霉素类和烯二炔类抗生素,放线菌素,氮丝菌素,博来霉素,表柔比星,他莫昔芬,伊达比星,多拉司汀,澳瑞斯汀(例如mmae,mmaf,澳瑞斯汀pye,澳瑞斯汀tp,澳瑞斯汀2-aq,6-aq,eb(aeb),efp(aefp)和它们的同系物),多卡霉素,格尔德霉素或其它的hsp90抑制剂,centanacycin,甲氨喋呤,噻替派,长春地辛,长春新碱,erbulins,,半米塔林,nazumamides,微晶蛋白,放射敏素,streptonigtin,sn38或其它喜树碱类似物或降解物,alterobactin,microsclerodermins,theonellamides,esperamicin,pnu-及其类似物和衍生物,药学上可接受的盐,酸,衍生物,水合物或水合盐;或晶体结构;或任何上述药物的旋光异构体,外消旋物,非对映异构体或对映异构体。 tubulysin是优选的用于本发明偶联物的细胞毒性剂,其为本领域公知,并可以根据已知方法从天然来源分离或者根据已知方法合成制备,如balasubramanian,r.等,j.med.chem.2009,52,238–240;wipf,p.等,org.lett.2004,6,4057–4060;pando,o.等,j.am.chem.soc.2011,133,7692–7695;reddy,j.a.等,mol.pharmaceutics,2009,6,1518–1525;raghavan,b.等,j.med.chem.2008,51,1530–1533;patterson,a.w.等,j.org.chem.2008,73,4362–4369;pando,o.等,org.lett.2009,11(24),pp5567–5569;wipf,p.等,org.lett.2007,9(8),1605–1607;friestad,g.k.org.lett.2004,6,pp3249–3252;hillarym.peltier,h.m.等,j.am.chem.soc.2006,128,16018–16019;chandrasekhars.等,j.org.chem.2009,74,9531–9534;liu,y.等,mol.pharmaceutics,2012,9,168–175;friestad,g.k.等,org.lett.2009,11,1095–1098;kubicek,k.等,angew.chem.int.ed.eng.,2010.49,4809-12;chai,y.等,chembiol,2010,17296-309;ullrich,a.等,angew.chem.int.ed.eng.,2009,48,4422-5;sani,m.等,angew.chem.int.ed.eng.,2007,46,3526-9;domling,a.等,angew.chem.int.ed.eng.,2006.45,7235-9;zanda,m.等,加拿大专利ca(2011);chai,y.等,欧盟专利(2010),pctwo;leamon,c.等,pctwo,wo;ellman,j.等,pctwo,pctwo,美国专利,;matschiner,g.等,pctwo;vlahov,i.等,pctwo,wo;low,p.等,pctwo;richter,w.pctwo;kjems,j.等,pctwo;davis,m.等,pctwo;diener,j.等,美国专利申请,wo;matschiner,g.等,pctwo;vaghefi,f.等,pctwo;doemling,a.德国专利7,pctwo,wo,wo;stanton,m.等,美国专利申请;hoefle,g.等,德国专利,,;leung,d.等,wo;reichenbach,h.等,德国专利;wolfgang,r.美国专利;chen,h.美国专利申请。在专利申请pct/ib2012/053554中描述了优选的与细胞结合分子偶联的tubulysin的结构。 通过双链连接子连接的抗体-tubulysin偶联物的例子如t01、t02、t03、t04、t05、t06、t07、t08、t09、t10、t11、t12、t13、t14、t15、t16t017、t18、t19、t20、t21、t22及t23: t01, 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、和n的定义如前文所述;优选地y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;mab为抗体,优选地为单克隆抗体;r12为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、nhoh、nhor1、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nhso3h、nh(ch2ch2o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh(ch2ch2nh)pch2ch2nh2、nh(ch2ch2s)pch2ch2nh2、nh(ch2ch2nh)pch2ch2oh、nh(ch2ch2s)pch2ch2oh、nh-r1-nh2、或nh(ch2ch2o)pch2ch2nhpo3h2、其中aa为1-8个氨基酸;n为1-20;p为1-5000;r1、r1’、r2、r3、r4和r5独立地为h、c1-c8直链或支链烷基、酰胺或胺;c2-c8芳基、烯基、炔基、杂芳基、杂烷基、烷基环烷基、酯、醚、杂环烷基或酰氧基胺;或含有1-8个氨基酸的肽或(och2ch2)p或(och2ch(ch3))p、其中p是1到约5000的整数;两个r:r1r2、r2r3、r1r3或r3r4可以形成烷基、芳基、杂芳基、杂烷基或烷基环烷基的3~8环状;x3是h、ch3、ch2ch3、c3h7或x1’r1’,其中x1’是nh、n(ch3)、nhnhnh、o或s;r1’为h或c1-c8直链或支链烷基、芳基、杂芳基、杂烷基、烷基环烷基或酰氧基胺;r3’为h或c1-c6直链或支链烷基;z3为h、coor1、nh2、nhr1、or1、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1、o-糖苷(葡萄糖苷、半乳糖苷、甘露糖苷、葡萄糖醛酸苷/葡糖苷酸、阿洛糖苷、果糖苷等)、nh糖苷、s-糖苷或ch2糖苷;m1和m2独立地是h、na、k、ca、mg、nh4或nr1r2r3。 加利车霉素及其相关的烯二炔抗生素为本发明的细胞结合分子-药物偶联物中优选的细胞毒性分子,可参考文献:nicolaou,k.c.等,science1992,256,1172-1178;proc.natl.acad.sci.usa.1993,90,5881-8;美国专利,,,,,,,,,,,,,,,。通过双连接子连接的抗体-加利车霉素类似物的偶联物的实例如下所示: c01. c02 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;q优选地为单克隆抗体。 优选用于本发明的美登木素生物碱包括美登醇及其类似物,可参考美国专利:、、、、、、、、、、、、、、、、、、、、、、、、、、、、和。通过本专利连接子连接的抗体-美登木素生物碱偶联物的结构实例如下:my01、my02、my03、my04、my05、my06、my07和my08: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文;优选地x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;q优选地为单克隆抗体。 紫杉烷,包括紫杉醇(一种细胞毒性天然产物)和多西紫杉醇(一种半合成衍生物)及其类似物,是本发明优选的细胞毒性分子,在如下文献中有描述:kc.nicolaou等,j.am.chem.soc.117,2409-20,(1995);ojima等,j.med.chem.39:3889-3896(1996);40:267-78(1997);45,5620-3(2002);ojima等,proc.natl.acad.sci.96:4256-61(1999);kim等,bull.koreanchem.soc.20,1389-90(1999);miller等,j.med.chem.47,4802-5(2004);美国专利:,,,,,,6.,,,,,,,,和。 经本发明的连接子连接的抗体-紫杉烷偶联物的实例如tx01、tx02和tx03: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义同前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;优选地,q为单克隆抗体。 cc-1065类似物和多卡霉素类似物也是与本发明的双键连接子连接的优选细胞毒性剂。cc-1065类似物和多卡霉素类似物的实例及其合成可见于:warpehoski等,j.med.chem.31:(1988);d.boger等,j.org.chem66,6654-61,2001;美国专利:、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、,、、、和。由本发明的连接子连接的抗体-cc1065类似物偶联物的结构实例如cc01、cc02、cc03、cc04、cc05、cc06和cc07: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;q优选地为单克隆抗体;z3是h、po(om1)(om2)、so3m1、ch2po(om1)(om2)、ch3n(ch2ch2)2nc(o)-、o(ch2ch2)2nc(o)-、r1或糖苷。 柔红霉素/多柔比星同系物也是优选的,与本发明中的双链连接子连接的细胞毒性剂。其结构及合成可参考:hurwitz,e.等,cancerres.35,1175-81(1975);yang,h.m.reisfeld,r.a.proc.natl.acad.sci.85,1189-93(1988);pietersz,c.a.e.等,cancerres.48,926-311(1988);trouet等,79,626-29(1982);z.brich等,j.controlledrelease,19,245-58(1992);chen等,syn.comm.33,2377-90,2003;king等,bioconj.chem.10,279-88,1999;king等,j.med.chem.45,4336-43,2002;kratz等,jmedchem.45,5523-33,2002;kratz等,biol.pharm.bull.jan.21,56-61,1998;lau等,bioorg.med.chem.3,1305-12,1995;scott等,bioorg.med.chem.lett.6,1491-6,1996;watanabe等,tokaij.experimentalclin.med.15,327-34,1990;zhou等,j.am.chem.soc.126,15656-7,2004;wo01/38318;美国专利:;;;;;;;;;;;。 通过本发明的连接子的链接的抗体-cc-1065类似物的偶联物的结构如下da01、da02、da03、da04、da05、da06、da07、da08、da09、da10和da11: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义如前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;r12为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、nhoh、nhor1、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nh-so3h、nh(ch2ch2o)pch2ch2nh-so3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2-ch2nhpo3h2、nh(ch2ch2o)pch2-ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh(ch2ch2nh)pch2-ch2nh2、nh(ch2ch2s)pch2ch2nh2、nh(ch2ch2nh)pch2ch2oh、nh(ch2ch2s)pch2-ch2oh、nh-r1-nh2、或nh(ch2ch2o)pch2ch2nhpo3h2、其中aa是1-8个氨基酸;p是1-5000;q是抗体,优选地为单克隆抗体。 澳瑞斯汀和多拉司汀是优选的和双链连接子连接的细胞毒性剂。澳瑞斯汀,如澳瑞斯汀e(ae),澳瑞斯汀eb(aeb),澳瑞斯汀efp(aefp),单甲基澳瑞斯汀e(mmae),单甲基澳瑞斯汀f(mmaf),澳瑞斯汀f苯二胺(afp)和mmae的苯丙氨酸变体,是多拉司汀的同系物,在如下文献中有描述:int.j.oncol.15367-72(1999);molecularcancertherapeutics,vol.3,no.8,pp.921-32(2004);美国专利申请:、、,美国专利:、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、、。 抗体-澳瑞斯汀通过本发明的连接子连接的偶联物的实例如au01、au02、au03、au04、au05、au06、au07、au08、au09、au10、au11、au12、au13、au14、au15、au16、au17、au18、au19、au20、au21、au22、au23、au24、au25、au26和au27: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义同前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;r12是oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、nhoh、nhor1、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nh-so3h、nh(ch2ch2o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2-ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh(ch2ch2nh)pch2-ch2nh2、nh(ch2ch2s)pch2ch2nh2、nh(ch2ch2nh)pch2ch2oh、nh(ch2ch2s)pch2-ch2oh、nh-r1-nh2或nh(ch2ch2o)pch2ch2nhpo3h2,其中aa为1-8个氨基酸;p为1-5000;q优选为单克隆抗体;r1、r2、r3、r4和r5独立地为h,c1-c8直链或支链烷基,芳基,杂芳基,杂烷基,烷基环烷基,酯,醚,酰胺,胺,杂环烷基或酰氧基胺;或含有1-8个氨基酸的肽,或具有式(och2ch2)p或(och2ch(ch3))p的聚乙烯基氧单,其中p是1至约5000的整数。两个r:r1r2,r2r3,r1r3或r3r4可形成烷基,芳基,杂芳基,杂烷基或烷基环烷基的3~8个成员环;x3为h,ch3或x1’r1’,其中x1’为nh,n(ch3),nhnh,o或s,r1’是h或c1-c8直链或支链烷基,芳基,杂芳基,杂烷基,烷基环烷基,酰氧基胺;r3’是h或c1-c6直链或支链烷基;z3’是h、coor1、nh2、nhr1、or1、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1,r1,或o-糖苷(葡糖苷,半乳糖苷,甘露糖苷,葡糖苷酸/葡糖苷酸,阿洛糖苷,果糖苷等),nh糖苷,s-糖苷或ch2糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 苯并二氮卓二聚体(例如吡咯并苯并二氮卓(pbd)或托霉素的二聚体,吲哚并苯并二氮卓,咪唑并苯并噻吩并二氮卓也是本发明优选的细胞毒性剂,其在本领域中的实例如:美国专利,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,美国专利申请,,。以双链连接子连接的抗体-苯并二氮杂卓二聚体偶联物的实例如:pb01、pb02、pb03、pb04、pb05、pb06、pb07、pb08、pb09、pb10、pb11、pb12、pb13、pb14、pb15、pb16、pb17、pb18、pb19、pb20、pb21、pb22、pb23、pb24、pb25、pb26、pb27、pb28、pb29、pb30、pb31和pb32。 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;r1、r2、r3、r1’、r2’和r3’独立地为h,f,cl,=o,=s,oh,sh,c1-c8直链或支链烷基、芳基、烯基、杂芳基、杂烷基、烷基环烷基、酯(coor5or–oc(o)r5)、醚(or5),酰胺(conr5),氨基甲酸酯(oconr5),胺(nhr5,nr5r5′),杂环烷基或酰氧基胺(-c(o)nhoh,-onhc(o)r5),含20种天然或非天然氨基酸的多肽,或如式(och2ch2)p或(och2ch(ch3))p的聚乙烯氧基单,其中p是1至约5000的整数。两个r:r1r2,r2r3,r1r3,r1’r2’,r2’r3’或r1’r3’可独立形成烷基,芳基,杂芳基,杂烷基或烷基环烷基的3~8个环;x3和y3独立地为n,nh,ch2或cr5,其中r5,r6,r12和r12’独立地为h,oh,nh2,nh(ch3),nhnh2,cooh,sh,oz3,sz3,f,cl,或c1-c8直链或支链烷基,芳基,杂芳基,杂烷基,烷基环烷基,酰氧基胺;z3为h,op(o)(om1)(om2),och2op(o)(om1)(om2),oso3m1或o-糖苷(葡萄糖苷,半乳糖苷,甘露糖苷,葡糖苷酸/葡糖苷酸,阿洛糖苷,果糖等),nh-糖苷,s-糖苷或ch2-糖苷;m1和m2独立地为h,na,k,ca,mg,nh4,nr1r2r3。 鹅膏毒肽包括至少有十种有毒化合物,它们最初在几个有毒蘑菇属中被发现,尤其是伞形毒菌和其他几个蘑菇种类。鹅膏毒肽也是优选的通过本发明连接子链接的细胞毒性分子。目前,十种已知的鹅膏毒肽,α-鹅膏蕈碱,β-鹅膏蕈碱,γ-鹅膏蕈碱,ε-鹅膏蕈碱,鹅膏无毒环肽,一羟基鹅膏毒肽羧酸,鹅膏毒肽酰胺,三羟基鹅膏毒肽和鹅膏毒肽酰胺原均是双环多肽,在合成时经历了一个35个氨基酸的前蛋白,而后被脯氨酰寡肽酶切断,得到最终的八个氨基酸肽(litten,w.scientificamerican1975,232(3)90–101;h.e.hallen等,proc.nat.aca.sci.usa2007,104,19097–101;k.baumann等biochemistry1993,32(15)4043–50;karlson-stiberc,perssonh.toxicon2003,42(4)339–49;horgen,p.a.等,arch.microbio.1978,118(3):317-9)。鹅膏毒肽通过抑制rna聚合酶ii(polii),阻断基因转录和蛋白质生物合成,来杀死细胞(brodner,o.g.和wieland,t.biochemistry1976,15(16)3480–4;fiume,l.,currproblclinbiochem,1977,723-8;karlson-stiberc,perssonh.toxicon2003,42(4)339–49;chafin,d.r.,guo,h.和price,d.h.,j.biol.chem.1995,270(32)19114–19;wieland,int.j.pept.proteinres.1983,22(3)257-76)。鹅膏毒肽可以从采集的伞形毒菌蘑菇中分离得到(yocum,r.r.biochemistry1978,17(18)3786-9;zhang,p.等femsmicrobiol.lett.2005,252(2),223-8),或用担子菌发酵(muraoka,s.和shinozawat.,j.bioscibioeng.2000,89(1)73-6,美国专利)或a.fissa进行发酵获得,或通过培养簇生盔孢菌或黄褐盔孢菌产生(wo/1990/009799,日本专利)。然而,些分离和发酵的产量非常低(低于5mg/l培养物)。在过去的三十年中,有文献报道了鹅膏毒肽及其类似物的几种合成方法(w.e.savige,a.fontana,chem.commun.1976,600–1;zanotti,g.等,int.j.pept.proteinres.,1981.18(2)162-8;wieland,t.等,eur.j.biochem.1981,117,161–4;p.a.bartlett等,tetrahedronlett.1982,23,619–22;zanotti,g.等,biochimbiophysacta,1986.870(3)454-62;zanotti,g.等,int.j.peptideproteinres.1987,30,323–9;zanotti,g.等,int.j.peptideproteinres.1987,30,450–9;zanotti,g.等,int.j.pept.proteinres,1988.32(1)9-20;g.zanotti,t.等,int.j.peptideproteinres.1989,34,222–8;zanotti,g.等,int.j.pept.proteinres.,1990.35(3)263-70;mullersman,j.e.和j.f.preston,3rd,int.j.pept.proteinres.,1991.37(6)544-51;mullersman,j.e.等,int.j.pept.proteinres.,1991.38(5)409-16;zanotti,g.等,int.j.pept.proteinres.,1992.40(6)551-8;schmitt,w.等,j.am.chem.soc.1996,118,4380–7;anderson,m.o.等,j.org.chem.,2005,70(12)4578-84;j.p.may等,j.org.chem.2005,70,8424–30;f.brueckner,p.cramer,nat.struct.mol.biol.2008,15,811–8;j.p.may,d.m.perrin,chem.eur.j.2008,14,3404–9;j.p.may等,chem.eur.j.2008,14,3410–17;q.wang等,eur.j.org.chem.2002,834–9;may,j.p.和d.m.perrin,biopolymers,2007,88(5)714-24;may,j.p.等,chemistry,2008.14(11)3410-7;s.delamomarin等,eur.j.org.chem.2010,3985–9;pousse,g.等,org.lett.,2010.12(16)3582-5;luo,h.等,chem.biol.,2014.21(12)1610-7;zhao,l.等,chembiochem,2015.16(10)1420-5),其中大部分是通过部分合成实现的。由于其极高的效力和独特的细胞毒性机制,鹅膏毒肽已被用作偶联物的有效载荷(fiume,l.,lancet,1969.2(7625)853-4;barbanti-brodano,g.和l.fiume,natnewbiol,1973.243(130)281-3;bonetti,e.,m.等,archtoxicol,1976.35(1)p.69-73;davis,m.t.,preston,j.f.science1981,213,1385–1388;preston,j.f.等,archbiochembiophys,1981.209(1)63-71;h.faulstich等,biochemistry1981,20,6498–504;barak,l.s.等,procnatlacadsciusa,1981.78(5)3034-8;faulstich,h.和l.fiume,methodsenzymol,1985.-37;zhelev,z.,a.等,toxicon,1987.25(9)981-7;khalacheva,k.等,ekspmedmorfol,1990.29(3)26-30;u.bermbach,h.faulstich,biochemistry1990,29,6839–45;mullersman,j.e.和j.f.preston,int.j.peptideproteinres.1991,37,544–51;mullersman,j.e.和j.f.preston,biochemcellbiol,1991.69(7)418-27;j.anderl,h.echner,h.faulstich,beilsteinj.org.chem.2012,8,2072–84;moldenhauer,g.等,j.natl.cancerinst.2012,104,622–34;a.moshnikova等,biochemistry2013,52,1171–8;zhao,l.等,chembiochem,2015.16(10)1420-5;zhou,b.等,biosensbioelectron,2015.68189-96;wo2014/043403,us,ep)。我们也一直在研究鹅膏毒肽的偶联。通过双链连接子连接的抗体—鹅膏毒肽偶联物的实例如am01、am02、am03、am04、am05、am06、am07、am08和am09的结构: 其中x1、x2、q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh,nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、chc(o)nh-nhc(o)、c(o)nr1或缺省;r7、r8和r9独立地为h、oh、or1、nh2、nhr1、c1-c6烷基或缺省;y2为o、o2、nr1、nh或缺省;r10是ch2、o、nh、nr1,nhc(o)、nhc(o)nh、nhc(o)o、oc(o)o、c(o)、oc(o)、oc(o)(nr1)、(nr1)c(o)(nr1)、c(o)r1或缺省;r11为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2-ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nhso3h、nh(ch2ch2-o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2c-h2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、或nh(ch2ch2o)pch2ch2nhpo3h2其中aa为1-20个氨基酸;n和m1独立地为1-30;p为1-5000;z3为h、oh、coor1、nh2、nhr1、or1、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1或o-糖苷(葡萄糖苷,半乳糖苷,甘露糖苷,葡糖苷/葡糖苷酸,阿洛糖苷,果糖苷等)nh糖苷、s-糖苷或ch2-糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 喜树碱(cpts)及其衍生物sn-38,拓扑替康,伊立替康(cpt-11),西利替康(db-67,ar-67),科西特康(bnp-1350),etirinotecan,exatecan,lurtotecan,gimatecan(st1481),贝洛替康(ckd-602),鲁比替康(rubitcan)和其他拓扑异构酶抑制剂,可阻止dna重新连接,因此引起dna损伤并导致细胞凋亡。迄今为止,已有拓扑替康,伊立替康这两种cpt类似物获批用于癌症化疗(palakurthi,s.,expertopindrugdeliv.2015;12(12):1911-21;在临床试验中,sn-38和exatecan还被用作adc偶联物的有效荷载(ocean,a.j.,cancer.2017,123(19):3843-3854;starodub,a.n.等,clincancerres.2015,21(17):3870-8;cardillo,t.m.等,bioconjugchem.2015,26(5):919-31;ogitani,y.等,bioorgmedchemlett.2016,26(20):5069-5072;takegawa,n.等,intjcancer.2017oct15;141(8):1682-1689;美国专利,,,;美国专利申请,,,)。 通过桥连接子连接的抗体-喜树碱类似物的偶联物的实例优选为cp01、cp02、cp03、cp04、cp05和cp06: 其中q、x1,x2,y1、y2、r1,r2,r3,r4,r5,r5’,z1、z2,和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)、c(o)nr1或缺省;z3为h、oh、coor1、nh2、nhr1、or1、ch3、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1、或o-糖苷(葡萄糖苷、半乳糖苷、甘露糖苷、葡糖醛酸苷/葡糖醛酸苷、阿洛糖苷、果糖苷等)、nh-糖苷、s-糖苷或ch2-糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 艾日布林主要与微管正电荷端的少数高亲和位点结合,具有细胞毒性和非细胞毒性作用机制。它的细胞毒性作用与其抗有丝分裂活性有关,在长期且不可逆的有丝分裂阻断后诱导了癌细胞的凋亡(kuznetsov,g.等,cancerresearch.2004,64(16):5760-6;towle,m.j.等,cancerresearch。2010,71(2):496-505)。除了基于细胞毒性、抗有丝分裂的机制外,在人类乳腺癌模型中的临床前研究还表明,艾日布林还对存活的癌细胞和残余肿瘤的生物学功能产生复杂影响,而这些似乎与它的抗有丝分裂作用无关。艾日布林已被美国fda批准用于治疗转移性乳腺癌,病人已接受至少两种针对晚期乳腺癌的前期化疗方案,包括基于蒽环类和紫杉烷类的化疗,以及用于治疗不能通过手术去除(无法切除)或已进展(转移)的脂肪肉瘤(一种软组织肉瘤)。艾日布林也已被用作adc偶联物的有效荷载(us)。通过双链连接子连接抗体-艾日布林偶联物的结构优选为以下eb01和eb02: 其中q、x1、x2、y1、r1、r2、r3、r4、r5、r5’、z1、z2、和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)、c(o)nr1或缺省。 烟酰胺磷酸核糖基转移酶(nampt)抑制剂也是adc有效荷载,因为它们具有独特的高活性的机制(sampathd等,pharmacolther2015;151,16-31)。nampt调节细胞中烟酰胺腺嘌呤二核苷酸(nad)的水平,而nad是维持能量和组成代谢的重要氧化还原辅助因子。nad在新陈代谢中具有几个重要作用。它在氧化还原反应中充当辅酶,在adp-核糖基化反应中作为adp-核糖部分的供体,作为第二信使分子环状adp-核糖的前体,并作为细菌dna连接酶的底物,一类被称为sirtuins的酶使用nad+去除蛋白质中乙酰基。除了这些代谢功能外,nad+还是可以自发地或通过调节机制从细胞中释放出腺嘌呤核苷酸(smythl.m.等,j.biol.chem.2004,279(47),48893–903;billingtonr.a.等,molmed.2006,12,324–7),因此具有重要的细胞外功能(billingtonr.a.等,molmed.2006,12,324–7)。当存在nampt抑制剂时,nad的水平降至代谢所需的水平以下,从而产生能量危机并因此导致细胞死亡。到目前为止,nampt抑制剂候选药物fk-866,chs-828和gmx-1777已经进入临床试验,但每种药物在产生任何客观缓解之前都遇到了剂量限制性毒性(holenk.等,investnewdrugs2008,26,45-51;hovstadiusp.等,clincancerres2002,8,2843-50;pishvaianm.j.等,jclinoncol2009,27,3581)。因此,使用adc靶向递送nampt抑制剂可能会避免系统毒性,从而获得更大的治疗益处。双链连接子链接的抗体-nampt抑制剂偶联物的结构优选为式np01,np02,np03,np04,np05,np06,np07,np08和np09: 其中q、x1、x2、y1、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;x5为f、cl、br、i、oh、or1、r1、opo3h2、oso3h、nhr1、ocor1、nhcor1;优选地,x1、x2、y1和y2为独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)、c(o)nr1或缺省。 在另外的实施例中,可以将免疫毒素通过双链连接子链接至细胞结合分子。免疫毒素是一种大分子药物,通常是由细菌或植物蛋白衍生的细胞毒性蛋白,如白喉毒素(dt)、霍乱毒素(ct)、天花粉蛋白(tcs)、石竹素、假单胞菌外毒素a(eta)、红原毒素、白喉毒素、ab毒素、iii型外毒素等,它也可能是一种剧毒的细菌成孔原毒素,需要蛋白水解激活。这种原毒素的一个例子是前溶氧素及其基因修饰的形式topalysin。topalysin是一种经修饰的重组蛋白,经过工程设计,可以被前列腺中的一种酶选择性激活,从而在不损伤邻近组织和神经的情况下导致局部细胞死亡和组织破坏。 在又一个实施方案中,细胞结合配体或细胞受体激动剂可以通过本专利的双链连接子偶联至细胞结合分子。这些偶联的细胞结合配体或细胞受体激动剂,特别是抗体-受体偶联物,不仅可以用作靶向导体/导向器以将偶联物递送至恶性细胞,而且还可以用于调节或共刺激期望的免疫应答或改变信号传导途径。 在免疫治疗中,细胞结合配体或受体激动剂优选与tcr(t细胞受体)t细胞的抗体偶联,或与car(嵌合抗原受体)t细胞或b细胞受体(bcr),自然杀伤(nk)细胞,或细胞毒性细胞的抗体偶联。这种抗体优选是抗cd3,cd4,cd8,cd16(fcγriii),cd27,cd40,cd40l,cd45ra,cd45ro,cd56,cd57,cd57bright,tnfβ,fas配体,mhci类分子(hla-a,b,c),或nkr-p1。细胞结合配体或受体激动剂选自但不限于:叶酸衍生物(结合叶酸受体,在卵巢癌和其他恶性肿瘤中过表达的蛋白质)(low,p.s.等,2008,acc.chem.res.41,120-9);谷氨酸尿素衍生物(与前列腺特异性膜抗原结合,前列腺癌细胞的表面标志物)(hillier,s.m.等,2009,cancerres.69,6932-40);生长抑素(也称为生长激素抑制激素(ghih)或生长激素释放抑制因子(srif))或生长激素释放抑制激素)及其类似物如奥曲肽(sandostatin)和兰瑞肽(somatuline)(特别用于神经内分泌肿瘤,gh产生性垂体腺瘤,副神经节瘤,无功能性垂体腺瘤,嗜铬细胞瘤)(ginj,m.等,2006,proc.natl.acad.sci.u.s.a.103,16436-41)。一般而言,生长抑素及其受体亚型(sst1,sst2,sst3,sst4和sst5)已在许多类型的肿瘤中被发现,如神经内分泌肿瘤,特别是在分泌gh的垂体腺瘤中(reubij.c.,landolta.m.,1984j.clin.endocrinolmetab–51;reubij.c.,landolta.m.,1987jclinendocrinolmetab6565–73;moysee.等,jclinendocrinolmetab6198–103)和胃肠胰腺肿瘤(reubij.c.等,1987jclinendocrinolmetab–34;reubij.c.等,1990cancerres50,5969–77),嗜铬细胞瘤(epel-baumj,等,1995jclinendocrinolmetab80:1837–44;reubij.c.等,1992jclinendocrinolmetab74,1082–9),成神经细胞瘤(prevostg,1996neuroendocrinology63:188–197;moertel,c.l.等,1994amjclinpath102:752–756),甲状腺髓样癌(reubi,j.c.,等,1991labinvest64:567–573)小细胞肺癌(sagmanu.等,1990cancer66:2129–2133),非神经内分泌肿瘤包括脑肿瘤如脑膜瘤,成神经管细胞瘤或神经胶质瘤(reubij.c.等,1986jclinendocrinolmetab63433–8;reubij.c.等,1987cancerres–64;fruhwald,m.c.等,1999pediatrres45697–708),乳腺癌(reubij.c.等,1990intjcancer46416–20;srkalovicg等,1990jclinendocrinolmetab70661–669),淋巴瘤(reubij.c.等,1992,intjcancer50895–900),肾细胞癌(reubij.c.等,1992,cancerres–6078),间叶组织肿瘤(reubij.c.等,1996cancerres–31),前列腺癌(reubij.c.等,1995,j.clin.endocrinolmetab–14;等,1989,prostate14:191–208;halmosg等,j.clin.endo-crinolmetab–71),卵巢癌(halmos,g.等,2000jclinendocrinolmetab–12;reubij.c.等,1991amjpathol138:1267–72),胃癌(reubij.c.等,1999,intjcancer81376–86;miller,g.v,1992brjcancer66391–95),肝细胞癌(kouroumalise.等,1998gut42442–7;reubij.c.等,1999gut4566–774)和鼻咽癌(lohk.s.等,2002virchowsarch–8);某些芳香磺酰胺类化合物,尤其是碳酸酐酶ix(缺氧和肾细胞癌标志物)(nerid.等,nat.rev.drugdiscov.2011,10,767-7);垂体腺苷酸环化酶激活肽(pacap)(pac1)用于嗜铬细胞瘤和副神经节瘤;血管活性肠肽(vip)及其受体亚型(vpac1,vpac2)用于肺癌,胃癌,结肠癌,直肠癌,乳腺癌,前列腺癌,胰腺导管癌,肝癌,膀胱癌和上皮肿瘤的癌症;各种肿瘤的α-黑素细胞刺激激素(α-msh)受体;胆囊收缩素(cck)/胃泌素受体及其受体亚型(cck1(以前称为cck-a)和cck2),用于小细胞肺癌,甲状腺髓样癌,星形细胞瘤,胰岛素瘤和卵巢癌;蛙皮素(pyr-gln-arg-leu-gly-asn-gln-trp-ala-val-gly-his-leu-met-nh2)/胃泌素释放肽(grp)及其受体亚型(bb1,grp受体亚型(bb2),bb3和bb4)用于肾细胞癌,乳腺癌,肺癌,胃癌和前列腺癌以及神经母细胞瘤(和神经母细胞瘤(ohlssonb.等,1999,scand.j.gastroenterology34(12)1224–9;weberh.c.2009,cur.opin.endocri.diab.obesity16(1)66–71,gonzalezn.等,2008,cur.opin.endocri.diab.obesity15(1),58-64);神经降压素受体及其受体亚型(ntr1,ntr2,ntr3),用于小细胞肺癌,成神经细胞瘤,胰腺癌,结肠癌和尤因肉瘤;物质p受体及其受体亚型(例如神经胶质肿瘤的nk1受体,hennigi.m.等,1995int.j.cancer61,786–792);神经肽y(npy)受体及其受体亚型(y1-y6)用于乳腺癌;归巢肽包括rgd(arg-gly-asp),ngr(asn-gly-arg),二聚和多聚环状rgd肽(例crgdfv)其识别肿瘤表面上的受体(整联蛋白)(laakkonenp.,vuorinenk.,2010,integrbiol(camb),2(7–8)326–337;chenk,chenx.,2011,theranostics.1:189–200;garangere.等,anti-canceragentsmedchem.7(5)552–558;kerrj.s.等,anticancerresearch,19(2a),959-968;thumshirng.等,2003chem.eur.j.9,2717-2725),和taasgvrsmh或ltlrwvglms(硫酸软骨素蛋白多糖ng2受体)和f3肽(结合细胞表面表达的核素受体的31个氨基酸的肽)(zitzmann,s.2002cancerres.62,18,pp.5139–5143,temminga,k.2005,drugresistanceupdates,8,381–402;p.laakkonen和k.vuorinen,2010,integrativebiol,2(7-8),326–337;m.a.burg,1999cancerres.59(12),2869–2874;k.porkka等2002,proc.nat.acad.sci.usa99(11),7444-9);细胞穿透肽(nakasei.等,2012,j.controlrelease.159(2),181–188);肽激素,如促黄体激素释放激素(lhrh)激动剂和拮抗剂,和促性腺激素释放激素(gnrh)激动剂,通过靶向卵泡刺激素(fsh)和黄体生成素(lh)起作用,以及睾酮产物,例如布舍瑞林(pyr-his-trp-ser-tyr-d-ser(otbu)-leu-arg-pro-nhet),戈那瑞林(pyr-his-trp-ser-tyr-gly-leu-arg-pro-gly-nh2),戈舍瑞林(pyr-his-trp-ser-tyr-d-ser(otbu)-leu-arg-pro-azgly-nh2),组氨瑞林(pyr-his-trp-ser-tyr-d-his(n-benzyl)-leu-arg-pro-nhet),醋酸亮丙瑞林(pyr-his-trp-ser-tyr-d-leu-leu-arg-pro-nhet),那法瑞林(pyr-his-trp-ser-tyr-2nal-leu-arg-pro-gly-nh2),曲普瑞林(pyr-his-trp-ser-tyr-d-trp-leu-arg-pro-gly-nh2),德舍瑞林,阿巴瑞克(ac-d-2nal-d-4-氯-d-3-(3-吡啶基)ala-ser-(n-me)tyr-d-asn-leu-异丙基-lys-pro-d-ala-nh2),西曲瑞克(ac-d-2nal-d-4-chloro-phe-d-3-(3-pyridyl)ala-ser-tyr-d-cit-leu-arg-pro-d-ala-nh2),地加瑞克(ac-d-2nal-d-4-氯苯酚-d-3-(3-吡啶基)ala-ser-4-氨基苯丙氨酸(l-hydroorotyl)-d-4-氨基苯丙氨酸(氨基甲酰基)-leu-异丙基赖氨酸-pro-d-ala-nh2)和加尼瑞克(ac-d-2nal-d-4-氯苯酚-d-3-(3-吡啶基)ala-ser-tyr-d-(n9,n10-二乙基)-homoarg-leu-(n9,n10-二乙基)-homoarg-pro-d-ala-nh2)(thundimadathilj.,j.aminoacids,2012,,doi:10.1155/2012/;boccon-gibodl.等,2011,therapeuticadvancesinurology3(3)127–140;debruynef.,2006,futureoncology,2(6),677–696;schallya.v,nagya.,1999eurjendocrinol141:1–14;koppanm.等,1999prostate38:151–158);和模式识别受体(prr),如类toll受体(tlr),c型凝集素和nodlike受体(nlrs)(fukatam.等,2009,semin.immunol.21,242–253;maisonneuvec.等,2014,proc.natl.acad.sci.u.s.a.111,1–6;botosi.等,2011,structure19,447–459;meanst.k.等,2000,lifesci.68,241–258)范围为小分子(咪喹莫特,鸟嘌呤和腺苷类似物)到大而复杂的生物大分子如脂多糖(lps),核酸(cpgdna,polyi:c)和脂肽(pam3csk4)(kasturis.p.等,2011,nature470,543–547;lanet.2001,j.r.soc.med.94,316;hotzc.和bourquinc.,2012,oncoimmunology1,227-228;dudeka.z.等,2007,clin.cancerres.13,7119–25);降钙素受体,一种32-氨基酸神经肽,在很大程度上通过其对破骨细胞和肾脏的作用来调节钙水平(zaidim.等,1990critrevclinlabsci28,109–174;gorna.h.等1995jclininvest95:2680–91);整联蛋白受体及其受体亚型(例如αvβ1,αvβ3,αvβ5,αvβ6,α6β4,α7β1,αlβ2,αiibβ3,等),其通常在血管发生中起重要作用,表现在各种细胞的表面上,特别是破骨细胞,内皮细胞和肿瘤细胞(ruoslahtie.等,1994cell77,477-8;albeldas.m.等,1990cancerres.50,6757-64);短肽,grgdspk和环状rgd五肽,如环(rgdfv)(l1)及其衍生物(环(-n(me)r-gdfv),环(r-sar-dfv),环-(rg-n(me)d-fv),环(rgd-n(me)f-v),环(rgdf-n(me)v)(西仑吉肽))已显示整联蛋白受体的高结合亲和力(dechantsreiterm.a.等,1999j.med.chem.,42,3033-40;goodmans.l.等,2002j.med.chem.45,1045-51)。 细胞结合配体或细胞受体激动剂可以是基于ig的和基于非ig的蛋白质支架分子。基于ig的支架可以选自但不限于纳米抗体(vhh的衍生物(骆驼ig))(muyldermanss.,2013annurevbiochem。82,775–97);域抗体(dab,vh或vl域的衍生物)(holtl.j.等,2003,trendsbiotechnol.21,484–90);双特异性t细胞engager(bite,双特异性双抗体)(baeuerlep.a.等,2009,curr.opin.mol.ther.11,22–30);双亲和重新定位(dart,双特异性双抗体)(moorep.a.p.等2011,blood117(17),4542–51);四价串联抗体(tandab,二聚双特异双抗体)(cochloviusb.等,2000,cancerres.60(16):4336–4341);非ig支架,可以选自但不限于anticalin(lipocalins的衍生物)(skerraa.,2008,febsj.275(11)2677–83;besteg等,1999proc.nat.acad.usa.96(5):1898–903;skerraa.,2000biochimbiophysacta,1482(1-2)337–50;skerraa.,2007,curropinbiotechnol.18(4)295–304;skerraa.,2008,febsj.275(11):2677–83);adnectins(10thfn3(fibronectin))(koidea.等,1998j.mol.biol.284(4):1141–51;batoriv.2002,proteineng.15(12)1015–20;tolchera.w.2011,clin.cancerres.17(2)363–71;hackelb.j.,2010,proteineng.des.sel.23(4)211–19);设计的锚蛋白重复蛋白(darpins)(ankrin重复蛋白的衍生物)(boersmay.l.等,2011curropinbiotechnol.22(6)849–57),如darpinc9,darpinec4和darpine69_lz3_e01(winklerj.等,2009molcancerther.8(9),2674–83;patriciam-k.m.等,clincancerres.2011;17(1):100–10;boersmay.l.等,2011j.biol.chem.286(48),41273–85);avimers(域a/低密度脂蛋白(ldl)受体)(boersmay.l.,2011j.biol.chem.286(48)41273–41285;silvermanj.等,2005nat.biotechnol.23(12):1556–61)。 通过本专利申请的双链连接子链接的抗体-细胞结合配体或抗体-细胞受体激动剂或抗体-药物偶联物的结构实例如下:lb01(叶酸偶联物),lb02(pmsa配体偶联物),lb03(pmsa配体偶联物),lb04(pmsa配体偶联物),lb05(生长抑素偶联物),lb06(生长抑素偶联物),lb07(奥曲肽,生长抑素类似物偶联物),lb08(兰瑞肽,生长抑素类似物偶联物),lb09(伐普肽(sanvar),生长抑素类似物偶联物),lb10(caix配体偶联物),lb11(caix配体偶联物),lb12(胃泌素释放肽受体(grpr),mba偶联物),lb13(促黄体激素释放激素(lh-rh)配体和gnrh偶联物),lb14(促黄体激素释放激素(lh-rh)和gnrh配体偶联物),lb15(gnrh拮抗剂,abarelix偶联物),lb16(钴胺素,维生素b12类似物偶联物),lb17(钴胺素,维生素b12类似物偶联物),lb18(αvβ3整联蛋白受体,环状rgd五肽偶联物),lb19(vegf受体的异二价肽配体偶联物),lb20(神经髓质素b偶联物),lb21(g蛋白偶联受体蛙皮素偶联物),lb22(类toll受体tlr2偶联物),lb23(雄激素受体偶联物),lb24(αv整合素受体西仑吉肽/环(-rgdfv-)偶联物),lb25(利福布汀类似物偶联物),lb26(利福布汀类似物偶联物),lb27(利福布汀类似物偶联物),lb28(氟氢可的松偶联物),lb29(地塞米松偶联物),lb30(丙酸氟替卡松偶联物),lb31(丙酸倍氯米松偶联物),lb32(曲安奈德偶联物),lb33(泼尼松偶联物),lb34(泼尼松龙偶联物),lb35(甲基强的松龙偶联物),lb36(倍他米松偶联物),lb37(伊立替康类似物偶联物),lb38(克唑替尼类似物偶联物),lb39(硼替佐米类似物偶联物),lb40(卡菲佐米类似物偶联物),lb41(卡菲佐米类似物偶联物),lb42(亮丙瑞林类似物偶联物),lb43(曲普瑞林类似物偶联物),lb44(克林霉素偶联物),lb45(利拉鲁肽类似物偶联物),lb46(索马鲁肽类似物偶联物),lb47(瑞他帕林类似物偶联物),lb48(indibulin类似物偶联物),lb49(长春碱类似物偶联物),lb50(利西那肽类似物偶联物),lb51(奥希替尼类似物偶联物),lb52(核苷类似物偶联物),lb53(厄洛替尼类似物偶联物)和lb54(拉帕替尼类似物偶联物),其结构如下所示: lb01(叶酸偶联物) lb02(pmsa-配体偶联物)、 lb03(pmsa-配体偶联物)、 lb04(pmsa-配体偶联物)、 lb05(生长抑素偶联物)、 lb06(生长抑素偶联物) lb07(奥曲肽、生长抑素类似物偶联物)、 lb08(兰瑞肽、生长抑素类似物偶联物)、 lb09(氨肽(sanvar)、生长抑素类似物偶联物)、 lb10(caix配体偶联物)、 lb11(caix配体偶联物)、 lb12(胃泌素释放肽受体(grpr)、mba偶联物)、 lb13(促黄体激素释放激素(lh-rh)配体和和促性腺激素释放激素gnrh配体偶联物)、 lb14(促黄体激素释放激素(lh-rh)和促性腺激素释放激素gnrh配体偶联物)、 lb15(gnrh拮抗剂、阿巴瑞克偶联物)、 lb16(钴胺素、维生素b12类似物偶联物)、 lb17(钴胺素、维生素b12类似物偶联物)、 lb18(环rgd五肽,作用于αvβ3整联蛋白受体)、 lb19(异源二价肽配体偶联物,作用于血管内皮生长因子vegf受体)、 lb20(神经髓质素b偶联物)、 lb21(蛙皮素偶联物,作用于g蛋白偶联受体)、 lb22(tlr2偶联物,作用于类toll受体)、 lb23(雄激素受体)、 lb24(西伦吉肽/环(-rgdfv-)偶联物,作用于αv整合素受体) lb25(利福布丁类似物偶联物)、 lb26(利福布丁类似物偶联物)、 lb27(利福布丁类似物偶联物)、 lb28(氟氢可的松偶联物)、 lb29(地塞米松偶联物)、 lb30(丙酸氟替卡松偶联物)、 lb31(倍氯米松丙酸酯)、 lb32(曲安奈德偶联物)、 lb33(泼尼松偶联物)、 lb34(泼尼松龙偶联物)、 lb35(甲基强的松龙偶联物)、 lb36(倍氟美松偶联物)、 lb37(伊立替康类似物)、 lb38(克唑替尼类似物偶联物)、 lb39(硼替佐米类似物偶联物);其中y5是n、ch、c(cl)、c(ch3)或c(coor1)的r1是h、c1-c6烷基、c3-c8芳基; lb40(卡非佐米类似物偶联物)、 lb41(卡非佐米类似物偶联物)、 lb42(亮丙瑞利类似物)、 lb43(曲普瑞林类似物偶联物)、 lb44(克林霉素偶联物)、 lb45(利拉鲁肽类似物偶联物)、 lb46(索马鲁肽类似物偶联物)、 lb47(瑞他帕林类似物偶联物)、 lb48(丁布尔类似物偶联物)、 lb49(长春碱类似物偶联物)、 lb50(利西森肽类似物偶联物)、 lb51(奥西丁尼类似物偶联物)、 lb52(核苷类似物偶联物)、 lb53(埃罗替尼类似物偶联物)、 lb54(拉帕替尼类似物偶联物)、 其中“—–”、x1、x2、q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;x3为ch2、o、nh、nhc(o)、nhc(o)nh、c(o)、oc(o)、oc(o)(nr3)、r1、nhr1、nr1、c(o)r1或缺省;x4为h、ch2、oh、o、c(o)、c(o)nh、c(o)n(r1)、r1、nhr1、nr1、c(o)r1或c(o)o;x5为h、ch3、f、或cl;m1和m2为独立的h、na、k、ca、mg、nh4、nr1r2r3;r6为5′-脱氧腺苷、me、oh、或cn; 在另一个实施例中,一种,两种或更多种dna,rna,mrna,小干扰rna(sirna),微rna(mirna)和piwi相互作用rna(pirna)通过本专利的双链连接子与细胞结合分子偶联。短链的rna(sirna,mirna,pirna)和长链的非编码反义rna与细胞内的表观遗传变化相关(goodchild,j(2011),methodsinmolecularbiology(clifton,n.j.),7641–15)。本发明中的dna,rna,mrna,sirna,mirna或pirna可以是单链或双链,核苷酸单为一百万至三百万,并且部分核苷酸可以是非天然(合成)形式,例如具有硫代磷酸酯键的寡核苷酸,如fomivirsen,或以硫代磷酸酯键而不是磷酸酯键连接的天然rna和dna的核苷酸,分子中间的糖部分是脱氧核糖,在两端是2′-o-甲氧基乙基修饰的核糖的核苷酸,如mipomersen,或含肽核酸(pna),吗啉代,硫代磷酸酯,硫代磷酰胺,或2′-o-甲氧基乙基(moe),2′-o-甲基,2′-氟,锁核酸(lna),或双环核酸(bna)核糖的寡核苷酸,或糖环中的2′-3’碳键被去除的核酸(whitehead,k.a.等,(2011),annualreviewofchemicalandbiomolecularengineering277–96;bennettc.f.,swayzee.e.,(2010),annu.rev.pharmacol.toxicol.50259–29)。优选地,寡核苷酸的长度为约8至超过200个核苷酸。核苷酸偶联物的例子如下所示: 其中“—–”、q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)和c(o)nr1;是单链或双链的dna、rna、mrna、sirna、mirna或pirna。 在另一个实施方案中,igg抗体与一种,两种或多种不同功能的分子或药物偶联,优选通过轻链和重链之间的一对巯基(通过还原二硫键),或轻重链之间一对巯基,或两个重链之间的上部一对巯基,以及两个重链之间的下部一对巯基特异性偶联,结构如st1,st2,st3,st4,st5或st6所示: st2、 st4、 st6、 其中“—–”、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选的x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)和c(o)nr1;m1、m2、m3和m4独立地为1-30。 此外,含有相同或不同双链连接子的药物或细胞毒性分子,依次地与细胞结合分子偶联,或者,含有相同或不同双链连接子的不同细胞毒性分子,逐步加入含有细胞结合分子的偶联反应混合物中反应,在细胞结合分子的不同偶联位点处的细胞毒性分子和y1,、y2,、r1,、r2,、r3,、r4,、r5,、r5’,、z1,、z2和n可以是不同的。 偶联物的制剂及其应用 本专利申请的偶联物被配制成液体,冻干后可被复溶成液体的形态。在病人上施用时,不产生高水平抗体聚集的制剂配方包含0.1克/升-300克/升的偶联物活性成分、一种或多种多醇(例如糖)、ph值为4.5至7.5的缓冲液、表面活性剂(如聚山梨酸20或80)、抗氧化剂(例如抗坏血酸和/或蛋氨酸)、强化剂(如甘露醇、山梨醇或氯化钠)、螯合剂(如edta)、金属络合物(如锌-蛋白络合物)、可生物降解聚合物(如聚酯)、防腐剂(如苯甲醇)和/或游离氨基酸。 用于制剂的合适缓冲液包括但不限于,有机酸盐,例如柠檬酸、抗坏血酸、葡糖酸、碳酸、酒石酸、琥珀酸、乙酸或邻苯二甲酸的钠、钾、铵或三羟乙基氨基盐,氨基丁三醇盐酸、硫酸或磷酸缓冲液。此外,氨基酸阳离子也可用作缓冲液。这些氨基酸包括但不限于,精氨酸、甘氨酸、甘氨酰甘氨酸和组氨酸。精氨酸缓冲液包括精氨酸乙酸盐、精氨酸氯化物、精氨酸磷酸盐、精氨酸硫酸盐,精氨酸琥珀酸盐等。在一个实施例中,精氨酸缓冲液是精氨酸乙酸盐。组氨酸缓冲液的实例包括组氨酸氯化物-精氨酸氯化物、组氨酸乙酸盐-精氨酸乙酸盐、组氨酸磷酸盐-精氨酸磷酸盐、组氨酸硫酸盐-精氨酸硫酸盐、组氨酸琥珀酸盐-精氨酸琥珀酸盐等。缓冲液的ph是4.5至ph7.5,优选约4.5至约6.5,更优选约5.0至约6.2。在一些实施例中,缓冲液中有机酸盐的浓度为约10mm至约500mm。 在制剂中可选地含有的“多醇”是具有多个羟基的物质。多醇可用作液体和冻干制剂中的稳定辅料和/或等渗剂。多醇可以保护生物药物免受物理和化学降解。最好能被排除的共溶剂增加了蛋白质接口处溶剂的有效表面张力,能量最有利的结构构像是表面积最小的那些溶剂。多醇包括糖(还原和非还原糖)、糖醇和糖酸。“还原糖”是指含有半缩醛基团的糖,它能够还原金属离子,或与蛋白质中的赖氨酸和其他氨基发生反应,“非还原糖”是指不具有还原糖性质的糖。还原糖的例子有果糖、甘露糖、麦芽糖、乳糖、阿拉伯糖、木糖、核糖、鼠李糖、半乳糖和葡萄糖。非还原糖包括蔗糖、海藻糖、山梨糖、松解糖和棉子糖。糖醇选自甘露醇、木糖醇、赤藓糖醇、麦芽糖醇、乳糖醇、赤藓糖醇、苏糖醇、山梨醇和甘油。糖酸包括l-葡萄糖酸盐及其金属盐。液体配方或冻干制剂中的多醇含量,按重量计,为0.0%-20%。在配方中优选浓度约为0.1%到15%的非还原糖,蔗糖或海藻糖,其中由于海藻糖的溶液稳定性,海藻糖更优。 在制剂中可选的表面活性剂可选自聚山梨醇酯(聚山梨醇酯20、聚山梨醇酯40、聚山梨醇酯65、聚山梨醇酯80、聚山梨醇酯81、聚山梨醇酯85等);泊洛沙姆(如泊洛沙姆188、聚(环氧乙烷)-聚(环氧丙烷)、泊洛沙姆407或聚丙二醇-丙二醇等);triton;十二烷基硫酸钠(sds);月桂基硫酸钠;辛基糖苷钠;十二烷基、肉荳蔻酰基、亚油基或硬脂基磺基甜菜碱;十二烷基、肉荳蔻酰基、亚油基或硬脂基肌氨酸;亚油酸、肉荳蔻基或十六烷基甜菜碱;月桂酰胺基丙基、椰油酰胺丙基、亚油酰胺基丙基、肉荳蔻酰基丙基、棕榈酰基丙基或异硬脂酰胺基丙基-甜菜碱(例如月桂酰胺丙基);肉荳蔻酰胺丙基、棕榈酰丙基或异硬脂酰胺基丙基-二甲胺;甲基椰油酰基钠或甲基油基牛磺酸二钠;十二烷基甜菜碱、十二烷基二甲基氧化胺、椰油酰胺丙基甜菜碱和可可两性甘氨酸酯;monaquattm系列(如异硬脂基乙基亚胺鎓乙基硫酸盐);聚乙二醇,聚丙二醇,乙二醇和丙二醇的共聚物(如pluronic、pf68等)。优选的表面活性剂是聚氧乙烯山梨糖醇脂肪酸酯,如聚山梨醇酯20、40、60或80(吐温tween20、40、60或80)。制剂中表面活性剂的浓度范围,按照重量计,为0.0%至约2.0%。在某些特定实施例中,表面活性剂浓度为约0.01%至约0.2%。在一个实施例中,表面活性剂浓度为约0.02%。 在制剂中可选的“防腐剂”是从根本上可以减小其中细菌的化合物。防腐剂的实例包括十八烷基二甲基芐基氯化铵、六甲基氯化铵、苯扎氯铵(烷基芐基二甲基氯化铵的混合物,其中烷基为长链烷基)和芐索氯铵。其他类型的防腐剂包括芳香醇如苯酚,丁基和芐基醇,对羟基苯甲酸烷基酯,如甲酯或丙酯,儿茶酚、间苯二酚、环己醇、3-戊醇和间甲酚。液体配方或冻干粉末中的防腐剂含量,按照重量计,为0.0%-5.0%。在一个实施例中,所用防腐剂是苯甲醇。 在制剂中合适的游离氨基酸,选自但不限于精氨酸、胱氨酸、甘氨酸、赖氨酸、组氨酸、鸟氨酸、异亮氨酸、亮氨酸、丙氨酸、甘氨酸谷氨酸或天冬氨酸中的一种或多种。优选碱性氨基酸为精氨酸、赖氨酸和/或组氨酸。如果组成中包含组氨酸,它可以充当缓冲剂和游离氨基酸,但是当使用组氨酸缓冲液时,通常还要包含一个非组氨酸的游离氨基酸,如赖氨酸。氨基酸可以以d-和/或l-型存在,但l-型比较常见。氨基酸可以任何合适的盐的形式存在,如精氨酸盐酸盐。液体配方或冻干粉末中的氨基酸含量,以重量计,为0.0001%-15.0%,优选为0.01%至5%。 可选地,制剂还包含甲硫氨酸或抗坏血酸作为抗氧化剂,浓度为约0.01至5毫克/毫升;可选地,制剂包含金属螯合剂,例如edta,egta等,浓度为约0.01至2mm。 最终的制剂可以用缓冲调节剂(如一种酸,包括hcl、h2so4、乙酸,h3po4、柠檬酸等,或是碱,如naoh、koh、nh4oh、乙醇胺、二乙醇胺或三乙醇胺、磷酸钠、磷酸钾、柠檬酸三钠、氨基丁三醇等)调节至优选的ph值。制剂还应当被调节至“等渗”,即目标制剂具有与人血基本相同的渗透压。等渗制剂渗透压通常为250至350mosm。可以使用蒸气压或冰冻型渗透压计测量等渗性。 在液体或冻干制剂中可能有用的其他辅料包括,例如,岩藻糖、纤维二糖、麦芽三糖、褪黑糖、辛酮糖、核糖、木糖醇、精氨酸、组氨酸、甘氨酸、丙氨酸、蛋氨酸、谷氨酸、赖氨酸、咪唑、甘氨酸、甘露糖基甘油酯、tritonx-100、puloronicf-127、纤维素、环糊精、(2-羟丙基)-β-环糊精、右旋糖酐(10、40和/或70kd)、聚葡萄糖、麦芽糊精、无花果胶、明胶、羟丙基甲基、磷酸钠、磷酸钾、氯化锌、锌、氧化锌、柠檬酸钠、柠檬酸三钠、氨丁三胺、铜、纤维粘连蛋白、肝素、人血清白蛋白、鱼精蛋白、甘油、edta、间甲酚、苯甲醇、苯酚、多醇、被还原的糖、其中一羰基被还原为一级或二级醇。 其它可以在本专利申请的液体制剂中使用的辅料还包括:例如调味剂、抗微生物剂、甜味剂、抗氧化剂、抗静电剂、脂质如磷脂或脂肪酸脂、类固醇如胆固醇、蛋白质辅料如血清白蛋白(人血清白蛋白)、重组人白蛋白、明胶、酪蛋白、成盐反离子如钠等。这些和另外的适用于本发明制剂的,已知的药物辅料和/或加入剂为本领域公知,如在由美国医药协会罗威(rowe)等人编著的第四版《药用辅料手册》(thehandbookofpharmaceuticalexcipients)中所列;以及由威尔金斯出版公司出版(2005),热纳罗(gennaro)等人编著的第21版《雷明顿:药学科学与实践》(remington:thescienceandpracticeofpharmacy)中所列。 在更进一步的实施例中,本发明提供了制剂的制备方法,包括以下步骤:(a)将包含偶联物,辅料和缓冲体系的制剂冻干至粉末状;(b)在介质中复溶步骤(a)中的冻干混合物,以使得复溶的制剂稳定。步骤(a)中的液体可进一步包含稳定剂和一种或多种辅料,选自前述填充剂、盐、表面活性剂和防腐剂。稀释的有机酸或水,例如无菌水、注射用抑菌水(bwfi)、可以用作复溶介质。复溶介质可选用水,如无菌水、抑菌性注射用水(bwfi)、乙酸、丙酸、琥珀酸、氯化钠、氯化镁溶液、氯化钠的酸性溶液、氯化镁的酸性溶液或精氨酸的酸性溶液,其浓度为约10-约250mm。 本专利申请的偶联物的液体制剂应具有各种设定的特征。需要考虑的主要问题之一是其稳定性,因为蛋白质/抗体在制造和储存期间,常会形成可溶及不溶的聚集体。此外,溶液中会发生各种化学反应(脱酰胺、氧化、剪切、异构化等),导致降解产物水平增加和/或生物活性丧失。液体或冻干制剂中的偶联物最好应在25℃下,具有超过18个月的货架期。更优的液体或冻干制剂中的偶联物应在25℃下具有超过24个月的货架期。最为优选的液体制剂应该在2-8℃下具有约24-36个月的货架期,冻干粉末在2-8℃下,应该具有长达约60个月的货架期。液体制剂和冻干制剂优选地具有在-8℃,-20℃或-70℃下至少两年货架期。 在一些实施例中,该制剂在冷冻(例如-20℃或-70℃)和融化之后是稳定的,例如在1、2或3个冷冻和融化循环之后是稳定的。可以用不同的方式定性和/或定量地评估稳定性,包括评估药物/抗体(蛋白质)的比例和聚集体的形成(例如,使用uv、尺寸排阻色谱法、通过测量浊度和/或通过目测);通过使用阳离子交换色谱、图像毛细管等电聚焦(icief)或毛细管区带电泳评估电荷异质性;进行氨基末端或羧基末端序列分析、质谱分析或基质辅助激光解吸电离/飞行时间质谱(maldi/tofms),hplc-ms/msce-sds或sds-page分析以比较还原抗体和完整抗体;进行肽图分析(例如胰蛋白酶或lys-c);评估抗体的生物学活性或抗原结合功能。不稳定可能涉及以下一种或多种:聚集、脱酰胺作用(例如asn脱酰胺作用)、氧化作用(例如met氧化作用)、异构化作用(例如asp异构化作用)、剪切/水解/断裂作用(例如铰链区断裂)、生成琥珀酰亚胺、未成对半胱氨酸、n末端延伸、c末端加工、糖基化差异等。 稳定的偶联物应当在药物制剂中“保持其生物学活性”,例如,如果偶联物的生物活性在给定时间内,例如12个月,按照抗原结合测定和/或体外细胞毒性测定的方法,生物活性可以保持在相差20%以内,优选10%(在测定误差内)。 药物容器或容器用于容纳专利申请的任何偶联物的药物制剂。该容器是小瓶,瓶子,预填充注射器或预填充自动注射器注射器。 对于临床体内使用,偶联物给药方式的实例如下:每天一次、每周一次、每两周一次、每三周一次、每次四周一次或每月一次、共周,静脉推注。注射的剂量是在50-1000ml生理盐水中,可任选地向其中加入人血清白蛋白(例如0.5-1ml人血清白蛋白浓缩溶液,100mg/ml)。每周一次、每两周一次、每三周一次的剂量约为50μg/kg-30mg/kg体重,静脉推注(每次注射10μg-200mg/kg的范围)。治疗后周,患者可能会接受第二个疗程。关于给药方式,辅料,稀释剂,剂量,时间等的具体临床方案可以由熟练的临床医生确定。 可以根据体内或体外的方法杀死选定的细胞群进行治疗的医学病症,包括任何类型的癌症的恶性肿瘤,自身免疫性疾病,移植排斥和感染(病毒,细菌或寄生虫)。 获得满意的生物学效应所需的偶联物的量将取决于许多因素,包括偶联物的化学特性,效力和生物利用度,疾病类型,患者的种族,患者的疾病状态,给药途径,这些决定了所需剂量,给药方式和给药方案。 一般而言,可以通过包含本发明的药物为含0.1-10%w/v偶联物的生理缓冲水溶液,用于肠胃外施用。典型剂量范围为1μg/kg-0.1g/kg体重,每天、每周、每两周、每三周或每月一次,优选的剂量范围是人体等效剂量0.01mg/kg-30mg/kg体重,每周,每两周,每三周或每月一次。待给药物的优选剂量可能取决于下列变量,如疾病的类型或病症的进展,患者的总体健康状况,所选化合物的相对生物学功效,药物的制剂,给药方式(静脉内,肌肉内或其他),药物在确定的给药途径的药代动力学特性,给药速度(推注或连续输注)和给药方案(在给定时间内重复次数)。 通过本发明的连接子的偶联物也能够以单位剂量形式给药,其中术语“单位剂量”是指能够给予患者并且可以容易地处理和包装的单一剂量,保持为物理和化学稳定的单位剂量,包括活性偶联物本身,或作为药学上可接受的组合物,如下所述。因此,典型的每日/每周/双周/每月总剂量范围为0.01-100mg/kg体重。通过一般指导,人体的单位剂量范围为每天1毫克-3000毫克,或每周,每两周(两周),三周或每月一次。优选地,单位剂量范围为每月施用1-4次1-500mg,甚至更优选1mg-100mg,每周一次或每两周一次或每三周一次。本文提供的偶联物可以通过与一种或多种药学上可接受的辅料混合而配制成药物组合物。这种单位剂量组合物可以制备成通过口服给药使用,特别是以片剂,简单胶囊或软凝胶胶囊的形式;或鼻内,特别是以粉末,滴鼻剂或气溶胶的形式;或皮肤,例如局部用软膏,乳膏,乳液,凝胶或喷雾剂,或通过透皮贴剂。 在又一个实施方案中,包含治疗有效量的式(i)偶联物或通过本专利描述的任何偶联物的药物组合物可以与其它治疗剂例如化学治疗剂、放射疗法、免疫治疗剂、用于协同有效治疗或预防癌症、自身免疫疾病或传染病的自身免疫疾病剂、抗感染剂或其他偶联物。协同剂优选选自以下一种或几种药物:阿巴西普、abemaciclib、乙酸阿比特龙、abraxane、阿杜卡奴单抗、对乙酰氨基酚/氢可酮、阿卡替尼、阿杜卡奴单抗、阿达木单抗、adxs31-142、adxs-her2、阿法替尼二马来酸盐、阿地白介素、阿乐替尼、阿伦单抗、艾力替尼、alitretinoin、ado-trastuzumabemtansine、安非他明/右旋安非他明、阿那曲唑、apatinib、阿立哌唑、蒽环类药物、阿立哌唑、atazanavir、阿特朱单抗、阿托伐他汀、avelumab、avxs-101、axicabtageneciloleucel、阿西替尼、贝利司他、bcg-live、贝伐单抗、贝沙罗汀、blinatumomab、硼替佐米、波舒替尼、本妥昔单抗、布格替尼、布地奈德、布地奈德/福莫特罗、丁丙诺啡、byl719(α特异性pi3k抑制剂)、卡巴他赛、卡博替尼、卡马替尼、卡培他滨、卡非佐米、嵌合抗原受体工程t(car-t)细胞、塞来昔布、色瑞替尼、西妥昔单抗、西奥罗尼、西达本胺、环孢素、cinacalcet、克唑替尼、考比替尼、cosentyx、克唑替尼、tisagenlecleucel、达比加群、达拉菲尼、达卡巴嗪、达利珠单抗、达科替尼、达托霉素、达拉木单抗、darbepoetinalfa、darunavir、达沙替尼、denileukindiftitox、地诺单抗、depakote、dexlansoprazole、dexmethylphenidate、地塞米松、l-3、4-二羟基苯基丙氨酸、dinutuximab、阿法链道酶、强力霉素、度洛西汀、德卫利昔、度伐鲁单抗、依托珠单抗、emicizumab、emtricibine/利匹韦林/替诺福韦、地索普西富马酸、恩曲他滨/替诺福韦/依非韦伦、依诺肝素、恩沙替尼、恩杂鲁胺、易吡替尼、阿法依伯汀、厄洛替尼、埃索美拉唑、eszopiclone、依那西普、依维莫司、依西美坦、依维莫司、艾塞那肽er、依泽替米贝、依泽替米贝/辛伐他汀、法米替尼、非诺贝特、非戈替尼、非格司亭、芬戈莫德、氟马替尼、丙酸氟替卡松、氟替卡松/沙美特罗、呋喹替尼、氟维司群、gazyva、吉非替尼、醋酸格拉替雷、醋酸戈舍瑞林、gsk(bcma-adc)、henatinib、埃克替尼、伊马替尼、替伊莫单抗、依鲁替尼、埃克替尼、艾代拉里斯、异环磷酰胺、英夫利昔单抗、咪喹莫特、immunocyst、immunobcg、iniparib、门冬胰岛素、地特胰岛素、甘精胰岛素、赖脯胰岛素、干扰素α、干扰素α-1b、干扰素α-2a、干扰素α-2b、干扰素β、干扰素β1a、干扰素β1b、干扰素γ-1a、拉帕替尼、易普利姆玛、异丙托溴铵/沙丁胺醇、伊沙唑米、卡努玛、莱地鲁单伉、醋酸兰瑞肽、来那度胺、来那度胺、甲磺酸乐伐替尼、来曲唑、左旋甲状腺素、左旋甲状腺素、利多卡因、利奈唑胺、利拉鲁肽、lisdexamfetamine、ln-144(肿瘤浸润淋巴细胞)、lorlatinib、德立替尼/delitinib、美金刚、甲氧基聚乙二醇epoetin-beta、哌醋甲酯、美托洛尔、曲美替尼、美西他滨/利匹韦林/替诺福韦、莫达非尼、莫米松、mycidac-c、霉酚酸、耐昔妥珠单抗、诺拉替尼、尼罗替尼、尼拉帕尼、尼沃鲁单抗、奥法木单抗、奥比曲妥珠单抗、奥瑞珠单抗、奥拉帕尼、奥美沙坦、奥美沙坦/氢氯苯噻哒嗪、奥马珠单抗、omega-3脂肪酸乙酯、oncorine、奥司他韦、奥希替尼、羟考酮、奥扎莫德、帕波克利、帕利珠单抗、帕尼单抗、帕比司他、帕唑帕尼、派姆单抗、pd-1抗体、pd-l1抗体、培美曲塞、帕妥珠单抗、吡非尼酮、肺炎球菌结合疫苗、泊马度胺、普瑞巴林、proscavax、普萘洛尔、普喹替尼、吡咯替尼、喹硫平、雷贝拉唑、氯化镭223、雷洛昔芬、raltegravir、雷莫芦单抗、雷珠单抗、瑞戈非尼、瑞博西尼、瑞莎珠单抗、利妥昔单抗、利伐沙班、罗米地辛、罗苏伐他汀、磷酸鲁索替尼、沙丁胺醇、索凡替尼、索马鲁肽、sevelamer、西地那非、司妥昔单抗、西莫替尼、西帕替尼/cipatinib、辛波莫德、sipuleucel-t、西他列汀、西他列汀/二甲双胍、solifenacin、索兰珠单抗、索尼吉布、索拉非尼、磺胺替尼、舒尼替尼、他克莫司、tacrimus、他达那非、他莫昔芬、甲磺酸达拉非尼、talimogenelaherparepvec、talazoparib、特拉瑞韦、talazoparib、替莫唑胺、替西罗莫司、替奈普酶、替诺福韦/恩曲他滨、富马酸替诺福韦酯、睾酮凝胶、替加卡托/依伐卡托、沙利度胺、theliatinib、ticebcg、噻托溴铵、tisagenlecleucel、托珠单抗、托瑞米芬、曲美替尼、曲妥珠单抗、曲贝替定(海鞘素743)、曲美替尼、替西木单抗、trifluridine/tipiracil、维甲酸、乌帕替尼、uro-bcg、优特克单抗、valoctocogeneroxaparvovec、缬沙坦、veliparib、凡德他尼、威罗菲尼、维特克拉、维莫德吉、索凡替尼、伏立诺他、阿柏西普、zostavax及其类似物、衍生物、药学上可接受的盐、载体、稀释剂或其辅料,或其以上的组合。 用本申请的连接子偶联的药物/细胞毒性剂可以是本专利中描述的的任何药物/细胞毒性剂类似物和/或衍生物。药物/细胞毒性剂领域的技术人员可以理解,本文所述的每种药物/细胞毒性剂都可以被修饰,使所得化合物仍保留起始化合物的特异性和/或活性。技术人员还应当理解,可以使用这些类似物或衍生物来代替本文所述的药物/细胞毒性剂。因此,本发明的药物/细胞毒性剂包括这些类似物和衍生物。 本发明以下列实施例做进一步说明,但不仅限于以下实施例。 实施例 以下实施例进一步说明本发明,但这些实施例无意于限制本发明的范围。以下示例中所述的细胞系,除非另有说明,根据美国典型培养物保藏中心(atcc)或德国deutschesammlungvonmikroorganismenundzellkulturengmbh(dmsz)或中国科学院上海细胞培养研究所指定的条件进行培养。除非另有说明,否则细胞培养试剂来自invitrogencorp.。所有无水溶剂都可以通过商业途径获得,并在氮气下储存在sure-seal瓶中。购买的所有其他试剂和溶剂均为可用的最高等级,无需进一步纯化即可使用。用varainprestarhplc进行制备hplc分离。nmr光谱在bruker500mhz仪器上分析测得。化学位移(δ)以百万分数(ppm)为单位报告,为对四甲基硅烷(0.00ppm)的相对值,偶合常数(j)以hz为单位报告。质谱数据是在装有watersacquityuplc分离模块和acquitytuv检测器的watersxevoqtof质谱上获得的。 实施例1.2,5-二氧代-2,5-二氢-1h-吡咯-1-羧酸甲酯的合成。 在0℃下,向马来酰亚胺(6.35g,65.4mmol,1.0eq)的乙酸乙酯(120ml)溶液中加入n-甲基吗啉(8.6ml,78.5mmol,1.2eq)和氯甲酸甲酯(6.0ml,78.5mmol,1.2eq)。在0℃下将反应搅拌30分钟,室温搅拌1小时。滤出固体,浓缩滤液。将残余物溶于ch2cl2中并通过硅胶过滤,并用ch2cl2洗脱以洗去颜色。浓缩适当的组分,将得到的固体用10%乙酸乙酯/石油醚打浆,得到白色固体(9.00g,收率89%)。 实施例2.(s)-3-((叔丁氧羰基)氨基)-2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酸的合成。 在0℃,向h-dap(boc)-oh(1.00g,4.9mmol)和饱和碳酸氢钠(20ml)溶液中加入2,5-二氧代-2,5-二氢-1h-吡咯-1-羧酸甲酯(2.30g,14.7mmol)。将反应在0℃下搅拌1小时,然后升温至室温并再搅拌1小时。然后加入1nkhso4以将ph调节至~6,并将所得混合物用乙酸乙酯(2×50ml)萃取。将合并的有机层用硫酸钠干燥,过滤并浓缩,得到标题化合物(0.42g,收率30%)。esim/zc12h15n2o6[m-h]-计算值:283.10,实测值:283.10。 实施例3.(2-(2,5-二氧代-2-,5-二氢-1h-吡咯-1-基)乙基)氨基甲酸叔丁酯的合成。 将n-boc-乙二胺(5.6ml,35.4mmol,1.1eq)和饱和碳酸氢钠(60ml)的混合物冷却至0℃,向其中分批加入2,5-二氧代-2,5-二氢-1h-吡咯-1-羧酸甲酯(5.00g,32.2mmol,1.0eq)。在0℃下搅拌30分钟后,将反应升温至室温并搅拌1小时。将沉淀物过滤收集并用冷水洗涤,然后溶于乙酸乙酯并用盐水洗涤,用无水硫酸钠干燥并浓缩,得到标题化合物,为白色固体(6.69g,收率87%)。 实施例4.(2-(1,3-二氧代-3a,4,7,7a-四氢-1h-4,7-环氧异吲哚-2(3h)-基)乙基)氨基甲酸叔丁酯的合成。 将(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙基)氨基甲酸叔丁酯(6.00g,25.0mmol),呋喃(18.0ml)的甲苯溶液(120ml)在高压管中加热回流并搅拌16小时。无色溶液在反应过程中变黄。然后将混合物冷却至室温并浓缩,将得到的白色固体用乙醚打浆,得到标题化合物(6.5g,收率84%)。 实施例5.2-(2-氨基乙基)-3a,4,7,7a-四氢-1h-4,7-环氧异吲哚-1,3(2h)-二酮盐酸盐的合成。 将(2-(1,3-二氧代-3a,4,7,7a-四氢-1h-4,7-环氧异吲哚-2(3h)-基)乙基)氨基甲酸叔丁酯(9.93g,32.2mmol)溶于二噁烷(15ml)中,并在室温下与浓hcl(15ml)搅拌3小时。浓缩反应物,过滤收集所得固体,用乙酸乙酯洗涤滤饼。将固体在烘箱(50℃)中干燥过夜,得到标题化合物(6.94g,收率88%)。 实施例6.2,8-二氧代-1,5-恶唑烷-5-羧酸叔丁酯的合成。 在4℃,向3,3′-氮杂二基二丙酸(10.00g,62.08mmol)的1.0mnaoh(300ml)溶液中加入二碳酸二叔丁酯(22.10g,101.3mmol)的四氢呋喃(200ml)溶液。加入后,将混合物在4℃下搅拌2小时。用0.2mh3po4将混合物小心酸化至ph~4,真空浓缩,用ch2cl2萃取,用硫酸钠干燥,蒸发并用快速sio2色谱纯化,用acoh/甲醇/二氯甲烷(0.01:1:5)洗脱,得到3,3′-((叔丁氧基羰基)氮杂二基)二丙酸(13.62g,收率84%)。esimsm/z:c11h19no6[m+h]+计算值:262.27,实测值:262.40。 在0℃下,向3,3′-(叔丁氧基羰基)氮杂二基)二丙酸(8.0g,30.6mmol)的二氯甲烷(500ml)溶液中加入五氧化二磷(8.70g,61.30mmol)。将混合物在0℃下搅拌2小时,然后搅拌1小时,通过短sio2柱过滤,并用乙酸乙酯/二氯甲烷(1:6)冲洗柱。浓缩滤液并用乙酸乙酯/正己烷打浆,得到标题化合物(5.64g,收率74%)。esimsm/z:c11h17no5[m+h]+,计算值:244.11,实测值:244.30。 实施例7.3-(2-(2-(2-(2-(甲苯磺酰氧基)乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 将3-(2-(2-(2-羟基乙氧基)乙氧基)丙酸叔丁酯(10.0g,35.95mmol)的乙腈(50.0ml)和吡啶(20.0ml)混合。然后在30分钟内通过加料漏斗滴加甲苯磺酰氯(7.12g,37.3mmol)的50ml乙腈溶液。5小时后tlc分析显示反应完成。滤出已形成的吡啶盐酸盐并除去溶剂。通过用20%乙酸乙酯的己烷溶液洗脱,用纯乙酸乙酯在硅胶上纯化残余物,得到11.2g(76%收率)标题化合物。1hnmr:1.40(s,9h),2.40(s,3h),2.45(t,2h,j=6.4hz),3.52-3.68(m,14h),4.11(t,2h,j=4.8hz),7.30(d,2h,j=8.0hz),7.75(d,2h,j=8.0hz);esimsm/z:c20h33o8s(m+h)计算值:433.18,实测值:433.30。 实施例8.3-(2-(2-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 一边搅拌一边向50mldmf中加入3-(2-(2-(2-(2-(甲苯磺酰氧基)乙氧基)乙氧基)乙氧基)丙酸叔丁酯(4.0g,9.25mmol)和叠氮化钠(0.737g,11.3mmol)。将反应加热至80℃。4小时后,tlc分析表明反应完成。将反应冷却至室温,并用水(25ml)淬灭。分离水层,并萃取到乙酸乙酯(3×35ml)中。合并的有机层经无水硫酸镁干燥,过滤,并真空除去溶剂。叠氮化物粗产物(2.24g,收率98%,hplc纯度约93%)无需进一步纯化即可用于下一步。1hnmr(cdcl3):1.40(s,9h),2.45(t,2h,j=6.4hz),3.33(t,2h,j=5.2hz),3.53-3.66(m,12h)。esimsm/z:c13h26n3o8(m+h),计算值:304.18,实测值:304.20。 实施例9.3-(2-(2-(2-(叠氮基乙氧基)乙氧基)乙氧基)丙酸的合成。 向在1,4-二氧六环(40ml)中的3-(2-(2-(2-叠氮基乙氧基)乙氧基)丙酸叔丁酯(2.20g,7.25mmol)中加入hcl(12m,10ml)。将混合物搅拌40分钟,用1,4-二氧六环(20ml)和甲苯(40ml)稀释,蒸发并与14-二氧六环(20ml)和甲苯(40ml)共蒸发至干,得到标题产物粗品,无需进一步纯化(1.88g,收率105%,hplc纯度约92%)。esimsm/z:c9h18n3o5[m+h]+计算值:248.12,实测值:248.40。 实施例10.13-氨基-4,7,10-三氧杂十二烷酸叔丁酯和13-氨基双(4,7,10-三氧杂十二烷酸叔丁酯)的合成。 在氢化反应容器内,将叠氮化物3-(2-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)丙酸(5.0g,约14.84mmol)粗品溶解在乙醇(80ml)中,向其中加入300mg10%pd/c。将该系统抽真空,并在剧烈搅拌下充入2atm的氢气。然后将反应在室温下搅拌过夜,tlc显示原料消失。将反应粗品用短硅藻土垫过滤,用乙醇洗。浓缩滤液,在硅胶柱上使用含1%三乙胺的甲醇/二氯甲烷混合物(5%至15%)作为洗脱剂纯化,得到13-氨基-4,7,10-三氧杂十二烷酸叔丁酯(1.83g,44%产率,esimsm/z:c13h27no5(m+h),计算值278.19,实测值278.30)和13-氨基-双(4,7,10-三氧杂十二烷酸叔丁酯)(2.58g,32%产率,esimsm/z:c26h52no10(m+h),计算值538.35,实测值538.40)。 实施例11.3-(2-(2-(2-氨基乙氧基)乙氧基)乙氧基)丙酸盐酸盐的合成。 在搅拌下向13-氨基-4,7,10-三氧杂十二烷酸叔丁酯(0.80g,2.89mmol)的1,4-二氧六环(30ml)溶液中加入10mlhcl(36%)。0.5小时后,tlc分析显示反应完成,浓缩反应混合物,并与乙醇和乙醇/甲苯共浓缩,得到标题盐酸盐(>90%纯度,0.640g,86%产率),无需进一步纯化。esimsm/z:c9h20no5(m+h),计算值222.12,实测值222.20。 实施例12.13-氨基-双(4,7,10-三氧杂十二烷酸)盐酸盐。 在搅拌下向13-氨基-双(4,7,10-三氧杂十二烷酸叔丁酯)(1.00g,1.85mmol)的1,4-二氧六环(30ml)溶液中加入10mlhcl(36%)。0.5小时后,tlc分析显示反应完成,浓缩反应混合物,并与乙醇和乙醇/甲苯共浓缩,得到标题产物盐酸盐(>90%纯度,0.71g,91%产率),无需进一步纯化。esimsm/z:c18h36no10(m+h),计算值426.22,实测值426.20。 实施例13.3-(2-(2-(2-(2-羟基乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 向2,2’-(乙烷-1,2-二基双(氧基))二乙醇(55.0ml,410.75mmol,3.0eq.)的无水四氢呋喃(200ml)溶液中加入钠块(0.1g)。搅拌混合物直至钠块消失,然后滴加丙烯酸叔丁酯(20.0ml,137.79mmol,1.0eq.)。将混合物搅拌过夜,然后在0℃下用盐酸(20.0ml,1n)淬灭。通过旋转浓缩除去四氢呋喃,加入盐水(300ml)并将所得混合物用乙酸乙酯(3×100ml)萃取。将有机层用盐水(3×300ml)洗涤,经无水硫酸钠干燥,过滤并浓缩,得到无色油状物(30.20g,79.0%产率),其不经进一步纯化而直接使用。esimsm/z:c13h27o6[m+h]+计算值278.1729,实测值278.1730。 实施例14.3-(2-(2-(2-(2-(甲苯磺酰氧基)乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 在0℃下,向3-(2-(2-(2-羟基乙氧基)乙氧基)乙氧基)丙酸叔丁酯(30.20g,108.5mmol,1.0eq.)和tscl(41.37g,217.0mmol,2.0eq.)的无水二氯甲烷(220ml)溶液中加入三乙胺(30.0ml,217.0mmol,2.0eq.)。将混合物在室温下搅拌过夜,然后用水(3×300ml)和盐水(300ml)洗涤,经无水硫酸钠干燥,过滤,浓缩并通过硅胶柱层析(3:1正己烷/乙酸乙酯)纯化得到无色油状物(39.4g,产率84.0%)。esimsm/z:c20h33o8s[m+h]+计算值433.1818,实测值433.2838。 实施例15.3-(2-(2-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 将3-(2-(2-(2-(甲苯磺酰氧基)乙氧基)乙氧基)乙氧基)丙酸叔丁酯(39.4g,91.1mmol,1.0eq.)溶解于无水dmf(100ml),接着加入nan3(20.67g,316.6mmol,3.5eq.)。将混合物在室温下搅拌过夜。加入水(500ml)并用乙酸乙酯(3×300ml)萃取。将合并的有机层用水(3×900ml)和盐水(900ml)洗涤,用无水硫酸钠干燥,过滤,浓缩并通过硅胶柱层析(5:1正己烷/乙酸乙酯)纯化,得到浅黄色油状物(23.8g,85.53%产率)。esimsm/z:c13h25o3n5na[m+na]+计算值326.2,实际值326.2。 实施例16.3-(2-(2-(2-(2-氨基乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 将raney-ni(7.5g,悬浮于水中)用水(三次)和异丙醇(三次)洗涤,并与异丙醇中的3-(2-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)丙酸叔丁酯(5.0g,16.5mmol)混合。在室温下,氢气球下搅拌该混合物16小时,然后用硅藻土垫过滤,用异丙醇洗涤垫。浓缩滤液并通过柱层析(5-25%甲醇/二氯甲烷)纯化,得到浅黄色油状物(2.60g,57%产率)。esimsm/z:c18h23no2na[m+na]+计算值279.19,实测值279.19。 实施例17.2-(2-(二(苄基氨基)乙氧基)乙醇的合成。 将2-(2-氨基乙氧基)乙醇(21.0g,200mmol)和碳酸钾(83.0g,600mmol)混合于乙腈(350ml)中,加入苄基溴(57.0ml,480mmol)。将混合物回流过夜后,加入水(1l),用乙酸乙酯(3×300ml)萃取。将合并的有机层用饱和食盐水(1000ml)洗涤,用无水硫酸钠干燥,过滤,浓缩并通过硅胶柱色谱(4:1石油醚/乙酸乙酯)纯化,得到无色油状物(50.97g,产率89.2%)。esimsm/z:c18h23no2na[m+na]+计算值:309.1729,实测值:309.1967。 实施例18.3-(2-(2-(2-(二苄氨基)乙氧基)乙氧基)丙酸叔丁酯的合成。 向2-(2-(二苄基氨基)乙氧基)乙醇(47.17g,165.3mmol),丙烯酸叔丁酯(72.0ml,495.9mmol)和四丁基碘化铵(6.10g,16.53mmol)的二氯甲烷(560ml)溶液中加入50%氢氧化钠水溶液(300ml)。将混合物搅拌过夜。分离有机层,水层用乙酸乙酯(3×100ml)萃取。合并有机层并用水(3×300ml)和饱和食盐水(300ml)洗涤,用无水硫酸钠干燥,过滤,浓缩并通过硅胶柱色谱(7:1石油醚/乙酸乙酯)纯化,得到无色油状物(61.1g,89.4%产率)。esimsm/z:c25h36no4[m+h]+计算值:414.2566,实测值:414.2384。 实施例19.3-(2-(2-(2-氨基乙氧基)乙氧基)丙酸叔丁酯的合成。 在氢化反应瓶中向3-(2-(2-(2-(二苄基氨基)乙氧基)乙氧基)丙酸叔丁酯(20.00g,48.36mmol,1.0eq.)的四氢呋喃(30ml)和甲醇(60ml)溶液中加入pd/c(2.00g,10wt%)。将混合物在氢气环境中(1atm)振荡过夜,通过硅藻土(助滤剂)过滤,浓缩滤液,得到无色油状物(10.58g,93.8%产率)。esimsm/z:c11h24no4[m+h]+:计算值234.1627,实测值234.1810。 实施例20.3-(2-(2-(2-羟基乙氧基)乙氧基)丙酸叔丁酯的合成。 向2,2’-氧代二乙醇(19.7ml,206.7mmol,3.0eq.)的无水四氢呋喃(100ml)溶液中加入钠(0.1g)。搅拌混合物直至钠块消失,然后滴加丙烯酸叔丁酯(10.0ml,68.9mmol,1.0eq.)。将混合物搅拌过夜,加入盐水(200ml)并用乙酸乙酯(3×100ml)萃取。将有机层用盐水(3×300ml)洗涤,经无水硫酸钠干燥,过滤,浓缩并通过硅胶柱层析(1:1正己烷/乙酸乙酯)纯化,得到无色油状物(8.10g,49.4%产率)。esimsm/z:c11h23o5[m+h]+的计算值235.1467,实测值235.1667。 实施例21.3-(2-(2-(甲苯磺酰氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 在0℃下,向3-(2-(2-羟基乙氧基)乙氧基)丙酸叔丁酯(6.24g,26.63mmol,1.0eq.)和tscl(10.15g,53.27mmol,2.0eq.)的无水二氯甲烷(50ml)溶液中加入吡啶(4.3ml,53.27mmol,2.0eq.)。将混合物在室温下搅拌过夜,然后用水(100ml)洗涤,水层用二氯甲烷(3×50ml)萃取。将合并的有机层用盐水(300ml)洗涤,经无水硫酸钠干燥,过滤,浓缩并通过硅胶柱层析(5:1正己烷/乙酸乙酯)纯化,得到无色油状物(6.33g,61.3%产率)。esimsm/z:c18h27o7s[m+h]+计算值389.1556,实测值389.2809。 实施例22.3-(2-(2-(2-叠氮基乙氧基)乙氧基)丙酸叔丁酯的合成。 向3-(2-(2-(甲苯磺酰氧基)乙氧基)乙氧基)丙酸叔丁酯(5.80g,14.93mmol,1.0eq.)的无水dmf(20ml)溶液中加入nan3(5.02g,77.22mmol),5.0eq.)。将混合物在室温下搅拌过夜,加入水(120ml)并用乙酸乙酯(3×50ml)萃取。将合并的有机层用水(3×150ml)和盐水(150ml)洗涤,用无水硫酸钠干燥,过滤,浓缩并通过硅胶柱层析(5:1正己烷/乙酸乙酯)纯化,得到无色油状物(3.73g,产率69.6%)。esimsm/z:c11h22o3n4na[m+h]+计算值260.1532,实测值260.2259。 实施例23.3-(2-(2-(2-氨基乙氧基)乙氧基)丙酸叔丁酯的合成。 将3-(2-(2-叠氮基乙氧基)乙氧基)丙酸叔丁酯(0.18g,0.69mmol)溶于甲醇(3.0ml,含60μl浓盐酸)中,并与pd/c(10wt%,20mg)氢化反应30分钟。将催化剂通过硅藻土垫过滤,用甲醇洗涤硅藻土垫。浓缩滤液,得到无色油状物(0.15g,93%产率)。esimsm/z:c11h24no4[m+h]+的计算值234.16,实测值234.14。 实施例24.3-(2-(2-叠氮基乙氧基)乙氧基)丙酸的合成。 将3-(2-(2-叠氮基乙氧基)乙氧基)丙酸叔丁酯(2.51g,9.68mmol)溶解于1,4-二恶烷(30ml)中并与10ml浓盐酸在室温下搅拌35分钟,用乙醇(30ml)和甲苯(30ml)稀释,并在真空下浓缩。将粗品在硅胶柱上使用甲醇/二氯甲烷(5%至10%)(含1%甲酸)纯化,得到标题化合物(1.63g,83%产率),esimsm/z:c7h12n3o4[m-h]-计算值202.06,实测值202.30。 实施例25.2,5-二氧吡咯烷基-1-基3-(2-(2-叠氮基乙氧基)乙氧基)丙酸酯的合成。 在搅拌下向3-(2-(2-叠氮基乙氧基)乙氧基)丙酸(1.60g,7.87mmol)的二氯甲烷(30ml)溶液中加入nhs(1.08g,9.39mmol)和edc(3.60g,18.75mmol)。8小时后tlc分析显示反应完成,浓缩反应混合物并在硅胶上纯化,乙酸乙酯/二氯甲烷(5%-10%)洗脱,得到标题化合物(1.93g,收率82%)。esimsm/z:c11h17n4o6[m+h]+,计算值:301.11,实测值:301.20。 实施例26.2,5-二氧代吡咯烷-1-基3-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)丙酸酯的合成。 向3-(2-(2-(2-叠氮基乙氧基)乙氧基)丙酸(4.50g,18.21mmol)的二氯甲烷(80ml)溶液中加入nhs(3.0g,26.08mmol)和edc(7.60g,39.58mmol),搅拌8小时后tlc分析显示反应完成,浓缩反应混合物并在硅胶上纯化,乙酸乙酯/二氯甲烷(5%-10%)洗脱,得到标题化合物(5.38g,收率86%)。esimsm/z:c13h20n4o7[m+h]+,计算值:345.13,实测值:345.30。 实施例27.(14s,17s)-1-叠氮基-17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-((叔丁氧基羰基)-氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸。 向(s)-2-((s)-2-氨基-6-((叔丁氧基羰基)氨基)己酰胺基)-4-(叔丁氧基)-4-氧代丁酸(2.81g,6.73mmol)在dma(70ml)和0.1mnah2po4(50ml,ph7.5)的混合物中加入2,5-二氧代吡咯烷-1-基3-(2-(2-叠氮基乙氧基)乙氧基)丙酸酯(3.50g,10.17)。将混合物搅拌4小时,真空蒸发,在硅胶上纯化,以甲醇(5%-15%)在含有0.5%乙酸的二氯甲烷溶液作为洗脱液,得到标题化合物(3.35g,收率77%)。esimsm/z:c28h51n6o11[m+h]+,计算值:647.35,实测值:647.80。 实施例28.(14s,17s)-1-叠氮基-14-(4-((叔丁氧基羰基)-氨基)丁基)-17-((4-(羟甲基)苯基)氨基甲酰基)-12,15-的合成二氧代-3,6,9-三氧杂-13,16-二氮杂癸烷-19-酸叔丁酯。 向(14s,17s)-1-叠氮基-17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-((叔丁氧基羰基)-氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸(3.30g,5.10mmol)和(4-氨基苯基)甲醇(0.75g,6.09)的dma(25ml)溶液中加入edc(2.30g,11.97mmol))。将混合物搅拌过夜,真空蒸发,使用甲醇/二氯甲烷(5%-8%)作为洗脱剂在硅胶上纯化,得到标题化合物(3.18g,收率83%)。esimsm/z:c35h58n7o11[m+h]+,计算值:752.41,实测值:752.85。 实施例29.(14s,17s)-1-氨基-14-(4-((叔丁氧基羰基)-氨基)丁基)-17-((4-(羟甲基)苯基)氨基甲酰基)-12,15-的合成二氧代-3,6,9-三氧杂-13,16-二氮杂并癸烷-19-酸叔丁酯。 向(14s,17s)-1-叠氮基-14-(4-((叔丁氧基羰基)氨基)丁基)-17-((4-(羟甲基)苯基)氨基甲酰基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂萘并癸烷-19-酸叔丁酯(1.50g,1.99mmol)的四氢呋喃(35ml)溶液中加入pd/c(200mg,10%pd,50%水)。将混合物在1psi的h2下振荡过夜,通过硅藻土(助滤剂)过滤,浓缩滤液,得到标题化合物(1.43g,99%收率),无需进一步纯化,立即用于下一步骤。esimsm/z:c35h60n5o11[m+h]+,计算值:726.42,实测值:726.70。 实施例30.(s)-15-叠氮基-5-异丙基-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十五烷-1-酸的合成。 向(s)-2-(2-氨基-3-甲基丁酰胺基)乙酸(val-gly)(1.01g,5.80mmol)的dma(50ml)和0.1mnah2po4(50ml,ph7.5)溶液中加入2,5-二氧代吡咯烷-1-基3-(2-(2-叠氮基乙氧基)乙氧基)丙酸酯(1.90g,6.33)。将混合物搅拌4小时,真空蒸发,在硅胶上纯化,以甲醇(5%-15%)在含有0.5%乙酸的二氯甲烷溶液作为洗脱液,得到标题化合物(1.52g,收率73%)。esimsm/z:c14h26n5o6[m+h]+,计算值:360.18,实测值:360.40。 实施例31.(s)-2,5-二氧代吡咯烷-1-基15-叠氮基-5-异丙基-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十五烷-1-酸酯的合成 向(s)-15-叠氮基-5-异丙基-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十五烷-1-酸(1.50g,4.17mmol)的二氯甲烷(40ml)溶液中加入nhs(0.88g,7.65mmol)和edc(2.60g,13.54mmol)。8小时后tlc分析显示反应完成,将反应混合物浓缩并在硅胶柱上纯化,使用5%至20%乙酸乙酯的二氯甲烷溶液作为洗脱液,得到标题化合物(1.48g,78%收率)。esimsm/z:c18h29n6o8[m+h]+,计算值:457.20,实测值:457.50. 实施例32.4-((苄氧基)羰基)氨基)丁酸的合成。 在0°c,将4-氨基丁酸(7.5g,75mmol)和naoh(6g,150mmol)溶解于水(40ml),加入氯甲酸苄酯(16.1g,95mmol)的四氢呋喃(32ml)溶液。将反应在0℃搅拌1小时,室温3小时。减压蒸馏除去四氢呋喃,用浓盐酸调节水溶液ph值至3。用乙酸乙酯萃取,饱和食盐水洗,无水硫酸钠干燥,浓缩得到白色固体(16.4g,92%)。msesim/z:c12h16no5[m+h]+计算值:238.10,实测值:238.08。 实施例33.4-(((苄氧基)羰基)氨基)丁酸叔丁酯的合成。 将dmap(0.8g,6.56mmol)和dcc(17.1g,83mmol)加入到4-((((苄氧基)羰基)氨基)丁酸(16.4g,69.2mmol)和叔丁醇(15.4g,208mmol)的二氯甲烷(100ml)溶液中。室温搅拌过夜,将反应物过滤并浓缩滤液。将残留物溶于乙酸乙酯中,用1nhcl,饱和食盐水洗涤,用硫酸钠干燥,过滤,浓缩后通过柱色谱(10至50%乙酸乙酯/石油醚)纯化,得到目标化合物(7.5g,37%产率)msesim/z:c16h23no4na[m+na]+计算值:316.16,实测值:316.13。 实施例34.4-氨基丁酸叔丁酯的合成。 将4-(((苄氧基)羰基)氨基)丁酸叔丁酯(560mg,1.91mmol)溶于甲醇(50ml)中,与pd/c催化剂(10wt%,100mg)混合,然后氢化(1atm)反应3小时。滤出催化剂,减压蒸馏除去所有挥发物,得到标题化合物(272mg,90%产率)。msesim/zc8h18no2[m+h]+计算值:160.13,实测值:160.13。 实施例35.3,3′-(苄基氮杂二基)二丙酸二叔丁酯的合成。 在80℃下,将苯基甲胺(2.0ml,18.29mmol,1.0eq.)和丙烯酸叔丁酯(13.3ml,91.46mmol,5.0eq.)的混合物回流过夜,然后浓缩。通过硅胶柱(20:1正己烷/乙酸乙酯)纯化粗产物,得到标题化合物,为无色油状物(5.10g,77%产率)。esimsm/z:c21h34no4[m+h]+计算值:364.2,实测值:364.2。1hnmr(400mhz,cdcl3)δ7.38–7.21(m,5h),3.58(s,2h),2.76(t,j=7.0hz,4h),2.38(t,j=7.0hz,4h),1.43(s,17h)。 实施例36.3,3′-氮杂二丙基二丙酸二叔丁酯的合成。 在氢化反应瓶中,向3,3′-(苄基氮杂二基)二丙酸二叔丁酯(1.37g,3.77mmol,1.0eq.)的甲醇(10ml)溶液中加入pd/c(0.20g,10%pd/c,含水50%)。将混合物在h2气中振荡过夜,然后通过硅藻土垫过滤。浓缩滤液得到标题化合物,为无色油状物(1.22g,89%产率)。esimsm/z:c14h28no4[m+h]+计算值:274.19,实测值:274.20。 实施例37.4-(2-(((苄氧基)羰基)氨基)丙酰胺基)-丁酸叔丁酯的合成。 在0℃下,向4-氨基丁酸叔丁酯(1.00g,6.28mmol,1.0eq.)和z-l-丙氨酸(2.10g,9.42mmol,1.5eq.)的无水二氯甲烷(50ml)溶液中加入hatu(3.10g,8.164mmol,1.3eq.)和三乙胺(2.6ml,18.8mmol,3.0eq.)。将反应物在0℃下搅拌10分钟,然后加热至室温并搅拌过夜。将混合物用二氯甲烷稀释,用水和盐水洗涤,经无水硫酸钠干燥,浓缩,并通过硅胶柱(10:3石油醚/乙酸乙酯)纯化,得到标题化合物,为无色油状物(1.39g,61%产率)。esimsm/z:c19h29n2o5na[m+h]+计算值387.2,实测值387.2。 实施例38.4-(2-氨基丙酰胺基)丁酸叔丁酯的合成。 在氢化反应瓶中,向4-(2-(((苄氧基)羰基)氨基)丙酰胺基)丁酸叔丁酯(1.39g,3.808mmol,1.0eq.)的甲醇(12ml)溶液中加入pd/c(0.20g,10wt%)。将混合物在氢气中振荡2小时,然后通过硅藻土(助滤剂)过滤,浓缩,得到标题化合物,为浅黄色油状物(0.838g,95%产率)。esimsm/z:c11h23n2o3[m+h]+计算值231.16,实测值231.15。 实施例39.3-(2-(2-(二苄基氨基)乙氧基)乙氧基)丙酸的合成。 在室温下,向3-(2-(2-(二苄基氨基)乙氧基)丙酸叔丁酯(2.3g,5.59mmol,1.0eq)的二氯甲烷(10ml)溶液中加入tfa(5ml)。搅拌90分钟后,将反应混合物用无水甲苯稀释并浓缩,重复该操作三次,得到标题化合物,为浅黄色油状物(2.0g,理论收率),将其直接用于下一步。esimsm/zc21h28no4[m+h]+计算值:358.19,实测值:358.19。 实施例40.五氟苯基3-(2-(2-(二苄基氨基)乙氧基)乙氧基)-丙酯的合成。 在0℃下,向3-(2-(2-(二苄基氨基)乙氧基)乙氧基)丙酸(2.00g,5.59mmol,1.0eq.)在无水二氯甲烷(30ml)的溶液中加入dipea直至ph为中性,然后加入五氟苯酚(1.54g,8.38mmol,1.5eq.)和dic(1.04ml,6.70mmol,1.2eq.)。10分钟后,将反应升温至室温并搅拌过夜。将混合物过滤,浓缩并通过硅胶柱柱色谱(15:1石油醚/乙酸乙酯)纯化,得到标题化合物,为无色油状物(2.10g,72%产率)。esimsm/z:c27h27f5no4[m+h]+计算值:524.2,实测值:524.2。 实施例41.2-苄基-13-甲基-11,14-二氧代-1-苯基-5,8-二氧杂-2,12,15-三氮杂十九烷-19-叔丁酯的合成。 0℃时,向4-(2-氨基丙酰胺基)丁酸叔丁酯(0.736g,3.2mmol,1.0eq.)和五氟苯基3-(2-(2-(二苄基氨基)乙氧基)乙氧基)丙酯(2.01g,3.84mmol,1.2eq.)的无水dma(20ml)溶液中加入dipea(1.7ml,9.6mmol,3.0eq.)。在0℃下搅拌10分钟,将反应升温至室温并搅拌过夜。加入水(100ml)并将混合物用乙酸乙酯(3×100ml)萃取。将合并的有机层用水(3×200ml)和盐水(200ml)洗涤,用无水硫酸钠干燥,过滤,浓缩并通过硅胶柱层析(25:2二氯甲烷/甲醇)纯化,得到标题化合物,为浅黄色油状物(1.46g,80%产率)。esimsm/z:c32h48n3o6[m+h]+计算值:570.34,实测值:570.33。 实施例42.2-苄基-13-甲基-11,14-二氧代-1-苯基-5,8-二氧杂-2,12,15-三氮杂十九烷-19-酸的合成。 在室温下,向2-苄基-13-甲基-11,14-二氧代-1-苯基-5,8-二氧杂-2,12,15-三氮杂十九烷-19-酸叔丁酯(0.057g,0.101mmol,1.0eq.)的二氯甲烷(3ml)溶液中加入tfa(1ml)并搅拌40分钟。用无水甲苯稀释反应物,然后浓缩。重复该操作三次,得到标题化合物,为无色油状物(0.052g,理论产率),将其直接用于下一步骤。esimsm/z:c28h40n3o6[m+h]+计算值:514.28,实测值:514.28。 实施例43.2-(2-(((苄氧基)羰基)氨基)丙酰胺基)-乙酸叔丁酯的合成。 将2-(((苄氧基)羰基)氨基)丙酸(0.84g,5mmol),2-氨基乙酸叔丁酯(0.66g,5mmol),hobt(0.68g,5mmol),edc(1.44g,7.5mmol)溶于二氯甲烷(20ml),然后加入dipea(1.7ml,10mmol)。将反应混合物在室温下搅拌过夜,用水(100ml)洗涤,并将水层用乙酸乙酯萃取。合并有机层,用硫酸镁干燥,过滤,减压浓缩,残余物在硅胶柱上纯化,得到标题产物(0.87g,52%)。esim/z:c17h25n2o5[m+h]+:计算值:337.17,实测值:337.17。 实施例44.2-(2-((苄氧基)羰基)氨基)丙酰胺基)乙酸的合成。 将2-(2-(((苄氧基)羰基)氨基)丙酰胺基)乙酸叔丁酯(0.25g,0.74mmol)溶于二氯甲烷(30ml)中,然后加入tfa(10ml)。将混合物在室温搅拌过夜,浓缩,得到标题化合物,其不经进一步纯化直接用于下一步。esim/z:c13h17n2o5[m+h]+:计算值:281.11,实测值:281.60。 实施例45.3-(2-(2-(2-羟基乙氧基)乙氧基)乙氧基)丙酸叔丁酯的合成。 在搅拌下向350ml无水四氢呋喃中加入80mg(0.0025mol)金属钠和三乙二醇(150.1g,1.00mol)。在钠完全溶解后,加入丙烯酸叔丁酯(24ml,0.33mol)。将溶液在室温下搅拌20小时,然后用8ml1.0mhcl中和。真空除去溶剂,将残余物悬浮在盐水(250ml)中,用乙酸乙酯(3×125ml)萃取。将合并的有机层用盐水(100ml)洗,水(100ml)洗,用硫酸钠干燥,除去溶剂。将得到的无色油状物真空干燥,得到69.78g(76%产率)标题产物。1hnmr:1.41(s,9h),2.49(t,2h,j=6.4hz),3.59-3.72(m,14h)。esimsm/zc13h25o6(m-h)计算值:277.17,实测值:277.20。 实施例46.2,5,8,11,14,17,20,23,26,29-十二氧杂三十一烷-31-酸叔丁基酯的合成。 将nah(60%,8.0g,200mmol)加入到2,5,8,11,14,17,20,23,26-九氧杂二十八烷-28-醇(42.8g,100mmol)的四氢呋喃(1.0l)溶液中。在室温搅拌30分钟后,向混合物中加入2-溴乙酸叔丁酯(48.8g,250mmol),并在室温下搅拌1小时。然后将混合物倒入冰水中,用二氯甲烷萃取,用盐水洗涤有机层,用无水硫酸钠干燥。用柱层析法(0%~5%甲醇:二氯甲烷)纯化,得到黄色油状化合物432(32g,收率59%)。 实施例47.2,5,8,11,14,17,20,23,26,29-十二氧杂三十一烷-31-酸的合成。 将2,5,8,11,14,17,20,23,26,29-十二氧杂三十一烷-31-酸叔丁酯(40.0g,73.8mmol)溶解于二氯甲烷(400ml)中,然后加入甲酸(600ml)。将所得溶液在25℃下搅拌过夜。在真空下除去所有挥发物,得到的标题产物,为黄色油状物(36.0g,理论收率)。esim/zc21h43o12[m+h]+计算值:487.27,实测值:487.24。 实施例48.2,5,8,11,14,17,20,23,26,29-十二氧杂三十一烷-31-酰氯的合成。 向2,5,8,11,14,17,20,23,26,29-十二氧杂三十一烷-31-酸(36.0g,73.8mmol)的二氯甲烷(640ml)溶液中加入(cocl)2(100ml)和dmf(52g,0.74mmol)。在室温下将所得溶液搅拌4小时。在真空下除去所有挥发物,得到黄色油状标题产物。 实施例49.(s)-37-(苄氧)羰基)氨基)-31-氧代-2,5,8,11,14,17,20,23,26,29-十二氧杂-32-氮杂三十八烷-38-酸的合成。 将z-l-lys-oh(41.4g,147.6mmol),na2co3(23.4g,221.4mmol)和naoh(5.9g,147.6mmol)溶于水(720ml)中。将混合物冷却至0℃,向其中加入2,5,8,11,14,17,20,23,26,29-十二氧杂三十一烷-31-酰氯(37.2g,73.8mmol)的四氢呋喃(20ml)溶液。将所得混合物在室温下搅拌1小时。在真空下除去四氢呋喃,并将浓hcl加入冰冷下的水溶液中直至ph达到3。用二氯甲烷萃取后,将有机层用盐水洗涤,用硫酸钠干燥并浓缩,得到标题产物,为黄色油状物(55g,收率99%)。esimsm/zc35h60n2o15[m+h]+:计算值:749.40,实测值:749.39。 实施例50.(s)-13-(2-(((苄氧基)羰基)氨基)-5-(叔丁氧基)-5-氧代戊烷酰胺基)十三烷酸叔丁酯的合成。 向(s)-2-(((苄氧基)羰基)氨基)-5-(叔丁氧基)-5-氧代戊酸(3.50g,10.38mmol)和13-氨基十三烷酸叔丁酯(3.00g,10.51mmol)的dmf(70ml)溶液中加入edc(10.00g,52.08mmol)和tea(1.60ml,11.16mmol)。将反应在室温下搅拌8小时,真空浓缩,用饱和盐水(80ml)和乙酸乙酯(100ml)稀释,分离。水层用乙酸乙酯(50ml×3)萃取,合并的有机相用100ml饱和盐水洗涤一次,然后用无水硫酸钠干燥,过滤并浓缩。通过硅胶柱色谱(乙酸乙酯/二氯甲烷,1:15)纯化残余物,得到标题化合物(5.45g,收率87%),esimsm/z:c34h57n2o7[m+h]+:计算值:605.41,实测值:605.38。 实施例51.(s)-13-(2-氨基-5-(叔丁氧基)-5-氧代戊烷酰胺基)十三烷酸叔丁酯的合成。 向13-(2-(((苄氧基)羰基)氨基)-5-(叔丁氧基)-5-氧代戊烷酰胺基)十三烷酸叔丁酯(2.80g,4.63mmol)的dma(100ml)溶液中加入10%pd/c(0.41g),将混合物在氢气下室温中搅拌18小时。然后通过硅藻土过滤除去pd/c,并用dma洗涤滤床。浓缩滤液,得到黄色泡沫状产物,其无需进一步纯化即可用于下一步(2.19g,收率101%)。esimsm/z:c26h51n2o5[m+h]+计算值:471.37,实测值:471.80。 实施例52.2,2-二甲基-4,17-二氧代-3,7,10,13,20,23,26-七氧杂-16-氮杂二十九烷-29-酸的合成 在3-(2-(2-(2-氨基乙氧基)乙氧基)丙酸叔丁酯(6.00g,21.64mmol)和3,3′-(氧代双(乙烷-2,1-二基))双(氧基))二丙酸(21.01g,84.00mmol)的dma(200ml)溶液中加入edc(18.00g,93.75mmol)和dipea(5.00g,38.75mmol)。将混合物搅拌过夜,然后浓缩并通过硅胶柱色谱法纯化(甲醇:二氯甲烷=1:12至1:5),得到标题化合物,为白色油状物(9.15g,86%收率)。esimsm/z:c23h44no11[m+h]+计算值:510.28,实测值:510.55。 实施例53.1-苄基39叔丁基14,26-二氧代-4,7,10,17,20,23,30,33,36-壬氧基-13,27-二氮杂三十九烷-1,39-二酯的合成。 在(s)-叔丁基13-(2-氨基-5-(叔丁氧基)-5-氧代戊烷酰胺基)十三烷酯(5.11g,10.03mmol)和3-(2-(2-氨基乙氧基)乙氧基)乙氧基)丙酸酯(3.21g,10.31mmol)的dma(100ml)溶液中加入edc(8.02g,41.77mmol)和dipea(3.00g,23.25mmol)。将混合物搅拌过夜,然后浓缩并通过硅胶柱色谱法纯化(乙酸乙酯:二氯甲烷=1:8至1:3),得到标题化合物,为白色油状物(7.01g,87%收率)。esimsm/z:c39h67n2o15[m+h]+计算值:803.44,实测值:803.80。 实施例54.3,16,28-三氧代-1-苯基-2,6,9,12,19,22,25,32,35,38-十氧杂-15,29-二氮杂四十一烷-41-酸的合成。 将1-苄基39叔丁基14,26-二氧代-4,7,10,17,20,23,30,33,36-十三烷-13,27-二氮杂三十九烷-1,39-二酯(6.90g,8.60mmol)溶于hcooh(50ml)中并在0-4℃下搅拌1小时。将反应混合物用甲苯(50ml)稀释,浓缩并与甲苯共蒸发两次,并将残余物置于真空泵上得标题化合物(6.45g,产率约101%,粗产物)。esimsm/z:c35h59n2o15[m+h]+计算值:747.38,实测值:747.50。 实施例55.1-苄基39-(2,5-二氧代吡咯烷-1-基)14,26-二氧代-4,7,10,17,20,23,30,33,36-九氧杂-13,27-二氮杂三十九烷-1,39-二酯。 在3,16,28-三氧代-1-苯基-2,6,9,12,19,22,25,32,35,38-十氧杂-15,29-二氮杂四十一烷-41-酸(4.01g,5.37mmol)和nhs(n-羟基琥珀酰亚胺)(0.68g,5.91mmol)的dma(100ml)溶液中加入edc(1.52g,7.92mmol)和dipea(0.50g,3.87mmol)。将混合物搅拌过夜,然后浓缩并通过硅胶柱色谱法纯化(乙酸乙酯:二氯甲烷=1:8至1:4),得到标题化合物,为白色泡沫状物(4.17g,收率92%)。esimsm/z:c39h62n3o17[m+h]+计算值:844.40,实测值:844.85。 实施例56.(s)-47-(((苄氧基)羰基)氨基)-3,16,28,41-四氧代-1-苯基-2,6,9,12,19,22,25,32,35,38-十氧杂-15,29,42-三氮四十八烷-48-酸的合成。 向(s)-6-氨基-2-(((苄氧基苄氧基)羰基)氨基)氨基)己酸(1.38g,4.92mmol)的dma(30ml)和100mmnah2po4,ph7.5缓冲液(40ml)中,在2小时内分4份加入1-苄基39-(2,5-二氧代吡咯烷-1-基)14,26-二氧代-4,7,10,17,17,20,23,30,33,33,36-九氧杂-13,27-二氮杂三十九烷-1,39-二酯(4.15g,4.92mmol)。将混合物搅拌4小时,然后浓缩并通过硅胶柱色谱法纯化(甲醇:二氯甲烷=1:7至1:4),得到标题化合物,为白色泡沫状物(4.07g,收率82%)。esimsm/z:c49h77n4o18[m+h]+计算值:1009.51,实测值:1009.90。 实施例57.(s)-1-苄基51-(2-(三甲基甲硅烷基)乙基)45-(((苄氧基)-羰基)氨基)-14,26,39,46-四氧代-4,7,10,17,20,23,30,33,36-九氧杂-13,27,40,47-四氮杂五十一烷-1,51-二酯的合成。 向(s)-47-(((苄氧基)羰基)氨基)-3,16,28,41-四氧代-1-苯基-2,6,9,12,19,22,25,32的溶液中加入35,38-十氧杂-15,29,42-三氮杂四十八烷-48-酸(4.00g,3.96mmol)和2-(三甲基甲硅烷基)4-氨基丁酸乙酯(0.90g,4.43mmol)的dma(25ml)溶液中,加入edc(2.03g,10.57mmol)。将混合物搅拌6小时,然后浓缩并通过硅胶柱色谱法纯化(甲醇:二氯甲烷=1:15至1:8),得到标题化合物,为白色泡沫状物(3.97g,收率84%)。esimsm/z:c58h96n5o19si[m+h]+计算值:1194.64,实测值:1194.90。 实施例58.12-氨基-2,2-二甲基-6,11,18,31,43-五氧代-5,21,24,27,34,37,40,47,50,53-十氧代-10,17,30,44-四氮杂-2-五十六烷-56-酸的合成。 在氢化瓶中向(s)-1-苄基51-(2-(三甲基甲硅烷基)乙基)45-(((苄氧基)-羰基)氨基)-14,26,39,46-四氧代-4,7,10,17,20,23,30,33,36-九氧杂-13,27,40,47-四氮杂苯基戊烷-1,51-二酯(3.90g,3.33mmol)的甲醇(40ml)溶液中加入pd/c(10wt%,0.20g)。将混合物在40psi氢气下振荡2小时,通过硅藻土(助滤剂)过滤,浓缩滤液,得到标题化合物(3.16g,收率98%),其不经进一步纯化直接用于下一步。esimsm/z:c43h83n5o17si[m+h]+计算值:970.55,实测值:970.70。 实施例59.2,5-二氧代吡咯烷-1-基4-((3ar,7r,7as)-1,3-二氧代-3a,4,7,7a-四氢-1h-4,7-环氧异吲哚-2(3h))-基)丁酸酯的合成。 在压力容器中将4-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丁酸(10.0g,54.62mmol)和呋喃(5ml,68.74mmol)的乙醚(90ml)溶液在170℃加热6小时,然后将溶液冷却至室温,真空浓缩并在etoh/正己烷中结晶,得到4-((3ar,7r,7as)-1,3-二氧代-3a,4,7,7a-四氢-1h-4,7-环氧异吲哚-2(3h)-基)丁酸(11.24g,44.76mmol,收率82%)。然后重新溶解在二氯甲烷(100ml)中,加入nhs(7.00g,60.86mmol)和edc(25.00g,130.20mmol)。将混合物搅拌6小时,然后浓缩并通过硅胶柱色谱法纯化(乙酸乙酯:二氯甲烷=1:8至1:5),得到标题化合物,为白色泡沫状物(13.57g,收率87%)。esimsm/z:c16h17n2o7[m+h]+:计算值:349.09,实测值:349.55。 计算值60.2,3-双(2-溴乙酰氨基)琥珀二酰氯的合成。 向thf/h2o/dipea(125ml/125ml/8ml)的混合物中加入2,3-二氨基琥珀酸(5.00g,33.77mmol)和2-溴乙酰溴(25.0g,125.09mmol)。将混合物搅拌过夜,蒸发并通过硅胶柱色谱法(水/乙腈5:95)纯化,得到浅黄色油状物2,3-双(2-溴乙酰氨基)琥珀酸(9.95g,收率76%)。esimsm/z:c8h11br2n2o6[m+h]+计算值:388.89,实测值:388.68。 向2,3-双(2-溴乙酰氨基)琥珀酸(3.50g,9.02mmol)的二氯甲烷(80ml)溶液中加入草酰氯(5.80g,46.05mmol)和dmf(0.01ml)。将混合物搅拌2.5小时,用甲苯稀释,浓缩并与二氯乙烷(2×20ml)和甲苯(2×15ml)共蒸发至干,得到2,3-双(2-溴乙酰氨基)琥珀二酰氯(粗品,不稳定),用于下一步而无需进一步纯化(3.90g,收率102%)。esimsm/z:c8h9br2cl2n2o4[m+h]+计算值:424.82,实测值:424.90。 实施例61.2,3-双(((苄氧基)羰基)氨基)琥珀酸的合成。 向2,3-二氨基琥珀酸(4.05g,27.35mmol)的四氢呋喃(250ml)和nah2po4(0.1m,250ml,ph8.0)的混合物中,在两小时内分4份加入苄基氯甲酸酯(15.0g,88.23mmol)。将混合物再搅拌6小时,浓缩并上样到硅胶柱上,用含有1%甲酸的水/乙腈(1:9)洗脱,得到标题化合物(8.65g,收率76%,纯度~95%)。esimsm/z:c20h21n2o8[m+h]+计算值:417.12,实测值:417.60。 实施例62.双(2,5-二氧代吡咯烷-1-基)2,3-双(((苄氧基)羰基)-氨基)琥珀酸酯的合成。 向2,3-双(((苄氧基)羰基)氨基)琥珀酸(4.25g,10.21mmol)的dma(70ml)溶液中加入nhs(3.60g,31.30mmol)和edc(7.05g,36.72mmol)。将混合物搅拌过夜,浓缩并上样到硅胶柱上,用乙酸乙酯/二氯甲烷(1:6)洗脱得到标题化合物(5.42g,收率87%,纯度~95%)。esimsm/z:c28h27n4o12[m+h]+计算值:611.15,实测值:611.60。 实施例63.4,4′-((2,3-双(((苄氧基)羰基)氨基)-琥珀酰基)双(氮杂二基))丁酸二叔丁酯的合成。 向2,3-双(((苄氧基)羰基)氨基)琥珀酸(4.25g,10.21mmol)的dma(70ml)混合物中加入4-氨基丁酸叔丁酯(3.25g,20.42mmol))和edc(7.01g,36.70mmol)。浓缩并上样到硅胶柱上,用乙酸乙酯/二氯甲烷(1:10)洗脱,得到标题化合物(6.56g,收率92%,纯度~95%)。esimsm/z:c36h51n4o10[m+h]+计算值:699.35,实测值:699.55。 实施例64.4,4′-((2,3-二氨基琥珀酰基)双(氮杂二基))-丁酸二叔丁酯的合成。 向4,4′-((2,3-双(((苄氧基)羰基)氨基)-琥珀酰基)双-(氮杂二基))二丁酸二叔丁酯(2.50g,3.58mmol)的甲醇(100ml)溶液中加入10%pd/c(0.30g,50%湿),将混合物在氢气中室温下搅拌18小时。然后通过硅藻土过滤除去pd/c,并用甲醇(~70ml)洗涤滤床。浓缩滤液,得到黄色泡沫状产物,其无需进一步纯化即可用于下一步(1.55g,收率101%)。esimsm/z:c20h39n2o6[m+h]+计算值:431.28,实测值:431.40。 实施例65.4,4′-((2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯的合成。 向3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酸(1.25g,7.39mmol)的dma(60ml)溶液中加入4,4′-((2,3-二氨基琥珀酰基)双(氮杂二基))-二丁酸二叔丁基酯(1.55g,)和edc(2.41g,12.61mmol)。将混合物搅拌过夜,浓缩并上样到硅胶柱上,用乙酸乙酯/二氯甲烷(1:10)洗脱,得到标题化合物(2.33g,收率89%)。esimsm/z:c34h49n6o12[m+h]+计算值:733.33,实测值733.50。 实施例66.4,4′-((2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸的合成。 向搅拌的4,4′-((2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯(2.30g,3.14mmol)的1,4-二氧六环(20ml)溶液中加入hcl(36%,7.0ml)。将混合物搅拌30分钟,用甲苯(20ml)稀释,浓缩并上样到硅胶柱上,用甲醇/二氯甲烷(1:10至1:4)洗脱,得到标题化合物(1.67g,收率85%)。esimsm/z:c26h33n6o12[m+h]+计算值:621.21,实测值:621.55。 实施例67.4,4′-((2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯的合成。 向2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酸(1.12g,7.22mmol)的dma(60ml)溶液中加入4,4′-((2,3-二氨基琥珀酰基)双-(氮杂二基))二丁酸二叔丁基酯(1.55g,~3.58mmol)和edc(2.40g,12.56mmol)。将混合物搅拌过夜,浓缩并上样到硅胶柱上,用乙酸乙酯/二氯甲烷(1:10)洗脱,得到标题化合物(2.27g,收率90%)。esimsm/z:c32h45n6o12[m+h]+计算值:704.30,实测值:704.55。 计算值68.4,4′-((2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)琥珀酰基)双(氮杂二基))二丁酸的合成。 向4,4′-((2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯(2.20g,3.12mmol)的1,4-二氧六环(20ml)溶液中加入hcl(36%,7.0ml)。将混合物搅拌30分钟,用甲苯(20ml)稀释,浓缩并上样到硅胶柱上,用甲醇/二氯甲烷(1:10至1:4)洗脱,得到标题化合物(1.67g,85%收率)。esimsm/z:c24h29n6o12[m+h]+593.18,found593.50。 实施例69.双(2,5-二氧代吡咯烷-1-基)4,4′-(2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)琥珀酰基)双(氮杂二基))二丁酸酯。 向4,4′-((2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-琥珀酰基)双(氮杂二基))二丁酸(1.10g,1.85mmol)的dma(30ml)溶液中加入nhs(1-羟基吡咯烷-2,5-二酮)(0.55g,4.78mmol)和edc(1.25g,6.54mmol)。将混合物搅拌过夜,浓缩并上样到硅胶柱上,用乙酸乙酯/二氯甲烷(1:10)洗脱,得到标题化合物(1.28g,收率88%)。esimsm/z:c32h35n8o16[m+h]+计算值:787.21,实测值:787.50。 实施例70.2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸的合成。 向2,3-二氨基琥珀酸(5.00g,33.77mmol)的thf/h2o/dipea(125ml/125ml/2ml)的混合溶液中加入马来酸酐(6.68g,68.21mmol)。将混合物搅拌过夜,蒸发,得到2,3-双((z)-3-羧基丙烯酰胺基)琥珀酸(11.05g,收率99%),为白色固体。esimsm/z:c12h13n2o10[m+h]+计算值:345.05,实测值:345.35。 向2,3-双((z)-3-羧基丙烯酰胺基)琥珀酸(11.05g,33.43mmol)在hoac(70ml),dmf(10ml)和甲苯(50ml)的混合溶液中的乙酸酐(30毫升)。将混合物搅拌2小时,用dean-stark分水器在100℃回流6小时,浓缩,用etoh(2×40ml)和甲苯(2×40ml)共浓缩,并在硅胶柱上纯化。水/乙腈(1:10)洗脱,得到标题化合物(7.90g,收率76%,纯度~95%)。esimsm/z:c12h9n2o8[m+h]+计算值:309.03,实测值:309.30。 实施例71.双(2,5-二氧代吡咯烷-1-基)2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸酯的合成。 向2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸(4.00g,12.98mmol)的dmf(70ml)混合溶液中加入nhs(3.60g,31.30mmol)和edc(7.05g,36.72mmol)。将混合物搅拌过夜,浓缩并上样到硅胶柱上,用乙酸乙酯/二氯甲烷(1:6)洗脱,得到标题化合物(5.73g,收率88%,hplc纯度~96%)。esimsm/z:c20h15n4o12[m+h]+计算值:503.06,实测值:503.45。 实施例72.(3s,6s,39s,42s)-6,39-二叔丁基(4-((叔丁氧基羰基)氨基)丁基)-22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,42-双((4-(羟甲基)苯基)氨基甲酰基)-5,8,21,24,37,40-六氧代-11,14,17,28,31,34-六氧杂-4,7,20,25,38,41-六氮杂四十四烷-1,44-二酯的合成。 向(14s,17s)-叔丁基1-氨基-14-(4-((叔丁氧羰基)氨基)丁基)-17-((4-(羟甲基)苯基)氨基甲酰基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十九烷-19-酯(1.43g,1.97mmol)和2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸的dma(25ml)溶液中,加入edc(1.30g,6.77mmol)。将混合物搅拌过夜,真空蒸发,减压浓缩,在硅胶柱上纯化,用甲醇/二氯甲烷(5%-8%)洗脱,得到标题化合物(1.33g,80%产率)。esimsm/z:c82h123n12o28[m+h]+,计算值1722.85,实测值1722.98。 实施例73.1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸叔丁酯的合成。 向3-(2-(2-(2-叠氮基乙氧基)乙氧基)乙氧基)丙酸(1.55g,6.27mmol),2-(2-氨基丙酰胺基)丙酸叔丁酯(1.35g,6.27mmol)的dma(60ml)溶液中,加入edc(3.05g,15.88mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:3)洗脱,得到标题化合物(2.42g,86%产率,hplc纯度约95%)。esimsm/z:c19h36n5o7[m+h]+计算值446.25,实测值446.60。 实施例74.1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸的合成。 向1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸叔丁酯(2.20g,4.94mmol)的1,4-二恶烷(40ml)溶液中加入浓hcl(12m,10ml)。将混合物搅拌40分钟,用二恶烷(20ml)和甲苯(40ml)稀释,浓缩,并与二恶烷(20ml)和甲苯(40ml)共浓缩至干,得到标题粗产物,用于下一步,无需进一步纯化(1.92g,100%产率,hplc纯度约94%)。esimsm/z:c15h28n5o7[m+h]+计算值390.19,实测值390.45。 实施例75.21,22-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧代-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二酸的合成。 在氢化反应器中,向1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸(1.90g,4.88mmol)的dma(40ml)溶液中加入pd/c(0.20克,含水50%)。将系统在真空下抽空,并在剧烈搅拌下通入2atm的氢气,在室温下搅拌6小时,tlc显示原料消失。将反应粗品通过短硅藻土垫过滤,用乙醇洗。滤液减压浓缩,得到粗产物1-氨基-1,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸的dma溶液,直接用于下一步。esimsm/z:c15h30n3o7(m+h),计算值364.20,实测值364.30。 向上述氨基化合物的dma(~30ml)溶液中加入0.1mnah2po4(ph7.5,20ml),然后加入双(2,5-二氧代吡咯烷-1-基)2,3-双(2,5-)二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸酯(1.30g,2.59mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用含8%水的乙腈溶液洗脱,得到标题化合物(1.97g,81%产率)。esimsm/z:c42h63n8o20[m+h]+,计算值999.41,实测值999.95。 实施例76.双(2,5-二氧代吡咯烷-1-基)21,22-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧代-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二酯的合成。 向21,22-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧代-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二酸(1.50g,1.50mmol)的dma(10ml)的溶液中加入nhs(0.60g,5.21mmol)和edc(1.95g,10.15mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:4至2:1)洗脱,得到标题化合物(1.50g,83%产率,hplc纯度约95%)。esimsm/z:c50h69n10o24[m+h]+计算值1193.44,实测值1193.95。 实施例77.(s)-2-(羟甲基)吡咯烷-1-羧酸叔丁酯的合成。 将溶解在50ml四氢呋喃中的boc-l-脯氨酸(10.0g,46.4mmol)冷却至0℃,向其中小心地加入bh3的四氢呋喃溶液(1.0m,46.4ml)。将混合物在0℃下搅拌1.5小时,然后倒入冰水中并用乙酸乙酯萃取。将有机层用盐水(50ml)洗涤,经无水硫酸钠干燥,并在减压下浓缩,得到标题化合物(8.50g,91%产率),为白色固体。1h-nmr(500mhz,cdcl3)δ3.94(dd,j=4.9,2.7hz,2h),3.60(ddd,j=18.7,11.9,9.3hz,2h),3.49–3.37(m,1h),3.34–3.23(m,1h),2.06–1.91(m,1h),1.89–1.69(m,2h),1.65–1.51(m,1h),1.49–.40(m,9h)。 实施例78.(s)-2-甲酰基吡咯烷-1-羧酸叔丁酯的合成。 向(s)-2-(羟甲基)吡咯烷-1-羧酸叔丁酯(13.0g,64.6mmol)的二甲基亚砜(90ml)的溶液中加入三乙胺(40ml),搅拌15分钟。将混合物在冰浴上冷却,并在40分钟内分批加入三氧化硫-吡啶络合物(35.98g,226mmol)。将反应升温至室温并搅拌2.5小时。加入冰(250g)后,将混合物用二氯甲烷(150ml×3)萃取。将有机相用50%柠檬酸溶液(150ml),水(150ml),饱和碳酸氢钠溶液(150ml)和盐水(150ml)洗涤,经无水硫酸钠干燥。在真空中除去溶剂,得到标题醛(10.4g,81%产率),为稠油状物,不经进一步纯化而使用。1h-nmr(500mhz,cdcl3)δ9.45(s,1h),4.04(s,1h),3.53(dd,j=14.4,8.0hz,2h),2.00–1.82(m,4h),1.44(d,j=22.6hz,9h)。 实施例79.(4r,5s)-4-甲基-5-苯基-3-丙酰基恶唑烷-2-酮的合成。 在-78℃,n2条件下,向正丁基锂的正己烷(21.6ml,2.2m,47.43mmol)溶液中滴加4-甲基-5-苯基恶唑烷-2-酮(8.0g,45.17mmol)的四氢呋喃(100ml)溶液。将溶液在-78℃保持1小时,然后缓慢加入丙酰氯(4.4ml,50.59mmol)。将反应混合物升温至-50℃,搅拌2小时,然后用饱和氯化铵溶液(100ml)淬灭。真空除去有机溶剂,用乙酸乙酯(3×100ml)萃取水溶液。用饱和碳酸氢钠溶液(100ml)和盐水(100ml)洗涤有机相,无水硫酸钠干燥,过滤并减压浓缩。通过柱层析(20%乙酸乙酯/正己烷)纯化残余物,得到标题化合物,为稠油状物(10.5g,98%产率)。1h-nmr(500mhz,cdcl3)δ7.45–7.34(m,3h),7.30(d,j=7.0hz,2h),5.67(d,j=7.3hz,1h),4.82–4.70(m,1h),2.97(dd,j=19.0,7.4hz,2h),1.19(t,j=7.4hz,3h),0.90(d,j=6.6hz,3h)。 实施例80.(s)-2-((1r,2r)-1-羟基-2-甲基-3-((4r,5s)-4-甲基-2-氧代-5-苯基恶唑烷-3-基))-3-氧代丙基)吡咯烷-1-羧酸叔丁基酯的合成。 在0℃下,向(4r,5s)-4-甲基-5-苯基-3-丙酰基恶唑烷-2-酮(9.40g,40.4mmol)的二氯甲烷(60ml)溶液中加入三乙胺(6.45ml,46.64mmol),然后加入1m二丁基硼三氟甲磺酸酯的二氯甲烷(42ml,42mmol)溶液。将混合物在0℃下搅拌45分钟,冷却至-70℃,然后在30分钟内缓慢加入(s)-2-甲酰基吡咯烷-1-羧酸叔丁酯(4.58g,22.97mmol)的二氯甲烷(40ml)溶液。将反应混合物在-70℃下搅拌2小时,0℃下搅拌1小时,室温下搅拌15分钟,然后用磷酸盐缓冲溶液(ph7,38ml)淬灭。在低于10℃下加入甲醇-30%h2o2溶液(2:1,100ml),搅拌20分钟后,加入水(100ml)并将混合物减压浓缩。向残余物中加入更多的水(200ml),用乙酸乙酯(3×100ml)萃取混合物。用1nkhso4(100ml),碳酸氢钠溶液(100ml)和盐水(100ml)洗涤有机相,用无水硫酸钠干燥并减压浓缩。通过快速柱层析(10%-50%乙酸乙酯/正己烷)纯化残余物,得到标题化合物,为白色固体(7.10g,71%产率).1h-nmr(500mhz,cdcl3)δ7.39(dt,j=23.4,7.1hz,3h),7.30(d,j=7.5hz,2h),5.67(d,j=7.1hz,1h),4.84–4.67(m,1h),4.08–3.93(m,3h),3.92–3.84(m,1h),3.50(d,j=9.0hz,1h),3.24(d,j=6.7hz,1h),2.15(s,1h),1.89(dd,j=22.4,14.8hz,3h),1.48(d,j=21.5hz,9h),1.33(d,j=6.9hz,3h),0.88(d,j=6.4hz,3h)。 实施例81.(s)-2-((1r,2r)-1-甲氧基-2-甲基-3-((4r,5s)-4-甲基-2-氧代-5-苯基恶唑烷-3-基)的合成)-3-氧代丙基)吡咯烷-1-羧酸叔丁酯。 在n2中,向(s)-2-((1r,2r)-1-羟基-2-甲基-3-((4r,5s)-4-甲基-2-氧代-5-苯基恶唑烷-3-基)-3-氧代丙基)吡咯烷-1-羧酸叔丁基酯(5.1g,11.9mmol)和分子筛(5g)的混合物中加入无水二氯乙烷(30ml)。将混合物在室温下搅拌20分钟并冷却至0℃,加入质子海绵(6.62g,30.9mmol),然后加入三甲基氧鎓四氟硼酸盐(4.40g,29.7mmol)。在0℃下继续搅拌2小时,在室温下搅拌48小时。过滤反应混合物,浓缩滤液,并通过柱层析(20-70%乙酸乙酯/正己烷)纯化,得到标题化合物,为白色固体(1.80g,35%产率)。1h-nmr(500mhz,cdcl3)δ7.46–7.27(m,5h),5.65(s,1h),4.69(s,1h),3.92(s,1h),3.83(s,1h),3.48(s,3h),3.17(s,2h),2.02–1.68(m,5h),1.48(d,j=22.3hz,9h),1.32(t,j=6.0hz,3h),0.91–0.84(m,3h)。 实施例82.(2r,3r)-3-((s)-1-(叔丁氧基羰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸的合成。 在0℃下,在5分钟内向(s)-2-((1r,2r)-1-甲氧基-2-甲基-3-((4r,5s)-4-甲基-2-氧代-5-苯基恶唑烷-3-基)-3-氧代丙基)吡咯烷-1-甲酸-(3)-氧代丙基)吡咯烷-1-羧酸叔丁酯(1.80g,4.03mmol)的四氢呋喃(30ml)和水(7.5ml)溶液中加入30%h2o2(1.44ml,14.4mmol)。然后加入lioh(0.27g,6.45mmol)的水溶液(5ml)。在0℃下搅拌3小时后,加入1n亚硫酸钠(15.7ml)并将混合物升温至室温且搅拌过夜。真空除去四氢呋喃,水相用二氯甲烷(3×50ml)洗涤,除去恶唑烷酮助剂。用1n盐酸将水相酸化至ph3并用乙酸乙酯(3×50ml)萃取。用盐水(50ml)洗涤有机层,用无水硫酸钠干燥,过滤并减压浓缩,得到标题化合物,为无色油状物(1.15g,98%产率)。1h-nmr(500mhz,cdcl3)δ3.99–3.74(m,2h),3.44(d,j=2.6hz,3h),3.23(s,1h),2.60–2.45(m,1h),1.92(tt,j=56.0,31.5hz,3h),1.79–1.69(m,1h),1.58–1.39(m,9h),1.30–1.24(m,3h)。 实施例83.(2r,3r)-3-甲氧基-2-甲基-3-((s)-吡咯烷-2-基)丙酸甲酯的合成。 在0℃下,向(2r,3r)-3-((s)-1-(叔丁氧基羰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸(0.86g,2.99mmol)的甲醇(10ml)溶液中缓慢加入氯化亚砜(1.08ml,14.95mmol)。将反应升温至室温并搅拌过夜。将混合物减压浓缩,与甲苯共浓缩,得到标题化合物(0.71g,100%产率),为白色固体,无需进一步纯化即可用于下一步。hrms(esi)m/z:c10h20no3[m+h]+计算值202.14,实测值202.14。 实施例84.(4s,5s)-4-((叔丁氧基羰基)氨基)-5-甲基-3-氧代庚酸乙酯的合成。 向用冰冷却的n-boc-l-异亮氨酸(4.55g,19.67mmol)的四氢呋喃(20ml)溶液中加入1,1’-羰基二咪唑(3.51g,21.63mmol)。待气体停止产生后,将所得混合物升温至室温,搅拌3.5小时。 5℃下,向新制备的异丙基溴化镁的四氢呋喃(123mmol,30ml)溶液中滴加预冷至(0℃)的丙二酸单乙酯(6.50g,49.2mmol)溶液。然后将混合物在室温下搅拌1.5小时。将该烯醇镁溶液在冰水浴上冷却,并在1小时内通过双头针向其中加入咪唑化物溶液。将所得混合物在0℃下搅拌30分钟,然后在室温下搅拌64小时。通过加入10%柠檬酸水溶液(5ml)淬灭反应,并用另外的10%柠檬酸水溶液(110ml)酸化至ph3。用乙酸乙酯(3×150ml)萃取混合物。将有机萃取液用水(50ml),饱和碳酸氢钠水溶液(50ml)和饱和氯化钠水溶液(50ml)洗涤,用无水硫酸钠干燥,并减压浓缩。残留物通过硅胶柱层析纯化,用乙酸乙酯/正己烷(1:4)作为洗脱液,得到标题化合物(5.50g,93%产率)。1h-nmr(500mhz,cdcl3)δ5.04(d,j=7.8hz,1h),4.20(p,j=7.0hz,3h),3.52(t,j=10.7hz,2h),1.96(d,j=3.7hz,1h),1.69(s,2h),1.44(s,9h),1.28(dd,j=7.1,2.9hz,3h),0.98(t,j=6.9hz,3h),0.92–0.86(m,3h)。 实施例85.(3r,4s,5s)-4-((叔丁氧基羰基)氨基)-3-羟基-5-甲基庚酸乙酯的合成。 在-60℃下向(4s,5s)-4-((叔丁氧基羰基)氨基)-5-甲基-3-氧代庚酸乙酯(5.90g,19.83mmol)的乙醇(6ml)溶液中一次性加入硼氢化钠(3.77g,99.2mmol)。将反应混合物在-55℃下搅拌5.5小时,然后用10%柠檬酸水溶液(100ml)淬灭。用另外的10%柠檬酸水溶液将所得溶液酸化至ph2,然后用乙酸乙酯(3×100ml)萃取。用饱和氯化钠水溶液(100ml)洗涤有机物,用无水硫酸钠干燥,并减压浓缩。通过柱层析(10-50%乙酸乙酯/正己烷)纯化残余物,得到标题化合物,为非对映异构体(2.20g,37%产率)和两种非对映异构体的混合物(2.0g,34%产率,约9:1比率)。1h-nmr(500mhz,cdcl3)δ4.41(d,j=9.3hz,1h),4.17(tt,j=7.1,3.6hz,2h),4.00(t,j=6.9hz,1h),3.55(dd,j=11.7,9.3hz,1h),2.56–2.51(m,2h),2.44(dd,j=16.4,9.0hz,1h),1.79(d,j=3.8hz,1h),1.60–1.53(m,1h),1.43(s,9h),1.27(dd,j=9.3,5.0hz,3h),1.03–0.91(m,7h)。 实施例86.(3r,4s,5s)-4-((叔丁氧基羰基)氨基)-3-羟基-5-甲基庚酸的合成。 向(3r,4s,5s)-4-((叔丁氧基羰基)氨基)-3-羟基-5-甲基庚酸乙酯(2.20g,7.20mmol)的乙醇(22ml)溶液中加入1n氢氧化钠(7.57ml,7.57mmol)。将混合物在0℃下搅拌30分钟,然后在室温下搅拌2小时,通过加入1n盐酸水溶液将所得溶液酸化至ph4,然后用乙酸乙酯(3×50ml)萃取。将有机萃取液用1n硫酸氢钾水溶液(50ml)和饱和氯化钠水溶液(50ml)洗涤,用无水硫酸钠干燥,并减压浓缩,得到化合物(1.90g,95%产率)。1h-nmr(500mhz,cdcl3)δ4.50(d,j=8.7hz,1h),4.07(d,j=5.5hz,1h),3.59(d,j=8.3hz,1h),2.56–2.45(m,2h),1.76–1.65(m,1h),1.56(d,j=7.1hz,1h),1.45(s,9h),1.26(t,j=7.1hz,3h),0.93(dd,j=14.4,7.1hz,6h)。 实施例87.(3r,4s,5s)-4-(((叔丁氧羰基)(甲基)氨基)-3-甲氧基-5-甲基庚酸的合成。 向(3r,4s,5s)-4-((叔丁氧基羰基)氨基)-3-羟基-5-甲基庚酸(1.90g,6.9mmol)的四氢呋喃(40ml)溶液中加入氢化钠(在0℃下,60%矿物油中,1.93g,48.3mmol)。搅拌1小时后,加入碘甲烷(6.6ml,103.5mmol)。在0℃下继续搅拌40小时,然后加入饱和碳酸氢钠水溶液(50ml)淬灭反应,接着加入水(100ml)。将混合物用乙醚(2×50ml)洗涤,并将水层用1n硫酸氢钾水溶液酸化至ph3,然后用乙酸乙酯(3×50ml)萃取。将合并的有机萃取液用5%硫代硫酸钠水溶液(50ml)和饱和氯化钠水溶液(50ml)洗涤,用无水硫酸钠干燥,减压浓缩,得到标题化合物(1.00g,48%产率)。1h-nmr(500mhz,cdcl3)δ3.95(d,j=75.4hz,2h),3.42(d,j=4.4hz,3h),2.71(s,3h),2.62(s,1h),2.56–2.47(m,2h),1.79(s,1h),1.47(s,1h),1.45(d,j=3.3hz,9h),1.13–1.05(m,1h),0.96(d,j=6.7hz,3h),0.89(td,j=7.2,2.5hz,3h)。 实施例88.boc-n-me-l-val-oh的合成。 在0℃下,向boc-l-缬氨酸-oh(2.00克,9.2mmol)和碘甲烷(5.74ml,92mmol)的无水四氢呋喃(40ml)溶液中加入氢化钠(3.68克,92mmol)。将反应混合物在0℃下搅拌1.5小时,然后升温至室温并搅拌24小时。用冰水(50ml)淬灭反应,加入水(100ml)后,将反应混合物用乙酸乙酯(3×50ml)洗涤,将水溶液酸化至ph3,然后用乙酸乙酯(3×50ml)萃取。将合并的有机相用无水硫酸钠干燥并浓缩,得到白色固体boc-n-me-val-oh(2.00g,94%产量)。1h-nmr(500mhz,cdcl3)δ4.10(d,j=10.0hz,1h),2.87(s,3h),2.37–2.13(m,1h),1.44(d,j=26.7hz,9h),1.02(d,j=6.5hz,3h),0.90(t,j=8.6hz,3h)。 实施例89.(2r,3r)-3-((s)-1-((3r,4s,5s)-4-((叔丁氧羰基)-(甲基)氨基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸甲酯的合成。 在0℃下,向(2r,3r)-3-甲氧基-2-甲基-3-((s)-吡咯烷-2-基)丙酸甲酯(0.71g,2.99mmol)和(3r,4s,5s)-4-((叔丁氧基羰基)(甲基)氨基)-3-甲氧基-5-甲基庚酸(1g,3.29mmol)的dmf(10ml)溶液中加入氰基膦酸二乙酯(545μl,3.59mmol),然后加入三乙胺(1.25ml,8.99mmol)。将反应混合物在0℃下搅拌2小时,然后升温至室温并搅拌过夜。反应混合物用乙酸乙酯(50ml)稀释,用1n硫酸氢钾水溶液(20ml),水(20ml),饱和碳酸氢钠水溶液(20ml)和饱和氯化钠水溶液(20ml)洗涤,用硫酸钠干燥,并减压浓缩。将残余物在硅胶柱色谱上纯化,用乙酸乙酯/正己烷(1:5至2:1)洗脱,得到标题化合物(0.9g,62%产率),为白色固体。hrms(esi)m/z:c25h46n2o7[m+h]+计算值487.33,实测值487.32。 实施例90.(s)-2-((1r,2r)-1-甲氧基-3-(((s)-1-甲氧基-1-氧代-3-苯基丙-2-基)氨基)-2-甲基-3-氧代丙基)吡咯烷-1-羧酸叔丁酯的合成。 在0℃下,向(2r,3r)-3-((s)-1-(叔丁氧基羰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸(100mg,0.347mmol)和l-苯丙氨酸甲酯盐酸盐(107.8mg,0.500mmol)的dmf(5ml)溶液中加入氰基膦酸二乙酯(75.6μl,0.451mmol),然后加入三乙胺(131μl,0.94mmol)。将反应混合物在0℃下搅拌2小时,然后升温至室温并搅拌过夜。然后将反应混合物用乙酸乙酯(80ml)稀释,用1n硫酸氢钾水溶液(40ml),水(40ml),饱和碳酸氢钠水溶液(40ml)和饱和氯化钠水溶液(40)洗涤。用无水硫酸钠干燥,减压浓缩。通过柱层析(15-75%乙酸乙酯/正己烷)纯化残余物,得到标题化合物(130mg,83%产率),为白色固体。1h-nmr(500mhz,cdcl3)δ7.28(dd,j=7.9,6.5hz,2h),7.23(t,j=7.3hz,1h),7.16(s,2h),4.81(s,1h),3.98–3.56(m,5h),3.50(s,1h),3.37(d,j=2.9hz,3h),3.17(dd,j=13.9,5.4hz,2h),3.04(dd,j=14.0,7.7hz,1h),2.34(s,1h),1.81–1.69(m,2h),1.65(s,3h),1.51–1.40(m,9h),1.16(d,j=7.0hz,3h)。 实施例91.用三氟乙酸去除boc官能团的一般操作。 向n-boc-氨基酸(1.0mmol)的二氯甲烷(2.5ml)的溶液中加入三氟乙酸(1.0ml)。在室温下搅拌1-3小时后,反应混合物在真空中浓缩。与甲苯共蒸发得到脱保护产物,未经进一步纯化即可使用。 实施例92.(2r,3r)-甲基3-((s)-1-((3r,4s,5s)-4-((s)-2-((叔丁氧羰基)氨基)-n,3-二甲基丁胺基)-3-甲氧基-5-甲基庚烷酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸酯的合成。 在0℃下,向(2r,3r)-3-甲氧基-3-((s)-1-((3r,4s,5s)-3-甲氧基-5-甲基-4-(甲氨基)庚酰基)吡咯烷-2-基)甲酯-2-甲基丙酸甲酯(715mg,1.85mmol)去boc保护产物和boc-val-oh(1.2g,5.56mmol)的二氯甲烷(20ml)溶液中加入brop(1.08g,2.78mmol)),然后加入二异丙基乙胺(1.13ml,6.48mmol)。将混合物在暗处,0℃下搅拌30分钟,然后在室温下搅拌48小时。反应混合物用乙酸乙酯(50ml)稀释,用1n硫酸氢钾水溶液(20ml),水(20ml),饱和碳酸氢钠水溶液(20ml)和饱和氯化钠水溶液(20ml))洗涤,用硫酸钠干燥,并减压浓缩。将残余物在硅胶柱上纯化,用乙酸乙酯/正己烷(1:5至4:1)洗脱,得到标题化合物(0.92g,85%产率),为白色固体。hrms(esi)m/z:c30h55n3o8[m+h]+计算值586.40,实测值586.37。 实施例93.(2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丁酰胺)-3-甲氧基-5-甲基庚基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸甲酯。 在0℃时,向(2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((叔丁氧基羰基)氨基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸甲酯(50mg,0.085mmol)的去boc保护产物和五氟苯基2-(二甲基氨基)-2-甲基丙酸酯(74.5mg,0.25mmol)的dmf(2ml)溶液中加入dipea(44μl,0.255mmol)。将反应混合物升温至室温并搅拌2小时,然后用乙酸乙酯(30ml)稀释,用水(10ml)和饱和氯化钠水溶液(10ml)洗涤,经硫酸钠干燥,并减压浓缩。将残余物在硅胶柱上纯化,用乙酸乙酯/正己烷(1:5至5:1)洗脱,得到标题化合物(50mg,100%产率)。hrms(esi)m/z:c31h58n4o7[m+h]+计算值599,实测值599。 实施例94.(2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丁胺基)-3-甲氧基-5-甲基庚烷酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸的合成。 在0-4℃下,向(2r,3r)-甲基3-((s)-1-((3r,4s,5s)-4-((s)-2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丁胺基)-3-甲氧基-5-甲基庚烷酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸酯(50mg,0.0836mmol)的1,4-二氧六环(3ml)溶液,逐滴加入氢氧化锂(14mg,0.334mmol)的水溶液(3ml)。将反应混合物升温至室温,搅拌2小时,用1nhcl酸化至ph7,真空浓缩,无需进一步纯化,直接用于下一步。hrms(esi)m/zc30h57n4o7[m+h]+计算值:585.41,实测值:585.80。 实施例95.(2r,3r)-五氟苯基3-((s)-1-((3r,4s,5s)-4-((s)-2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丁胺基)-3-甲氧基-5-甲基庚烷酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸酯的合成。 在0℃时,向(2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丁酰胺)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸(0.0836mmol)和五氟苯酚(18.5mg,0.1mmol)的二氯甲烷(2ml)溶液中加入dic(12.7mg,0.1mmol)。将混合物升温至室温并搅拌过夜。将反应混合物减压浓缩,不经进一步纯化即用于下一步。hrms(esi)m/z:c36h56f5n4o7[m+h]+计算值751.40,实测值751.70。 实施例96.(s)-2-((叔丁氧羰基)氨基)-3-(4-羟基-3-硝基苯)丙酸甲酯的合成。 向boc-l-酪氨酸甲酯(5g,16.9mmol)的四氢呋喃(50ml)溶液中加入亚硝酸叔丁酯(10ml,84.6mmol),然后将反应混合物在室温下搅拌5小时。浓缩反应混合物,并通过硅胶柱纯化,用乙酸乙酯/正己烷(1:10至1:5)洗脱,得到化合物(4.5g,78%产率),为黄色固体。hrms(esi)m/z:c15h21n2o7[m+h]+计算值341.13,实测值341.30。 实施例97.3-(3-氨基-4-羟基苯基)-2-(叔丁氧羰基)氨基)丙酸甲酯的合成。 向(s)-3-(3-氨基-4-羟基苯基)-2-(叔丁氧基羰基氨基)丙酸甲酯(2g,6.44mmol)的乙酸乙酯(20ml)溶液中加入pd/c(0.2g),在氢气环境下搅拌2小时。过滤混合物,减压浓缩滤液,得到标题化合物(1.7g,95%产率),为白色固体。hrms(esi)m/z:c15h23n2o5[m+h]+计算值311.15,实测值311.30。 实施例98.(2s)-甲基3-(8,9-双(3-(2,5-二氧基-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15-四氧基-3,4,5,6,7,8,9,10,11,12,13,14,15,16-十四氢-2h-苯并[b][1,4,9,14]氧杂三氮杂环十八烷-18-基)-2-((叔丁氧羰基)氨基)丙酸酯的合成。 于0℃下向4,4’-((2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰胺基)-琥珀酰)双(氮杂二酰基))二丁酸(108.0mg,0.182mmol)和(s)-3-(3-氨基-4-羟基苯基)-2-(叔丁氧基羰基氨基)丙酸甲酯(56.6mg,0.182mmol)的dmf(5ml)溶液中加入edc(130mg,0.678mmol),随后加入dipea(64μl,0.365mmol)。将反应混合物升温至室温并搅拌过夜。将混合物用乙酸乙酯(30ml)稀释,用水(10ml)和饱和氯化钠水溶液(10ml)洗涤,用硫酸钠干燥并真空浓缩。将残余物在硅胶柱色谱上纯化,用二氯甲烷/甲醇(20:1至10:1)洗脱,得到标题化合物(110.6mg,收率68%)。hrms(esi)m/zc41h51n8o15[m+h]+计算值:895.34,实测值:895.30。 实施例99.(2s)-2-氨基-3-(8,9-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15-四氧代-3,4,5,6,7,8,9,10,11,12,13,14,15,16-十四氢-2h-苯并[b][1,4,9,14]氧代三氮杂环十八烷-18-基)丙酸甲酯的合成。 在0℃,向(2s)甲基-3-(8,9-双(3-(3-(2,5,5-二氧代-2,5,5,5-二甲基-1-1-吡咯-1-基)丙炔基)-2,7,7,10,15,15-四氧代-3,5,6,7,8,9,10,11,12,13,14,15,15,16-十四氢-2h-苯并[b][1,4,9,9,14]氧代三氮杂环十八烷基-18-基)-2-((叔丁氧基羰基)氨基)氨基)丙酸酯(100.2mg,100.2mg,0.112mmol)的二氯甲烷(6ml)溶液中加入tfa(2ml)。将反应混合物升温至室温并搅拌30分钟,用甲苯稀释,浓缩,用甲苯共蒸发,然后无需进一步纯化即可用于下一步。hrms(esi)m/zc36h43n8o13[m+h]+计算值:795.29,实测值:795.45。 实施例100.(2s)-甲基3-(8,9-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15-四氧代-3,4,5,6,7,8,9,10,11,12,13,14,15,16-十四氢-2h-苯并[b][1,4,9,14]氧代三氮杂环十八烷-18-基)-2-(((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-(2-(甲基氨基)-(2-甲基丙酰胺基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)丙酸酯(a-01)的合成。 在0℃下,向(2r,3r)-五氟苯基3-((s)-1-((3r,4s,5s)-4-((s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酸酯(20mg,0.027mmol)和(2s)-2-氨基-3-甲基(8),9-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15-四氧代-3,4,5,6,7,8,9,10,11,12,13,14,15,16-十四氢-2h-苯并[b][1,4,9,14]氧杂三氮杂-环十八烷基-18-基)丙酸甲酯(31.7mg,0.04mmol)的dma(2ml)溶液中加入dipea(9μl,0.053mmol)。将反应混合物升温至室温并搅拌30分钟。将混合物真空浓缩并通过制备hplc纯化(c-18,250mm×10mm,用水/乙腈,9ml/分钟,40分钟内从90%调整到40%洗脱),得到标题化合物(16mg,收率43%)。hrms(esi)m/zc66h97n12o19[m+h]+计算值:1361.69实测值:1361.50。 实施例101.(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((叔丁氧基羰基)(甲基)氨基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯的合成。 在0℃下,向(s)-2-((1r,2r)-1-甲氧基-3-(((s)-1-甲氧基-1-氧代-3-苯基丙-2-基)氨基)-2-甲基-3-氧代丙基)吡咯烷-1-羧酸叔丁基酯(0.29mmol)和(3r,4s,5s)-4-((叔丁氧基羰基)(甲基)氨基)-3-甲氧基-5-甲基庚酸(96.6mg,0.318mmol)的dmf(5ml)溶液中加入氰基磷酸二乙酯(58μl,0.347mmol),然后加入et3n(109μl,0.78mmol)。将反应混合物在0℃下搅拌2小时,然后升温至室温并搅拌过夜。将反应混合物用乙酸乙酯(80ml)稀释,用1n硫酸氢钾水溶液(40ml),水(40ml),饱和碳酸氢钠水溶液(40ml)和饱和氯化钠水溶液(40ml)洗涤,用硫酸钠干燥并真空浓缩。通过柱色谱法(15-75%乙酸乙酯/正己烷)纯化残余物,得到标题化合物(150mg,81%收率),为白色固体。lc-ms(esi)m/zc34h55n3o8[m+h]+计算值:634.40,实测值:634.40。 实施例102.(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((叔丁氧基羰基)氨基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯的合成。 在0℃下,向(s)-甲基2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((叔丁氧羰基)(甲基)氨基)-3-甲氧基-5-甲基庚酰基)-吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸酯(0.118mmol)和boc-val-oh(51.8mg,0.236mmol)的dcm(5ml)溶液中加入brop(70.1mg,0.184mmol),然后加入二异丙基乙胺(70μl,0.425mmol)。将混合物避光,并在0℃下搅拌30分钟,然后在室温下搅拌2天。将反应混合物用乙酸乙酯(80ml)稀释,用1n硫酸氢钾水溶液(40ml),水(40ml),饱和碳酸氢钠水溶液(40ml)和饱和氯化钠水溶液(40ml)洗涤。用硫酸钠干燥并真空浓缩,残余物通过柱色谱法纯化(20-100%乙酸乙酯/正己烷),得到标题化合物(67mg,收率77%),为白色固体。lc-ms(esi)m/zc39h64n4o9[m+h]+计算值:733.47,实测值:733.46。 实施例103.(s)-2-((2r,3r)-3-((s)-1-((6s,9s,12s,13r)-12-((s)-仲丁基)-6,9-二异丙基-13-甲氧基-2,2,5,11-四甲基-4,7,10-三氧代-3-氧杂-5,8,11-三氮杂十五烷-15-基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯的合成。 在0℃下,向(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((叔丁氧基羰基)氨基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯(0.091mmol)的boc-脱保护产物和boc-n-me-val-oh(127mg,0.548mmol)的dmf(5ml)溶液中加入氰基磷酸二乙酯(18.2μl,0.114mmol),然后加入n-甲基吗啉(59μl,0.548mmol)。将反应混合物在0℃下搅拌2小时,然后升温至室温并搅拌过夜。将反应混合物用乙酸乙酯(80ml)稀释,用1n硫酸氢钾水溶液(40ml),水(40ml),饱和碳酸氢钠水溶液(40ml)和饱和氯化钠水溶液洗涤。用硫酸钠干燥,真空浓缩。通过柱色谱法(20-100%乙酸乙酯/己烷)纯化残余物,得到标题化合物(30mg,收率39%),为白色固体。lc-ms(esi)m/zc45h75n5o10[m+h]+计算值:846.55,实测值:846.56。 实施例104.(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-n,3-二甲基-2-((s)-3-甲基-2-(甲基氨基)丁酰胺基)丁酰胺基)-3-甲氧基-5-甲基-庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯的合成。 向(s)-甲基2-((2r,3r)-3-((s)-1-((6s,9s,12s,13r)-12-((s)-仲丁基)-6,9-二异丙基-13-甲氧基-2,2,5,11-四甲基-4,7,10-三氧代-3-氧杂-5,8,11-三氮杂十五烷-15-酰)吡咯烷-2-基)-3-甲氧基-2-甲基丙氨酰基)-3-苯基丙酸甲酯(75.0mg,0.0886mmol)的二氯甲烷(5ml)溶液中加入三氟乙酸(2ml),在室温下搅拌1小时后,真空浓缩反应混合物。与甲苯共蒸发得到脱保护的标题产物,无需进一步纯化即可使用。 实施例105.(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-n,3-二甲基-2-((s)-3-甲基-2-(甲基氨基)丁酰胺基)丁酰胺基)-3-甲氧基-5-甲基庚酰基)-吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸的合成。 将(s)-甲基2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-n,3-二甲基-2-((s)-3-甲基-2-(甲基氨基)丁酰胺基)丁酰胺基)-3-甲氧基-5-甲基-庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸酯(25mg,0.030mmol)的浓盐酸(0.3ml)和1,4-二氧六环(0.9ml)的溶液,在室温下搅拌35分钟。将混合物用etoh(1.0ml)和甲苯(1.0ml)稀释,浓缩并与etoh/甲苯共蒸发(2:1),得到标题化合物,为白色固体(22mg,收率约100%),其不经进一步纯化即用于下一步。lc-ms(esi)m/zc39h66n5o8[m+h]+计算值:732.48,实测值:732.60。 实施例106.(2s)-2-((2r,3r)-3-((2s)-1-((11s,14s,17s)-1-叠氮基-17-((r)-仲丁基)-11,14-二异丙基-18-甲氧基-10,16-二甲基-9,12,15-三氧代-3,6-二氧杂-10,13,16-三氮杂二十烷-20-酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸的合成。 向(s)-2-((2r,3r)-3-((s)-1-((3r,4s,4s,5)-4-((s)-n,3-二甲基-2-((s)-3-甲基-2-(甲基氨基)丁酰胺基)丁酰氨基)-3-甲氧基-5-甲基庚酰基基)-吡咯烷基-2-基-3-甲氧基-2-甲基丙甲酰氨基)-3-甲氧基-3-甲氧基-3-甲基丙酰胺基)-3-苯基丙酸(22mg,0.030毫摩尔)粗品在dma(0.8ml)和nah2po4缓冲溶液(ph7.5,1.0m,0.7ml)中,在2小时内分四次加入2,5-二氧代吡咯烷-1-基3-(2-(2-叠氮基乙氧基)丙酸酯(18.0mg,0.060mmol),搅拌过夜,浓缩并用硅胶柱色谱法纯化(ch3oh/二氯甲烷/hoac1:8:0.01),得到标题化合物(22.5mg,82%收率)。lc-ms(esi)m/zc46h77n8o11[m+h]+计算值:917.56,实测值:917.60。 实施例107.(2s)-2-((2r,3r)-3-((2s)-1-((11s,14s,17s)-1-氨基-17-((r)-仲丁基)-11,14-二异丙基-18-甲氧基-10,16-二甲基-9,12,15-三氧基-3,6-二氧基-10,13,16-三氮杂二十烷-20-酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸的合成。 在氢化瓶中,向(2s)-2-((2r,3r)-3-((2s)-1-((11s,14s,17s)-1-叠氮基-17-((r)-叔丁基)-11,14-二异丙基-18-甲氧基-10,16-二甲基-9,12,15-三氧-3,6-氧代-3,6-二氧杂-10,13,16-三氮杂-20-基-20-基基)吡咯烷基-2-基)-3-甲氧基-2-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸(22.0mg,0.024mmol)的甲醇(5ml)溶液中,加入pd/c(5mg,10%pd,50%水)。抽真空并导入h2(25psi)后,将混合物振荡4小时,通过硅藻土过滤。浓缩滤液,得到粗标题产物(~20mg,收率92%),用于下一步,无需进一步纯化。esimsm/zc46h79n6o11(m+h)计算值:891.57,实测值:891.60。 实施例108.(s)-2-((2r,3r)-3-((s)-1-((6s,9s,12s,13r)-12-((s)-仲丁基)-6,9-二异丙基-13-甲氧基-2,2,5,11-四甲基-4,7,10-三氧代-3-氧杂-5,8,11-三氮杂十五碳-15-基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸。 向(s)-(2r,3r)-3-((s)-1-((6s,9s,12s,13r)-12-((s)-仲丁基)-(s)-6,9-二异丙基-13-甲氧基2,2,5,1-1四甲基-4,7,10-三氧代-3-氧杂-5,8,11-三氮杂十五烷-15酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯(30mg,0.035mmol)的四氢呋喃(1.0ml)溶液中加入lioh水溶液(1.0m,0.8ml)。将混合物在室温下搅拌35分钟,用0.5mh3po4调节ph至6,浓缩并在硅胶柱上纯化(甲醇/二氯甲烷/hoac1:10:0.01),得到标题化合物(25.0mg,85%产率)。lc-ms(esi)m/z:c44h74n5o10[m+h]+计算值832.54,实测值832.60。 实施例109.(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-n,3-二甲基-2-(s)-3-甲基-2-(甲基氨基)丁酰胺基)丁酰胺基)-3-甲氧基-5-甲基庚酰基)-吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸的合成。 向(s)-2-((2r,3r)-3-((s)-1-((6s,9s,12s,13r)-12-((s)-仲丁基)-6,9-二异丙基-13-甲氧基-2,2,5,11-四甲基-4,7,10-三氧代-3-氧杂-5,8,11-三氮杂十五烷-15-酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸(25mg,0.030mmol)的二恶烷(2.0ml)溶液中加入浓盐酸(12n,0.6ml)。将混合物在室温下搅拌30分钟,用二恶烷(4ml)和甲苯(4ml)稀释,浓缩并用c18hplc纯化,用甲醇和水洗脱(l200mm×φ20mm,9ml/min,40分钟从5%甲醇至40%甲醇),得到标题化合物(20.0mg,90%产率)。lc-ms(esi)m/z:c39h66n5o8[m+h]+计算值732.48,实测值732.90。 实施例110.(s)-2-((2r,3r)-3-((s)-1-((5s,8s,11s,14s,15r)-14-((s)-仲丁基)-8,11-二异丙基-15-甲氧基-5,7,13三甲基-3,6,9,12-四氧代-1-苯基-2-氧杂-4,7,10,13-四氮杂十七烷-17-酰基)吡咯烷吡啶-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯的合成。 在0℃下,依次向mmaf-ome(0.132g,0.178mmol,1.0eq.)和z-l-丙氨酸(0.119g,0.533mmol,3.0eq.)的无水二氯甲烷(10ml)溶液中加入hatu(0.135g,0.356mmol,2.0eq.)和nmm(0.12ml,1.07mmol,6.0eq.)。将反应物在0℃下搅拌10分钟,然后升温至室温并搅拌过夜。将混合物用二氯甲烷稀释,用水和盐水洗涤,经无水硫酸钠干燥,浓缩,并通过硅胶柱色谱(20:1二氯甲烷/甲醇)纯化,得到标题化合物,为白色泡沫状固体(0.148g,88%产率)。esimsm/z:c51h79n6o11[m+h]+计算值951.6,实测值951.6。 实施例111.(s)-2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-((s)-2-氨基-n-甲基丙酰胺基)-3-甲基丁酰胺基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基庚基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯的合成。 在氢化反应瓶中,将pd/c(0.100g,10%pd/c,含水50%)加入到(s)-2-((2r,3r)-3-((s)-1-((5s,8s,11s,14s,15r)-14-((s)-仲丁基)-8,11-二异丙基-15-甲氧基-5,7,13三甲基-3,6,9,12-四氧代-1-苯基-2-氧杂-4,7,10,13-四氮杂十七烷-17-酰基)吡咯烷吡啶-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯(0.148g,0.156mmol,1.0eq.)的甲醇(5ml)溶液中。将混合物在氢气中振荡5小时,然后通过硅藻土垫过滤。浓缩滤液,得到标题化合物,为白色泡沫状固体(0.122g,96%产率)。esimsm/z:c43h73n6o9[m+h]+计算值817.5,实测值817.5。 实施例112.(2s)-2-(((2r,3r)-3-((2s)-1-((46s,49s,52s,55s,56r)-55-((s)-仲-丁基)-37,38-双(2-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)乙酰氨基)-1-羟基-49,52-二异丙基-56-甲氧基-46,48,54-三甲基-31,36,39,44,47,50,53-七氧代-3,6,9,12,15,18,21,24,27-九氧杂-30,35,40,45,48,51,54-七氮杂五十八烷-58-酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸甲酯(a-02)。 (a-2) 和(副产物) 向(s)-甲基2-((2r,3r)-3-((s)-1-((3r,4s,5s)-4-((s)-2-((s)-2-((s)-2-氨基-n-甲基丙酰胺基)-3-甲基丁酰胺基)-n,3-二甲基丁酰胺基)-3-甲氧基-5-甲基-庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸酯(0.122g,0.149mmol,1.0eq)和4,4′-((2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯)-1-基乙酰胺基)-琥珀酰基)双(氮杂二基)二丁酸(0.177g,0.298mmol,4.0eq)的无水dma(10ml)溶液中加入hatu(0.270g,0.712mmol)和nmm(0.030ml,0.267mmol)。将反应搅拌2小时,然后加入29-氨基-3,6,9,12,15,18,21,24,27-九氧杂烷-1-醇(0.205mg,0.448mmol)。将反应混合物继续搅拌过夜,然后真空浓缩并通过硅胶柱色谱(10:1至5:1,二氯甲烷/甲醇)纯化,得到标题化合物(a-2),为白色泡沫状固体(0.128g,47%收率,esimsm/z:c87h140n13o29[m+h]+计算值1830.98,实测值1830.70)和副产物2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-n1,n4-双(1-羟基-31-氧代-3,6,9,12,15,18,21,24,27-九氧杂-30-氮杂三十四烷-34-基)琥珀酰胺(84mg,收率38%),esimsm/z:c64h111n8o30[m+h]+计算值:1471.73,实测值:1471.95)。 实施例113.(2s)-2-(((2r,3r)-3-((2s)-1-((56s,59s,62s,63r)-62-((s)-仲丁基)-37,38-双(2-(2-,2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-1-羟基-56,59-二异丙基-63-甲氧基-55,61-二甲基-31,36,39,44,54,57,60-七氧代-3,6,9,12,15,18,21,24,27,48,51-十一烷-30,35,40,45,55,58,61-七氮杂六十五烷-65-酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸(a-3)的合成。 向(2s)-2-(((2r,3r)-3-((2s)-1-((11s,14s,17s)-1-氨基-17-((r)-仲丁基)-11,14-二异丙基-18-甲氧基-10,16-二甲基-9,12,15-三氧-3,6-二氧杂-10,13,16-三氮杂-20-酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸(0.155g,0.174mmol,1.0eq)的dma(10ml)和pbs缓冲液(10ml,0.1mnah2po4,ph5.0)的混合溶液中,加入双(2,5-二氧杂吡咯烷-1-基)4,4′-(((2,3-双(2-(2,5-二氧杂-2,5-二氢-1h-吡咯-1-基)乙酰氨基)琥珀酰基)双(氮杂二氮杂)二丁酸酯(0.275g,0.349mmol,4.0eq)。将混合物搅拌4小时,然后加入29-氨基-3,6,9,12,15,18,21,24,27-壬氧杂环戊烷-1-醇(0.205mg,0.448mmol)。用饱和碳酸氢钠溶液将反应混合物调节至ph7.5并继续搅拌过夜。将混合物真空浓缩并通过反相hplc(250mm×20mm,c18柱,10-80%乙腈/水,40分钟,v=10ml/min)纯化,得到标题化合物(142.1mg,收率43%),esimsm/z:calcdforc90h146n13o31[m+h]+计算值:1905.02,实测值:1905.80)和副产物2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-n1,n4-双(1-羟基-31-氧代-3,6,9,12,15,18,21,24,27-九氧杂-30-氮杂三十四烷-34-基)琥珀酰胺(89mg,收率35%),esimsm/z:c64h111n8o30[m+h]+计算值:1471.73,实测值:1471.95。 实施例114.(2s,2’s)-2,2′-((((2r,2’r,3r,3’r)-3,3′-((2s,2’s)-1,1′-((3r,4s,7s,10s,47s,50s,53s,54r)-4,53-二((s)-仲丁基)-28,29-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-7,10,47,50-四异丙基-3,54-二甲氧基-5,11,46,52-四甲基-6,9,12,22,27,30,35,45,48,51-十氧杂-15,18,39,42-四氧杂-5,8,11,21,26,31,36,46,49,52-十氮杂五十六烷-1,56-二芳基双(吡咯烷-2,1-二基)双(3-甲氧基-2-甲基丙酰基)双(氮杂二基)双(3-苯基丙酸)(a-04)的合成。 向(2s)-2-((2r,3r)-3-((2s)-1-((11s,14s,17s)-1-氨基-17-((r)-仲丁基)-11,14-二异丙基-18-甲氧基-10,16-二甲氧基-9,12,15-三氧基-3,6-二氧代-10,13,16-三氮杂-20-甲氧基-2-基吡啶-2-基)-3-甲氧基-2-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸(0.155g,0.174mmol,0.1eq)的dma(10ml)和pbs缓冲液(10ml,0.1mnah2po4,ph7.5)的混合溶液中,加入双(2,5-二氧代吡咯烷-1-基)4,4′-(2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰胺基)琥珀酰基)双(氮杂二基))二丁酸酯(0.068g,0.087mmol,1.0eq)。将混合物搅拌8小时,真空浓缩并通过反相hplc(250mm×20mm,c18柱,10-80%乙腈/水,40分钟,v=10ml/min)纯化,得到标题化合物(138.1mg,收率68%)。esimsm/z:c116h181n18o32[m+h]+计算值:2338.30,实测值:2338.90。 实施例115.(s,e)-2-甲基-n-(3-甲基丁-2-亚基)丙烷-2-磺酰胺的合成。 在n2保护下,室温向(s)-叔丁基亚磺酸胺(100g,0.825mol)的四氢呋喃(1l)溶液中加入ti(oet)4(345ml,1.82mol)和3-甲基-2-丁酮(81ml,0.825mol)。加热反应液,回流16小时后冷却至室温,然后倒入冰水(1l)。过滤并且用乙酸乙酯洗滤饼。分离滤液中的有机相,无水硫酸钠干燥后减压浓缩,其残留物减压蒸馏(15-20torr,95℃)得目标产物(141g,90%产率),为黄色油状物。1hnmr(500mhz,cdcl3)δ2.54–2.44(m,1h),2.25(s,3h),1.17(s,9h),1.06(dd,j=6.9,5.1hz,6h)。esimsm/z:c9h19nanos[m+na]+:计算值212.12,实测值212.11。 实施例116.(2s,3s)-2-叠氮-3-甲基戊酸的合成。 将nan3(20.0g,0.308mol)溶于水(50ml),加入二氯甲烷(80ml)并冷却至0℃,向该溶液中加入tf2o(10ml,59.2mmol)。加完后在0℃下继续搅拌2小时。分离出有机相,水相用二氯甲烷萃取(2×40ml)。合并有机相,用饱和碳酸氢钠(3×80ml)洗。室温下将此二氯甲烷溶液加入到(l)-异亮氨酸(4.04g,30.8mmol),碳酸钾(6.39g,46.2mmol),五水硫酸铜(77.4mg,0.31mmol)的混合甲醇/水(1:2v/v,300ml)溶液中。加料过程中反应体系内温度会稍微升高。混合液在室温下搅拌16小时,减压蒸去溶剂,水相用水(250ml)稀释,用浓盐酸(大约280ml)酸化至ph6,然后用磷酸盐缓冲液稀释(0.25m,ph6.2,250ml),用乙酸乙酯(5×100ml)洗去磺酸胺副产物。水相用浓盐酸酸化至ph2后用乙酸乙酯(3×150ml)萃取。合并有机相,无水硫酸钠干燥,过滤浓缩得标题化合物(4.90g,99%产率),为亮黄色油状物。1hnmr(500mhz,cdcl3)δ12.01(s,1h),3.82(d,j=5.9hz,1h),2.00(ddd,j=10.6,8.6,5.5hz,1h),1.54(dqd,j=14.8,7.5,4.4hz,1h),1.36–1.24(m,1h),1.08–0.99(m,3h),0.97–0.87(m,3h)。 实施例117.d-n-甲基哌啶酸的合成。 向d-呱啶酸(10.0g,77.4mmol,1.0eq)的甲醇(100ml)溶液中加入甲醛(37%水溶液,30.8ml,154.8mmol,2.0eq)和pd/c(10wt%,1.0g)。将该反应液在h2(1atm)环境中搅拌过夜,而后用硅藻土过滤,用甲醇洗涤滤垫。减压浓缩滤液,获得标题化合物,为白色固体(10.0g,收率90%)。 实施例118.(r)-五氟苯基1-甲基哌啶-2-羧酸酯的合成。 向d-n-甲基呱啶酸(2.65g,18.5mmol)的乙酸乙酯(50ml)溶液中加入五氟苯酚(3.75g,20.4mmol)和dcc(4.21g,20.4mmol)。反应在室温下搅拌16小时,硅藻土过滤,用10ml乙酸乙酯洗。滤液不用进一步纯化,直接使用。esimsm/z:c13h13f5no2[m+h]+计算值309.08;实测值309.60。 实施例119.五氟苯基2-(二甲基氨基)-2-甲基丙酸酯的合成。 在0℃下向2-(二甲基氨基)-2-甲基丙酸(5.00g,38.10mmol)的乙酸乙酯(200ml)溶液中加入2,3,4,5,6-五氟苯酚(10.4g,57.0mmol),然后加入dic(8.8ml,57.0mmol)。将反应混合物升温至室温,搅拌过夜并过滤。浓缩滤液,得到标题化合物(12.0g,>100%产率),不经进一步纯化即用于下一步。esimsm/z:c12h13f5no2[m+h]+计算值298.08;实测值298.60。 实施例120.2,2-二乙氧基乙烷硫代酰胺的合成。 将二乙氧基乙腈(100g,0.774mol)溶解于甲醇(1.5l),在室温下加入(nh4)2s(48%水溶液,143ml,1.05mol)。搅拌16h后,浓缩反应液。向残留物中加入二氯甲烷,用饱和碳酸氢钠溶液洗,饱和食盐水洗,之后用无水硫酸钠干燥,过滤后减压浓缩。粗品用石油醚和二氯甲烷打浆,真空抽滤,收集固体并用石油醚洗涤。总共得到100g(79%产率)目标产物,为白色固体。1hnmr(500mhz,cdcl3)δ7.81(d,j=71.1hz,2h),5.03(s,1h),3.73(dq,j=9.4,7.1hz,2h),3.64(dq,j=9.4,7.0hz,2h),1.25(t,j=7.1hz,6h)。 实施例121.2-(二乙氧基甲基)噻唑-4-羧酸乙酯的合成。 将分子筛(90g)加入2,2-二乙氧基乙烷硫代酰胺(100g,0.61mol,1.0eq)和3-溴丙酮酸乙酯(142ml,1.1mol,1.8eq.)的乙醇溶液(1l)。随后将反应液加热至回流(反应液温度约60℃)并搅拌1h,旋蒸除去乙醇。向残留物中加入二氯甲烷,过滤,滤液浓缩,通过硅胶柱纯化(1:5-1:3乙酸乙酯/石油醚),得到黄色油状物,为目标化合物(130g,82%产率)。 实施例122.2-甲酰基噻唑-4-羧酸乙酯的合成。 向2-(二乙氧基甲基)噻唑-4-羧酸乙酯(130g,0.50mol)的丙酮(1.3l)溶液中加入2nhcl溶液(85ml,0.165mmol),加热至回流(反应液温度约60℃)。tlc显示起始原料反应完全后(约1-2h),减压除去丙酮,残留物用二氯甲烷稀释(1.3l),并依次用饱和碳酸氢钠水溶液、水和食盐水洗,然后用无水硫酸钠干燥。滤出干燥剂后浓缩有机相,所得粗产品用石油醚/乙醚溶液打浆,析出的固体经真空过滤收集,得白色固体(40g,43%产率)。1hnmr(500mhz,cdcl3)δ10.08–10.06(m,1h),8.53–8.50(m,1h),4.49(q,j=7.1hz,2h),1.44(t,j=7.1hz,3h)。esimsm/z:c7h8no3s[m+h]+:计算值186.01,实测值186.01。 实施例123.2-((r,e)-3-(((s)-叔丁基亚硫酰基)亚氨基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯的合成。 在n2保护下,于-78℃下向二异丙胺(121ml,0.86mol)的四氢呋喃溶液中加入正丁基锂溶液(2.5m,302ml,0.76mol)。反应在30分钟内升温至0℃然后重新冷却至-78℃,向其中加入(s,e)-2-甲基-n-(3-甲基丁-2-亚基)丙烷-2-磺酰胺(57g,0.30mol)的四氢呋喃(200ml)溶液。搅拌1小时后滴加clti(oipr)3(168.5g,0.645mol)的四氢呋喃(350ml)溶液。搅拌1小时后再缓慢滴入2-甲酰基噻唑-4-羧酸乙酯(40g,0.215mol)的四氢呋喃(175ml)溶液,所得溶液在-78℃继续搅拌2小时。tlc监测反应进行完全后,用乙酸和四氢呋喃(体积比1:4,200ml)的混合液淬灭反应,而后将反应液倒入冰水,用乙酸乙酯萃取(4×500ml)。有机相用水和食盐水洗,无水硫酸钠干燥,过滤并浓缩。残留物经柱层析(二氯甲烷/乙酸乙酯/石油醚2:1:2)纯化,得标题化合物(60g,74%产率),为无色油状物。1h-nmr(500mhz,cdcl3)δ8.13(s,1h),6.63(d,j=8.2hz,1h),5.20–5.11(m,1h),4.43(q,j=7.0hz,2h),3.42–3.28(m,2h),2.89(dt,j=13.1,6.5hz,1h),1.42(t,j=7.1hz,3h),1.33(s,9h),1.25–1.22(m,6h)。esimsm/z:c16h26nan2o4s2[m+na]+计算值397.13,实测值397.11。 实施例124.2-((1r,3r)-3-((s)-1,1-二甲基乙基亚磺酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯的合成。 将2-((r,e)-3-(((s)-叔丁基亚磺酰基)亚氨基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯(23.5g,62.7mol)溶于四氢呋喃(200ml),冷却至-45℃,向其中缓慢加入ti(oet)4(42.9ml,188mol),加完后搅拌1小时。然后分批加入nabh4(4.75g,126mmol),反应在-45℃搅拌3小时。tlc监测发现起始原料仍有剩余。将反应用hoac/thf(v/v1:4,25ml)淬灭,缓慢加入乙醇(25ml),将反应液倒入冰水(100g),升至室温。经过硅藻土过滤,分离有机相,水洗、饱和食盐水洗、无水硫酸钠干燥,过滤并浓缩。残留物经柱层析(乙酸乙酯/石油醚1:1)纯化得标题化合物(16.7g,71%产率),为白色固体。1hnmr(500mhz,cdcl3)δ8.10(s,1h),5.51(d,j=5.8hz,1h),5.23–5.15(m,1h),4.41(q,j=7.0hz,2h),3.48–3.40(m,1h),3.37(d,j=8.3hz,1h),2.29(t,j=13.0hz,1h),1.95–1.87(m,1h),1.73–1.67(m,1h),1.40(t,j=7.1hz,3h),1.29(s,9h),0.93(d,j=7.3hz,3h),0.90(d,j=7.2hz,3h)。esimsm/z:计算值c16h28nan2o4s2[m+na]+:399.15,实测值399.14。 实施例125.2-((1r,3r)-3-氨基-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯盐酸盐的合成。 在0℃下向2-((1r,3r)-3-((s)-1,1-二甲基乙基亚磺酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯(6.00g,16.0mmol)的乙醇(40ml)溶液中加入4nhcl的1,4-二氧六环(40ml)溶液。反应逐渐升至室温后搅拌2.5小时。浓缩后用乙醚打浆,得白色固体,共4.54g(92%产率),并将其用于下一步。 实施例126.2-((1r,3r)-3-((2s,3s)-2-叠氮基-3-甲基戊胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯的合成。 将(2s,3s)-2-叠氮基-3-甲基戊酸(5.03g,28.8mol,2.0eq)溶于四氢呋喃(120ml)并冷却至0℃,依次加入nmm(6.2ml,56.0mmol)和氯甲酸异丁酯(3.7ml,28.8mol)。在0℃搅拌30分钟,室温1h,在0℃下,分批加入2-((1r,3r)-3-氨基-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯盐酸盐(4.54g,14.7mmol)。在0℃搅拌30分钟后,逐渐升至室温并继续搅拌2小时。反应在0℃下加冰水淬灭并用乙酸乙酯萃取三遍。合并有机相用1nhcl洗,饱和碳酸氢钠洗和食盐水洗,无水硫酸钠干燥。过滤浓缩,残留物经柱层析(0-30%乙酸乙酯/石油醚)纯化得到白色固体(4.55g,74%产率)。 实施例127.2-((1r,3r)-3-((2s,3s)-2-叠氮基-3-甲基戊胺基)-4-甲基-1-((三乙基甲硅烷基)氧基)戊基)噻唑-4-羧酸乙酯的合成。 在0℃下向2-((1r,3r)-3-((2s,3s)-2-叠氮基-3-甲基戊酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯(5.30g,12.8mmol)的二氯甲烷(50ml)溶液中依次加入咪唑(1.75g,25.6mmol)和三乙基氯硅烷(4.3ml,25.6mol)。反应液历时1小时升至室温后,继续搅拌1小时。加入饱和食盐水淬灭,分出有机相,水相用乙酸乙酯萃取。合并后的有机相经干燥、过滤、浓缩后用柱层析(15-35%乙酸乙酯/石油醚)纯化得标题化合物(6.70g,99%产率),为白色固体。1hnmr(500mhz,cdcl3)δ8.12(s,1h),6.75(d,j=8.0hz,1h),5.20–5.12(m,1h),4.44(q,j=7.0hz,2h),4.06–3.97(m,1h),3.87(d,j=3.8hz,1h),2.14(d,j=3.8hz,1h),2.01–1.91(m,3h),1.42(t,j=7.1hz,3h),1.34–1.25(m,2h),1.06(d,j=6.8hz,3h),1.00–0.93(m,18h),0.88(dd,j=19.1,6.8hz,6h)。esimsm/z:c24h44n5o4ssi[m+h]+:计算值526.28,实测值526.28。 实施例128.2-((1r,3r)-3-((2s,3s)-2-叠氮基-n,3-二甲基戊酰胺基)-4-甲基-1-((三乙基甲硅烷基)氧基)戊基)噻唑-4羧酸乙酯的合成。 将2-((1r,3r)-3-((2s,3s)-2-叠氮基-3-甲基戊酰胺基)-4-甲基-1-((三乙基甲硅烷基)氧基)戊基)噻唑-4-羧酸乙酯(5.20g,9.9mmol,1.0eq.)的四氢呋喃(50ml)溶液冷却至-45℃,加入khmds(1m甲苯溶液,23.8ml,23.8mmol,2.4eq.)。将所得混合物在-45℃下搅拌20分钟,然后加入碘甲烷(1.85ml,29.7mmol,3.0eq.)。将反应混合物升温至室温,搅拌超过4.5小时,然后用乙醇(10ml)淬灭反应。粗产物用乙酸乙酯(250ml)稀释并用盐水(100ml)洗涤。水层用乙酸乙酯(3×50ml)反萃取。将有机层干燥,过滤,浓缩并通过柱层析法用15-35%乙酸乙酯/石油醚梯度洗脱,得到标题产物(3.33g,63%产率),为浅黄色油状物。1hnmr(500mhz,cdcl3)δ8.09(s,1h),4.95(d,j=6.6hz,1h),4.41(q,j=7.1hz,2h),3.56(d,j=9.5hz,1h),2.98(s,3h),2.27–2.06(m,4h),1.83–1.70(m,2h),1.41(t,j=7.2hz,3h),1.29(ddd,j=8.9,6.8,1.6hz,3h),1.01(d,j=6.6hz,3h),0.96(dt,j=8.0,2.9hz,15h),0.92(d,j=6.6hz,3h),0.90(d,j=6.7hz,3h);esimsm/z:c25h46n5o4ssi[m+h]+计算值540.30,实测值540.30。 实施例129.2-((3s,6r,8r)-3-((s)-仲丁基)-10,10-二乙基-6-异丙基-5-甲基-1-((r)-1-甲基哌啶-2-基)-1,4-二氧代-9-氧杂-2,5-二氮杂-10-硅杂十二烷-8-基)噻唑-4-甲酸乙酯的合成。 向五氟苯基酯的乙酸乙酯溶液中加入干的pd/c(10wt%,300mg)和2-((1r,3r)-3-((2s,3s)-2-叠氮基-n,3-二甲基戊酰胺基)-4-甲基-1-乙基((三乙基甲硅烷基)氧基)戊基)噻唑-4-羧酸乙酯(3.33g,6.61mmol)。反应液在氢气(1atm)环境中搅拌27小时,而后用硅藻土过滤,乙酸乙酯洗。滤液旋干经柱层析(0-5%甲醇/乙酸乙酯)纯化得标题化合物(3.90g,86%产率)。esimsm/z:c32h59n4o5ssi[m+h]+计算值639.39,实测值639.39。 实施例130.2-((1r,3r)-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)戊酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯的合成。 将2-((3s,6r,8r)-3-((s)-仲丁基)-10,10-二乙基-6-异丙基-5-甲基-1-((r)-1-甲基哌啶-2)-)-1,4-二氧代-9-氧杂-2,5-二氮杂-10-基十二烷-8-基)噻唑-4-羧酸乙酯(3.90g,6.1mmol)溶于acoh/水/四氢呋喃(v/v/v3:1:1,100ml)中,并在室温下搅拌48小时。然后浓缩,残留物经柱层析(2:98至15:85甲醇/乙酸乙酯)纯化得到标题化合物(2.50g,两步产率72%)。esimsm/z:c26h45n4o5s[m+h]+计算值525.30,实测值525.33。 实施例131.2-((1r,3r)-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)戊酰胺基)-1-羟基-4-甲基戊基)噻唑-4-酸的合成。 在0℃下,将lioh水溶液(0.4n,47.7ml,19.1mmol,4.0eq.)加入到2-((1r,3r)-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)-戊酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯(2.50g,4.76mmol,1.0eq.)的1,4-二氧六环(47.7ml)溶液中。室温搅拌2小时后浓缩。残留物经柱层析(100%二氯甲烷至二氯甲烷/甲醇/氨水80:20:1)纯化,得到标题化合物(2.36g,99%产率),为无定形固体。esimsm/z:c24h41n4o5s[m+h]+计算值497.27,实测值497.28。 实施例132.2-((1r,3r)1-乙酰氧基-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)戊酰胺基)-4-甲基戊基)噻唑-4-酸的合成。 在0℃,向2-((1r,3r)-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)戊基)-1-羟基-4-甲基戊基)噻唑-4-羧酸(2.36g,4.75mmol)的吡啶(50ml)溶液中,缓慢加入乙酸酐(2.25ml,24mmol)。反应经2小时逐渐升至室温,并继续搅拌24小时。将反应浓缩并将残余物通过反相hplc(c18柱,50×250mm,50ml/min,10-90%乙腈/水,45分钟)纯化,得到标题化合物(2.25g,88%产率),呈无定形白色固体。esimsm/z:c26h43n4o6s[m+h]+计算值539.28,实测值539.28。 实施例133.(1r,3r)-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)戊烷基)-4-甲基-1-(4-(全氟苯甲酰基)噻唑-2-基)戊基乙酸酯的合成。 在0℃下,向2-((1r,3r)-1-乙酰氧基-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基-哌啶-2-甲酰胺基)戊酰胺的溶液)-4-甲基戊基)噻唑-4-羧酸(860mg,1.60mmol,1.0eq.)在二氯甲烷(20ml)的溶液中,加入五氟苯酚(440mg,2.40mmol,1.5eq.)和n,n’-二异丙基碳二亚胺(220mg,1.75mmol,1.1eq.)。将反应混合物升温至室温并搅拌过夜。减压除去溶剂后,将反应混合物用乙酸乙酯(20ml)稀释,然后经硅藻土过滤。浓缩滤液,在硅胶柱上纯化(1:10至1:3乙酸乙酯/二氯甲烷),得到标题化合物(935.3mg,82%产率),将其直接用于下一步骤。esimsm/z:c32h42f5n4o6s[m+h]+计算值704.28,实测值704.60。 实施例134.2-((6s,9r,11r)-6-((s)-仲丁基)-13,13-二乙基-9-异丙基-2,3,3,8-四甲基-4,7-二氧代-12-氧杂-2,5,8-三氮杂-13-硅十五烷-11-基)噻唑-4-羧酸乙酯的合成。 将干燥pd/c(10wt%,300mg)和2-((1r,3r)-3-((2s,3s)-2-叠氮基-n,3-二甲基戊酰胺基)-4-甲基-1-乙基((三乙基甲硅烷基)氧基)戊基)噻唑-4-羧酸乙酯(3.33g,6.16mmol)加到五氟苯基2-(二甲基氨基)-2-甲基丙酸酯(约2.75g,1.5eq.)的乙酸乙酯溶液中。将反应混合物在氢气下搅拌27小时,然后通过硅藻土过滤,并用乙酸乙酯洗涤滤垫。将合并的有机相浓缩并通过柱层析,用0-5%甲醇/乙酸乙酯溶液梯度洗脱,得到标题产物(3.24g,84%产率)。esimsm/z:c31h59n4o5ssi[m+h]+计算值626.39,实测值626.95。 实施例135.2-((1r,3r)-3-((2s,3s)-2-(2-(二甲胺基)-2-甲基丙酰胺)-n,3-二甲基戊烯基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯的合成。 将2-((6s,9r,11r)-6-((s)-仲丁基)-13,13-二乙基-9-异丙基-2,3,3,8-四甲基-4,7-二氧代-12-氧杂-2,5,8-三氮杂-13-硅杂十五烷-11-基)噻唑-4-羧酸乙酯(3.20g,5.11mmol)溶于脱氧的acoh/水/四氢呋喃(v/v/v3:1:1,100ml)中,并在室温下搅拌48小时。然后浓缩反应物并通过硅胶柱纯化(2:98至15:85甲醇/乙酸乙酯),得到标题化合物(2.33g,89%产率)。esimsm/z:c25h45n4o5s[m+h]+计算值512.30,实测值512.45。 实施例136.2-((1r,3r)-3-((2s,3s)-2-(2-(二甲胺基)-2-甲基丙酰胺)-n,3-二甲基戊烯基)-1-羟基-4-甲基戊基)噻唑-4-羧酸的合成。 在0℃,将lioh水溶液(0.4n,47.7ml,19.1mmol,4.0eq.)加入到2-((1r,3r)-3-((2s,3s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基戊酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸乙酯(2.30克,4.50毫摩尔,1.0eq.)的二恶烷(50毫升)溶液中,将反应混合物在室温下搅拌2小时,然后浓缩。用硅胶柱纯化(先用100%二氯甲烷,然后用二氯甲烷/甲醇/nh4oh80:20:1洗脱),得到标题化合物(2.13g,98%产率),为无定形固体。esimsm/z:c23h41n4o5s[m+h]+计算值485.27,实测值485.55。 实施例137.2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧基-12-氧杂-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸的合成。 在0℃下,向2-((1r,3r)-3-((2s,3s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基丙酰胺基)-1-羟基-4-甲基戊基)噻唑-4-羧酸(2.10g,4.33mmol)的吡啶(50ml)溶液中缓慢加入乙酸酐(2.25ml,24mmol)。2小时使反应混合物升温至室温,并在室温下搅拌24小时。将反应浓缩并将残余物通过反相hplc(c18柱,50mm×250,50ml/min,10-90%乙腈/水,45分钟)纯化,得到呈无定形白色固体的标题化合物(1.95g,86%产率)。esimsm/z:c25h43n4o6s[m+h]+计算值526.28,实测值526.80。 实施例138.五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸酯的合成。 在0℃下,向2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸(1.90g,3.61mmol,1.0eq.)的二氯甲烷(70ml)溶液中,加入五氟苯酚(1.00g,5.43mmol,1.5eq.)和n,n’-二异丙基碳二亚胺(512mg,3.96mmol,1.1eq.)。将反应混合物升温至室温并搅拌过夜。在减压下除去溶剂后,将反应混合物用乙酸乙酯(80ml)稀释,然后用硅藻土过滤。浓缩滤液,在硅胶柱上纯化(1:10至1:3乙酸乙酯/二氯甲烷),得到标题化合物(2.09mg,84%产率),将其直接用于下一步骤。esimsm/z:c31h42f5n4o6s[m+h]+计算值693.27,实测值693.60。 实施例139.2-(三苯基亚正膦基)丙酸叔丁酯的合成。 将2-溴代丙酸叔丁酯(15.5g,74.1mmol,1.0eq.)和三苯基膦(19.4g,74.1mmol,1.0eq.)在无水乙腈(45ml)中的混合物在室温下搅拌18小时。减压除去乙腈,加入甲苯使白色沉淀析出。倾倒出甲苯,将白色固体溶于二氯甲烷(100ml)中并转移至分液漏斗中。向漏斗中加入10%naoh(100ml),振荡后有机层立即变黄。将有机层分离,并将水层用二氯甲烷(30ml)萃取一次。将二氯甲烷层合并,用盐水(50ml)洗涤一次,然后用硫酸钠干燥,过滤并浓缩,得到叶立德,为黄色固体(16.8g,58%)。 实施例140.(s)-3-(4-(苄氧基)苯基)-2-((叔丁氧基羰基)氨基)丙酸甲酯的合成。 向boc-l-tyr-ome(20.0g,67.7mmol,1.0eq)、k2co3(14.0g,101.6mmol,1.5eq)和ki(1.12g,6.77mmol,0.1eq)在丙酮(100ml)中的混合物中缓慢加入bnbr(10.5ml,81.3mmol,1.2eq)。然后将混合物回流一夜。加入水(250ml),用乙酸乙酯(3×100ml)萃取反应混合物。用盐水(300ml)洗涤组合有机层,用无水硫酸钠干燥,通过硅胶柱层析(4:1己烷/乙酸乙酯)过滤、浓缩和纯化,得到白色固体标题化合物(26.12g,收率99%)。1hnmr(500mhz,cdcl3)δ7.44–7.41(m,2h),7.41–7.36(m,2h),7.35–7.30(m,1h),7.04(d,j=8.5hz,2h),6.93–6.89(m,2h),5.04(s,2h),4.97(d,j=7.7hz,1h),4.55(d,j=6.9hz,1h),3.71(s,3h),3.03(dd,j=14.4,5.7hz,2h),1.44(d,j=18.6hz,10h)。esimsm/z:c22h27no5na[m+na]+计算值:408.18,实测值:408.11。 实施例141.((s)-(1-(4-(苄氧基)苯基)-3-氧代丙-2-基)氨基甲酸叔丁酯的合成。 在-78℃时,1小时内向(s)-3-(4-(苄氧基)苯基)-2-((叔丁氧基羰基)氨基)-丙酸甲酯(26.1g,67.8mmol,1.0eq.)的无水二氯甲烷(450ml)溶液中加入dibal(1.0m正己烷溶液,163ml,2.2eq.)。将混合物在-78℃下搅拌3小时,然后用50ml乙醇淬灭。滴加1nhcl直至达到ph4。使得到的混合物升温至0℃,再进行分层,水层进一步用乙酸乙酯(3×100ml)萃取。将合并的有机溶液用盐水洗涤,经无水硫酸钠干燥并浓缩。用石油醚/乙酸乙酯打浆并过滤,得到标题化合物,为白色固体(18.3g,76%产率)。esimsm/z:c22h27no5na[m+na]+计算值378.11,实测值378.11。 实施例142.(s,z)-5-(4-(苄氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊-2-烯酸叔丁酯。 将(s)-(1-(4-(苄氧基)苯基)-3-氧代丙-2-基)氨基甲酸叔丁酯(0.84g,2mmol,1.0eq.)溶解于无水二氯甲烷(50ml)中,向其中加入2-(三苯基-亚磷酰基)丙酸叔丁酯(1.6g,4mmol,2.0eq.),将溶液在室温下搅拌1.5小时,用tlc确定反应完成。通过柱层析法(10-50%乙酸乙酯/正己烷)纯化反应液,得到标题化合物(1.16g,98%产率)。 实施例143.(4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基苯基)-2-甲基戊酸叔丁酯的合成。 将(s,z)-5-(4-(苄氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊-2-烯酸叔丁酯(467mg,1mmol)溶于甲醇(30ml)中,与pd/c催化剂(10wt%,250mg)混合,在室温下氢化(1atm)过夜。滤出催化剂,减压浓缩滤液,得到标题化合物(379mg,99%产率)。 实施例144.(4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸叔丁酯的合成。 将(4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基苯基)-2-甲基戊酸叔丁酯(379mg,1mmol,1.0eq.)溶于四氢呋喃(20ml)中,向其中加入亚硝酸叔丁酯(315mg,3mmol,3.0eq.)的四氢呋喃(2ml)溶液。将反应物在室温下搅拌3小时,然后倒入水中,用乙酸乙酯(2×50ml)萃取,将合并的有机相用盐水(50ml)洗涤,用无水硫酸钠干燥,过滤并浓缩。通过柱层析法(10-50%乙酸乙酯/正己烷)纯化,得到标题化合物(300mg,71%产率)。 实施例145.(4r)-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸叔丁酯(200mg,0.47mmol)溶于乙酸乙酯(30ml)并与钯催化剂(10wt%,100mg)混合,然后在室温下氢化(1atm)2小时。滤出催化剂,并在真空下除去所有挥发物,得到标题化合物(185mg,99%)。 或者,将(4r)4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸叔丁酯(56mg,0.132mmol)溶于乙酸乙酯(20ml)并与pd/c催化剂(10wt%,50mg)混合并在室温下氢化(1atm)3小时。滤出催化剂,真空除去所有挥发物,得到标题化合物(52mg,99%产率)。esimsm/z:c21h35n2o5[m+h]+计算值:395.25,实测值:395.26。 实施例146.(4r)-4-((叔丁氧基羰基)氨基)-5-(4-((叔丁基二甲基甲硅烷基)氧基)-3-硝基苯基)-2-甲基戊酸叔丁酯的合成。 向(4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸叔丁酯(424mg,1mmol)的二氯甲烷(20ml)溶液中加入咪唑(408mg,6mmol)和叔丁基二甲基氯硅烷(602mg,4mmol)。在室温下持续搅拌所得溶液3小时。之后,反应混合物用盐水(50ml)洗涤,用无水硫酸钠干燥,浓缩并通过柱色谱法(10%至30%乙酸乙酯/正己烷)纯化,得到标题化合物(344mg,64%产率)。 实施例147.(4r)-5-(3-氨基-4-((叔丁基二甲基甲硅烷基)氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(4r)-4-((叔丁氧基羰基)氨基)-5-(4-((叔丁基二甲基甲硅烷基)氧基)-3-硝基苯基)-2-甲基戊酸叔丁酯(200mg,0.37mmol)溶于乙酸乙酯(30ml)中,与钯碳催化剂(10wt%,100mg)混合,并在室温氢化反应(1atm)2小时。滤出催化剂,真空除去所有挥发物,得到标题化合物(187mg,99%产率)。 实施例148.2-(1-叠氮基-14,17二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)-4-((2r)-5-(叔丁氧基)-2–((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酯的合成 向1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-1,1,16-二氮杂十八烷-18-酸(1.50g,3.85mmol)和(4r)-叔丁基-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸酯(0.75g,1.90mmol)的dma(40ml)溶液中加入edc(2.05g,10.67mmol)和dipea(0.70ml,4.0mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:5至1:1)洗脱,得到标题化合物(2.01g,82%产率,hplc纯度约95%)。esimsm/z:c51h85n12o17[m+h]+计算值1137.61,实测值1137.90。 实施例149.(4r)-5-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂-七氮杂环四十六烷-46-基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将2-(1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)-4-((2r)-5-(叔丁氧基)-2–((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸酯(900mg,0.79mmol)溶于乙酸乙酯(30ml)中,与钯碳催化剂(10wt%,100mg)混合,并在室温下氢化反应(1atm)4小时。滤除催化剂并在真空下除去所有挥发物,得到2-(1-氨基-1,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)-4-((2r)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基1-氨基-1,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酯(815mg,96%产量),无需进一步纯化即可使用。esimsm/z:c51h88n8o17[m+h]+计算值1085.62,实测值1085.95。 将edc(1.25g,6.51mmol)和dipea(0.35ml,2.0mmol)加入到上述二氨基化合物(810mg,0.75mmol)和2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸(231mg,0.75mmol)的dma(10毫升)溶液中。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:5至1:1)洗脱,得到标题化合物(844mg,83%产率,hplc纯度约95%)。esimsm/z:c63h92n10o23[m+h]+计算值1357.63,实测值1357.95。 实施例150.(2r)-1-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂-七氮杂环四十六烷-46-基)-4-羧基戊-2-铵的合成。 将(4r)-5-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂-七氮杂环四十六烷-46-基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(840mg,0.62mmol)溶解在二氯甲烷(6ml)和tfa(4ml)的混合物中。将混合物搅拌过夜,用甲苯(10ml)稀释,浓缩,得到标题化合物(7.43g,100%产率,hplc纯度约91%),其不经进一步纯化即用于下一步骤。esimsm/z:c54h76n10o21[m+h]+计算值1200.51,实测值1200.95。 实施例151.(4r)-4-(2-((1r,3r)-1-乙酰氧基-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-基)甲酰胺基)戊酰胺基)-4-甲基戊基)噻唑-4-甲酰胺基)-5-(3-(3-(2-(2-叠氮基乙氧基)乙氧基)丙酰胺基)-4-羟基苯基)-2-甲基戊酸的合成。 向(4r)-4-(2-((1r,3r)-1-乙酰氧基-3-((2s,3s)-n,3-(二甲基-2-((r)-1-甲基哌啶-2-甲酰胺基)戊酰胺基)-4-甲基戊基)噻唑-4-甲酰胺基)-5-(3-氨基-4-羟基苯基)-2-甲基戊酸(100mg,0.131mmol)(huangy.等,medchem.#44,249thacsnationalmeeting,denver,co,mar.22-26,2015;wo)的dma(10ml)和nah2po4缓冲溶液(ph7.5,1.0m,0.7ml)的混合溶液中,两小时内分四次加入2,5二氧代吡咯烷-1-基3(2(2叠氮基乙氧基)乙氧基)丙酸酯(80.0mg,0.266mmol)。将混合物搅拌过夜,浓缩并在制备型hplc(3.0×25cm,25ml/min)上纯化,在45分钟内用80%水/甲醇至10%水/甲醇洗脱,得到标题化合物(101.5mg,82%产率)。lc-ms(esi)m/z:c45h70n9o11s[m+h]+计算值944.48,实测值944.70。 实施例152.(4r)-4-(2-((1r,3r)-1-乙酰氧基-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基-哌啶-2-羧酰胺基)戊酰胺基)-4-甲基戊基)噻唑-4-甲酰胺基)-5-(3-(3-(2-(2-氨基乙氧基)乙氧基)丙酰胺基)-4-羟基苯基)-2-甲基戊酸的合成。 在氢化反应瓶中,向(4r)-4-(2-((1r,3r)-1-乙酰氧基-3-((2s,3s)-n,3-二甲基-2-((r)-1-甲基哌啶-2-基)甲酰胺基)戊酰胺基)-4-甲基戊基)噻唑-4-甲酰胺基)-5-(3-(3-(2-(2-叠氮基乙氧基)乙氧基)丙酰胺基)-4-羟基苯基)-2-甲基戊酸(100.0mg,0.106mmol)的含有0.1%hcl的甲醇(25ml)溶液中,加入pd/c(25mg,10%pd,含水50%)。将容器中的空气抽真空后,加入35psi的氢气,将混合物振荡4小时,通过硅藻土过滤。将滤液浓缩并且在制备性hplc(3.0×25cm,25ml/min)上纯化,在45分钟内用85%水/甲醇至15%水/甲醇洗脱,得到标题化合物(77.5mg,79%产率)。lc-ms(esi)m/z:c45h72n7o11s[m+h]+计算值918.49,实测值918.60。 实施例153.(4r)-5-(4-乙酰氧基-3-硝基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 在0℃下,向(4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸叔丁酯(107.1mg,0.252mmol)的二氯甲烷(4.0ml)溶液中依次加入乙酸酐(0.11ml,1.17mmol)和三乙胺(0.16ml)。然后将反应物升温至室温并搅拌1小时,用二氯甲烷稀释并用水和盐水洗涤,用无水硫酸钠干燥,过滤并浓缩。通过柱层析(0-15%乙酸乙酯/石油醚)纯化残余物,得到无色油状物(120.3mg,理论产率)。esimsm/z:c23h35n2o8[m+h]+计算值467.23,实测值467.23。 实施例154.(4r)-5-(4-乙酰氧基-3-氨基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(4r)-5-(4-乙酰氧基-3-硝基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(120.3mg,0.258mmol)溶于乙酸乙酯(5ml)和乙酸(0.5ml)中。向其中加入pd/c(10wt%,10mg),在室温下,在氢气球下搅拌该混合物30分钟,然后通过硅藻土垫过滤,并用乙酸乙酯洗涤硅藻土垫。将滤液浓缩并通过柱层析(0-25%乙酸乙酯/石油醚)纯化,得到黄色油状物(120.9mg,理论产量)。esimsm/z:c23h37n2o6[m+h]+计算值437.26,实测值437.28。 实施例155.(4r)-5-(3-(4-(((苄氧基)羰基)氨基)丁酰胺基)-4-((叔丁基二甲基甲硅烷基)氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸乙酯。 将2,5-二氧代吡咯烷-1-基4-(((苄氧基)羰基)氨基)丁酸酯(0.396g,1.2mmol)和(4r)-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸乙酯(0.44g,1.2mmol)溶于乙醇(10ml)中,然后加入磷酸盐缓冲溶液(ph=7.5,0.1m,2ml)。反应混合物在室温下搅拌过夜,然后减压除去溶剂,并将残余物通过硅胶柱层析纯化,得到标题产物(0.485g,70%)。esimsm/z:c31h44n3o8[m+h]+计算值:586.31,实测值:586.31。 实施例156.(4r)-5-(3-(4-氨基丁酰胺基)-4-((叔丁基二甲基甲硅烷基)氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸乙酯的合成。 将(4r)-5-(3-(4-(((苄氧基)羰基)氨基)丁酰胺基)-4-((叔丁基二甲基-甲硅烷基)氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸乙酯(0.35g,0.5mmol)溶于甲醇(5ml)中,然后加入pd/c(10wt%,35mg)。将反应混合物在室温下,在氢气球下搅拌过夜,然后通过硅藻土过滤,并将滤液减压浓缩,得到标题产物(0.22g,79%产率)。esimsm/z:c29h52n3o6si[m+h]+计算值:566.35,实测值:566.35。 实施例157.(2r,3s)-2,3-双(((苄氧基)羰基)氨基)琥珀酸的合成。 向(2r,3s)-2,3-二氨基琥珀酸(4.03g,27.30mmol)的四氢呋喃(250ml)和nah2po4(0.1m,250ml,ph8.0)的混合物中,在2小时内分4份加入碳酸氯苄酯(15.0g,88.23mmol)。将混合物搅拌6小时,浓缩并在硅胶柱上纯化,用含有1%甲酸的水/乙腈(1∶9)洗脱,得到标题化合物(8.63g,收率75%)。esimsm/z:c20h21n2o8[m+h]+计算值:417.12,实测值:417.50。 实施例158.(2r,3s)-双(2,5-二氧杂吡咯烷-1-基)2,3-双(((苄氧基)-羰基)氨基)琥珀酸酯的合成。 向(2r,3s)-2,3-双((((苄氧基)羰基)氨基)琥珀酸(4.25g,10.21mmol)的dma(70ml)溶液中加入nhs(3.60g,31.30mmol)和edc(7.00g,36.65mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶6)洗脱,得到标题化合物(5.48g,88%收率)。esimsm/z:c28h27n4o12[m+h]+计算值:611.15,实测值:611.45。 实施例159.4,4′-((((2r,3s)-2,3-双(((苄氧基)羰基)-氨基)琥珀酰基)双(氮杂二基))二丁酸二叔丁基酯的合成。 向(2r,3s)-2,3-双((((苄氧基)羰基)氨基)琥珀酸(4.25g,10.21mmol)的dma(70ml)溶液中加入4-氨基丁酸叔丁酯(3.25g,20.42mmol)和edc(7.00g,36.65mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶10)洗脱,得到标题化合物(6.50g,收率91%)。esimsm/z:c36h51n4o10[m+h]+计算值:699.35,实测值:699.55。 实施例160.4,4′-((((2r,3s)-2,3-双(((苄氧基)羰基)-氨基)琥珀酰基)双(氮杂二基))二叔丁基酯。 向4,4′-(((((2r,3s)-2,3-双(((苄氧基)羰基)氨基)-琥珀酰基)双(氮杂二烷基))二丁酸二叔丁基酯(2.50g,3.58mmol)的甲醇(100ml)溶液中加入10%pd/c(0.30g,50%wet),将混合物在氢气下于室温搅拌18小时。然后通过硅藻土过滤除去pd/c,并用甲醇洗涤滤床。浓缩滤液,得到黄色泡沫状产物,其无需进一步纯化即可用于下一步骤(1.54g,收率100%)。esimsm/z:c20h39n2o6[m+h]+计算值:431.28,实测值:431.50。 实施例161.4,4′-(((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))丁酸二叔丁酯的合成。 向3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酸(1.25g,7.39mmol)的dma(60ml)溶液中加入二叔丁基4,4′-(((2r,3s)-2,3-二氨基琥珀酰基)-双(氮杂二基))二丁酸酯(1.54g,~3.57mmol)和edc(2.40g,12.56mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶10)洗脱,得到标题化合物(2.35g,收率90%)。esimsm/z:c34h49n6o12[m+h]+计算值:733.33,实测值:733.60。 实施例162.4,4′-(((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸的合成。 向4,4′-(((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基))丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯(2.30g,3.14mmol)的1,4-二氧六环(20ml)溶液搅拌加入hcl(36%,7.0ml)。将混合物搅拌30分钟,用甲苯(20ml)稀释,浓缩并硅胶柱上纯化,用甲醇/二氯甲烷(1:10至1:4)洗脱,得到标题化合物(1.69g,收率86%)。esimsm/z:rc26h33n6o12[m+h]+计算值:621.21,实测值:621.70。 实施例163.4,4′-((((2r,3s)-2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-)酰基)乙酰胺基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯的合成。 向2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酸(1.12g,7.22mmol)的dma(60ml)溶液中加入4,4′-二叔丁基(((2r,3s)-2,3-二氨基琥珀酰)-双(氮杂二基))二丁酸二叔丁酯(1.54g,3.58mmol)和edc(2.40g,12.56mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:10)洗脱,得到标题化合物(2.29g,收率91%)。esimsm/z:c32h45n6o12[m+h]+计算值:704.30,实测值:704.60。 实施例164.4,4′-(((2r,3s)-2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰胺基)琥珀酰)双(氮杂二酰基))二丁酸的合成。 向4,4′-(((2r,3s)-2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基))乙酰氨基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯(2.20g,3.12mmol)的1,4-二氧六环(20ml)溶液中加入hcl(36%,7.0ml)。将混合物搅拌30分钟,用甲苯(20ml)稀释,浓缩并在硅胶柱上纯化,并用甲醇/二氯甲烷(1:10至1:4)洗脱,得到标题化合物(1.69g,收率86%)。esimsm/z:c24h29n6o12[m+h]+计算值:593.18,实测值:593.40。 实施例165.双(2,5-二氧代吡咯烷-1-基)4,4′-(((2r,3s)-2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰胺基)琥珀酰基)双(氮杂二基))二丁酸酯的合成。 向4,4′-(((2r,3s)-2,3-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)琥珀酰基)双(氮杂二基))二丁酸(1.10g,1.85mmol)的dma(30ml)溶液中加入nhs(1-羟基吡咯烷-2,5-二酮)(0.55g,4.78mmol)和edc(1.25g,6.54mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:10)洗脱,得到标题化合物(1.30g,收率90%)。esimsm/z:c32h35n8o16[m+h]+计算值:787.21,实测值:787.60。 实施例166.(2s,3s)-2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸的合成。 向(2r,3r)-2,3-二氨基琥珀酸(5.00g,33.77mmol)在thf/h2o/dipea(125ml/125ml/2ml)中加入马来酸酐(6.68g,68.21mmol)。将混合物搅拌过夜,蒸发,得到(2s,3s)-2,3-双((z)-3-羧基丙烯酰胺基)琥珀酸(11.05g,收率99%),为白色固体。esimsm/z:c12h13n2o10[m+h]+计算值:345.05,实测值:345.35。 向(2s,3s)-2,3-双((z)-3-羧基丙烯酰胺基)琥珀酸(11.05g,33.43mmol))的hoac(70ml),dmf(10ml)和甲苯(50ml)混合溶液中加入乙酸酐(30毫升)。将混合物搅拌2小时,用dean-stark分水器在100℃下回流6小时,浓缩,与乙醇(2×40ml)和甲苯(2×40ml)共浓缩,并在硅胶柱上纯化,用水/乙腈(1∶10)洗脱,得到标题化合物(8.10g,收率78%)。esimsm/z:c12h9n2o8[m+h]+计算值:309.03,实测值:309.50。 实施例167.(2s,3s)-双(2,5-二氧杂吡咯烷-1-基)2,3-双(2,5-二氧杂-2,5-二氢-1h-吡咯-1-基)琥珀酸酯的合成。 向(2s,3s)-2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸(4.00g,12.98mmol)的dmf溶液(70ml)中加入nhs(3.60g,31.30mmol)和edc(7.00g,36.65mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶6)洗脱,得到标题化合物(5.79g,收率89%,hplc纯度约为96%)。esimsm/z:c20h15n4o12[m+h]+计算值:503.06,实测值:503.60。 实施例168.(4r)-5-(3-(4-((((苄氧基)羰基)氨基)-丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将hatu(39.9g,105mmol)加入到4-(((苄氧基)羰基)氨基)丁酸(26.1g,110mmol)的dmf(300ml)溶液中。在室温下搅拌后30分钟后,将混合物加入到(4r)5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(39.4g,100mmol)和tea(20.2g,200mmol)的dmf(300毫升)溶液中。将得到的混合物在室温搅拌2小时。然后加入水,用乙酸乙酯萃取,有机层用盐水洗涤,用硫酸钠干燥。通过柱色谱法纯化(20%至70%乙酸乙酯/石油醚),得到标题产物,为白色固体(45g,收率73%)。esim/z:c33h48n3o8[m+h]+计算值:614.34,实测值614.15。 实施例169.(4r)-5-(3-(4-(4-氨基丁亚氨基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(4r)-5-(3-(4-((((苄氧基)羰基)氨基)-丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(100g,163mmol)溶于甲醇(500ml)中,并在室温下与pd/c催化剂(10wt%,10g)氢化(1atm)过夜。滤出催化剂,减压浓缩滤液,得到标题化合物(75.8g,收率97%),为棕色泡沫状固体。1hnmr(400mhz,cdcl3)δ7.11(s,1h),6.83(d,j=10.3hz,2h),5.04–4.52(m,6h),3.90–3.56(m,1h),2.81(d,j=5.3hz,2h),2.63(dd,j=12.5,6.1hz,2h),2.54-2.26(dd,j=14.0,7.6hz,4h),1.94-1.64(m,3h),1.44–1.36(m,18h),1.08(d,j=6.9hz,3h)。esimsm/z:c25h42n3o6[m+h]+计算值:480.30,实测值:480.59。 实施例170.(4r)-5-(3-((s)-37-((((苄氧基)羰基)氨基)氨基)-31,38-二氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32,39-二氮杂四十三酰胺基)-4-羟基苯基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯的合成。 在0℃下,向(4r)5-(3-(4-(4-氨基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(130g,174mmol,1.1eq)的dmf(500ml)溶液中依次加入tea(66ml,474mmol,3eq)和hatu(72g,190mmol,1.2eq)。然后将反应混合物升温至室温并搅拌2小时。在0℃下将(s)-37-((((苄氧基)羰基)氨基)-31-氧-2,5,8,11,14,17,20,23,26,29-十氧杂-32-氮杂三十八烷-38-酸(75.8g,158mmol,1.0eq)的dmf(500ml)溶液加入反应混合物,在室温搅拌1小时。将反应混合物倒入水(4l)中,水层用乙酸乙酯(3×500ml)萃取,合并有机层,用盐水(2l)洗涤,经硫酸钠干燥,浓缩,得到粗标题产物(190g),直接用于下一步。esimsm/z:c60h100n5o20[m+h]+计算值:1210.69,实测值:1210.69。 实施例171.(4r)-叔丁基5-(3-((s)-37-氨基-31,38-二氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32,39-二氮杂四十三酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸酯的合成。 将(4r)-叔丁基5-(3-((s)-37-(((苄氧基)羰基)氨基)-31,38-二氧基-2,5,8,11,14,17,20,23,26,29-癸氧基-32,39-二氮杂四十三酰胺基)-4-羟基苯基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸盐(190g)的粗产物溶解在甲醇(900ml)中,并和pd/c催化剂(10wt%,19g)混合,在室温下氢气(1atm)中搅拌过夜。过滤催化剂,减压浓缩滤液,将粗产物通过硅胶柱纯化,用(二氯甲烷/甲醇)梯度纯化,得到标题产物(105g,两步收率62%)为褐色油状物。esimsm/z:c52h95n5o18[m+h]+计算值:1077.65,实测值:1077.65。 实施例172.2-((6s,9s,12r,14r)-9-((s)-仲丁基)-14-羟基-6,12-二异丙基-2,2,5,11-四甲基-4,7,10-三氧基-3-氧代-5,8,11-三氮杂十四烷-14-基)噻唑-4-羧酸的合成。 向boc-n-me-l-val-oh(33mg,0.14mmol)的乙酸乙酯溶液中加入五氟苯酚(39mg,0.21mmol)及dcc(32mg,0.154mmol)。在室温下将反应混合物搅拌16小时,然后在硅藻土垫上过滤,并用乙酸乙酯洗涤。滤液浓缩并在dma(2ml)中重新溶解,然后加入2-((1r,3r)-3-((2s,3s)-2-氨基-n,3-二甲基戊酰胺)-1-羟基-4-甲基戊基)噻唑-4-羧酸(52mg,0.14mmol)和dipea(48.5μl,0.28mmol)。反应混合物在室温搅拌24小时,然后通过反相高效液相色谱(c18柱,10-100%乙腈/水)浓缩和纯化得到标题化合物(40.2mg,收率49%)。esimsm/z:c28h49n4o7s[m+h]+计算值:585.32,实测值:585.32。 实施例173.2-((6s,9s,12r,14r)-9-((s)-仲丁基)-6,12-二异丙基-2,2,5,11-四甲基-4,7,10,16-四氧杂-3,15-二氧杂-5,8,11-三氮杂十七烷-14-基)噻唑-4-羧酸的合成。 在0℃下,将2-((6s,9s,12r,14r)-9-((s)-仲丁基)-14-羟基-6,12-二异丙基-2,2,5,11-四甲基-4,7,10将(三氧杂-3-氧杂-5,8,11-十四烷-14-基)噻唑-4-甲酸(40mg,0.069mmol)溶解于吡啶(8ml)中,加入乙酸酐(20.4mg,0.2mmol),使反应物升温至室温并搅拌过夜,将混合物浓缩,通过硅胶柱纯化,用甲醇/二氯甲烷梯度洗脱,得到标题产物(48.1mg,收率)。esimsm/z:c30h51n4o8s[m+h]+计算值:627.33,实测值:627.33。 实施例174.(4r)-4-(2-(((6s,9s,12r,14r))-9-((s)-仲丁基)-6,12-二异丙基-2,2,5,11-四甲基-4,7,10,16-四氧代-3,15-二氧杂-5,8,11-三氮杂十四烷-14-基)噻唑-4-羧酰胺基)-2-甲基-5-苯基戊酸的合成。 将五氟苯酚(21.2mg,0.115mmol)和dcc(17.4mg,0.085mmol)加入到2-((6s,9s,12r,14r)-9-((s)-仲丁基)-6,12-二异丙基-2,2,5,11-四甲基-4,7,7,10,16-四氧基-3,15-二氧杂-5,8,11-三氮杂十七烷-14-基)噻唑-4-羧酸(48.1mg,0.077mmol)的乙酸乙酯溶液中。在室温下将反应混合物搅拌16小时,然后在硅藻土垫上过滤,并用乙酸乙酯洗涤。滤液浓缩并在dma(4ml)中重新溶解,然后加入(4r)-4-氨基-2-甲基-5-苯基戊酸(20.7mg,0.1mmol)和dipea(26.8μl,0.154mmol)。反应混合物在室温下搅拌24小时,然后通过反相hplc(c18柱,10-100%乙腈/水)浓缩和纯化,得到标题化合物(63mg,收率~100%)。esimsm/z:c42h66n5o9s[m+h]+计算值:816.45,实测值:816.45。 计算值175.(4r)-4-(2-((3s,6s,9r,11r)-6-((s)-仲丁基)-3,9-二异丙基-8-甲基-4,7,13-三氧基-12-氧杂-2,5,8-三氮杂十四烷-11-基)噻唑-4-甲酰胺基)-2-甲基-5-苯基戊酸盐酸盐的合成。 向(4r)-4-(2-((6s,9s,12r,14r)-9-((s)-仲丁基)-6,12-二异丙基-2,2,5,11-四甲基-4,7,10,16-四氧代-3,15-二氧杂-5,8,11-三氮杂十四烷-14-基)噻唑-4-甲酰氨基)-2-甲基-5-苯基戊酸(60mg,0.073mmol)的乙酸乙酯溶液(3ml)中加入盐酸(0.8ml,12m)。将混合物搅拌30分钟并用甲苯(5ml)和1,4-二氧六环(5ml)稀释。将混合物蒸发并与1,4-二氧六环(5ml)和甲苯(5ml)共蒸发至干。得到的粗标题产物(57.1mg,收率103%),不经纯化直接应用于下一步。esimsm/z:c37h58n5o7s[m+h]+计算值:716.40,实测值:716.60。 实施例176.(4r)-叔丁基-5-(3-(2-(2-((苄氧基)羰基)氨基)-丙酰胺基)乙酰氨基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸酯的合成。 将2-(2-((((苄氧基)羰基)氨基)丙酰胺基)乙酸(0.2g,0.7mmol),(4r)-叔丁基-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基氨基)-2-甲基戊酸酯(0.19g,0.48mmol)和hatu(0.18g,0.48mmol)溶解在二氯甲烷(20ml)中,然后加入tea(134ul,0.96mmol)。将反应混合物在室温搅拌过夜,减压浓缩并将残余物在硅胶柱上纯化,得到标题产物(0.3g,95%)。esimsm/z:c34h49n4o9[m+h]+计算值:657.34,实测值:657.34。 实施例177.(4r)-叔丁基-5-(3-(2-(2-(2-氨基丙酰胺基)乙酰氨基)-4-羟苯基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸酯的合成 在氢化瓶中,将pd/c(0.1g,33wt%,50%水),(4r)-叔丁基-5-(3-(2-(2-((((苄氧基))羰基)氨基)丙酰胺基)乙酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸酯(0.3g,0.46mmol)和甲醇(10ml)混合。将混合物在1个大气压的h2下振摇过夜,然后将通过硅藻土(助滤剂)过滤,并浓缩,得到标题化合物(0.21g,87%),其无需进一步纯化即可用于下一步。esimsm/z:c26h43n4o7[m+h]+计算值:523.31,实测值:523.31。 实施例178.2-羧基-n,n,n-三甲基丙烷-2-氨基溴化物的合成。 向2-溴-2-甲基丙酸(3.00g,17.9mmol)的四氢呋喃(30ml)的溶液中加入三甲胺(1mthf溶液,17.9ml,35.9mmol)。反应混合物在室温下搅拌过夜。通过过滤收集沉淀物,并用乙酸乙酯洗涤,得到呈白色固体的标题化合物(4.00g,理论产率)。esimsm/z:c7h16no2[m+h]+计算值:146,实测值:146。 实施例179.n,n,n,2-四甲基-1-氧代-1-(五氟苯氧基)丙-2-溴化铵的合成。 向2-羧基-n,n,n,n-三甲基丙烷-2-溴化铵(1.55g,6.9mmol)和五氟苯酚(2.50g,13.8mmol)的二氯甲烷(20ml)溶液中加入dcc(2.80g,13.8)。将反应混合物在室温搅拌过夜,将反应过滤,并在真空下浓缩,得到无色油状标题化合物,将其直接用于下一步。esimsm/z:c13h15f5no2[m+h]+计算值:312,实测值:312。 实施例180.(5r,7r,10s)-10-(仲丁基)-5-(4-(乙氧基羰基)噻唑-2-基)-3,3-二乙基-7-异丙基-n,n,n,8,13-五甲基-9,12-二氧代-4-氧杂-8,11-二氮杂-3-硅酸酯十三烷-13-铵的合成。 在0℃下,向2-((1r,3r)-3-((2s)-2-氨基-n,3-二甲基戊酰胺)-4-甲基-1-((三乙基甲硅烷基)氧基)戊)噻唑-4-乙基羧酸乙酯(1.78g,3.4mmol)和n,n,n,2-四甲基-1-氧-1-(五氟苯氧基)丙烷-2-铵溴化物(6.9mmol,10.4mmol)的dmf(20ml)中加入dipea(1.8ml)。将反应混合物升温至室温并搅拌1小时,然后在真空下浓缩,并通过硅胶柱(100:1至5:1二氯甲烷/甲醇)纯化,得到泡沫状标题化合物(1.20g,收率54%)。esimsm/z:c32h61n4o5ssi[m+h]+计算值:642,实测值:642。 实施例181.1-(((2s)-1-((1r,3r)-1-(4-(乙氧羰基)噻唑-2-基)-1-羟基-4-甲基戊烷-3-基)(甲基)氨基)-3-甲基-1-氧代戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-胺的合成。 将(5r,7r,10s)-10-(仲丁基)-5-(4-(乙氧基羰基)噻唑-2-基)-3,3-二乙基-7-异丙基-n,n,8,13-五甲基-9,12-二氧基-4-氧杂-8,11-二氮杂-3-十三烷-13-胺(1,20g,1,86mmol)溶解于acoh/thf/h2o(v/v/v3:1:1,20ml)并搅拌过夜。然后在真空下浓缩反应物,用于下一步,无需进一步纯化。esimsm/z:c26h47n4o5s[m+h]+计算值:527,实测值:527。 实施例182.1-(((2s)-1-(((1r,3r)-1-(4-羧基噻唑-2-基)-1-羟基-4-甲基戊烷-3-基)(甲基)氨基)-3-甲基-1-氧代戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-铵的合成。 向1-(((2s)-1-((((1r,3r)-1-(4-(乙氧基羰基)噻唑-2-基)-1-羟基-4-甲基戊基-3-基)(甲基)氨基)-3-甲基-1-氧代戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-铵(1.86mmol)的1,4-二氧六环(10ml)溶液加入1nnaoh(9.3ml)。然后将反应混合物搅拌2小时并在真空下浓缩。将残余物用水(10ml)稀释,并加入1nhcl以将ph调节至4。将混合物真空浓缩,得到标题化合物,为白色固体。esimsm/z:c24h43n4o5s[m+h]+计算值:499,实测值499。 实施例183.1-(((2s)-1-((1r,3r)-1-乙酰氧基-1-(4-羧噻唑-2-基)-4-甲基戊烷-3-基)(甲基)氨基)-3-甲基-1-氧代戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-铵的合成。 在0℃下,向1-(((2s)-1-(((1r,3r)-1-(4-羧基噻唑-2-基)-1-羟基-4-甲基戊烷-3-基-甲基)-3-甲基-3-甲基-1-氧代戊烷-2-基)-氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-铵(1.86mmol)的吡啶(10ml)溶液中加入乙酸酐(884μl,9.36mmol)。然后升温至室温并搅拌过夜。反应在真空下浓缩,然后用水(20ml)稀释并用乙酸乙酯(3×10ml)洗涤。在真空下浓缩水层,使标题化合物为黄色固体。esimsm/z:c26h45n4o6s[m+h]+计算值:541,实测值:541。 实施例184.1-(((2s)-1-((1r,3r)-1-乙酰氧基-4-甲基-1-(4-((五氟苯酚氧基)羰基)噻唑-2-基)戊烷-3-基)(甲基)氨基)-3-甲基-1-氧代戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-铵的合成。 向1-(((2s)-1-((((1r,3r)-1-乙酰氧基-1-(4-羧基噻唑-2-基)-4-甲基戊三-3-基)(甲基)氨基)-3-甲基-1-氧戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧丙烷-2-铵(150mg,0.277mmol)和五氟苯酚(76.5mg,0.415mmol)的二氯甲烷(2ml)溶液中加入edci(63.7mg,0.33mmol),将反应混合物搅拌小时并真空浓缩,得到标题化合物,为黄色油状物。esimsm/z:c32h44f5n4o6s[m+h]+计算值:707,实测值:707。 实施例185.(s)-4-异丙基-3-丙酰基丙二唑烷-2-酮的合成。 在约-70℃,n2中向(s)-4-异丙基恶唑烷-2-酮(400g,3.09mol,1.0eq)的四氢呋喃(8l)溶液中加入正丁基锂(2.5m正己烷溶液,1.36l,3.4mol,1.1eq)。将混合物在-70℃下搅拌1小时,然后缓慢加入丙酰氯(315g,3.4mol,1.1eq)。再将此混合物在-70℃下搅拌1小时,并逐渐升温至室温。将反应混合物加入到冰冷的饱和氯化铵溶液(7l)中,并用乙酸乙酯(3×2l)萃取。有机层用水(2l)和盐水(2l)依次洗涤,用硫酸钠干燥,过滤,浓缩并通过柱色谱法纯化(3kg硅胶,纯石油醚至5:1石油醚/乙酸乙酯),得标题化合物,为无色油状物(500g,收率87%)。esimsm/z:c9h16no3[m+h]+计算值:186.10,实测值:186.10。 实施例186.(s)-3-(4-(苄氧基)苯基)-2-((叔丁氧羰基)氨基)丙酸甲酯的合成。 向boc-l-tyr-ome(900g,3.05mol,1.0eq),k2co3(632g,4.58mol,1.5eq)和ki(20g,0.150mol,0.05eq)的乙腈混合物(3l)中缓慢加入苄基溴(547g,3.20mol,1.05eq)。然后将混合物回流并通过tlc监测。4小时后,将反应冷却至室温并过滤,将滤液浓缩并用水(3l)和乙酸乙酯(3.5l)稀释,分离有机相,用乙酸乙酯(2×1.5l)萃取水相。洗涤合并的有机层,依次用盐水(2×3l)洗涤,用硫酸钠干燥,过滤并浓缩。将从4批900g的和一批400g初始原料得到的产物混合,称重为5.4kg,然后用石油醚分18批打浆(每批4l石油醚)。收集固体,滤液浓缩后用硅胶柱层析法(4:1正己烷/乙酸乙酯)纯化,合并组分得到标题化合物,总重量为4.85千克白色固体(收率93%)。1hnmr(500mhz,cdcl3)δ7.43(d,j=7.0hz,2h),7.38(t,j=7.4hz,2h),7.32(t,j=7.2hz,1h),7.04(d,j=8.5hz,2h),6.91(d,j=8.6hz,2h),5.04(s,2h),4.55(d,j=6.9hz,1h),3.71(s,3h),3.03(qd,j=14.0,5.8hz,2h),1.43(s,9h)。esimsm/z:c22h28no5[m+h]+计算值:386.19,实测值:386.19。 实施例187.(s)-叔丁基(1-(4-(苄氧基)苯基)-3-氧代丙烷-2-基)氨基甲酸酯的合成。 在-78℃下,向(s)-3-(4-(苄氧基)苯基)-2-((叔丁氧基羰基)氨基)丙酸甲酯(288g,0.74mol,1.0eq.)的无水二氯甲烷中缓慢加入的dibal(在甲苯中1.5m,1.0l,2.0eq),加入完成后,继续搅拌2小时,然后将反应混合物倒入冰水(2l)中。加入2nhcl(2l)以溶解形成的白色沉淀。分离有机相,水相用二氯甲烷(2×500ml)萃取。将合并的有机相用2nhcl(500ml)和水(500ml)洗涤,用无水硫酸钠干燥,过滤并浓缩。将粗产物溶于二氯甲烷(1l)中并上样到硅胶柱(1kg硅胶),用二氯甲烷洗脱。浓缩洗脱溶液并用石油醚/乙酸乙酯打浆,得到标题化合物的白色固体(152g,收率57%)。1hnmr(500mhz,cdcl3)δ9.65(s,1h),7.45(d,j=7.1hz,2h),7.41(t,j=7.4hz,2h),7.35(t,j=7.1hz,1h),7.11(d,j=8.6hz,2h),6.95(d,j=8.6hz,2h),5.07(s,2h),4.42(dd,j=12.4,6.1hz,1h),3.09(d,j=6.2hz,2h),1.46(s,9h)。esimsm/z:c21h26no4[m+h]+计算值:356.18,实测值:356.19。在柱子上也收集到了过度还原的产物醇(65克)。 实施例188.((2s,3s,4s)-1-(4-(苄氧基)苯基)-3-羟基-5-((s)-4-异丙基-2-氧代恶唑烷-3-基)-4-甲基-5-氧代戊烷-2-基)氨基甲酸叔丁酯的合成。 在室温下,向(s)-4-异丙基-3-丙酰基丙二唑烷-2-酮(92.6g,0.50mol,1.1eq)的无水二氯甲烷溶液(1.5l)中加入dipea(70.5g,0.54mol,1.2eq)。将混合物冷却至-10℃,并在n2下加入n-bu2botf(在1.0m二氯甲烷中,500ml,1.1eq)。在加入期间,反应混合物的温度保持在0℃以下。然后将反应在0℃下搅拌1小时,然后冷却至-78℃,逐滴加入(s)-4-异丙基-3-丙酰基恶唑烷丁-2-酮(161g,0.45mol,1.0eq)的二氯甲烷(1l)溶液。在加入期间,反应混合物的温度控制在0℃以下。将混合物在-78℃下搅拌2小时,然后缓慢升温至室温并搅拌过夜。加入pbs(0.1m,ph7.0,2l)。相分离后,将水相进一步用二氯甲烷(2×500ml)萃取。合并的有机层经无水硫酸钠干燥,过滤并浓缩。将粗产物再溶解于甲醇(2l)中,冷却至0℃,然后与h2o2(30%水溶液,500ml)混合并搅拌1小时。通过旋转蒸发除去甲醇,并加入水(3l)。所得混合物用二氯甲烷(3×800ml)萃取。用水(500ml),饱和碳酸氢钠(500ml)和盐水(500ml)洗涤合并有机层,用无水硫酸钠干燥,过滤并浓缩。将残余物与400g硅胶混合,并通过柱色谱法纯化(2kg硅胶,石油醚至5:1石油醚/乙酸乙酯),得到标题化合物,为泡沫状固体(150g,收率61%)。1hnmr(400mhz,cdcl3)δ7.36(ddd,j=24.2,14.2,7.1hz,5h),7.12(d,j=8.4hz,2h),6.90(d,j=8.5hz,2h),5.02(s,2h),4.69(d,j=9.0hz,1h),4.45(d,j=4.1hz,1h),4.33(t,j=8.4hz,1h),4.15(d,j=8.6hz,1h),3.90(dd,j=16.6,8.0hz,1h),3.85–3.77(m,2h),2.81(d,j=7.6hz,2h),2.27(dd,j=11.4,6.7hz,1h),1.35(s,9h),0.89(dd,j=14.3,6.9hz,6h)。esimsm/z:c30h41n2o7[m+h]+计算值:541.28,实测值:541.30。 实施例189.o-((2s,3s,4s)-5-(4-(苄氧基)苯基)-4-((叔丁氧基羰基)氨基)-1-((s)-4-异丙基-2-氧杂恶唑烷-3-基)-2-甲基-1-氧杂戊烷-3-基)1h-咪唑-1-碳硫酸酯的合成。 将((2s,3s,4s)-1-(4-(苄氧基)苯基)-3-羟基-5-((s)-4-异丙基-2-氧恶唑烷-3-基)-4-甲基-5-氧杂戊烷-2-基)氨基甲酸叔丁酯(200g,0.37mol,1.0eq)和1,1′-硫代羰基二咪唑(198g,1.11mol,3.0eq)在无水四氢呋喃(3.5l)中得混合物回流8小时。之后补充加入1,1’-硫代羰基二咪唑(65g,0.37mol,1.0eq),并将混合物回流过夜。通过旋转蒸发除去四氢呋喃,将残余物与500g硅胶混合,并通过柱色谱法纯化(2kg硅胶,石油醚至3:1石油醚/乙酸乙酯),得到标题化合物,为黄色泡沫状物(170g,收率83%)。1hnmr(400mhz,cdcl3)δ8.41(s,1h),7.67(s,1h),7.36(dt,j=16.0,6.9hz,6h),7.09(s,1h),7.05(d,j=8.4hz,2h),6.86(d,j=8.4hz,2h),6.32(d,j=9.5hz,1h),5.01(s,2h),4.56–4.43(m,2h),4.32(ddd,j=16.2,15.6,7.8hz,3h),4.19(d,j=8.7hz,1h),2.96(dd,j=14.6,4.4hz,1h),2.49(dd,j=14.5,10.5hz,1h),2.29(td,j=13.4,6.7hz,1h),1.73(s,1h),1.29(s,9h),0.91(dd,j=13.9,6.9hz,6h)。esimsm/z:c34h43n4o7s[m+h]+计算值:651.27,实测值:651.39。 实施例190.((2r,4s)-1-(4-(苄氧基)苯基)-5-((s)-4-异丙基-2-氧代恶唑烷-3-基)-4-甲基-5-氧戊烷-2-基)氨基甲酸叔丁酯的合成。 向o-((2s,3s,4s)-5-(4-(苄氧基)苯基)-4-((叔丁氧羰基)氨基)-1-((s)-4-异丙基-2-氧杂恶唑烷-3-基)-2-甲基-1-氧杂戊烷-3-基)1h-咪唑-1-碳硫酸酯(210g,0.323mol,1.0eq)的无水甲苯(3l)溶液中依次加入n-bu3snh(182g,0.646mol,2.0eq)和偶氮二异丁腈(0.5g,3.23mmol,0.1eq)。将混合物回流1.0小时,然后浓缩。将残余物与500g硅胶混合并通过柱色谱法纯化(2kg硅胶,石油醚至5:1石油醚/乙酸乙酯),得到标题化合物,为白色泡沫状物(141g,收率83%)。1hnmr(400mhz,cdcl3)δ7.36(ddd,j=24.5,14.5,7.1hz,5h),7.08(d,j=8.5hz,2h),6.90(d,j=8.5hz,2h),5.04(d,j=5.1hz,2h),4.48(d,j=4.2hz,1h),4.33(t,j=8.4hz,1h),4.22(d,j=9.7hz,1h),4.15(d,j=8.8hz,1h),3.81(s,2h),2.73(dd,j=14.1,5.9hz,1h),2.61(dd,j=14.0,7.2hz,1h),2.29(dq,j=13.5,6.8hz,1h),2.11–2.00(m,1h),1.60(dd,j=15.2,6.2hz,2h),1.35(s,9h),1.20(d,j=6.9hz,3h),0.89(dd,j=14.0,6.9hz,6h)。esimsm/z:c30h41n2o6[m+h]+计算值:525.28,实测值:525.37。 实施例191.(2s,4r)-5-(4-(苄氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸的合成。 在0℃下,向((2r,4s)-1-(4-(苄氧基)苯基)-5-((s)-4-异丙基-2-氧代恶唑烷-3-基)-4-甲基-5-酮戊烷-2-基)氨基甲酸叔丁酯(208g,0.39mol,1.0eq)的四氢呋喃(2.1l)和水(700ml)溶液中加入lioh(23.7g,0.99mmol,2.5eq)的h2o2溶液(30%水溶液,336ml,2.97mol,7.6eq)。在0℃下搅拌3小时后,加入亚硫酸氢钠溶液(1.5m,2l)以淬灭反应,滴加2nhcl直至达到ph4。然后用乙酸乙酯(3×800ml)萃取反应混合物。乙酸乙酯溶液用水(500ml)和盐水(500ml)洗涤,用无水硫酸钠干燥,过滤并浓缩。将残余物与硅胶(400g)混合并通过柱色谱(2kg硅胶,石油醚至3:1石油醚/乙酸乙酯)纯化,得到标题化合物,为白色固体(158g,收率96%)。1hnmr(400mhz,cdcl3)δ7.46–7.28(m,5h),7.07(d,j=7.7hz,2h),6.91(d,j=7.8hz,2h),5.04(s,2h),4.52(d,j=8.5hz,1h),3.87(d,j=41.8hz,1h),2.82–2.43(m,3h),1.85(t,j=12.2hz,1h),1.41(s,9h),1.17(d,j=6.9hz,3h)。esimsm/z:c24h32no5[m+h]+计算值:414.22,实测值:414.21。 实施例192.(2s,4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基苯基)-2-甲基戊酸的合成。 将(2s,4r)-5-(4-(苄氧基)苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸(158g,0.38mol,1.0eq.)和pd/c(10%,15g)的甲醇(1.5l)溶液在1atmh2下反应16小时,然后通过硅藻土(助滤剂)过滤。浓缩滤液,得到标题化合物,为白色固体(123g,收率>100%)。1hnmr(400mhz,cdcl3)δ7.00(d,j=7.5hz,2h),6.80(s,2h),4.51(d,j=9.0hz,1h),3.88(s,1h),2.66(dd,j=65.6,22.6hz,4h),1.88(t,j=12.2hz,1h),1.42(s,9h),1.14(d,j=6.6hz,3h)。esimsm/z:c17h26no5[m+h]+计算值:324.17,实测值:324.16。 实施例193.(2s,4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸的合成。 向(2s,4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基苯基)-2-甲基戊酸(113g,0.35mol,1.0eq.)的四氢呋喃(1.5l)溶液中逐滴加入t-buono(360g,3.5mol,10.0eq),并在室温下搅拌3小时,然后与硅胶(300g)混合并浓缩,装载在柱(1.5kg硅胶)上,用石油醚洗脱(5:1石油醚/乙酸乙酯和2:1石油醚/乙酸乙酯),得到标题化合物,为黄色固体(85g,收率61%)。1hnmr(400mhz,dmso)δ12.00(s,1h),10.68(s,1h),7.67(s,1h),7.34(d,j=8.4hz,1h),7.03(d,j=8.4hz,1h),6.69(d,j=8.9hz,1h),3.56(d,j=3.8hz,1h),2.67(dd,j=13.5,5.1hz,1h),2.41(dd,j=13.8,6.6hz,1h),1.78–1.65(m,1h),1.27(s,9h),1.18(s,1h),1.05(d,j=7.1hz,3h)。esimsm/z:c17h25n2o7[m+h]+计算值:369.15,实测值:369.14。 实施例194.(2s,4r)-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸的合成。 将(2s,4r)-4-((叔丁氧基羰基)氨基)-5-(4-羟基-3-硝基苯基)-2-甲基戊酸(51.6g,0.14mol,1.0eq.)和pd/c(10wt%,5g)的甲醇(500ml)溶液在室温下氢化(1atm)反应2小时,然后通过硅藻土(助滤剂)过滤。浓缩滤液,得到标题化合物,为棕色泡沫状物(43.8g,收率93%)。esimsm/z:c17h27n2o5[m+h]+计算值:339.18,实测值:339.17。 实施例195.4-((苄氧基)羰基)氨基)丁酸的合成。 在-20℃下,向naoh(23.3g,0.58mol,2.0eq)的水(140ml)溶液中加入4-氨基丁酸(30.0g,0.29mol,1.0eq)和四氢呋喃(60ml),然后逐滴加入cbzcl(54ml,0.38mol,1.3eq)的四氢呋喃(57ml)溶液。将反应混合物在室温下搅拌4小时,然后浓缩并用乙酸乙酯(4×100ml)洗涤。加入浓盐酸调节溶液ph至3,用乙酸乙酯(4×150ml,2×100ml)萃取,合并的有机相用盐水洗涤,用无水硫酸钠干燥,过滤并浓缩,得到标题化合物,为白色固体(48.3g,70.3%)。esimsm/z:c12h16no4[m+h]+计算值:238.1,实测值:238.1。 实施例196.4-(((苄氧基)羰基)氨基)丁酸叔丁酯的合成。 在0℃下,向4-((((苄氧基)羰基)氨基)丁酸(48.0g,0.2mol,1.0eq)和t-buoh(58.0ml,0.6mol,3.0eq)的无水二氯甲烷(480ml)溶液中加入dcc(50.0g,0.24mol,1.2eq)和dmap(2.5g,0.02mol,0.1eq),然后将混合物升温至室温并搅拌过夜。滤出固体并将滤液浓缩,然后用乙酸乙酯(400ml)稀释,并用5%碳酸氢钠溶液和盐水洗涤,经无水硫酸钠干燥,过滤,然后浓缩。残余物通过硅胶柱色谱纯化(石油醚/乙酸乙酯=5∶1),得到标题化合物,为无色油状物(32.8g,55.1%)。esimsm/z:c16h24no4[m+h]+计算值:294.2,实测值:294.2。 实施例197.4-氨基丁酸叔丁酯的合成。 在氢化瓶中,向4-((((苄氧基)羰基)氨基)丁酸叔丁酯(29.0g,0.099mol,1.0eq.)的甲醇(100ml)溶液中加入pd/c(2.9g,10%pd/c,50%水)。将混合物在1atmh2下振动过夜。将反应混合物过滤,并将滤液浓缩,得到标题化合物,为无色油状物(13.8g,收率83.7%)。esimsm/z:c8h18no2[m+h]+计算值:160.1,实测值:160.1。 实施例198.2,5,8,11,14,17,20,23,26-壬氧二十八烷-28-酸叔丁酯的合成。 将nah(60%,24g,600mmol)加入到八乙二醇单甲醚(115g,300mmol)的四氢呋喃(3.0l)溶液中。在室温搅拌后搅拌1小时,将2-溴乙酸叔丁酯(146g,750mmol)加入到混合物中,并在室温搅拌1小时。然后将混合物用二氯甲烷(4l)稀释并倒入冰水(2kg)中。分离有机相,水相用二氯甲烷(1l)萃取。合并的有机相用水洗涤,用无水硫酸钠干燥。通过柱色谱法纯化(20%乙酸乙酯/石油醚,然后纯二氯甲烷至5%甲醇/二氯甲烷洗脱),得到标题化合物,为黄色油状物(108g,收率72%)。 实施例199.2,5,8,11,14,17,20,23,26-九氧杂二十八烷-28-酸的合成。 将2,5,8,11,14,17,20,23,26-九氧杂二十八烷-28-叔丁酯(210g,422mmol)溶解在二氯甲烷(400ml)和无水甲酸(1l)中。将所得溶液在室温搅拌,过夜。真空除去所有挥发物,得到标题化合物,为黄色油状物(200g,收率>100%)。 实施例200.2,5,8,11,14,17,20,23,26-九氧杂二十八烷-28-酰氯的合成。 于室温下将2,5,8,11,14,17,20,23,26-九氧杂二十八烷-28-酸(198g,422mmol)溶于二氯甲烷(2.6l),加入(cocl)2(275ml)和dmf(0.5ml)。将所得溶液在室温持续搅拌3小时。真空除去所有挥发物,得到标题化合物,为黄色油状物(210g,收率>100%)。 实施例201.(s)-34-(((苄氧基)羰基)氨基)-28-氧-2,5,8,11,14,17,20,23,26-九氧杂-29-氮杂三十五烷-35-酸的合成。 将z-l-lys-oh(236g,844mmol),na2co3(89.5g,844mmol)和naoh(33.8g,844mmol)溶于水(1.6l)中。并将混合物用冰盐浴冷却至0℃以下,向其中加入2,5,8,11,14,17,20,23,26-九氧杂二十八烷-28-酰氯(210g,422mmol)的四氢呋喃溶液(160ml)。将所得混合物在室温下搅拌1小时,然后用乙酸乙酯(1l)稀释。分离水层,在冰浴上使用浓hcl将ph调节至3。用二氯甲烷萃取,将有机层用盐水洗涤,用硫酸钠干燥并浓缩,得到标题化合物,为黄色油状物(290g,收率97%)。 实施例202.(s)-五氟苯基34-(((苄氧基)羰基)氨基)-28-氧代-2,5,8,11,14,17,20,23,26-九氧杂-29-氮杂三十五烷-35-酯的合成。 向(s)-34-(((苄氧基)羰基)氨基)-28-氧杂-2,5,8,11,14,17,20,23,26-九氧杂-29-氮杂三十五烷-35-酸(183g,260mmol)的二氯甲烷(2l)溶液中加入五氟苯酚(95.4g,520mmol)和dic(131g,1.04mol)。将反应在室温下搅拌1小时,然后浓缩,得到粗标题产物(430g)。 实施例203.(s)-34-(((苄氧基)羰基)氨基)-28,35-二氧代-2,5,8,11,14,17,20,23,26-九氧杂-29,36-二氮杂四十烷-40-叔丁酯的合成。 在0℃下,向4-氨基丁酸叔丁酯(62.0g,390mmol)的dmf(1.5l)溶液中加入dipea(134g,1.04mol),然后在10-20℃下加入(s)-五氟苯基34-((苄氧基)羰基)-氨基)-28-氧代-2,5,8,11,14,17,20,23,26-九氧杂-29-氮杂三十五烷-35-酯(430g,粗制),将所得混合物在室温下搅拌1小时。在真空下除去dmf,残留物用二氯甲烷稀释,用水洗涤。水相用二氯甲烷反萃取。合并的有机相用0.2nhcl和盐水洗涤,用无水硫酸钠干燥,过滤并浓缩。柱色谱(25%乙酸乙酯/石油醚至纯乙酸乙酯,然后0-5%甲醇/二氯甲烷)纯化,得到黄色油状标题化合物(180g,收率82%)。 实施例204.(s)-34-氨基-28,35-二氧代-2,5,8,11,14,17,20,23,26-九氧杂-29,36-二氮杂四十烷-40-叔丁酯的合成。 向(s)-34-(((苄氧基)羰基)氨基)-28,35-二氧代-2,5,8,11,14,17,20,23,26-九氧杂-29,36-二氮杂四十烷-40-叔丁酯(78.0g,92.3mmol,1.0eq.)的甲醇(500ml)溶液中加入pd/c(13g,10%pd/c,50%水)。将混合物在1atmh2下室温反应过夜,然后过滤并浓缩。通过柱色谱法(0-20%甲醇/二氯甲烷)纯化残余物,得到标题化合物,为绿黄色油状物(70.2g,收率92%)。 实施例205.11-(苄氧基)-11-氧杂十一烷酸的合成。 向十一烷二酸(1.73g,8mmol)的dmf(30ml)溶液中加入k2co3(1.1g,8mmol)和bnbr(1.36g,8mmol)。将混合物在室温搅拌过夜,然后浓缩,并通过柱色谱法(石油醚/乙酸乙酯)纯化,得到标题化合物(1.1g,收率45%)。esimsm/z:c18h27o4[m+h]+计算值:307.18,实测值307.15。 实施例206.3-(2-(2-(二(苄基氨基)乙氧基)乙氧基)丙酸的合成。 向3-(2-(2-(2-(二(苄基氨基)乙氧基)乙氧基)丙酸叔丁酯(2.00g,4.84mmol)的二氯甲烷(5ml)溶液中加入hco2h(5ml)。将反应物在室温下搅拌过夜,然后浓缩至干,并与二氯甲烷共蒸发两次,并将残余物置于油泵上抽干,得到标题化合物(1.72g,收率)。esimsm/z:c21h27no4[m+h]+计算值:358.19,实测值:358.19。 实施例207.2-苄基-11-氧代-1-苯基-5,8,15,18-四氧杂-2,12-二氮杂二十一烷-21-叔丁酯的合成。 在0℃下,向3-(2-(2-(2-(二苄基氨基)乙氧基)乙氧基)丙酸(1.12g,4.83mmol)和3-(2-(2-(2-氨基乙氧基)乙氧基)丙酸叔丁酯(1.72g,4.83)的二氯甲烷(30ml)溶液中加入hatu(1.83g,4.83mmol)和tea(0.68ml,4.83mmol)。反应升温至室温,并搅拌1小时,然后用50ml二氯甲烷稀释,倒入装有50ml水的分液漏斗中。分离有机相,并用盐水(50ml)洗涤,经无水硫酸钠干燥,过滤并浓缩。残余物通过柱色谱法(甲醇/二氯甲烷)纯化,得到标题化合物(2.21g,收率80%)。esimsm/z:c32h48n2o7[m+h]+计算值:573.35,实测值573.35。 实施例208.1-氨基-9-氧代-3,6,13,16-四氧杂-10-氮杂十九烷-19-叔丁酯的的合成。 在氢化瓶中,向2-苄基-11-苄基-1-氧-1-苯基叔丁基-5,8,15,18-四氧杂-2,12-二氮杂二十烷-21-叔丁酯(2.21g,3.86mmol)的甲醇(20ml)溶液中加入pd/c(10wt%,0.2g)。将混合物在1atmh2下搅拌过夜,通过硅藻土(助滤剂)过滤,并将滤液浓缩,得到标题化合物(1.5g,收率)。esimsm/z:c18h36n2o7[m+h]+计算值:393.25,实测值:393.25。 实施例209.31-苄基1-叔丁基11,21-二氧代-4,7,14,17-四氧杂-10,20-二氮杂三十一烷-1,31-二酯的合成。 向1-氨基-9-氧代-3,6,13,16-四氧杂-10-氮杂十九烷-19-叔丁酯(1.50g,3.86mmol)和11-(苄氧基)-11-氧杂十一酸(1.10g,3.6mmol)的二氯甲烷(50ml)溶液中加入hatu(1.48g,3.9mmol)和tea(0.55ml,3.9mmol)。将反应混合物在室温下搅拌1小时,然后用50ml二氯甲烷稀释并倒入含有50毫升水的分液漏斗中。分离有机相,用盐水(50ml)洗涤,用无水硫酸钠干燥,过滤并浓缩。通过柱色谱法(甲醇/二氯甲烷)纯化残余物,得到标题化合物(1.50g,61%收率)。esimsm/z:c36h61n2o10[m+h]+计算值:681.42,实测值:681.42。 实施例210.3,13,23-三氧-1-苯基-2,17,20,27,30-五氧杂-14,24-二氮杂三十三烷-33-酸的合成。 向31-苄基1-11,21-二氧代-4,7,14,17-四氧杂-10,20-二氮杂三十一烷-1,31-二酯(1.50g,2.2mmol)的二氯甲烷(1ml)溶液中加入tfa(3ml)。将反应在室温下搅拌1小时,然后浓缩至干并用二氯甲烷共浓缩两次,并将残余物置于油泵上抽干,得到标题化合物(0.09g,2.2mmol,粗产物)。esimsm/z:c32h53n2o10[m+h]+计算值:625.36,实测值:625.35。 实施例211.(s)-39-(((苄氧基)羰基)氨基)-3,13,23,33-四氧代-1-苯基-2,17,20,27,30-五氧杂-14,24,34-三氮杂四十烷-40-酸的合成。 向3,13,23-三氧代-1-苯基-2,17,20,27,30-五氧杂-14,24-二氮杂三十三烷-33-酸(1.50g,2.20mmol)和z-lys-oh(0.62g,2.20mmol)的二氯甲烷(50ml)溶液中加入hatu(0.84g,2.20mmol)和tea(0.31ml,2.20mmol)。将反应混合物在室温下搅拌1小时,然后用50ml二氯甲烷稀释,倒入含有100ml水的分液漏斗中。分离有机相,并用盐水(100ml)洗涤,经无水硫酸钠干燥,过滤并浓缩。残余物通过柱色谱法(甲醇/二氯甲烷)纯化,得到标题化合物(1.00g,收率53%)。esimsm/z:c46h71n4o13[m+h]+计算值:887.49,实测值:887.50。 实施例212.(s)-5-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-3,11,21,31-四氧-1-苯基-2,14,17,24,27-五氧杂-4,10,20,30-四氮杂四十一烷-41-苄酯的合成。 向(s)-39-((((苄氧基)羰基)氨基)氨基)-3,13,23,33-四氧-1–1-苯基-2,17,20,27,30-五氧杂-14,24,34-三氮杂四十烷-40-酸(0.50g,0.56mmol)的dmf(5ml)溶液中加入hatu(0.21g,0.56mmol),在室温下搅拌反应30分钟。之后在0℃下,依次加入(2s,4r)5-(3-(4-(氨基氨基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.27g,0.56mmol))的dmf(5ml)的溶液和tea(85μl,0.6mmol),并将反应搅拌1小时。将反应混合物倒入装有100ml水的分液漏斗中,并用50ml乙酸乙酯萃取两次。将有机相用100ml盐水洗涤一次,用无水硫酸钠干燥,过滤并浓缩。通过柱色谱(甲醇/二氯甲烷)纯化残余物,得到标题化合物(0.40g,收率55%)。esimsm/z:c71h110n7o18[m+h]+计算值:1348.78,实测值:1348.78。 实施例213.(s)-5-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基甲酰基)-3,11,21,31-四氧代-1-苯基-2,14,17,24,27-五氧杂-4,10,20,30-四氮四十一烷-41-苄酯的合成。 向(s)-39-(((苄氧基)羰基)氨基)-3,13,23,33-四氧代-1-苯基-2,17,20,27,30-五氧杂-14,24,34-三氮杂四十烷-40-酸(0.50g,0.56mmol)的dmf(5ml)溶液中加入hatu(0.21g,0.56mmol),并将反应在室温下搅拌30分钟。之后在0℃下,加入(2s,4r)-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.22g,0.56mmol)的dmf(5ml)溶液和tea(85μl,0.60mmol)。搅拌1小时后,将反应混合物倒入含有100ml水的分液漏斗中,用50ml乙酸乙酯萃取两次。分离有机相并用100ml盐水洗涤,用无水硫酸钠干燥,过滤并浓缩。通过柱色谱法(甲醇/二氯甲烷)纯化残余物,得到标题化合物(0.20g,收率26%)。esimsm/z:c67h103n6o17[m+h]+计算值:1263.73,实测值:1263.73。 实施例214.3,3′-((氧基双(乙烷-2,1-二基))双(氧化))丙二酸二叔丁酯的合成。 向二甘醇(20g,0.188mol)的四氢呋喃(200ml)溶液中加入na(0.43g,0.018mol)。在室温下搅拌1小时后,加入丙烯酸叔丁酯(48g,0.376mol)并将反应混合物在室温下搅拌2天。将反应物真空浓缩并通过柱色谱纯化,得到标题化合物(34g,收率50%)。esimsm/z:c18h35o7[m+h]+计算值:363.23,实测值:363.23。 实施例215.3,3′-((氧基双(乙烷-2,1-二基))双(氧基))二丙酸的合成。 在室温下,将3,3′-((氧双(乙烷-2,1-二基))双(氧))二丙酸二叔丁酯(34g,0.093mol)溶解在甲酸(100ml)中并搅拌过夜,将反应真空浓缩,得到标题化合物。esimsm/z:c10h19o7[m+h]+计算值:251.11,实测值:251.11。 实施例216.2,2-二甲基-4、14、24-三氧杂-3、7、10、17、20、27、30、33-八氧杂-13、23-二氮杂三十六烷-36-酸的合成。 向1-氨基-9-氧代-3,6,6,16-四氧杂-10-氮杂十九烷-19-叔丁酯(1.50g,3.82mmol)和3,3′-((氧化双(乙烷-2,1,1-二基))双(氧基))丙二酸(1.90g,7.64mmol)的dmf(10ml)溶液中加入hatu(1.45g,3.82mmol)和dipea(0.66ml,3.82mmol)。在0℃下将反应混合物升温至室温并搅1小时,然后用二氯甲烷(80ml)稀释,用水(10ml)洗涤,用硫酸钠干燥,过滤,浓缩并通过硅胶柱色谱法纯化,得到标题化合物,为无色液体(1.75g,收率75%)。esimsm/z:c28h53n2o13[m+h]+计算值:625.35,实测值:625.35。 实施例217.1-叔丁基33-(2,5-二氧代吡咯烷-1-基)11,21-二氧代-4,7,14,17,24,27,30-七氧杂-10,20-二氮杂三恶烷-1,33-二酯的合成。 在0℃下,向2,2-二甲基-4,14,24-三氧杂-3,7,10,17,20,27,30,33-八氧杂-13,23-二氮杂三十六烷-36-酸(1.75g,2.8mmol)的二氯甲烷(20ml)溶液中加入edci(1.07g,5.6mmol)和nhs(0.64g,5.6mmol)。将反应升温至室温并搅拌过夜,然后用二氯甲烷(80ml)稀释,用水(10ml)洗涤,再用硫酸钠干燥,过滤并真空浓缩,得到标题化合物(2.00g,收率约100%)。esimsm/z:c32h56n3o15[m+h]+计算值:722.36,实测值:722.36。 实施例218.(s)-42-(((苄氧基)羰基)氨基)-2,2-二甲基-4,14,24,36-四氧代-3,7,10,17,20,27,30,33-八氧杂-13,23,37-三氮杂四十三烷-43-酸的合成。 向n-α-cbz-l-赖氨酸(1.17g,4.2mmol)的水(10ml)溶液中加入碳酸氢钠(0.47g,5.6mmol),将反应混合物冷却至5℃,之后加入1-叔丁基33-(2,5-二氧代吡咯烷-1-基)11,21-二氧代-4,7,14,17,24,27,30-七氧杂-10,20-二氮杂三恶烷-1,33-二酯(2.00g,2.8mmol)的1,4-二氧六环(10ml)溶液。将反应升温至室温并搅拌1小时,加入1nhcl将ph调节至3,用二氯甲烷(50ml×3)萃取。将有机萃取物用水(20ml)洗涤,用硫酸钠干燥,过滤并浓缩,得到标题产物(2.3g,收率92%)。esimsm/z:c42h71n4o16[m+h]+计算值:887.48,实测值:887.48。 实施例219.(s)-5-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-3,11,23,33-四氧代-1-苯基-2,14,17,20,27,30,37,40-八氧杂-4,10,24,34-四氮杂四十三烷-43-叔丁酯的合成。 在0℃下,向(2s,4r)-5-(3-(4-氨基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(1.87g,3.9mmol)和(s)-42-(((苄氧基)-羰基)氨基)-2,2-二甲基-4,14,24,36-四氧代-3,7,10,17,20,27,30,33-十氧杂-13,23,37-三氮杂四十三烷-43-酸(2.3g,2.59mmol)的二氯甲烷(30ml)中加入hatu(0.98g,2.59mmol)和dipea(450μl,2.59mmol)。将反应混合物升温至室温并搅拌1小时,然后真空浓缩并通过硅胶柱色谱纯化,得到标题化合物(2.4g,70%收率)。esimsm/z:c67h110n7o21[m+h]+计算值:1348.77,实测值:1348.77。 实施例220.(s)-43苄基1-叔丁基7-(((苄氧基)羰基)氨基)-6,13,23,33-四氧代-16,19,26,29-四氧杂-5,12的合成,22,32-四氮杂四十三烷-1,43-二酯的合成。 将(s)-39-((苄氧基)羰基)氨基)-3,13,23,33-四氧代-1-苯基-2,17,20,27,30-五氧杂-14,24,34-三氮杂十四烷-40-酸(200mg,0.225mmol)溶于dmf(5ml)中并冷却至0℃,依次加入4-氨基丁酸叔丁酯(71.8mg,0.45mmol)和edc(86.2mg,0.45mmol)。将反应升温至室温并搅拌过夜,倒入冰水中,并用二氯甲烷(3×10ml)萃取。将合并的有机相用水(5ml),盐水(5ml)洗涤,用无水硫酸钠干燥,过滤并浓缩,得到标题化合物(231mg,100%收率)。esimsm/z:c54h86n5o14[m+h]+计算值:1028.61,实测值:1028.61。 实施例221.(s)-43苄基1-(2-((s)-39-(((苄氧基)羰基)氨基)-3,13,23,33,40-五氧代-1-苯基-2,17,20,27,30-五氧杂-14,24,34,41-四氮杂四十五酰胺基)-4-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基)7-((苄氧基)羰基)氨基)-6,13,23,33-四氧代-16,19,26,29-四氧杂-5,12,22,32-四氮杂四十三烷-1,43-二酯的合成。 将(s)-43-苄基1-叔丁基7-((((苄氧基)羰基)氨基)-6,13,23,33-四氧代-16,19,26,29-四氧杂-5,12,22,32-四氮杂四十三烷-1,43-二酯(231mg,0.225mmol)溶于二氯甲烷(3ml)中,并在室温下于tfa(3ml)反应1小时。将反应浓缩并重新溶解在dmf(5ml)中,冷却至0℃,向(2s,4r)-5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(44mg,0.112mmol)中依次加入hatu(86mg,0.225mmol)和dipea(39μl,0.225mmol)。将反应升温至室温并搅拌过夜,倒入冰水中,并用二氯甲烷(3×10ml)萃取。将合并的有机相用1nhcl(5ml),水(5ml),盐水(5ml)洗涤,用无水硫酸钠干燥,过滤并浓缩,通过硅胶柱色谱法(0-5%甲醇/二氯甲烷),得到白色泡沫状物(209mg,收率81%)。esimsm/z:c121h185n12o31[m+h]+计算值:2302.32,实测值:2302.80。 实施例222.(s)-7-氨基-1-((2-((r)-7-氨基-42-羧基-6,13,23,33-四氧代-16,19,26,29-四氧代-5,12,22,32-四氮杂-1-酰基)氧基)-5-((2r,4s)-5-(叔丁氧基)-2-(叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基)氨基-1,6,13,23,33-五氧杂-16,19,26,29-四氧杂-5,12,22,32-四氮杂四十三烷-43-酸的合成 将(s)-43苄基1-(2-((s)-39-((((苄氧基)羰基)氨基)-3,13,23,33,40-五氧代-1-苯基-2,17,20,27,30-五氧杂-14,24,34,41-四氮杂戊四酮氨基)-4-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基)7-((苄氧基)-羰基)氨基)-6,13,23,33-四氧代-16,19,26,29-四氧杂-5,12,22,32-四氮杂四十三烷-1,43-二酯(206mg,0.089mmol)溶于甲醇(5ml)中,并与pd/c(10wt%,20mg)混合,在1atm压力h2下反应过夜。然后将混合物通过硅藻土(助滤剂)过滤,浓缩滤液,得到标题化合物(166mg,收率100%)。esimsm/z:c91h161n12o27[m+h]+计算值:1854.15,实测值:1854.80。 实施例223.1,1′-(((8r,27s)-36-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5)-氧代戊基)-17,18-双(2-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)乙酰基)-2,7,10,15,20,25,28,33-八氧代-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34-十二烷二氢-2h-苯并[b][1,4,9,12,17,20,21,24,29,32]氧杂九氮杂环三十六烷-8,27-二基)双(6,16,26-三氧代-9,12,19,22-四氧杂-5,15,25-三氮杂三十六烷-36-酸)的合成。 在0℃下,向(s)-7-氨基-1-((2-((r)-7-氨基-42-羧基-6,13,23,33-四氧代-16,19,26,29-四氧杂-5,12,22,32-四氮杂四十二烷-1-酰基)氧基)-5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)苯基)氨基)-1,6,13,23,33-五氧杂-16,19,26,29-四氧杂-5,12,22,32-四氮杂四十三烷-43-酸(165mg,0.089mmol)的乙醇(10ml)溶液中加入双(2,5-二氧吡咯烷-1-基)4,4′-((2,2′-(1,2-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰基)肼-1,2-二(乙酰基))双(氮杂二酰基))二丁酯(70mg,0.089mmol)和磷酸盐缓冲液(0.5m,ph7.5,3ml)。将反应物在室温下搅拌过夜,然后浓缩并通过硅胶柱色谱法(0-6%甲醇/二氯甲烷)纯化,得到标题化合物666(130mg,收率62%)。esimsm/z:c115h185n18o37[m+h]+计算值:2410.31,实测值:2410.60。 实施例224.1,1′-((8r,27s)-36-((2r,4s)-2-氨基-4-羧基戊基)-17,18-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰基)-2,7,10,15,20,25,28,33-八氧代-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34-三十二烷-2h-苯并[b][1,4,9,12,17,20,21,24,29,32]氧杂九氮杂环三十六烷-8,27-二基)双(6,16,26-三氧杂-9,12,19,22-四氧杂-5,15,25-三氮杂三十烷-36-酸)的合成。 将1,1′-((8r,27s)-36-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-17,18-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰基)-2,7,10,15,20,25,28,33-八氧代-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34-三十二烷-2h-苯并[b][1,4,9,12,17,20,21,24,29,32]氧杂七氮杂环三十六烷-8,27-二基)双(6,16,26-三氧-9,12,19,22-四氧杂-5,15,25-三氮杂三十六烷-36-酸(128mg,0.053mmol)溶于二氯甲烷(3ml)中,并在室温下与tfa(3ml)反应2小时。将反应浓缩并与二氯甲烷共浓缩3次,得到标题化合物(120mg,收率100%)。esimsm/z:c106h169n18o35[m+h]+计算值:2254.19,实测值:2254.30。 实施例225.1,1′-(((8r,27s)-36-((2r,4s)-2-(2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧杂-12-氧杂-2,5,8-三氮杂异烟酸酯-11-基)噻唑-4-羧酰胺基)-4-羧基戊基)-17,18-双(2-(2-,2,5-二氧-2-,5-二氢-1h-吡咯-1-基)乙酰基)-2,7,10,15,20,25,28,33-八氧-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34-十二烷二氢-2h-苯并[b][1,4,9,12,17,20,21,24,29,32]-氧杂杂氮杂环六三十烷-8,27-二基)双(6,16,26-三氧代-9,12,19,22-四氧代-5,15,25-三氮杂三十烷-36-酸)(b-01)的合成。 将1,1′-(((8r,27s)-36-((2r,4s)-2-(2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧杂-12-oxa-2,5,8-三氮杂异烟酸酯-11-基)噻唑-4-羧酰胺基)-4-羧基戊基)-17,18-双(2-(2-,2,5-二氧-2-,5-二氢-1h-吡咯-1-基)乙酰基)-2,7,10,15,20,25,28,33-八氧-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34-十二烷二氢-2h-苯并[b][1,4,9,12,17,20,21,24,29,32]-氧杂氮杂环六三十烷-8,27-二基)双(6,16,26-三氧代-9,12,19,22-四氧代-5,15,25-三氮杂三十烷-36-酸)(120mg,0.053mmol)和41a(36.6mg,0.053mmol)溶于dma(5ml)中,冷却至0℃。加入dipea(18μl,0.106mmol),并将反应升温至室温,搅拌1小时。浓缩反应混合物后,将残余物通过制备型hplc纯化(c18,10-90%乙腈/水),得到标题化合物(b-1)(70mg,收率49%)。esimsm/z:c131h209n22o40s[m+h]+计算值:2762.46,实测值:2762.85。 实施例226.(7s,10r,11s,14s)-10,11-二叔丁基(((苄氧基)-羰基)氨基)-6,9,12,15-四氧代-7,14-双(31-氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32-氮杂三十六烷-36-基)-5,8,13,16-四氮杂二十烷-1,20-二酯的合成。 将(s)-叔丁基37-(((苄氧基)羰基)氨基)-31,38-二氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32,39-二氮杂四十三烷-43-酯(5.98g,6.73mmol)和pd/c(10wt%,0.6g)的甲醇(30ml)溶液在1atmh2压力下氢化过夜,然后通过硅藻土过滤(助滤剂)。浓缩滤液并重新溶于四氢呋喃(60ml)中,在0℃下,加入(2r,3s)-2,3-双(((苄氧基)羰基)氨基)琥珀酸(1.01g,2.42mmol),hobt(817mg,6.05mmol)dcc(1.25g,6.05mmol)和dipea(2.1ml,12.10mmol)。将反应物在室温下搅拌过夜,然后用乙酸乙酯(400ml)稀释,并用0.1nhcl,饱和碳酸氢钠和盐水洗涤,用无水无水硫酸钠干燥,过滤,浓缩并通过硅胶柱色谱法(24:1二氯甲烷/甲醇)纯化,得到标题化合物(5.65g,收率49%)。esimsm/z:c90h154n8o34[m+h]+计算值:1892.06,实测值:1892.60。 实施例227.(7s,10r,11s,14s)-10,11-二氨基-6,9,12,15-四氧代-7,14-双(31-氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32-氮杂三十六烷-36-基)-5,8,13,16-四氮杂二十烷-1,20-二叔丁酯的合成。 将(7s,10r,11s,14s)-10,11-双((((苄氧基)-羰基)氨基)-6,9,12,12,15-四氧-7,14-双(31-氧代2、5、8、11、14、17、20、23、26、29-十氧杂-32-氮杂三十六烷-36-基)-5、8、13、16-四氮杂二十烷-1,20-二叔丁酯(3.71g,1.96mmol)和pd/c(10wt%,0.40g)的甲醇(50ml)溶液在1atmh2压力反应过夜,然后通过硅藻土(助滤剂)过滤,得到标题化合物(3.18g,收率100%)。esimsm/z:c74h142n8o30[m+h]+计算值:623.98,实测值:1624.50。 实施例228.(7s,10r,11s,14s)-10,11-双(4-(2,5-二氧2-,5-二氢-1h-吡咯-1-基)丁酰胺基)-6,9,12、15-四氧杂-7、14-双(31-氧杂-2,5,8,11,14,17,20,23,26,29-十氧杂-32-氮杂三十六烷-36-基)-5,8、13、16-四氮杂二十烷-1、20-二酸的合成。 向(7s,10r,11s,14s)-二叔丁基10,11-二氨基-6,9,12,12,15-四氧-7,14-双(31-氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32-氮杂三十六烷-36-基)-5、8、13、16-四氮杂二十烷-1、20-二酯(315mg,0.194mmol))的dma(10ml)溶液中加入edc(150mg,0.785mmol)和4-马来酰基丁酸(72mg,0.57mmol)。将混合物在室温搅拌12小时,浓缩并通过硅胶柱色谱法纯化(1:4甲醇/二氯甲烷),得到油状物(329mg,收率87%),将其溶于二氯甲烷(25ml)中并与tfa(5ml)在室温下反应1小时,然后浓缩,得到标题化合物(309mg,收率99%)。esimsm/z:c82h140n10o36[m+h]+计算值:1841.94,实测值:1842.50。 实施例229.(2s,4r)-5-(((8s,11s,12r,15s)-11,12-双(4-(2,5-二氧代-2,5-二氢代-1h-))吡咯-1-基)丁酰胺基)-2,7,10,13,16,21-六氧代-8,15-双(31-氧代-2,5,8,11,14,17,20,23,26,29-十氧代-32-氮杂六三十烷-36-基)-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22-二十二氢-2h-苯并[b][1、4、9、12、17、20]氧杂五氮杂环二十四烷-24-基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(7s、10r、11s、14s14s)-10,11-11-双(4-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基-正丁胺基亚基)-6,9,12,12,15-四氧代-7,14-双(31-氧代-2,5,8,11,14,17,20,20,23,26,29,29-十氧代烷-32-氮杂三十六烷-36-基]-5,8,13,16-四氮杂二十烷-1,20-二酸(154mg,0.0837mmol)和(2s,4r)-5-(3-氨基-4-羟基苯基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯(33mg,0.0837mmol)的dmf(6ml)溶液冷却至0℃,并依次加入hatu(64mg,0.167mmol)和tea(46μl,0.335mmol)。将反应搅拌1小时,然后用水(100ml)稀释,并用乙酸乙酯(3×100ml)萃取。用盐水洗涤乙酸乙酯溶液,在无水无水硫酸钠上干燥,过滤,浓缩并通过硅胶柱层析法(6:1二氯甲烷/甲醇)纯化,得到标题化合物(95mg,收率52%)。esimsm/z:c103h170n12o39[m+h]+计算值:2200.17,实测值:2200.90。 实施例230.(2s,4s)-5-(((8s,11s,12r,15s)-11,12-双(4-(2,5-二氧代-2,5-二氢-1h-吡咯-1)-基)丁酰胺基)-2,7,10,13,16,21-六氧代-8,15-双(31-氧代-2,5,8,11,14,17,20,23,26,29-十氧代-32-氮杂三十六烷-36-基)-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22-icosahydro-2h-苯并[b][1、4、9、12、17、20]氧杂五氮杂环二十四烷24-基)-4-(2-((6s,9r,11r)-6-((s)-仲-丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧十二烷基-氧杂-2,5,8-三氮杂十一烷-11-基)噻唑-4-甲酰胺基)-2-甲基戊酸的合成(b-02)。 向(2s,4r)-5-(((8s,11s,12r,15s)-11)-1-基)丁酰胺基)-2,7,10,13,16,21-是氧代-8,15-双(31-氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-32-氮杂三十六烷-36-基)-3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22-二十氢-2h-苯并[b][1,4,9,12,17,20]氧杂五氮杂环二十四烷24-基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯(98mg,0.045mmol)的二氯甲烷(3ml)溶液中加入tfa(6ml)。将反应混合物在室温搅拌1小时,然后浓缩并重新溶于dma(1ml),加入2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧杂十二-氧代-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸酯(31mg,0.045mmol)和dipea(12μl,0.068mmol)。将反应混合物在室温搅拌90分钟,然后浓缩,并通过反相hplc(c18柱,10-100%乙腈/水)纯化,得到标题化合物(b-2)(36.2mg,62%产率)。esimsm/z:c119h194n16o42s[m+h]+计算值:1276.66,实测值:1276.65。 实施例231.(s)-11-(5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-5-氧戊二酰氨基)十一酸的合成。 向boc-glu(otbu)-oh(0.50g,1.65mmol)的dmf(10ml)溶液中加入hatu(0.69g,1.82mmol)和tea(0.26ml,1.82mmol)。搅拌30分钟后,加入11-氨基十一酸(0.33g,1.65mmol)的dmf(10ml)溶液,并将反应混合物在室温搅拌1小时,然后倒入装有200ml1nhcl的分液漏斗中,并用二氯甲烷(3×50ml)萃取。有机相用100ml盐水洗涤一次,然后用无水无水硫酸钠干燥,过滤并浓缩。残余物通过柱色谱法(甲醇/二氯甲烷)纯化,得到标题化合物(1.0g,收率>100%)。esimsm/z:c25h47n2o7[m+h]+计算值:487.33,实测值:487.34。 实施例232.(s)-11-(2-氨基-4-羧基丁二酰胺基)十一酸的合成。 向(s)-11-(5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-5-氧戊二酰氨基)十一酸(1.0g,2.05mmol)的二氯甲烷(20ml)溶液中加入tfa(5ml)。将反应在室温下搅拌30分钟,然后浓缩至干,并用二氯甲烷共旋蒸干燥两次。最后置于真空泵上抽干,得到标题化合物(0.68g,2.06mmol,收率100%)。esimsm/z:c16h31n2o5[m+h]+计算值:331.22,实测值:331.22。 实施例233.(2s,4r)-5-(3-(2-((((苄氧基)羰基)氨基)-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(2s,4r)5-(3-氨基-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.2g,0.51mmol),2-(((苄氧基)将羰基)氨基)-3-甲基丁酸(0.13g,0.51mmol),hatu(0.20g,0.51mmol)溶解于二氯甲烷(20ml)中,然后加入tea(110μl,0.8mmol)。将反应混合物在室温搅拌过夜。然后减压除去溶剂,用硅胶柱纯化,得到标题产物(0.30g,91%)。esimsm/z:c34h50n3o8[m+h]+计算值:628.35,实测值:628.45。 实施例234.(2s,4r)5-(3-(3-(2-氨基-3-甲基丁亚氨基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 在氢化瓶中,将pd/c(0.1g,33wt%,50%水)加入到(2s,4r)-5-(3-(2-(((苄氧基)羰基)氨基)-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.29g,0.46mmol)的甲醇(10ml)溶液中。将混合物在1atmh2下振摇过夜,然后通过硅藻土(助滤剂)过滤。浓缩滤液,得到标题化合物(0.23g,),无需进一步纯化即可用于下一步。esimsm/z:c26h44n3o6[m+h]+计算值:494.64,实测值494.75。 实施例235.(2s,4r)-5-(3-(2-(2-(((((苄氧基)羰基)氨基)丙酰胺基)-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(2s,4r)5-(3-(2-氨基-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.23g,0.46mmol),2-(((苄氧基)羰基)-氨基丙酸(0.10g,0.46mmol)和hatu(0.18g,0.46mmol)溶解在二氯甲烷(20ml)中,然后加入tea(110ul,0.8mmol)。将反应混合物在室温下搅拌过夜,在减压下浓缩,并在硅胶柱上纯化,得到标题产物(0.3g,95%)。esimsm/z:c37h55n4o9[m+h]+计算值:699.39,实测值:699.50。 实施例236.(2s,4r)-5-(3-(2-(2-(2-氨基丙酰胺基)-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 在氢气瓶中,将pd/c(0.1g,33wt%,50%wet)加到(2s,4r)-5-(3-(2-(2-(((苄氧基于甲醇(10ml)中的(羰基)氨基)丙酰胺基)-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.3g,0.43mmol)。将混合物在1atmh2下振摇过夜,然后通过硅藻土(助滤剂)过滤,浓缩滤液,得到标题化合物(0.22g,93%),其无需进一步纯化即可用于下一步。esimsm/z:c29h49n4o7[m+h]+计算值:565.35,实测值:565.60。 实施例237.(2s,4r)-5-((3s,6s,14r,15s)-14,15-双(2-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)乙酰氨基)-3-异丙基-6-甲基-2,5,8,13,16,21-十氧基-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21-二十氢-1h-苯并[b][1,4,7,10,15,20]氧杂五氮杂环二十五烷-25-基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 将(2s,4r)-5-(3-((s)-2-((s)-2-氨基丙酰胺基)-3-甲基丁酰胺基)-4-羟基苯基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯(0.150g,0.27mmol),4,4′-((((2r,3s)-2,3-双(2-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基(乙酰胺基)琥珀酰基)双(氮杂二基)-二丁酸(0.160g,0.270mmol),hatu(0.402g,1.080mmol)溶于二氯甲烷(30ml)中,然后加入tea(55μl,0.4mmol)。将反应混合物在室温搅拌过夜,减压浓缩并在硅胶柱上纯化(用乙酸乙酯/二氯甲烷,1:10至1:5洗脱),得到标题化合物(0.187g,62%)。esimsm/z:c53h73n10o17[m+h]+计算值:1121.51,实测值:1121.75。 实施例238.(2s,4r)-4-氨基-5-((3s,6s,14r,15s)-14,15-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-3-异丙基-6-甲基-2,5,8,13,16,21-十氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21-二十氢-1h-苯并[b][1,4,7,10,15,20]-氧杂五氮杂环二十五烷-25-基)-2-甲基戊酸的合成。 将(2s,4r)-5-((3s,6s,14r,15s)-14,15-双(2-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)乙酰氨基)-3-异丙基-6-甲基-2,5,8,13,16,21-十氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21-二十碳氢-1h-苯并[b][1,4,7,10,15,20]-氧杂五氮杂环二十五烷-25-基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.175g,0.156mmol)溶解在二氯甲烷(6ml)中,然后加入tfa(2ml)。将反应混合物在室温搅拌2小时,用甲苯(8ml)稀释,浓缩,得到标题化合物(150mg,收率100%),其无需进一步纯化即可用于下一步。esimsm/z:c44h57n10o15[m+h]+计算值:965.39,实测值:965.70。 实施例239.1-(((2s)-1-((((1r,3r)-1-乙酰氧基-1-(4-(((2r,4s)-1-((3s,6s,14r,15s)-14,15-双(2-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)乙酰氨基)-3-异丙基-6-甲基-2,5,8,13,16,21-十氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21-二十氢-1h-苯并[b][1,4,7,10,15,20]氧杂五氮杂二十五烷-25-基)-4-羧基戊基-2-基)氨基甲酰基)噻唑-2-基)-4-甲基戊基-3-基)(甲基)氨基)-3-甲基-1-氧杂戊-2-基)氨基)-n,n,n,2-四甲基-1-氧代戊基-2-铵(b-03)的合成。 向(2s,4r)-4-氨基-5-((3s,6s,14r,15s)-14,15-双(2-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)乙酰氨基)-3-异丙基-6-甲基-2,5,8,13,16,21-七氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21-二十氢-1h-苯并[b][1,4,7,10,15,20]-氧杂五氮杂环二十五烷-25-基)-2-甲基戊酸(约50mg,0.051mmol)的dma(4ml)溶液中加入1-(((2s)-1-((((1r,3r)-1-乙酰氧基-4-甲基-1-(4-((五氟苯氧基)羰基)噻唑-2-基)戊三基)(甲基)氨基)-3-甲基-1-氧戊烷-2-基)氨基)-n,n,n,2-四甲基-1-氧代丙烷-2-铵(37mg,0.052mmol)和dipea(3.4μl,0.02mmol)。将反应混合物搅拌过夜,浓缩并用hplc纯化,用mecn/h2o梯度洗脱(c-18柱,10mm(d)x250mm(l),在45分钟内10%mecn至70%mecn,9ml/min),得到标题产物(37.1mg,收率49%)。esimsm/z:c70h99n14o20s[m]+计算值:1487.69,实测值:1487.45。 实施例240.(4r)-5-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十烷-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂七氮杂环四十六烷-46-基)-4-(2-(((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧代-2,5,8-三氮杂十一烷基-11-基)噻唑-4-甲酰胺基)-2-甲基戊酸(b-04)的合成。 向(2r)-1-(22,23-双(2,5-二氧-2-),5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-六三水-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂七氮杂环四十六烷-46-基)-4-羧基戊烷-2-铵三氟乙酸盐(60mg,0.050mmol)的dma(15ml)溶液中,加入五氟苯基活性酯(44mg,0.06mmol)和0.1mnah2po4(ph7.5,8.0ml)。将反应混合物搅拌过夜,浓缩并用hplc纯化,用mecn/h2o(c-18柱,10mm(d)x250mm(l),在45分钟内10%mecn至70%mecn,8ml/min)洗脱,得到标题产物b-4(44mg,收率52%)。esimsm/z:c79h117n14o26s[m+h]+计算值:1709.79,实测值:1709.55。 实施例241.(1r,3r)-1-(4-((((2r)-5-((2-氨基乙基)氨基)氨基)-1-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂七氮杂环四十六烷-46-基)-4-甲基-5-氧戊烷-2-基)氨基甲酰基)噻唑-2-基)-3-((2s,3s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基戊酰胺基)-4-甲基戊基乙酸酯(b-5)的合成。 向化合物b-4(22.0mg,0.0129mmol)的dma(1ml)溶液中,加入edc(15.0mg,0.078mmol),乙基-1,2-二胺盐酸盐(8.0mg,0.060mmol)和dipea(0.010ml,0.060mmol)。将混合物搅拌过夜,浓缩,并通过反相hplc纯化(250(l)mm×10(d)mm,c18柱,在40分钟内10-100%乙腈/水,流速8ml/min),得到标题化合物(14.0mg,产率62%)。esimsm/z:c81h123n16o25s[m+h]+计算值:1751.85,实测值:1751.20。 实施例242.(1r,3r)-1-(4-((((28r)-1-氨基-29-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯)-1-yl)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,28,41,44]七氧杂七氮杂环四十六烷-46-基)-26-甲基-25-氧代-3,6,9,12,15,18,21-十氧杂-24-氮杂二十八烷-28-基)氨基甲酰基)噻唑-2-基)-3-((2s,3s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基戊酰胺基)-4-甲基戊基乙酸酯(b-06)的合成。 向化合物b-4(22.0mg,0.0129mmol)的dma(1ml)溶液中加入edc(15.0mg,0.078mmol),3,6,9,12,15,18,21-七氧杂二十三烷-1,23-二胺盐酸盐(26.0mg,0.059mmol)和dipea(0.010ml,0.060mmol)。将混合物搅拌过夜,浓缩,并通过反相hplc(250(l)mmx10(d)mm,c18柱,在40分钟内10-100%乙腈/水,流速8ml/min)纯化,得到标题化合物(14.5mg,收率55%)。esimsm/z:c95h151n16o32s[m+h]+计算值:2060.03,实测值:2060.80。 实施例243.(1r,3r)-1-(4-((((28r)-29-(22,23-双(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基))-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂七氮杂环四十六烷-46-基)-1-羟基-26-甲基-25-氧代-3,6,9,12,15,18,21-十氧杂-24-氮杂二十八烷-28-基)氨基甲酰基)噻唑-2-基)-3-((2s,3s)-2-(2-(二甲基氨基)-2-甲基丙酰胺基)-n,3-二甲基戊酰胺基)-4-甲基戊基乙酸酯(b-07)的合成。 向化合物b-4(22.0mg,0.0129mmol)的dma(1ml)溶液中加入edc(15.0mg,0.078mmol)和23-氨基-3,6,9,12,15,18,21-七氧杂二十三烷-1-醇(22.0mg,0.059mmol)。将混合物搅拌过夜,浓缩,并通过反相hplc(250(l)mmx10(d)mm,c18柱,在40分钟内10-100%乙腈/水,流速8ml/min)纯化,得到标题化合物(b-7)(14.1mg,收率53%)。esimsm/z:c95h150n15o33s[m+h]+计算值:2061.02,实测值:2061.74。 实施例244.(2s)-叔丁基2-((4r)-5-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3)的合成,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂七氮杂环四十六烷-46-基)-4-(2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十一烷-11-基)噻唑-4-羧酰胺基)-2-甲基戊酰胺基)-6-((叔丁氧羰基)氨基)己酯(b-08)的合成。 向化合物b-4(25.0mg,0.0146mmol)的dma(1ml)溶液中,加入edc(15.0mg,0.078mmol)和2-氨基-6-(叔丁氧基羰基)氨基)己酸叔丁酯(9.0mg,0.030mmol)。将混合物搅拌过夜,浓缩,并通过反相hplc(250(l)mmx10(d)mm,c18柱,在40分钟内10-100%乙腈/水,流速8ml/min)纯化,得到标题化合物(20.5mg,收率71%)。esimsm/z:c94h144n16o29s[m+h]+计算值:1994.00,实测值:1994.85。 实施例245.(2s)-6-氨基-2-((4r)-5-(22,23-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)-3,6,39,42-四甲基-2,5,8,21,24,37,40,43-八氧代-3,4,5,6,7,8,9,10,12,13,15,16,18,19,20,21,22,23,24,25,26,27,29,30,32,33,35,36,37,38,39,40,41,42,43,44-三十六氢-2h-苯并[b][1,14,17,20,31,34,37,4,7,10,23,28,41,44]七氧杂七氮杂环四十六烷-46-基)-4-(2-(((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十一烷-11-基)噻唑-4-羧酰胺基)-2-甲基戊酰胺基己酸(b-09)的合成。 将化合物b-8(20.0mg,0.010mmol)溶于二氯甲烷(1ml)中,然后加入tfa(1ml)。将反应混合物在室温下搅拌2小时,然后浓缩,并通过反相hplc(250(l)mm×10(d)mm,c18柱,10-100%乙腈/水,40分钟,流速8ml/min)纯化,得到标题化合物(13.5mg,收率73%)。esimsm/z:c85h129n16o27s[m+h]+计算值:1837.89,实测值:1838.20。 实施例246.(s)-叔丁基39-氨基-45-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧戊基)-2-羟基苯基)氨基)-11,21,33,40,45-五氧四,7,14,17,24,27,30-七氧十,10,20,3441-四氮杂四十五烷-1-叔丁酯的合成。 向(s)-5-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基氨基甲酰基)-3,11,23,33-四氧-1-苯基-2,14,17,20,27,30,37,40-八氧杂-4,10,24,34-四氮杂三四十三烷-43-叔丁酯(1.00g,0.742mmol)的甲醇(50ml)溶液中,加入pd/c(10wt%,20mg),然后在1atmh2压力下反应过夜。将混合物通过硅藻土(助滤剂)过滤,并将滤液浓缩,得到标题化合物(900mg,收率100%)。esimsm/z:c59h104n7o19[m+h]+计算值:1214.73,实测值:1214.90。 实施例247.(42s,50s,51r)-42-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-50,51-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,2-二甲基-4,14,24,36,4449,52-七氧代-3,7,10,17,20,27,30,33-八氧杂-13,23,37,43,48,53-六氮杂五十七烷-57-酸和38-((8s,16r,17s)-27-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)-氨基)-4-甲基-5-氧代戊基)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15,18,23-六氧基-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂五氮杂环二十六烷-8-基)-11,21,33-三氧代-4,7,14,17,24,27,30-七氧杂-10,20,34-三氮杂三十八烷-1-叔丁酯的合成。 向(s)-39-氨基-45-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-11,21,33,40,45-五氧代-4,7,14,17,24,27,30-七氧杂-10,20,34,41-四氮四十五烷-1-叔丁酯(450mg,0.370毫摩尔)和4,4′-(((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸(230mg,0.370mmol)的dma(40ml)溶液中加入edc(300mg,1.570mmol)和dipea(100mg,0.775mmol)。将反应混合物在室温搅拌过夜,减压浓缩并在硅胶柱上纯化(用乙酸乙酯/二氯甲烷,1:10至1:5洗脱),得到(42s,50s,51r)-42-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-50,51-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,2-二甲基-4,14,24,36,44,49,52-七氧代-3,7,10,17,20,27,30,33-八氧代-13,23,37,43,48,53-六氮杂五十七烷-57-酸(0.221g,收率33%)。esimsm/z:c85h134n13o30[m+h]+计算值:1816.93,实测值1817.25;和38-((8s,16r,17s)-27-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)-氨基)-4-甲基-5-氧代戊基)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15,18,23-十氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,2021,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂五氮杂环八烷-8-基)-11,21,33-三氧代-4,7,14,17,24,27,30-七氧杂-10,20,34-三氮三十八烷-1-酸酯(0.260g,收率39%)。esimsm/z:c85h132n13o29[m+h]+计算值:1797.92,实测值:1798.20。 实施例248.(39s,47r,48s,56s)-二叔丁基39,56-双((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧羰基)叔叔丁氧基)氨基)-4-甲基-5-氧代戊基)-4-氧代丁基)甲酰基)-47,48-双(3-(2,5-二氧代-2,5-二氧代-2,5-二氢-1-基吡咯-1-基)丙氨基甲酰基)11,21,33,41,46,49,54,62,74,84-十氧代-4,7,14,17,24,27,30,65,68,71,78,81,88,91-十四氧杂-10,20,34,40,45,50,55,61,75,85-十氮杂九十四烷-1,94-二酯的合成。 向(s)-39-氨基-45-(((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧戊基)-2-羟基苯基)氨基)-11,21,33,40,45-五氧-4,7,14,17,24,27,30-七氧杂-10,20,34,41-四氮四十五烷-1-叔丁酯(450mg,0.370mmol)和4,4′-((((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二烷基))二丁酸(115mg,0.185mmol)的dma(40ml)溶液中加入edc(300mg,1.570mmol)。将反应混合物在室温搅拌过夜,减压浓缩,并在硅胶柱上纯化(用1:10至1:3乙酸乙酯/二氯甲烷洗脱),得到标题化合物(0.378g,68%产率)。esimsm/z:c144h235n20o48[m+h]+计算值:3012.65,实测值:3012.95。 实施例249.(33r,34s,42s)-叔丁基42-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-33,34-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙烷胺)-27,32,35,40,48,60,70-七氧代-2,5,8,11,14,17,20,23,51,54,57,64,67,74,77-十五氧杂-26,31,36,41,47,61,71-七氮杂八十烷-80-酯的合成。 向(42s,50s,51r)-42-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-50,51-双(3-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,2-二甲基-4,14,24,36,44,49,52-七氧代-3,7,10,17,20,27,30,33-八氧杂-13,23,37,43,48,53-六氮杂五十七-57-酸(100mg,0.055mmol)的dma(30ml)溶液中加入2,5,8,11,14,17,20,23-八氧杂二十五烷-25-胺盐酸盐(30mg,0.071mmol)和edc(25mg,0.130mmol)。将反应混合物在室温搅拌过夜,减压浓缩,并在硅胶柱上纯化(用1:8至1:3乙酸乙酯/二氯甲烷洗脱),得到标题化合物(92.2mg,收率76%)。esimsm/z:c102h169n14o37[m+h]+计算值2182.17,实测值2182.95。 实施例250.(38s,46s,47r)-38-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-46,47-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基))丙烷胺)-32,40,45,48-四氧代-2,5,8,11,14,17,20,23,26,29-十氧代-33,39,44,49-四氮杂五十三烷-53-酸和(2s,4r)-5-(((8s,16r,17s)-16,17-双(3-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丙烷胺)-2,7,10,15,18,23-十氧代-8-(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十烷-35-基)-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]-氧杂五氮杂二十七烷-27-基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯的合成。 向(2s,4r)-5-(3-((s)-36-氨基-30,37-二氧代-2,5,9,12,15,18,21,24,27-九氧杂-31,38-二氮杂四十二烷酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(400mg,0.377mmol)和4,4′-(((2r,3s)-2,3-双(3-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸(234mg,0.377mmol))的dma(50ml)中溶液加入edc(300mg,1.570mmol)和dipea(100mg,0.775mmol)。将反应混合物在室温搅拌过夜,减压浓缩,并在硅胶柱上纯化(用1:10至1:5乙酸乙酯/二氯甲烷洗脱),得到(38s,46s,47r)-38-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-46,47-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-32,40,45,48-四氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-33-39,39,44,49-四氮杂五十三烷-53-酸(0.192g,31%产率)。esimsm/z:c78h124n11o28[m+h]+计算值:1662.85,实测值:1662.60;和(2s,4r)-5-(((8s,16r,17s)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15,18,23-七氧代-8-(30-氧代-2,5,9,12,15,18,21,24,27-九氧代-31-氮杂三十五烷-35-基)-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二烷-1h-苯并[b][1,4,9,12,17,22]-氧杂五氮杂环二十七烷-27-基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.260g,39%产率)。esimsm/z:c78h122n11o27[m+h]+计算值:1644.84,实测值:1645.25。 实施例251.(2s,2’s,4r,4’r)-二叔丁基5,5′-((((((7s,15r,16s,24s)-15,16-双(3-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丙酰胺)-6,9,14,17,22,25-十氧代-7,24-双(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-5,8,13,18,23,26-六氮杂三十烷-1,30-二基)双(氮杂二烯基))双(4-羟基-3,1-亚苯基)双(4-((叔丁氧基羰基)氨基)-2-甲基戊酸酯)的合成。 向(2s,4r)-5-(3-((s)-36-氨基-30,37-二氧代-2,5,9,12,15,18,21,24,27-九氧杂-31,38-二氮杂四十二烷酰胺基)-4-羟基苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(400mg,0.377mmol)和4,4′-(((2r,3s)-2,3-双(3-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸(115mg,0.185mmol)的dma(50ml)溶液中加入edc(300mg,1.570mmol)。将反应混合物在室温搅拌过夜,减压浓缩并在硅胶柱上纯化(用1:10至1:3乙酸乙酯/二氯甲烷洗脱),得到标题化合物(0.325g,收率65%)。esimsm/z:c130h215n16o44[m+h]+计算值:2704.50,实测值2704.90。 实施例252.(2s,4r)-5-(3-(((34r,35s,43s)-34,35-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-1-羟基-28,33,36,41,44-五氧代-43-(32-氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-33-氮杂三十七烷-37-基)-3,6,9,12,15,18,21,24-八氧杂-27,32,37,42,45-五氮杂四十九烷酰胺)-4-羟苯基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯的合成。 向(38s,46s,47r)-38-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-46,47-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-32,40,45,48-四氧代-2,5,8,11,14,17,20,23,26,29-十氧杂-33,39,44,49-四氮杂五十三烷-53-酸(100mg,0.060mmol)的dma(30ml)溶液中加入26-氨基-3,6,9,12,15,18,21,24-八氧杂二十六烷-1-醇盐酸盐(31mg,0.069mmol)和edc(35mg,0.183mmol)。将反应混合物在室温搅拌过夜,减压浓缩并在硅胶柱上纯化(用1:8至1:3乙酸乙酯/二氯甲烷洗脱),得到标题化合物(86.5mg,收率69%)。esimsm/z:c97h163n12o37[m+h]+计算值:2088.12,实测值:2088.85。 实施例253.(39s,47r,48s)-39-((4-((5-((2r,4s)-2-(2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三叠氮基十三烷基十一烷基)噻唑-4-甲酰胺)-4-羧基戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-47,48-双(3-(2,5-二氧杂-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-11,21,33,41,46,49-七氧代-4,7,14,17,24,27,30-七氧杂-10,20,34,40,45,50-六氮杂五十四烷-1,54-二酸(b-10)的合成。 将(42s,50s,51r)-42-((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)氨基)-4-甲基-5-氧戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-50,51-双(3-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,2-二甲基-4,14,24,36,44,49,52-七氧代-3,7,10,17,20,27,30,33-八氧杂-13,23,37,43,48,53-六氮杂五十七烷-57-酸(0.120g,0.066mmol)溶解于二氯甲烷(6ml)中,然后加入tfa(2ml)。将反应混合物在室温搅拌45分钟,用甲苯(8ml)稀释,浓缩,得到(39s,47r,48s)-39-((4-((5-((5-((2r,4s)-2-氨基-4-羧基戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-47,48-双(3-(2,5-二氧杂-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-11,21,33,41,46,49-六氧代-4,7,14,17,24,27,30-七氧杂-10,20,34,40,45,50-七氧杂五十四烷-1,54-二酸三氟乙酸盐(106mg,100%产率),无需进一步纯化即可用于下一步。将化合物溶解于dma(15ml),加入2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氧杂十四-11-基)噻唑-4-羧酸五氟苯酯(46mg,0.066mmol)和dipea(10ul,0.055mmol)。将反应混合物搅拌过夜,浓缩并通过hplc纯化,用mecn/h2o梯度洗脱(c-18柱,20mm(d)x250mm(l),在45分钟内10%mecn至70%mecn,9ml/min),得到标题产物(64.1mg,收率46%)。esimsm/z:c97h150n17o33s[m+h]+计算值:2113.02,实测值:2113.80。 实施例254.38-((8s,16r,17s)-27-((2r,4s)-2-(2-((6s,9r,11r)-6-((s)-仲丁基)的合成-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧代-2,5,8-三氮杂十三烷基十一烷基)噻唑-4-羧酰胺基)-4-羧基戊基)-16,17-双(3-(2,5-二氧-2-,5-二氢-1h-吡咯-1-基)丙酰胺)-2,7,10,15,18,23-七氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂五氮杂环二十六烷-8-基)-11,21,33-三氧代-4,7,14,17,24,27,30-七氧杂-10,20,34-三氮杂三十八烷-1-酸(b-11)的合成。 将38-((8s,16r,17s)-27-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧基羰基)-氨基)-4-甲基-5-氧戊基)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺)-2,7,10,15,18,23-七氧杂-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂氧杂五氮杂环二十六烷-8-基)-11,21,33-三氧代-4,7,14,17,24,27,30-七氧杂-10,20,34-三氮杂三十八烷1-叔丁酯(0.150g,0.083mmol)溶解于二氯甲烷(6ml)中,然后加入tfa(2ml)。将反应混合物在室温搅拌45分钟,用甲苯(8ml)稀释,浓缩,得到38-((8s,16r,17s)-27-((2r,4s)-2-氨基-4-羧基戊基)-16,17-双(3-(2,5-二氧-2-,5-二氢-1h-吡咯-1-基)丙酰胺)-2,7,10,15,18,23-七氧代-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂五氮杂环二十六烷-8-基)11,21,33-三氧代-4,7,14,17,24,27,30-七氧杂-10,20,34-三氮杂三十八烷-1-酸的tfa盐(135毫克,收率101%)无需进一步纯化即可用于下一步。然后将该化合物溶解在dma(15ml)中,加入五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧代-2,5,8-三氮杂十一烷-11-基)噻唑-4-羧酸酯(60mg,0.084mmol)和dipea(10μl,0.055mmol)。将反应混合物搅拌过夜,浓缩并通过hplc纯化,用mecn/h2o梯度洗脱(c-18柱,20mm(d)x250mm(l),45分钟内10%mecn至70%mecn,9ml/min),得到标题产物(81.6mg,收率47%)。esimsm/z:c97h149n17o32s[m+h]+计算值:2095.01,实测值:2095.65。 实施例255.化合物b-12的合成。 将(39s,47r,48s,56s)-二叔丁基39,56-双((4-((5-((2r,4s)-5-(叔丁氧基)-2-((叔丁氧羰基)氨基)-4-甲基-5-氧代戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-47,48-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-11,21,33,41,46,49,54,62,74,84-十氧代-4,7,14,17,24,27,30,65,68,71,178,81,88,91-十四氧代-10,20,34,40,45,50,55,61,75,85-十氮杂九十四烷-1,94-二酯(175mg,0.058mmol)溶于二氯甲烷(6ml),然后加入tfa(2ml)。将反应混合物在室温搅拌45分钟,用甲苯(8ml)稀释,浓缩,得到(39s,47r,48s,56s)-39,56-双((4-((5-((2r,4s)-2-氨基-4-羧基戊基)-2-羟基苯基)氨基)-4-氧代丁基)氨基甲酰基)-47,48-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-11,21,33,41,46,49,54,62,74,84-十氧代-4,7,14,17,24,27,30,65,68,71,78,81,88,91-十四氧代-10,20,34,40,45,50,55,61,75,85-十氮杂九十四烷-1,94-二甲酸的tfa盐(151mg,收率99%)。然后将化合物溶解于dma(15ml),加入五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十一烷基十一烷基)噻唑-4-羧酸酯(85mg,0.123mmol)和dipea(18ul,0.103mmol)。将反应混合物搅拌过夜,浓缩并通过hplc纯化,用mecn/h2o梯度洗脱(c-18柱,20mm(d)x250mm(l),在45分钟内从10%mecn至70%mecn,9ml/min),得到标题产物(81.6mg,收率47%)。esimsm/z:c168h267n28o54s2[m+h]+计算值:3604.84,实测值:3604.80。 实施例256.(36s,44s,45r)-36-((4-((5-((2r,4s))-2-(2-((6s,9r,11r))-6-((s))-仲-丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十四烷-11-基)噻唑-4-甲酰胺)-4-羧基戊基)-2-羟基苯基)氨基)-4-氧丁基)氨基甲酰基)-44,45-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-30,38,43,46-四氧代-2,5,9,9,12,15,18,21,24,27-九氧杂-31,37,42,47-四氮杂五十一烷-51-酸(b-13)的合成。 将(2s,4r)-5-((8s,16r,17s)-16,17-双(3-(2,5-二氧基-2,5-二氢-1h-吡咯-1-基)丙酰胺)-2,7,10,15,18,23-六氧基-8-(30-氧基-2,5,9,12,15,18,21,24,27-九氧代-31-氮杂戊三氮杂环五十三烷-35-基)-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]-氧杂五氮杂环二十六烷-27-基)-4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯(0.175g,0.152mmol)溶解在二氯甲烷(6ml)中,然后加入tfa(2ml)。将反应混合物在室温搅拌1小时,用甲苯(8ml)稀释,浓缩,得到(36s,44r,45s)-36-((4-((5-((5-((2r,4s)-2-氨基-4-羧基戊基)-2-羟基苯基)氨基)-4-氧代丁基氨基甲酰基)-44,45-双(3-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)-30,38,43,46-四氧代-2,5,9,12,15,18,21,24,27-九氧代-31,37,42,47-四氮杂五十一烷-51-酸(230mg,收率101%),无需进一步纯化即可用于下一步。然后将化合物溶解于dma(15ml),加入五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸酯(106mg,0.152mmol)和dipea(20ul,0.115mmol)。将反应混合物搅拌过夜,浓缩并通过hplc纯化,用mecn/h2o梯度洗脱(c-18柱,20mm(d)x250mm(l),45分钟内从10%mecn至70%mecn,9ml/min),得到标题产物(149.1mg,收率49%)。esimsm/z:c94h148n15o31s[m+h]+计算值:2015.01,实测值:2015.65。 实施例257.(2s,4r)-5-(3-((34r,35s,43s)-34,35-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺)-1-羟基-28,33,36,41,44-五氧代-43-(32-氧代-2,5,8,11,14,17,20,23,26,29-十氧代-33-氮杂三十七烷-37-基)-3,6,9,12,15,18,21,24-八氧杂-27,32,37,42,45-五氮杂四十九烷酰胺基)-4-羟苯基)-4-(2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧代-2,5,8-三氮杂十三烷-11-基)噻唑-4-羧酰胺基)-2-甲基戊酸(b-14)的合成。 将(2s,4r)-5-(3-((34r,35s,43s)-34,35-双(3-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丙酰胺)-1-羟基-28,33,36,41,44-五氧代-43-(32-氧代-2,5,8,11,14,17,20,23,26,29-十氧代-33-氮杂三十七烷-37-基)-3,6,9,12,15,18,21,24-八氧代-27,32,37,42,45-五氮杂四十九烷酰胺基)-4-羟苯基)4-((叔丁氧羰基)氨基)-2-甲基戊酸叔丁酯(0.085g,0.040mmol)溶解在二氯甲烷(6ml)中,然后加入tfa(2ml)。在室温下将反应混合物搅拌1小时,用甲苯(8ml)稀释,浓缩得到2,5,8,11,14,17,20,23,26,29-十氧杂-33-氮杂三十七烷-37-基)-3,6,9,12,15,18,21,24-八氧杂-27,32,37,42,45-五氮杂四十九烷酰胺基)-4-羟基苯基)-2-甲基戊酸的tfa盐(78mg,100%产率),用于下一步,无需进一步纯化。然后将化合物溶解于dma(15ml)中,加入五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧基-12-氧基-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸酯(40mg,0.056mmol)和dipea(7μl,0.040mmol)。将反应混合物搅拌过夜,通过高效液相色谱(hplc)纯化,用mecn/h2o梯度(c-18柱,20mm(d)x250mm(l),45分钟从10%mecn至70%mecn,9ml/min)洗脱,得到标题产物(51.3mg,收率52%)。esimsm/z:c113h187n16o40s[m+h]+计算值:2440.27,实测值:2440.90。 实施例258.(2s,4r)-5-((8s,16r,17s)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺)-2,7,10,15,18,23-七氧代-8-(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂五氮杂环二十六烷-27-基)-4-(2-(((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧代-12-氧杂-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酰胺基)-2-甲基戊酸酸(b-15)的合成。 将(2s,4r)-5-(((8s,16r,17s)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15,18,23-七氧代8-(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-十二氢-1h-苯并[b][1,4,9,12,17,22]-氧杂五氮环二十六烷-27-基)-4-((叔丁氧基羰基)氨基)-2-甲基戊酸叔丁酯(0.145g,0.0882mmol)溶于二氯甲烷(6ml),然后加入tfa(2ml)。将反应混合物在室温搅拌1小时,用甲苯(8ml)稀释,浓缩,得到(2s,4r)-4-氨基-5-((8s,16r,17s)-16,17-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-2,7,10,15,18,23-七氧代-8-(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23-二十二氢-1h-苯并[b][1,4,9,12,17,22]氧杂五氮杂环二十六烷-27-基)-2-甲基戊酸的tfa盐(133mg,101%产率),无需进一步纯化即可用于下一步。然后将化合物溶解于dma(15ml)中,加入五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧杂-12-氧代-2,5,8-三氮杂十四烷基-11-基)噻唑-4-羧酸酯(62mg,0.0885mmol)和dipea(15ul,0.086mmol)。将反应混合物搅拌过夜,浓缩并通过hplc纯化(c-18柱,20mm(d)x250mm(l),在45分钟内10%mecn至70%mecn洗脱,9ml/min),得到标题产物(83.1mg,收率47%)。esimsm/z:c94h146n15o30s[m+h]+计算值:1997.00,实测值:1997.60。 实施例259.(s,s,r,r,2s,2’s,4r,4’r)-5,5′-(((((7s,15r,16s,24s)-15,16-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)-6,9,14,17,22,25-七氧代-7,24-双(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-5,8,13,18,23,26-六氮杂三十烷-1,30-二基)双(氮杂二烷基))双(4-羟基-3,1-亚苯基))双(4-(2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,7,13-三氧杂-12-氧代-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酰胺基)-2-甲基戊酸)(b-16)的合成。 将(2s,2’s,4r,4’r)-二叔丁基5,5′-((((((7s,15r,16s,24s)-15,16-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基丙酰胺)-6,9,14,17,22,25-六氧代-7,24-双(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-5,8,13,18,23,26-六氮杂三十烷-1,30-二基)双-(氮杂二烯基))双(4-将羟基-3,1-亚苯基))双(4-((叔丁氧基羰基)氨基)-2-甲基戊酸酯)(0.175g,0.0647mmol)溶解在二氯甲烷(6ml)中,然后加入tfa(2毫升)。将反应混合物在室温搅拌1小时,用甲苯(8ml)稀释,浓缩,得到(2s,2’s,4r,4’r)-5,5′-(((((7s,15r,16s,24s)-15,16-双(3-(2,5-二氧-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)-6,9,14,17,22,25-六氧-7,24-双(30-氧代-2,5,9,12,15,18,21,24,27-九氧杂-31-氮杂三十五烷-35-基)-5,8,13,18,23,26-六氮杂三十烷-1,30-二甲酰基双(氮杂二烷基)双(4-羟基-3,1-亚苯基))双(4-氨基-2-甲基戊酸)(155mg,100%产率)无需进一步纯化即可用于下一步。然后将化合物溶于dma(15ml)中,加入五氟苯基2-((6s,9r,11r)-6-((s)-仲丁基)-9-异丙基-2,3,3,8-四甲基-4,46,0.065mmol,7,13-三氧代-12-氧代-2,5,8-三氮杂十四烷-11-基)噻唑-4-羧酸酯和dipea(10μl,0.0575mmol)。将反应混合物搅拌过夜,浓缩并通过hplc纯化,用mecn/h2o梯度(c-18柱,20mm(d)x250mm(l),45分钟内从10%mecn至70%mecn,9ml/min)洗脱,得到标题产物(105.3mg,收率48%)。esimsm/z:c162h263n24o50s2[m+h]+计算值:3408.81,实测值:3408.60。 实施例260.(2s,4r)-4-羟基吡咯烷-2-羧酸甲酯盐酸盐的合成。 在0-4℃下,向反式-4-羟基-l-脯氨酸(15.0g,114.3mmol)的无水甲醇(250ml)溶液中滴加氯化亚砜(17ml,231mmol)。将所得混合物在室温搅拌过夜,浓缩,用etoh/正己烷结晶,得到标题化合物(18.0g,收率87%)。esimsm/z168.2([m+na]+)。 实施例261.(2s,4r)-1-叔丁基2-甲基4-羟基吡咯烷-1,2-二羧酸酯的合成。 向反式-4-羟基-l-脯氨酸甲酯(18.0g,107.0mmol)的甲醇(150ml)和碳酸氢钠溶液(2.0m,350ml)中,在4小时内分三批加入boc2o(30.0g,137.6),再搅拌4小时后,将反应浓缩至350ml,并用乙酸乙酯(4×80ml)萃取。合并的有机层用盐水(100ml)洗涤,用mgso4干燥,过滤,浓缩并通过硅胶柱色谱法(1∶1正己烷/乙酸乙酯)纯化,得到标题化合物(22.54g,收率86%)。esimsm/z268.2([m+na]+). 实施例262.(s)-1-叔丁基2-甲基4-氧代吡咯烷-1,2-二羧酸酯的合成。 可通过dess-martin氧化制备标题化合物,参考francomanfre等j.org.chem.1992,57,2060-2065。此外,也可用swern的氧化制备,操作步骤如下:将草酰氯(13.0ml,74.38mmol)的二氯甲烷(350ml)溶液冷却至-78℃,加入无水dmso(26.0ml)。将溶液在-78℃下搅拌15分钟,然后将(2s,4r)-1-叔丁基-2-甲基-4-羟基吡咯烷-1,2-二羧酸酯(8.0g,32.63mmol)的二氯甲烷(100ml)溶液加入。在-78℃下搅拌2小时后,滴加三乙胺(50ml,180.3mmol),将反应溶液升温至室温。将反应混合物用nah2po4溶液稀释(1.0m,400ml),分层,用二氯甲烷(2×60ml)萃取水层,合并有机层,用硫酸镁干燥,过滤,浓缩并通过硅胶柱层析(7:3正己烷/乙酸乙酯)纯化,得到标题化合物(6.73g,85%产率)。esimsm/z:266.2([m+na]+)。 实施例263.(s)-1-叔丁基2-甲基4-亚甲基吡咯烷-1,2-二羧酸酯的合成。 在0℃下,向溴化甲基三苯基鏻(19.62g,55.11mmol)的四氢呋喃(150ml)悬浮液中加入叔丁醇钾(6.20g,55.30mmol)的无水四氢呋喃(80ml)溶液。在0℃下搅拌2小时后,将得到的黄色叶立德加入到(s)-1-叔丁基-2-甲基4-氧代吡咯烷-1,2-二羧酸酯(6.70g,27.55mmol)的四氢呋喃(40ml)溶液中。在室温下搅拌1小时,浓缩反应混合物,用乙酸乙酯(200ml)稀释,用水(150ml),盐水(150ml)洗涤,经硫酸镁干燥,浓缩并在硅胶柱层析上纯化(9:1正己烷/乙酸乙酯),得到标题化合物(5.77g,87%产率)。eimsm/z:264([m+na]+)。 实施例264.(s)-甲基4-亚甲基吡咯烷-2-羧酸酯盐酸盐的合成。 在4℃下,向(s)-1-叔丁基-2-甲基-4-亚甲基吡咯烷-1,2-二羧酸酯(5.70g,23.63mmol)的乙酸乙酯(40ml)溶液中加入盐酸(12m,10ml)。将混合物搅拌1小时,用甲苯(50ml)稀释,浓缩,之后用乙醇/正己烷重结晶,得到标题化合物(3.85g,92%产率)。eimsm/z:142.2([m+h]+)。 实施例265.(s)-2-(羟甲基)-4-亚甲基吡咯烷-1-酸叔丁酯的合成。 在0℃下,向(s)-1-叔丁基2-甲基-4-亚甲基吡咯烷-1,2-二酸酯(5.20g,21.56mmol)的无水四氢呋喃(100ml)溶液中加入lialh4(15ml,2m四氢呋喃溶液)。在0℃下搅拌4小时后,通过加入甲醇(5ml)和水(20ml)淬灭反应。将反应混合物用1mhcl中和至ph7,用乙酸乙酯(80ml)稀释,通过硅藻土过滤,分离,水层用乙酸乙酯萃取。合并有机层,用硫酸钠干燥,浓缩并在硅胶柱色谱(1:5乙酸乙酯/二氯甲烷)上纯化,得到标题化合物(3.77g,82%产率)。eimsm/z:236.40([m+na]+)。 实施例266.(s)-(4-亚甲基吡咯烷-2-基)甲醇盐酸盐的合成。 在4℃下,向(s)-2-(羟甲基)-4-亚甲基吡咯烷-1-羧酸叔丁酯(3.70g,17.36mmol)的乙酸乙酯(30ml)溶液中加入hcl(12m,10ml)。将混合物搅拌1小时,用甲苯(50ml)稀释,浓缩,并用乙醇/正己烷结晶,得到标题盐酸盐(2.43g,94%产率)。eimsm/z:115.1([m+h]+)。 实施例267.4-(苄氧基)-3-甲氧基苯甲酸的合成。 向4-羟基-3-甲氧基苯甲酸(50.0g,297.5mmol)在乙醇(350ml)和氢氧化钠(2.0m,350ml)混合溶液中加入苄溴(140.0g,823.5mmol)。将混合物在65℃下搅拌8小时,浓缩,与水(2×400ml)共浓缩至约400ml,用6n盐酸酸化至ph3.0。过滤收集固体,用乙醇重结晶,在45℃下真空干燥,得到标题化合物(63.6g,83%产率)。esimsm/z:281.2([m+na]+)。 实施例268.4-(苄氧基)-5-甲氧基-2-硝基苯甲酸的合成。 向4-(苄氧基)-3-甲氧基苯甲酸(63.5g,246.0mmol)的二氯甲烷(400ml)和乙酸(100ml)溶液中加入发烟硝酸(25.0ml,528.5mmol)。将混合物搅拌6小时,浓缩,用乙醇结晶,在40℃下真空干燥,得到标题化合物(63.3g,85%产率)。esimsm/z:326.1([m+na]+)。 实施例269.(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(羟甲基)-4-亚甲基吡咯烷-1–1-基)甲酮的合成。 将催化量的dmf(30μl)加入到4-(苄氧基)-5-甲氧基-2-硝基苯甲酸(2.70g,8.91mmol)和草酰氯(2.0ml,22.50mmol)的无水二氯甲烷溶液中,将所得混合物在室温下搅拌2小时。用旋转蒸发仪除去过量的二氯甲烷和草酰氯。在n2条件下,0℃将乙酰氯重新悬浮在新鲜的二氯甲烷(70ml)中,并缓慢加入到预混合的((s)-(4-亚甲基吡咯烷-2-基)甲醇盐酸盐(1.32g,8.91mmol)和et3n(6ml)的二氯甲烷溶液中。将反应混合物升温至室温,继续搅拌8小时。除去二氯甲烷和et3n后,将残余物在水和乙酸乙酯(70/70ml)之间分配。用乙酸乙酯(2×60ml)进一步萃取水层。将合并的有机层用盐水(40ml)洗涤,干燥(硫酸镁)并浓缩。用快速硅胶柱层析(2:8正己烷/乙酸乙酯)纯化残余物,得到标题化合物(2.80g,76%产率)。eimsm/z:449.1([m+na]+)。 实施例270.(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(((叔丁基二甲基甲硅烷基)氧基)甲基)-4-亚甲基吡咯烷-1-基)甲酮的合成。 向(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(羟甲基)-4-亚甲基吡咯烷-1-基)甲酮(2.78g,8.52mmol)在二氯甲烷(10ml)和吡啶(10ml)的混合物中,加入叔丁基氯二甲基硅烷(2.50g,16.66mmol)。将混合物搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:6)洗脱,得到标题化合物(3.62g,83%产率,纯度95%)。msesim/z:c27h37n2o6si[m+h]+计算值513.23,实测值513.65。 实施例271.(s)-(4-羟基-5-甲氧基-2-硝基苯基)(2-(羟甲基)-4-亚甲基吡咯烷-1-基)甲酮的合成。 向(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(羟甲基)-4-亚甲基吡咯烷-1-基)甲酮(2.80g,7.03mmol)在二氯甲烷(30ml)和甲磺酸(8ml)的混合物中,加入phsch3(2.00g,14.06mmol)。将混合物搅拌0.5小时,用二氯甲烷(40ml)稀释,小心地用0.1mna2co3溶液中和。分离混合物,用二氯甲烷(2×10ml)萃取水溶液。合并有机层,用无水硫酸钠干燥,浓缩并在硅胶柱上纯化,用甲醇/二氯甲烷(1:15至1:6)洗脱,得到标题化合物(1.84g,85%产率,约95%纯度)。msesim/z:c14h17n2o6[m+h]+计算值309.10,实测值309.30。 实施例272.(s)-((戊烷-1,5-二基双(氧基))双(5-甲氧基-2-硝基-4,1-亚苯基))双(((s)-2-(羟甲基))-4-亚甲基吡咯烷-1-基)甲酮)的合成。 向(s)-(4-羟基-5-甲氧基-2-硝基苯基)(2-(羟甲基)-4-亚甲基吡咯烷-1-基)甲酮(0.801g,2.60mmol)的丁酮(10ml)溶液中,加入碳酸铯(2.50g,7.67mmol),然后加入1,5-二碘戊烷(415mmol,1.28mmol)。将混合物搅拌26小时,浓缩并在硅胶柱上纯化,用甲醇/二氯甲烷(1:15至1:5)洗脱,得到标题化合物(0.675g,77%产率,约95%纯度)。msesim/z:c33h41n4o12[m+h]+计算值685.26,实测值685.60。 实施例273.(s)-((戊烷-1,5-二基双(氧基))双(2-氨基-5-甲氧基-4,1-亚苯基))双(((s)-2-(羟甲基))-4-亚甲基吡咯烷基-1-基)甲酮)的合成。 在(s)-((戊烷-1,5-二基二(氧基))双(5-甲氧基-2-硝基-4,1-亚苯基))二(((s)-2-(羟甲基)-4-亚甲基吡咯-1-基)甲酮)(0.670g,0.98mmol)的甲醇(10ml)溶液中,加入na2s2o4(1.01g,5.80mmol)的水(8ml)溶液。将混合物在室温下搅拌超过30小时。浓缩反应混合物,并在高真空下与dma(2×10ml)和乙醇(2×10ml)共浓缩至干,得到含有无机盐的标题化合物(总重1.63g),其无需进一步纯化,直接用于下一步反应。eimsm/z:647.32([m+na]+)。 实施例274.c-01(具有双连接子的pbd二聚体类似物)的合成。 在0℃下,向含有吡啶(0.100ml,1.24mmol)的(3s,6s,39s,42s)-6,39-双(4-((叔丁氧基羰基)氨基)丁基)-22,23-双(2,5-二氧代-2,5-)二氢-1h-吡咯-1-基)-3,42-二((4-(羟甲基)苯基)氨基甲酰基)-5,8,21,24,37,40-六氧代-11,14,17,28,31,34-六氧杂-4,7,20,25,38,41-六氮杂四十四烷-1,44-二酸二叔丁酯的四氢呋喃(8ml)溶液中,滴加三光气(0.290mg,0.977mmol)的四氢呋喃(3.0ml)溶液。将反应混合物在0℃下搅拌15分钟,然后直接用于下一步骤。 在0℃下,向含有无机盐的(s)-((戊烷-1,5-二基二(氧基))双(2-氨基-5-甲氧基-4,1-亚苯基))二(((s)-2-(羟甲基)-4-亚甲基吡咯-1-基)甲酮(0.842mg,约0.49mmol)的乙醇(10ml)悬浮液中,加入前述四氢呋喃溶液。将混合物在0℃下搅拌4小时,然后升温至室温1小时,浓缩,并通过反相hplc(c18柱,10mm×250mm)纯化,用mecn/h2o梯度洗脱(10%mecn至100%mecn,40分钟,8ml/min),得到标题化合物(561.1mg,三步产率48%)。 实施例275.c-02(具有双连接子的pbd二聚体类似物)的合成。 在0℃下,将dess-martin试剂(138.0mg,0.329mmol)加入到化合物c-1(132.0mg,0.055mmol)的二氯甲烷(5.0ml)溶液中。将反应混合物升温至室温并搅拌2小时。然后加入饱和碳酸氢钠/na2so3溶液(5.0ml/5.0ml),用二氯甲烷(3×25ml)萃取混合物。将合并的有机层用碳酸氢钠/na2so3(5.0ml/5.0ml),盐水(10ml)洗涤,用无水硫酸钠干燥,过滤,浓缩并用反相hplc(c18柱,10mm×250mm)纯化,用mecn/h2o梯度洗脱(10%mecn至100%mecn,40分钟,8ml/min),得到标题化合物(103.1mg,78%产率),为泡沫状物。esimsm/z:c117h158n16o38[m+h]+计算值2396.09,实测值2396.65。 实施例276.c-03(具有双连接子的pbd二聚体类似物)的合成。 将c-2化合物(55.0mg,0.023mmol)溶于二氯甲烷(3ml)中,然后加入tfa(3ml)。将反应混合物在室温下搅拌2小时,然后浓缩,并与二氯甲烷/甲苯共浓缩至干,得到粗产物c-3(48.0mg,100%产率,hplc纯度92%),通过反相hplc(c18柱,10mm×250mm)纯化,用mecn/h2o梯度洗脱(10%mecn至100%mecn,40分钟,8ml/min),得到c-3(42.1mg,88%产率,96%纯度),为泡沫状固体。esimsm/z:c99h126n16o34[m+h]+计算值2083.86,实测值2084.35。 实施例277.c-04(具有双连接子的pbd二聚体类似物)的合成。 将c-03化合物(35.0mg,0.017mmol)溶于四氢呋喃(3ml)和nah2po4(0.1m,ph7.5,3ml)的混合溶液中,然后在2小时内分4批加入n-琥珀酰亚胺2,5,8,11,14,17,20,23-八氧杂二十六烷-26-酸酯(43.0mg,0.084mmol)。然后将反应混合物在室温下继续搅拌4小时,并与dmf(10ml)共蒸发至干,得到粗产物c-4,将其通过反相hplc进一步纯化(250(l)mm×20(d)mm,c18色谱柱,40分钟内20-60%乙腈/水,流速8ml/min),得到纯产物c-04(39.4mg,收率81%,纯度96%),为泡沫状物。esimsm/z:c135h195n16o52[m+h]+计算值:2872.30,实测值:2871.65。 实施例278.c-05(具有连接子的pbd二聚体类似物)的合成。 向c-04化合物(35.0mg,0.012mmol)和2,5,8,11,14,17,20,23-八氧二十五烷25-胺(15.1mg,0.0394mmol)的无水dma(2ml)溶液中加入edc(30.0mg,0.156mmol)。将反应混合物在室温搅拌14小时,浓缩,通过反相hplc纯化(250(l)mmx20(d)mm,c18柱,40分钟内20-60%乙腈/水,流速8ml/min),得到纯产物c-05(31.2mg,收率77%,hplc纯度97%),为泡沫状物。esimsm/z:c161h249n18o62[m+h]+计算值:3426.68,实测值:3427.21。 实施例279.(s)-1-(4-(苄氧基)-5-甲氧基-2-硝基苯甲酰基)-4-亚甲基吡咯烷-2-羧酸甲酯的合成。 在0℃,n2下,将催化量的dmf(30μl)加入到4-(苄氧基)-5-甲氧基-2-硝基苯甲酸(2.70g,8.91mmol)和草酰氯(2.0ml,22.50mmol)的无水二氯甲烷(70ml)溶液中,并将所得混合物在室温搅拌2小时。用旋转蒸发仪除去过量的溶剂和草酰氯。将乙酰氯重新悬浮在新鲜的二氯甲烷(70ml)中,并缓慢加入到预先混合的(s)-4-亚甲基吡咯烷-2-羧酸甲酯盐酸盐(1.58g,8.91mmol)和et3n(6ml)的二氯甲烷中。使反应混合物升温至室温,继续搅拌8小时。除去二氯甲烷和et3n后,将残留物在分配在水和乙酸乙酯(70/70ml)。将水层进一步用乙酸乙酯(2×60ml)萃取。合并的有机层用盐水(40ml)洗涤,干燥(mgso4)并浓缩。用快速柱色谱(2:8正己烷/乙酸乙酯)纯化残余物,得到标题化合物(2.88g,收率76%)。eimsm/z:449.1([m+na]+)。 实施例280.(s)-1-(4-(苄氧基)-5-甲氧基-2-硝基苯甲酰基)-4-亚甲基吡咯烷-2-甲醛的合成。 在-78℃和n2中,剧烈搅拌下向(s)-1-(4-(苄氧基)-5-甲氧基-2-硝基苯甲酰基)-4-亚甲基吡咯烷-2-羧酸甲酯(2.80g,6.57mmol)的无水二氯甲烷(60ml)溶液中滴加dibal-h(1n二氯甲烷,10ml)。将混合物再搅拌90分钟后,加入2ml甲醇,之后加入5%hcl(10ml)分解过量的试剂。将所得混合物升温至0℃,分离各层,将水层进一步用二氯甲烷(3×50ml)萃取。合并的有机层用盐水洗涤,干燥(mgso4)并浓缩。用快速柱色谱(95:5chcl3/甲醇)纯化残余物,得到标题化合物(2.19g,收率84%)。eimsm/z:419.1([m+na]+)。 实施例281.(s)-8-(苄氧基)-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]-吡咯并[1,2-a]氮杂-5(11ah)-酮的合成。 将(s)-1-(4-(苄氧基)-5-甲氧基-2-硝基苯甲酰基)-4-亚甲基吡咯烷-2-甲醛(2.18g,5.50mmol)和na2s2o4(8.0g,45.97mmol)的四氢呋喃(60ml)和水(40ml)溶液在室温搅拌20小时。在高真空下除去溶剂,将残余物重悬于甲醇(60ml)中,并逐滴加入hcl(6m)直至达到ph2。将得到的混合物在室温搅拌1小时。除去大部分甲醇,然后用乙酸乙酯(100ml)稀释,用饱和碳酸氢钠,盐水洗涤乙酸乙酯溶液,干燥(mgso4),浓缩。用快速柱色谱(97:3氯仿/甲醇)纯化残余物,得到标题化合物(1.52g,80%)。eimsm/z372.1([m+na]+)。 实施例282.(s)-8-羟基-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]-吡咯并[1,2-a]氮杂-5(11ah)-酮的合成。 在0℃下,向(s)-8-(苄氧基)-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]-吡咯并[1,2-a]氮杂-5(11ah)-酮(1.50g,4.32mmol)的二氯甲烷(70ml)溶液中加入25mlch3so3h。将混合物在0℃下搅拌10分钟,然后在室温下搅拌2小时,用二氯甲烷稀释,用冷的1.0n碳酸氢钠调节ph至4,并过滤。用二氯甲烷(3×60ml)萃取水层。合并有机层,经无水硫酸钠干燥,过滤,蒸发,并用硅胶柱色谱法纯化(ch3oh/二氯甲烷1∶15),得到811mg(收率73%)的标题产物。eimsm/z281.1([m+na]+)。 实施例283.(11as,11a’s)-8,8′-(戊烷-1,5-二基双(氧))二(7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(11ah)-酮)的合成。 向搅拌的碳酸铯(0.761g,2.33mmol)的丁酮(8ml)悬浮液中加入(s)-8-羟基-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯[1,2-a]氮杂-5(11ah)-酮(401mg,1.55mmol)和1,5-二碘戊烷(240mg,0.740mmol)。将混合物在室温下搅拌过夜,浓缩,并在硅胶柱上纯化(乙酸乙酯/二氯甲烷1:10),得到337mg(78%产率)标题产物。eimsm/z:607.2([m+na]+)。 实施例284.(s)-7-甲氧基-8-((5-((s)-7-甲氧基-2-亚甲基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧基)-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,22-a][1,4]二氮杂-5(11ah)-酮的合成。 在0℃下,向(11as,11a’s)-8,8’-(戊烷-1,5-二基双(氧))双(7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯烷[1,2-a][1,4]二氮杂-5(11ah)-酮)(150mg,0.256mmol)的无水二氯甲烷(1ml)和无水乙醇(1.5ml)的溶液中,加入硼氢化钠的甲氧基乙醚溶液(0.5m,85μl,0.042mmol)。5分钟后撤去冰浴,将混合物在室温下搅拌3小时,然后冷却至0℃,用饱和氯化铵淬灭,用二氯甲烷稀释,并分层。将有机层用盐水洗涤,用无水硫酸钠干燥,通过硅藻土过滤并浓缩。通过反相hplc(c18,乙腈/水)纯化残余物。将合适的组分用二氯甲烷萃取并浓缩,得到标题化合物(64.7mg,43%),msm/z:609.2([m+na]+),625.3([m+k]+),627.2([m+na+h2o]+);和完全还原的产物(16.5mg,11%),msm/z:611.2([m+na]+),627.2([m+k]+),629.2([m+na+h2o]+);回收未反应的原料(10.2mg,7%),msm/z:607.2([m+na]+),625.2([m+na+h2o]+)。 实施例285.(s)-8-((5-(((s)-10-(3-(2-(2-叠氮基乙氧基)乙氧基)丙酰基)-7-甲氧基-2-亚甲基-5-氧代-23,5,10,11,11a六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧)-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(11ah)-酮的合成。 向(s)-7-甲氧基-8-((5-(((s)-7-甲氧基-2-亚甲基-5-氧代-2,3,5,10,11,11a-六氢)-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-8-基)氧基)戊基)氧基)-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(11ah)-酮(60.0mg,0.102mmol)和2,5-二氧代吡咯烷-1-基3-(2-(2-叠氮基乙氧基)乙氧基)丙酸酯(40.5mg,0.134mmol)的二氯甲烷(5ml)的混合物中加入edc(100.5mg,0.520mmol)。将混合物在室温下搅拌过夜,浓缩并在硅胶柱上纯化(乙酸乙酯/二氯甲烷,1:6),得到63.1mg(81%产率)标题产物。esimsm/z:c40h50n7o9[m+h]+计算值772.36,实测值772.30。 实施例286.(s)-8-((5-((s)-10-(3-(2-(2-氨基乙氧基)乙氧基)丙酰基)-7-甲氧基-2-亚甲基-5-氧代-23,5,10,11,11a六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧)-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(11ah)-酮的合成。 向(s)-8-((5-(((s)-10-(3-(2-(2-叠氮基乙氧基)乙氧基)丙酰基)-7-甲氧基-2-亚甲基-5-氧代-2,3,5,10,11,11a六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧基)-7-甲氧基-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(11ah)-酮(60mg,0.078mmol),四氢呋喃(5ml)和nah2po4缓冲溶液(ph7.5,1.0m,0.7ml)的混合物中加入pph3(70mg,0.267mmol)。将混合物在室温下搅拌过夜,浓缩后在制备hplc上纯化,用水/乙腈(35分钟,从90%水至35%水)洗脱,在高真空下干燥后得到45.1mg(79%产率)标题产物。esimsm/z:c40h52n5o9[m+h]+计算值746.37,实测值746.50。 实施例287.(s)-n-(2-((s)-8-((5-(((11s,11as)-10-((s)-15-叠氮基-5-异丙基-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十七烷-1-酰基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)-氧基)-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-10(5h)-基)-2-氧代乙基)-2-(3-(2-(2-叠氮基乙氧基)乙氧基)丙酰胺基)-3-甲基丁酰胺的合成。 向(s)-7-甲氧基-8-((5-(((s)-7-甲氧基-2-亚甲基-5-氧代2,3,5,10,11,11a六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧基)-2-亚甲基-2,3-二氢-1h-苯并[e]吡咯并[1,2a][1,4]二氮杂-5(11ah)-酮(60.0mg,0.102mmol)和(s)-15-叠氮基-5-异丙基-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十七-1-酸(90.2mg,0.25mmol)在dma(8ml)的混合物中,加入brop(240.2mg,0.618mmol)。在室温下搅拌该混合物过夜,浓缩并在硅胶柱色谱(甲醇/二氯甲烷,1:10至1:5)上纯化,得到97.1mg(74%产率)标题产物。esimsm/z:c61h87n14o17[m+h]+,计算值1287.63,实测值1287.95。 实施例288.(s)-n-(2-((s)-8-((5-(((11s,11as)-10-((s)-15-氨基-5-异丙基-4,7-二氧代10,13-二氧杂-3,6-二氮杂十七烷-1-酰基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代2,3,5,10,11,11a六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧基)-7-甲氧基-2-亚甲基-5-氧代2,3,11,11a四氢1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-10(5h)-基)-2-氧代乙基)-2-(3-(2-(2-氨基乙氧基)乙氧基)-丙酰胺基)-3-甲基丁酰胺(c-06)合成。 向(s)-n-(2-((s)-8-((5-(((11s,11as)-10-((s)-15-叠氮基-5-异丙基-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十七烷-1-酰基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代2,3,5,10,11,11a六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)-氧基)-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a四氢-1h-苯并[e]吡咯并[1,2,2-a][1,4]二氮杂-10(5h)-基)-2-氧代乙基)-2-(3-(2-(2-叠氮基乙氧基)乙氧基)丙酰胺基)-3-甲基丁酰胺(85mg,0.066mmol)在四氢呋喃(5ml)和nah2po4缓冲溶液(ph7.5,1.0m,0.7ml)的混合物中加入pph3(100mg,0.381mmol)。将混合物在室温下搅拌过夜,经lc-ms确认形成(s)-n-(2-((s)-8-((5-(((11s,11as)-10-((s)-15-氨基-5-异丙基)-4,7-二氧代-10,13-二氧杂-3,6-二氮杂十七烷-1-酰基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-8-基)氧基)戊基)氧)-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-α][1,4]二氮杂-10(5h)-基)-2-氧代乙基)-2-(3-(2-(2-氨基乙氧基)乙氧基)丙酰胺基)-3-甲基丁酰胺(esimsm/z:c61h90n10o17[m+na]+,计算值1257.66,实测值1257.90)后,加入双(2,5-二氧代吡咯烷-1-基)2,3-双(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)琥珀酸酯(33mg,0.066mmol)。将混合物继续搅拌4小时,浓缩后在制备型hplc上纯化,用水/ch3cn(从90%水至30%水,35分钟)洗脱,在高真空下干燥后,得到40.1mg(40%产率)标题产物。esimsm/z:c73h95n12o23[m+h]+,计算值1507.66,实测值1507.90。 实施例289.4,4′-(戊烷-1,5-二基双(氧基))双(3-甲氧基苯甲酸)的合成。 在4小时内将二碘丙烷(19.0g,58.6mmol)的四氢呋喃(75ml)溶液滴加到65℃,剧烈搅拌的香草酸(20.0g,119mmol)在四氢呋喃(150ml)和naoh(340ml)水溶液中(避光,铝箔包裹烧瓶)。在暗处加热回流48小时后,将溶液冷却,真空蒸发除去四氢呋喃。残余物用乙酸乙酯萃取,分离水层,并用浓盐酸酸化至ph2。过滤收集得到的沉淀物,洗涤,干燥,并用冰醋酸重结晶,得到相应的双羧酸(14.0g,34.7mmol),为白色固体,收率60%。 实施例290.4,4′-(戊烷-1,5-二基双(氧基))双(5-甲氧基-2-硝基苯甲酸)的合成。 向悬浮在hoac(80ml,1800mmol)中的4,4′-(戊烷-1,5-二烷基双(氧基))双(3-甲氧基苯甲酸)(18.0g,66.8mmol),在室温下滴加hno3(80ml,1778mmol)。搅拌2小时后,将混合物倒入100g冰中,用乙酸乙酯萃取(2×200ml)。分离有机层,并用水(2×100ml)洗涤,然后加入4nnaoh(400ml)。用乙酸乙酯(2×100ml)萃取后,分离碱性水层,并用浓盐酸酸化至ph2。用乙酸乙酯(2×250ml)萃取混合物。合并的有机萃取物用盐水洗涤,干燥,过滤并浓缩。通过快速柱色谱纯化残余物(二氯甲烷/甲醇4:1),得到4,4′-(戊烷-1,5-二基双(氧基))双(5-甲氧基-2-硝基苯甲酸)浅黄色固体(6.1g,12.3mmol),产率为18%。rf=0.3(二氯甲烷/甲醇3:1)。 实施例291.(s)-((戊烷-1,5-二基双(氧基))双(5-甲氧基-2-硝基-4,1-亚苯基))双(((s)-2-(羟甲基))吡咯烷-1-基)甲酮)的合成。 在室温下,向4,4′-(戊烷-1,5-二烷基双(氧基))双(5-甲氧基-2-硝基苯甲酸)(5.0g,10.0mmol)和l-(+)-脯氨醇(2.25g)的dmf(100ml)溶液中加入tea(4.0g)。搅拌10分钟后,加入hatu(10.77g,28.3mmol)。将混合物在室温搅拌过夜。反应完成后,将混合物用水(100ml)稀释,并用乙酸乙酯(2×100ml)和二氯甲烷(2×50ml)萃取,将合并的有机萃取物用盐水洗涤,干燥,过滤并浓缩。残余物通过柱色谱法纯化(二氯甲烷/甲醇15:1),得到(s)-((戊烷-1,5-二基双(氧基))双(5-甲氧基-2-硝基-4,1-亚苯基)双(((s)-2-(羟甲基)吡咯烷-1-基)甲酮)(6.0g,9.1mmol),为白色泡沫状,收率91%。 实施例292.(s)-((戊烷-1,5-二基双(氧基))双(2-氨基-5-甲氧基-4,1-亚苯基))双(((s)-2-(羟甲基))的合成)吡咯烷-1-基)甲酮)的合成。 将(s)-((戊烷-1,5-二基双(氧基))双(5-甲氧基-2-硝基-4,1-亚苯基))-双((((s)-2-(羟甲基)吡咯烷-1-基)甲酮(6.0g,9.1mmol)的甲醇(100ml)溶液和10%pd/c(2.4g)混合,将混合物在氢气氛下于室温搅拌过夜。搅拌14小时后,过滤除去pd/c,并用甲醇洗涤,浓缩,并将残余物通过柱色谱法纯化(10:1二氯甲烷/甲醇),得到(s)-((戊烷-1),5-二基双(氧基))双(2-氨基-5-甲氧基-4,1-亚苯基))双((((s)-2-(羟甲基)吡咯烷-1-基)甲酮)(3.54g,5.9mmol)为白色泡沫状,收率为65%。 实施例293.双(4-((s)-2-((s)-2-((((烯丙氧基)羰基)氨基)-3-甲基丁亚酰胺基)丙酰胺基)苄基)((s)-(戊烷-1,5-二基双(氧基)双(2-((s)-2-(羟甲基)吡咯烷-1-羰基)-4-甲氧基-5,1-亚苯基))二氨基甲酸酯的合成。 在5℃下,向((s)-1-(((s)-1-((4-(羟甲基)苯基)氨基)-1-氧丙烷-2-基)氨基)-3-甲基-1-氧代丁烷-2-基)氨基甲酸烯丙基酯(8.0g,21.3mmol)的无水四氢呋喃(300ml)溶液中加入dipea(5.5g,40.3mmol)和三光气的无水四氢呋喃(50ml)溶液(3.2g,10.8mmol)。搅拌15分钟后,将溶液重新冷却至5℃,加入(s)-((戊烷-1,5-二烷基双(氧基))双(2-氨基-5-甲氧基-4,1-亚苯基)双(((s)-2-(羟甲基)-吡咯烷-1-基)甲酮)(3.2g,5.3mmol)和dipea(2.75g,21.6mmol)的无水四氢呋喃(150ml)溶液。使所得溶液升温至室温,并搅拌过夜。通过真空蒸发除去四氢呋喃。残余物通过柱色谱法纯化(20:1二氯甲烷/甲醇),得到双(4-((s)-2-((s)-2-(((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基。)-苄基)((s)-(戊烷-1,5-二基双(氧基))双(2-((s)-2-(羟甲基)吡咯烷-1-羰基)-4-甲氧基-5,1-亚苯基))二氨基甲酸酯(7.0g,4.97mmol),为黄色泡沫,收率94%。 实施例294.(11s,11as,11’s,11a’s)-双(4-((s)-2-((s)-2-((((烯丙氧基)羰基)-氨基)-3-甲基丁酰胺基)丙酰胺基)的合成苄基)8,8′-(戊烷-1,5-二基双(氧基))双(11-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 在室温下,氮气中,向双(4-((s)-2-((s)-2-((((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基)苄基)((s)-(戊烷-1),5-二基双(氧基)双(2-((s)-2-(羟基甲基)吡咯烷-1-羰基)-4-甲氧基-5,1-亚苯基))二氨基甲酸酯(300mg,0.21mmol)的无水二氯甲烷(15ml)溶液中加入dmp(280mg,0.66mmol)。反应完成后,向反应溶液中加入na2so3水溶液,然后加入碳酸氢钠水溶液,将混合物再搅拌15分钟,并用二氯甲烷(3×20ml)萃取。合并的有机萃取物用盐水洗涤,干燥,过滤并浓缩。残余物通过柱色谱法纯化(20:1二氯甲烷/甲醇),得到(11s,11as,11’s,11a’s)-双(4-((s)-2-((s)-2-(((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基)8,8′-(戊烷-1,5-二基双(氧基))双(11-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(270mg,0.19mmol),为白色泡沫状,产率92%。 实施例295.(11s,11as,11’s,11a’s)-双(4-((s)-2-((s)-2-((((烯丙氧基)羰基)-氨基)-3-甲基丁酰胺基)丙酰胺基)苄基)8,8′-(戊烷-1,5-二基双(氧基))双(11-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 向(11s,11as,11’s,11a’s)-双(4-((s)-2-((s)-2-((((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基)苄基)8,8′-(戊烷-1,5-二基双(氧基))双(11-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂10(5h)-羧酸酯(774mg,0.55mmol)与吡咯烷(196mg,2.76mmol)的无水二氯甲烷(8ml)溶液中,加入(pd(pph3)4(76mg,0.066mmol)。反应在氩气中室温下搅拌2小时,然后将反应物用二氯甲烷稀释并依次用饱和nh4cl水溶液和盐水洗涤。有机相经无水硫酸钠干燥,过滤并浓缩。残余物通过柱色谱法纯化(6:1二氯甲烷/甲醇),得到(11s,11as,11’s,11a’s)-双(4-((s)-2-((s)-2-(((烯丙氧基)羰基)氨基)-3-甲基-丁酰胺基)丙酰胺基)8,8′-(戊烷-1,5-二基双(氧基))双(11-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]-吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(420mg,0.34mmol),为白色固体,收率62%。 实施例296.(s)-2-((((烯丙氧基)羰基)氨基)-3-甲基丁酸的合成。 将氯甲酸烯丙酯(24.8g,205mmol)滴加到搅拌的l-缬氨酸(20g,171mmol)和k2co3(35.4g,257mmol)在水(250ml)和四氢呋喃(250ml)溶液中。将反应混合物在室温搅拌过夜,然后将溶剂减压浓缩,并将剩余溶液用乙醚(100ml)洗。用浓盐酸将水部分酸化至ph2,并用二氯甲烷(3×200ml)萃取。合并的有机相用盐水洗涤,经无水硫酸钠干燥,过滤并浓缩,得到产物(35g,174mmol),为白色固体,收率100%。 实施例297.(s)-2,5-二氧杂吡咯烷-1-基2-(((烯丙氧基)羰基)氨基)-3-甲基丁酸酯的合成。 在室温下,向搅拌的(s)-2-(((烯丙氧基)羰基)氨基)-3-甲基丁酸(35g,174mmol)的无水二氯甲烷(500ml)溶液中,加入edc(66.9g,348mmol)和n-羟基琥珀酰亚胺(30g,261mmol)。搅拌14小时后,将反应物用二氯甲烷稀释并用水和盐水洗涤。有机相经无水硫酸钠干燥,过滤并浓缩,得到产物(54.5g),为粘性无色油,其无需进一步纯化即可用于下一步骤。rf=0.5(2:1石油醚/乙酸乙酯) 实施例298.(s)-2-((s)-2-((((烯丙氧基)羰基)氨基)-3-甲基丁亚氨基)-丙酸的合成。 在室温下,向h-ala-oh(15.7g,176mmol)和碳酸氢钠(15.5g,185mmol)的四氢呋喃(200ml)和水(200ml)溶液中加入(s)-2,5-二氧吡咯烷-1-基2-(((烯丙氧基)-羰基)氨基)-3-甲基丁酯(50g,168mmol)的四氢呋喃(100ml)溶液。搅拌72小时后,减压蒸发四氢呋喃。用柠檬酸将残余物酸化至ph3,并用乙酸乙酯(3x350ml)萃取,将合并的萃取物用盐水洗涤,干燥,过滤并浓缩,得到白色固体。用乙醚(过量)打浆,得到纯的产物,为白色粉末(25.2g,93mmol,55%)。 实施例299.((s)-1-(((s)-1-((4-(羟甲基)苯基)氨基)-1-氧代丙烷-2-基)氨基)-3-甲基-1-氧代丁烷-2-基)氨基甲酸烯丙酯的合成。 室温下,向(s)-2-((s)-2-(((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)-丙酸(25.2g,92.6mmol)和对氨基苄醇(12.0g,97.6mmol)的四氢呋喃(300ml)溶液中加入eedq(24.0g,97.2mmol)。搅拌18小时后,减压蒸发除去溶剂,得到浅棕色固体。将固体用乙醚打浆并过滤,用过量乙醚洗涤,得到白色固体(40g,106mmol,100%)。 实施例300.4-(((苄氧基)羰基)氨基)丁酸的合成。 在5℃下,将na2co3(41.1g,387mmol)加入到4-氨基丁酸(20g,193mmol)的水溶液(300ml)中。搅拌10分钟后,滴加cbzcl(33.2ml,232mmol)的四氢呋喃(100ml)溶液。使反应升温至室温,并搅拌过夜。反应完成后,将混合物用水(100ml)稀释,并用乙酸乙酯(2×100ml)洗。用浓盐酸将水层酸化至ph2。并用乙酸乙酯(3×100ml)萃取。合并的有机物用盐水洗涤,经无水硫酸钠干燥,过滤并浓缩,得到白色固体。用石油醚(过量)打浆,得到纯的产物,为白色粉末(31.6g,70%)。 实施例301.4-((((苄氧基)羰基)氨基)丁酸叔丁酯的合成。 在5℃下,向4-((((苄氧基)羰基)氨基)丁酸(5.9g,24.9mmol)和叔丁醇(14.7g,199mmol)的无水二氯甲烷(250ml)溶液中加入dmap(0.61)和dic(4.7g,37.3mmol)。搅拌16小时后,将反应物过滤并用二氯甲烷(2×200ml)萃取,合并的有机萃取物用1nhcl,盐洗涤,用无水硫酸钠干燥,过滤并浓缩。残余物通过柱色谱法纯化(100%二氯甲烷),得到4-((((苄氧基)羰基)氨基)氨基叔丁酸叔丁酯(4.26g,14.5mmol,58%),为粘性无色油状物。 实施例302.4-氨基丁酸叔丁酯的合成。 将4-((((苄氧基)羰基)氨基)丁酸叔丁酯(1.69g,5.77mmol)的甲醇(40ml)溶液与10%pd/c(400mg)混合,在氢气下将混合物于室温下搅拌过夜,搅拌14小时后,过滤除去pd/c,并用甲醇洗涤。浓缩滤液,得到产物,其无需进一步纯化即可用于下一步(897mg,5.64mmol),无色液体,收率98%。 实施例303.(2r,3s)-2,3-双(苄基氨基)琥珀酸的合成。 向内消旋-2,3-二溴丁二酸(50g,181mmol)的乙醇(400ml)溶液中滴加苄胺(150ml),加入完成后,加热至90℃,搅拌过夜。将该混合物冷却至室温并用水稀释,加入6nhcl直至ph为4,得到白色沉淀物,将沉淀物过滤,用水洗涤并干燥,得到(2r,3s)-2,3-双(苄基氨基)琥珀酸(50g,152mmol,84%)。 实施例304.(2r,3s)-2,3-二氨基琥珀酸的合成。 将(2r,3s)-2,3-双(苄氨基)琥珀酸(18g,55mmol)的acoh(100ml)和hcl(100ml)溶液与10%pd/c(3g)混合,在氢气中于50℃搅拌过夜,搅拌48h后,过滤除去pd/c,用水洗涤。加入acoh直至ph为5,得到白色沉淀,将沉淀过滤,用水洗并干燥,得到(2r,3s)-2,3-二氨基琥珀酸(8.7g,58.8g,100%)。 实施例305.2,3-双(((苄氧基)羰基)氨基)琥珀酸的合成。 在0℃下,向(2r,3s)-2,3-二氨基琥珀酸(31.74g,214mmol)的四氢呋喃(220ml)和4nnaoh(214ml)溶液中滴加cbzcl(61ml,428mmol)。加入完成后,将混合物升温至室温并搅拌2小时,将反应混合物用水(1600ml)稀释,并用乙酸乙酯(2×15600ml)萃取。分离水层并用浓hcl酸化直至达到ph2,将所得溶液搅拌1小时并在5℃下静置以得到白色沉淀物,将沉淀物过滤,用水洗并干燥,得到2,3-双((((苄氧基)羰基)氨基)氨基)琥珀酸(52.2g,125mmol,59%)。 实施例306.((3r,4s)-2,5-二氧四氢呋喃-3,4-二基)二氨基甲酸二苄基酯的合成。 将2,3-双((((苄氧基)羰基)氨基)琥珀酸琥珀酸(5.0g,12mmol)在ac2o(37.5ml)中回流20分钟,冷却并浓缩,得到酸酐。将非对映异构体混合物与氯仿(37ml)混合,过滤收集不溶的内消旋异构体,并用石油醚洗涤,得到((3r,4s)-2,5-二氧四氢呋喃-3,4-二基)二氨基甲酸二苄酯(2.0g,5mmol,42%)。 实施例307.4,4′-((((2r,3s)-2,3-双((((苄氧基)羰基)-氨基)琥珀酰基)双(氮杂二基))二丁酸二叔丁酯的合成。 在0℃下,向((3r,4s)-2,5-二氧四氢呋喃-3,4-二基)二氨基甲酸二苄酯(2.03g,5.1mmol)和4-氨基丁酸叔丁酯(1.79g,11.3mmol)的dmf(45ml)溶液加入dipea(1.98g,15.3mmol)。搅拌5分钟后,加入hatu(4.66g,12.3mmol),将混合物升温至室温并搅拌2小时。反应完成后,将混合物用水(90ml)稀释并用乙酸乙酯(2×200ml)和二氯甲烷(2×90ml)萃取,将合并的有机萃取物用盐水洗涤,并用无水硫酸钠干燥。减压除去大部分溶剂,将白色沉淀收集并干燥,得到4,4′-((((2r,3s)-2,3-双(((苄氧基)))羰基)氨基)琥珀酰基)双(氮杂二烷基))二丁酸二叔丁酯(2.8g,4.0mmol),为白色固体,收率为80%。 实施例308.4,4′-((((2r,3s)-2,3-二氨基琥珀酰基)双-(氮杂二基))二丁酸二叔丁酯的合成。 将4,4′-((((2r,3s)-2,3-双((((苄氧基)羰基)氨基)琥珀酰基)双-(氮杂二烷基))二丁酸二叔丁酯(2.8g,4.0mmol)的甲醇(100ml)溶液与10%pd/c(1.1g)混合,在氢气下于室温搅拌过夜,搅拌18小时后,过滤除去pd/c,用甲醇洗涤。浓缩滤液,得到产物,为无色液体(940mg,2.2mmol,收率55%),其无需进一步纯化即可用于下一步。 实施例309.4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-)基)丁二酰胺)琥珀酰基)双(氮杂二基)二丁酸二叔丁酯。 在0℃下,向4,4′-(((((2r,3s)-2,3-二氨基琥珀酰)双(氮杂二烯基))-二丁酸二叔丁酯(940mg,2.19mmol)和4-(2,5-二氧代2,5-二氢-1h-吡咯-1-基)丁酸(840mg,4.59mmol)的dmf(25ml)溶液中加入dipea(1.13g,8.76mmol)。搅拌5分钟后加入hatu(1.74g,4.58mmol)。将混合物升温至室温并搅拌1小时,反应完成后,将混合物用水(50ml)稀释,并用乙酸乙酯(2×100ml)和二氯甲烷(2×50ml)萃取,合并的有机萃取物经盐水洗涤并经无水硫酸钠干燥。减压除去大部分溶剂,将白色固体收集并干燥,得到4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丁二酰亚胺基)琥珀酰基双(氮杂二基)二丁酸二叔丁酯(1.36g,1.79mmol,产率82%)。 实施例310.4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丁酰胺基)琥珀酰亚胺)琥珀酰基)双(氮杂二基)二丁酸的合成。 在0℃下,向4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丁酰胺基)琥珀酰基)双(氮杂二烷基))二丁酸二叔丁酯(1.36g,1.79mmol)的二氯甲烷(15ml)溶液中加入tfa(30ml)。搅拌18小时后,将反应浓缩,并将残余物溶于无水甲苯中。真空蒸发除去溶剂,得到白色沉淀物(1.3mg,2.0mmol,收率100%),无需进一步纯化即可用于下一步骤。 实施例311.pbd产物c-07的合成。 在0℃下,向(11s,11as,11’s,11a’s))-双(4-((s)-2-((s)-2-((((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基)苄基8,8′-(戊烷-1,5-二基双(氧基))双(11-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯[1],2-a][1,4]二氮杂-10(5h)-羧酸酯)(215mg,0.17mmol)和4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丁酰胺基)琥珀酰基)双(氮杂二基))二丁酸(115mg,0.18mmol)的dmf(18ml)溶液中加入dipea(90mg,0.70mmol)。搅拌5分钟后,加入hatu(132mg,0.35mmol),使混合物升温至室温,并搅拌过夜。反应完成后,将混合物用水(20ml)稀释,并用乙酸乙酯(2×40ml)和二氯甲烷(2×20ml)萃取,将合并的有机萃取液用盐水洗涤,干燥,过滤并浓缩。残余物通过hplc纯化,得到pbd产物c-07(10mg),为白色粉末。esimsm/z:c91h115n16o26[m+h]+,计算值:1847.81,实测值:1847.60。 实施例312.4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)琥珀酰)双(氮杂二基)二丁酸二叔丁酯。 在0℃下,向4,4′-((((2r,3s)-2,3-二氨基琥珀酰基)双(氮杂二基))-二丁酸二叔丁酯(900mg,2.09mmol)和3-(2,5-二氧代2,5-二氢-1h-吡咯-1-基)丙酸(840mg,4.97mmol)的dmf(25ml)溶液中加入dipea(0.93g,7.21mmol)。搅拌5分钟后,加入edc(1.74g,9.06mmol)。使混合物升温至室温,并搅拌1小时。反应完成后,将混合物用水(50ml)稀释,并用乙酸乙酯(2×100ml)和二氯甲烷(2×50ml)萃取,将合并的有机萃取物用盐水洗涤并用无水硫酸钠干燥。减压浓缩除去大部分溶剂,沉淀出白色固体,将其收集并干燥,得到4,4′-((((2r,3s)-2,3-双(3-(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)丙酰胺基)琥珀酰基)双-(氮杂二基))二丁酸二叔丁酯(1.27g,1.79mmol,产率83%)。esimsm/z:c34h49n6o12[m+h]+,计算值:733.33,实测值:733.55。 实施例313.4,4′-((((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基)丙酰胺基)琥珀酰基)双(氮杂二基))二丁酸的合成。 在4℃下,向4,4′-((((2r,3s)-2,3-双(4-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丁酰胺基)琥珀酰)双(氮杂二烷基))二丁酸二叔丁酯(502.0mg,0.685mmol)的1,4-二氧六环中加入hcl(3ml),然后将混合物在室温搅拌30分钟,用1,4-二氧六环(8ml)稀释,浓缩,与1,4-二氧六环/甲苯(1:1,2×10ml)共同蒸发至干,并用乙醇/正己烷结晶,得到标题化合物(289.0g,收率68%)。esimsm/z:c26h33n6o12[m+h]+,计算值:621.21,实测值:621.55。 实施例314.((s)-3-甲基-1-(((s)-1-((4-((((4-硝基苯氧基)羰基)-氧代)甲基)苯基)氨基)-1-氧代丙烷-2-基)氨基)-1-氧代丁-2-基)氨基甲酸烯丙酯的合成。 向((s)-1-((((s)-1-((4-(羟甲基)苯基)氨基)-1-氧丙烷-2-基)氨基)-3-甲基-1-氧代丁基-2-基)氨基甲酸烯丙酯(2.21g,5.86mmol)的无水吡啶(5ml)和二氯甲烷(20ml)的混合物中加入4-硝基苯基碳酰氯(1.82g,9.05mmol)。将混合物在室温搅拌8小时,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:12)洗脱,得到标题化合物(2.63g,收率83%)。esimsm/z:c26h31n4o9[m+h]+计算值:543.21,实测值:543.60。 实施例315.(11as,11a’s)-双(4-((s)-2-((s)-2-(((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基)苄基8,8′-(戊烷-1,5-二基双(氧基))双(7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 向(11as,11a’s)-8,8′-(戊烷-1,5-二基双(氧基))双(7-甲氧基-2-亚甲基-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂-5(10h)-酮)(288.2mg,0.490mmol)的无水乙腈(5ml)溶液中加入((s)-3-甲基-1-(((s)-1-((4-(((((4-硝基苯氧基)羰基)氧基)-甲基)苯基)氨基)-1-氧丙烷-2-氨基)-1-氧丁基-2-基)氨基甲酸烯丙酯(770.2mg,1.420mmol)和dipea(2ml)。将混合物在45℃下搅拌8小时,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶8)洗脱,得到标题化合物(492.0mg,收率72%)。msesim/z:c73h91n10o18[m+h]+计算值:1395.64,实测值:1395.95。 实施例316.(11as,11a’s)-双(4-((s)-2-((s)-2-氨基-3-甲基丁酰胺基)-丙酰胺基)苄基)8,8′-(戊烷-1,5-二基双(氧基)双(7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯)的合成。 向(11as,11a’s)-双(4-((s)-2-((s)-2-(((烯丙氧基)羰基)氨基)-3-甲基丁酰胺基)丙酰胺基)苄基)8,8′-(戊烷-1,5-二基双(氧基))双(7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(274.2mg,0.197mmol)的二氯甲烷(5ml)溶液中加入吡咯烷(49mg,6.90mmol)和pd(pph3)4(152.0mg,0.132,mmol)。将反应在氩气下室温搅拌2小时,然后用二氯甲烷稀释,并依次用饱和氯化铵水溶液和盐水洗涤。有机相经无水硫酸钠干燥,过滤并浓缩。残余物通过柱色谱法纯化(二氯甲烷/甲醇/三乙胺=6/1/0.02),得到标题化合物(166.7mg,收率69%),为灰白色固体。msesim/z:c65h83n10o14[m+h]+计算值:1227.60,实测值:1227.93。 实施例317.pbd产物c-08的合成。 向(11as,11a’s)-双(4-((s)-2-((s)-2-氨基-3-甲基丁亚氨基)-丙酰胺基)苄基)8,8′-(戊烷-1,5-二基双(氧基)))双(7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯)(151.1mg,0.123mmol)和4,4′-((((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢代-1h-吡咯-1-基)丙酰胺)琥珀酰基)双(氮杂二基)二丁酸(77.1mg,0.124mmol)的dma(5ml)溶液中加入edc(95.2mg,0.496mmol)。将混合物在室温下搅拌8小时,浓缩并通过c-18hplc(3μm,25×4cm)纯化,用乙腈(a)和0.1%甲酸/水(b)梯度洗脱(15%a至25%a,5分钟;35%a,15分钟;60%a至50%a,15分钟;15%a,5分钟;流速为8ml/min)。合并含有标题化合物组分,浓缩,并在干燥器中用p2o5干燥,得到c-8化合物(149.2mg,收率67%)。msesim/z:c91h111n16o24[m+h]+计算值:1811.79,实测值:1812.35。 实施例318.(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(羟基-乙基)吡咯烷基-1-基)甲酮的合成。 向4-(苄氧基)-5-甲氧基-2-硝基苯甲酸(10.20g,33.65mmol)和(s)-吡咯烷-2-基甲醇(3.85g,38.09mmol)的无水dmf(150ml)溶液中加入edc(19.50g,101.56mmol)。将混合物在室温搅拌过夜,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶4)洗脱,得到标题化合物(11.56g,89%产率)。msesim/z:c20h23n2o6[m+h]+计算值:387.15,实测值:387.65。 实施例319.(s)-1-(4-(苄氧基)-5-甲氧基-2-硝基苯甲酰基)吡咯烷-2-甲醛的合成。 在室温下氮气中,向(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(羟甲基)-吡咯烷-1-基)甲酮(3.80g,9.84mmol)的无水二氯甲烷(15ml)溶液中加入dess-martin试剂(dmp)(5.80g,13.67mmol)。反应完成后,向反应溶液中加入na2so3水溶液,然后加入碳酸氢钠水溶液,将混合物再搅拌15分钟,并用二氯甲烷(3×20ml)萃取。合并的有机萃取物用盐水洗涤,干燥,过滤并浓缩。残余物通过硅胶柱色谱纯化(二氯甲烷/乙酸乙酯=4/1),得到标题化合物(3.13g,收率83%),为灰白色泡沫。msesim/z:c20h21n2o6[m+h]+计算值:385.13,实测值:385.60;404.75[m+h2o+h]+。 实施例320.8-羟基-7-甲氧基-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(10h)-酮的合成。 在氢化反应器中,将pd/c(10%pd,50%wet,250mg)加入到(s)-1-(4-(苄氧基)-5-甲氧基-2-硝基苯甲酰基)吡咯烷-2-甲醛(3.00g,7.80mmol)的甲醇(75ml)溶液中。抽空反应器中的空气后,充入氢气(5psi)。将反应容器振荡过夜,并通过硅藻土过滤。将滤液浓缩并通过硅胶柱色谱纯化(二氯甲烷/甲醇/三乙胺=4/1/0.05),得到标题化合物(1.66g,收率86%),为灰白色泡沫。msesim/z:c13h17n2o3[m+h]+计算值:249.12,实测值:249.50。 实施例321.4-((14s,17s)-1-叠氮基17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-((叔丁氧基羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺基)苄基8–羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 在4-8℃下,向(14s,17s)-1-叠氮基-14-(4-((叔丁氧基羰基)氨基)丁基)-17-((4-(羟甲基)苯基)氨基甲酰基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氧杂十九烷-19-叔丁酯(10.15g,13.50mmol)的无水四氢呋喃(300ml)溶液中加入dipea(3.15g,24.41mmol)和三光气的无水四氢呋喃(50ml,5.15g,17.36mmol)溶液。搅拌15分钟后,在45分钟内滴加完成8-羟基-7-甲氧基-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-5(10h)-酮(2.92g,11.76mmol)的四氢呋喃(100ml)溶液。使所得溶液升温至室温,并搅拌过夜。将混合物用甲苯(50ml)稀释,真空蒸发并通过硅胶柱色谱纯化(二氯甲烷/甲醇=15/1),得到标题化合物(10.02g,收率82%),为黄色泡沫。msesim/z:c50h74n9o15[m+h]+计算值:1040.52,实测值:1040.90。 实施例322.(s)-4-((14s,17s)-1-叠氮基17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-((叔丁氧基羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)苄基8-(3-碘丙氧基)-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 向4-((14s,17s)-1-叠氮基17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-((叔丁氧基羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺基)苄基8-羟基-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(2.02g,1.94mmol)的丁酮(50ml)溶液中加入cs2co3(2.50g,7.67mmol)和1,3-二碘丙烷(2.50g,8.45mmol)。将混合物在暗处于45℃搅拌36小时,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶5)洗脱,得到标题化合物(2.08g,收率90%)。msesim/z:c52h77in9o15[m+h]+计算值:1194.45,实测值:1194.95。 实施例323.(s)-2-((s)-1-叠氮基-14-甲基-12-氧代-3,6,9-三氧杂-13-氮杂十五烷酰胺基)-n-(4-(羟甲基)苯基丙酰胺的合成。 向(14s,17s)-1-叠氮基14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷-18-酸(3.02g,7.75mmol)和(4-氨基苯基)甲醇(1.05g,8.53mmol)的dma溶液中加入edc(4.90g,25.52mmol)。将混合物在室温搅拌14小时,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶8至1∶3)洗脱,得到标题化合物(3.52g,收率92%)。msesim/z:c22h35in6o7[m+h]+计算值:495.25,实测值:495.60。 实施例324.(11r-11as)-4-((14s-17s)-1-叠氮-14-17-二甲基-12,15-二氧基-3,6,9-三氧基-13,16-二氮杂十八烷酰胺)苄基8-(苄氧基)-11-羟基-7-甲氧基-2-亚甲基-5-氧基-2,3,11,11a-四氢-1h-苯并[e]吡咯[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 在室温下,将(s)-(4-(苄氧基)-5-甲氧基-2-硝基苯基)(2-(羟甲基)-4-亚甲基-吡咯烷-1-基)甲酮(3.90g,9.80mmol),na2s2o4(6.0g,34.47mmol),四氢呋喃(60ml)和水(40ml)的混合物搅拌20小时,用na2co3调节ph到10,浓缩,在c-18短柱上纯化,用水/甲醇/et3n洗脱(从99.4/0.5/0.2到50/49.8/0.2)。合并含有氨基产物的组分,浓缩,用四氢呋喃(50ml)稀释,然后冷却至4-8℃。在4-8℃下,向2-(1-叠氮基-14-甲基-12-氧代-3,6,9-三氧杂-13-氮杂十五酰胺基)-n-(4-(羟甲基)苯基)-丙酰胺(6.70g,13.56mmol)的无水四氢呋喃(150ml)溶液中加入dipea(3.50g,27.12mmol)和三光气(4.10g,13.80mmol)的无水四氢呋喃(20ml)溶液。在4-8℃下搅拌15分钟后,将其在45分钟以内滴加到上述胺溶液中。将该混合物升温至室温并继续搅拌2小时,浓缩,用二氯甲烷(3×30ml)萃取,经无水硫酸钠干燥,浓缩,并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1∶10至1∶5)洗脱,得到标题化合物(7.23g,两步收率83%)。msesim/z:c45h57in8o12[m+h]+计算值:889.40,实测值:889.90。 实施例325.(11s,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺)苄基8-(苄氧基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 在氮气中,室温下向(11r,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺)苄基8-(苄氧基))-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(3.80g,4.27mmol)的无水二氯甲烷(40ml)溶液中加入dess-martin试剂(dmp)(2.80g,6.60mmol)。反应完成后,向反应溶液中加入na2so3水溶液,然后加入碳酸氢钠水溶液,将混合物再搅拌15分钟,并用二氯甲烷(3×20ml)萃取。合并的有机萃取物用盐水洗涤,干燥,过滤并浓缩。残余物通过硅胶柱色谱纯化(二氯甲烷/乙酸乙酯=5/1至2∶1),得到标题化合物(2.99g,收率79%),为灰白色泡沫。msesim/z:c44h55n8o12[m+h]+计算值:886.39,实测值:886.80。 实施例326.(11s,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺)苄基8,11-二羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 在0℃下,向(11s,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)苄基8-(苄氧基))-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(2.90g,3.27mmol)的二氯甲烷(40ml)溶液中加入15ml的ch3so3h。将混合物在0℃下搅拌10分钟,然后在室温下搅拌1小时,用二氯甲烷稀释,用冷的1.0n碳酸氢钠调节ph至4,并过滤。用二氯甲烷(3×60ml)萃取水层,合并有机层,经无水硫酸钠干燥,过滤,蒸发并在硅胶柱色谱上纯化(甲醇/二氯甲烷1∶15至1∶5),得到标题产物1.95g(收率75%)。msesim/z:c37h48in8o12[m+h]+计算值:797.34,实测值:797.90。 实施例327.(11s,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺)苄基8-(3-((((s)-10-)(((4-((14s,17s)-1-叠氮基17-(2-(叔丁氧基)-2-氧乙基)-14-(4-(((叔丁氧羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺基)苄基)氧)羰基)-7-甲氧基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-a][1,4]-8-基)氧基)丙氧基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 向(11s,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺基)苄基8,11-二羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(402mg,0.504mmol)和(s)-4-((14s,17s)-1-叠氮基17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-((叔-丁氧羰基)氨基)-丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)苄基8-(3-碘丙氧基)-7-甲氧基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(650mg,0.544mmol)的丁酮(50ml)溶液中加入cs2co3(0.50g,1.53mmol)。将混合物在暗处中于45℃搅拌36小时,浓缩并在硅胶柱上纯化,用乙酸乙酯/二氯甲烷(1:8至1:3)洗脱,得到标题化合物(809mg,收率86%)。msesim/zc89h124n17o27[m+h]+计算值:1862.89,实测值:1863.45。 实施例328.(11s,11as)-4-((14s,17s)-1-氨基-14,17-二甲基-12,15-二氧代-3,6,9-三氧代-13,16-二氮杂十八烷酰胺基)苄基8-(3-(((s)-10-(((4-((14s,17s)-1-氨基-17-(2-(叔丁氧基)-2-氧乙基)-14-(4-((叔-丁氧羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)苄基)氧)羰基)-7-甲氧基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-8-基)氧基)丙氧基)-11-羟基-7-甲氧基-2-亚甲基-5-氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的合成。 在0-4℃,n2环境下,向(11s,11as)-4-((14s,17s)-1-叠氮基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)苄基8-(3-(((s)-10-(((4-((14s,17s)-1-叠氮基17-(2-(叔丁氧基)-2-氧乙基)-14-(4-((叔-丁氧羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)-苄基)氧)羰基)-7-甲氧基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-8-基)氧基)丙氧基)-11-羟基-7-甲氧基-2-亚甲基-5–氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯(750mg,0.402mmol)的四氢呋喃(8ml)溶液中加入me3p(1.0m的甲苯溶液,2.0ml,2.0mmol)。搅拌5分钟后,移去冰浴,将反应混合物在室温搅拌2小时。然后,加入水(1ml),并将混合物搅拌10分钟。将混合物用1,4-二氧六环(10ml)稀释,浓缩并与二氧六环/甲苯共浓缩至干,得到产物粗品(725mg,收率),无需进一步操作即可直接用于下一步。msesim/zc89h128n13o27[m+h]+计算值:1810.90,实测值:1811.50。 实施例329.不对称交联的pbd二聚体c-09的合成。 向上述所得的氨基化合物((11s,11as)-4-((14s,17s)-1-氨基-14,17-二甲基-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八烷酰胺基)苄基8-(3-(((s)-10-((((4-((14s,17s)-1-氨基-17-(2-(叔丁氧基)-2-氧代乙基)-14-(4-(((叔丁氧基羰基)氨基)丁基)-12,15-二氧代-3,6,9-三氧杂-13,16-二氮杂十八酰胺基)苄基)氧基)羰基)-7-甲氧基-5-氧代-2,3,5,10,11,11a-六氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-8-基)氧基)丙氧基)-11-羟基-7-甲氧基-2-亚甲基-5–氧代-2,3,11,11a-四氢-1h-苯并[e]吡咯并[1,2-a][1,4]二氮杂-10(5h)-羧酸酯的干燥的dma(8ml)溶液中,加入4,4′-((((2r,3s)-2,3-双(3-(2,5-二氧代-2,5-二氢-1h-吡咯-1-基)丙酰胺基))琥珀酰基)双(氮杂二基))二丁酸(248.0mg,0.400mmol)和edc(500.0mg,2.60mmol)。将混合物搅拌24小时,浓缩并在制备型hplc(c18,250mm×50mm)上纯化,用水/乙腈洗脱(从80%水至30%水,45min,9ml/min)。在高真空下浓缩,得到488.1mg(51%收率)c-9产物。esimsm/zc115h156n19o37[m+h]+:计算值2395.08,实测值2395.90。 实施例330.不对称交联的pbd二聚体c-10的合成。 在0-4℃下,将c-9化合物(465.0mg,0.194mmol)溶于二氯甲烷(4ml),然后加入tfa(2ml)。然后将反应混合物在室温搅拌1h,用甲苯(5ml)稀释,然后浓缩,并与二氯甲烷/甲苯共蒸发至干,得到粗产物(48.0mg,100%收率,92%hplc纯)。将其通过反相hplc(250mm×20mm,c18柱,5-60%乙腈/水,40min,v=8ml/min)进一步纯化,得到泡沫状纯产品c-10(纯度96%,373.1mg,产率85%)。esimsm/zc106h140n19o35[m+h]+:计算值2238.97,实测值2239.50。 实施例331.不对称交联的pbd二聚体c-11的合成。 将c-10化合物(235.0mg,0.105mmol)溶于四氢呋喃(3ml)和0.1mph7.5的nah2po4溶液(3ml)中,在2小时内分4批加入2,5,8,111,14,17,20,23-八氧杂二十六烷-26-n-琥珀酰亚胺酯(43.0mg,0.084mmol)。然后将反应混合物继续在室温搅拌4小时,并与dmf(10ml)共同蒸发至干,得到粗产物,将其通过反相hplc进一步纯化(250mm×50mm,c18柱,20-60%乙腈/水,40min,v=8ml/min),得到泡沫状纯产物c-11(纯度95%,215.5mg,产率78%)。esimsm/zc124h174n19o44[m+h]+:计算值2633.20,实测值2633.85。 实施例332.不对称交联的pbd二聚体c-12的合成。 向c-11化合物(65.0mg,0.0246mmol)和2,5,8,11,14,17,20,23-八氧杂二十五烷25-胺(15.1mg,0.0394mmol)的无水dma(2ml)溶液中加入edc(30.0mg,0.156mmol)。将反应混合物在室温搅拌15h,浓缩,通过反相hplc(250mm×30mm,c18柱,20-60%乙腈/水,40min,v=8ml/分钟)纯化,得到产物c-12(hplc纯度95%,60.2mg,81%产率),为泡沫状固体。esimsm/zc141h209n20o51[m+h]+:计算值2998.43,实测值2999.40。 实施例333.硝基-α-鹅膏毒素的合成。 在0℃下,向α-鹅膏毒素(15.0mg,0.0163mmol,pct/ib2016/052246)的乙酸(0.5ml)和二氯甲烷(1ml)溶液中加入70%hno3(0.3ml)。将反应在0℃下搅拌1小时,然后在室温下搅拌2小时。加入水(5ml)和dma(4ml),将混合物浓缩并通过制备型hplc(h2o/mecn)纯化,得到浅黄色固体(9.8mg,62%产率)。esimsm/z:c39h54n11o16s[m+h]+计算值963.34,实测值964.95。 实施例334.硝基-β-鹅膏毒素的合成。 在0℃下,向β-鹅膏毒素(15.0mg,0.0163mmol,pct/ib2016/052246)的乙酸(0.5ml)和二氯甲烷(1ml)溶液中加入70%hno3(0.3ml)。将反应在0℃下搅拌1小时,然后在室温下搅拌2小时。加入水(5ml)和dma(4ml),将混合物浓缩并通过制备型hplc(h2o/mecn)纯化,得到浅黄色固体(9.8mg,62%产率)。esimsm/z:c39h53n10o17s[m+h]+计算值965.32,实测值965.86。 实施例335.可偶联的α-鹅膏毒素类似物d-01和d-02的合成。 向硝基-α-鹅膏毒素(9.0mg,0.0093mmol)的dma(1ml)溶液中加入pd/c(3mg,50%水),在室温下氢化(1atm)6小时。滤出催化剂,然后加入0.5ml,0.1mph7.5nah2po4和双(2,5-二氧杂吡咯烷-1-基)21,22-双(2,5-二氧杂-2,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧代-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二酸酯(11.0mg,0.0092mmol)。将混合物在室温搅拌过夜,浓缩,并在c18制备型hplc上纯化,用水/乙腈洗脱(在45分钟内从95%水至25%水)。合并组分,浓缩并在高真空下干燥,得到产物d-01(6.1mg,35%的产率),esimsm/zc81h114n19o32s[m+h]+,计算值:1896.75,实测值:1897.20;和产品d-02(4.9mg,收率27%),esimsm/zc81h116n19o33s[m+h]+,计算值:1914.76,实测值:1914.40。 实施例336.可偶联的β-鹅膏毒素类似物d-03和d-04的合成。 向硝基-β-鹅膏毒素(9.0mg,0.0093mmol)的dma(1ml)溶液中加入pd/c(3mg,50%水),然后在室温下氢化(1atm)6小时。滤出催化剂,然后加入0.5ml,0.1mph7.5的nah2po4,和双(2,5-二氧杂吡咯烷-1-基)21,22-双(2,5-二氧杂-2-,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧代-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二酸酯(11.0mg,0.0092mmol)。将混合物在室温搅拌过夜,浓缩,并在c18制备型hplc上纯化,用水/乙腈洗脱(在45分钟内从95%水至25%水)。合并组分,浓缩并在高真空下干燥,得到产物d-03(7.0mg,收率40%),esimsm/zc81h113n18o33s[m+h]+,计算值:1896.74,实测值:1897.20;和产物d-04(4.7mg,收率25%),esimsm/zc81h115n18o34s[m+h]+,计算值:1915.75,实测值:1916.30。 实施例337.具有双连接子的可偶联的α-鹅膏毒素类似物d-05的合成。 向硝基-α-鹅膏毒素(9.0mg,0.0093mmol)的无水dma(1ml)溶液中加入pd/c(3mg,50%水),然后在室温下氢化(1atm)6小时。滤出催化剂,先用dma(1ml)洗涤,然后加入双(2,5-二氧杂吡咯烷-1-基)21,22-二(2,5-二氧杂-2,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧代-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二甲酸酯(40.0mg,0.033mmol)和dipea(2μl,0.011mmol)。将混合物在室温下搅拌4小时,然后加入26-氨基-3,6,9,12,15,18,21,24-八氧杂二十六烷-1-醇(30.0mg,0.072mmol)。将混合物继续搅拌过夜,通过c18制备hplc纯化,用水/乙腈洗脱(在45分钟内从95%水到30%水),在高真空下浓缩干燥后,得到标题产品d-05(14.5mg,收率69%)。esimsm/zc99h153n20o41s[m+h]+,计算值:2310.01,实测值:2310.90;和副产物2,3-双(2,5-二氧基-2,5-二氢-1h-吡咯-1-基)-n1,n4-双(1-羟基-29,32-二甲基-28,31,34-三氧基-3,6,9,12,15,18,21,24,37,40,43-十一氧杂-27,30,33-三氮杂四十五烷-45-基)丁二酰胺(24.3mg,0.013mmol),esimsm/zc78h136n10o36[m+h]+,计算值:1789.91,实测值:1790.20。 实施例338.具有双连接子的可偶联的β-鹅膏毒素类似物d-06的合成。 向硝基-β-鹅膏毒素(9.0mg,0.0093mmol)的无水dma(1ml))溶液中加入pd/c(3mg,50%水),然后在室温下氢化(1atm)6h。过滤掉催化剂,用dma(1ml)洗涤,然后加入双(2,5-二氧吡咯烷-1-基)21,22-双(2,5-二氧基-2,5-二氢-1h-吡咯-1-基)-2,5,38,41-四甲基-4,7,20,23,36,39-六氧基-10,13,16,27,30,33-六氧杂-3,6,19,24,37,40-六氮杂四十二烷-1,42-二酯(40.0mg,0.033mmol)和dipea(2μl,0.011mmol)。将混合物在室温下搅拌4小时,然后加入26-氨基-3,6,9,12,15,18,21,24-八氧杂二十六烷-1-醇(30.0mg,0.072mmol)。将混合物继续搅拌过夜,在c18制备hplc上纯化,用水/乙腈洗脱(在45分钟内从95%水到30%水),在高真空下浓缩和干燥后,得到标题产物d-06(14.9mg,收率69%)。esimsm/zc99h152n19o42s[m+h]+,计算值:2311.00,实测值:2311.90;和副产物pg-04,2,3-双(2,5-二氧基-2,5-二氢-1h-吡咯-1-基)-n1,n4-双(1-羟基-29,32-二甲基-28,31,34-三氧基-3,6,9,12,15,18,21,24,37,40,43-十一氧杂-27,30,33-三氮杂四十五烷-45-基)丁二酰胺(24.8mg,0.013mmol),esimsm/zc78h136n10o36[m+h]+,计算值:1789.91,实测值:1790.20。 实施例339.制备偶联物的一般方法。 向2.0ml10mg/mlph6.0-8.0的her2抗体中分别加入0.70-2.0ml100mmnah2po4缓冲液,ph6.5-8.5缓冲液,tcep(16-20μl,20mm水溶液)和化合物a-01、a-02、a-03、a-04、b-01、b-02、b-03、b-04、b-05、b-06、b-07、b-08、b-09、b-10、b-11、b-12、b-13、b-14、b-15、b-16、c-02、c-03、c-04、c-05、c-06、c-07、c-08、c-09、c-10、c-11、c-12、d-01、d-02、d-03、d-04、d-05或d-06(28-32μl,20mmdma溶液)。将混合物在室温下温育4-18小时,然后加入dhaa(135μl,50mm)。在室温下温育过夜后,将混合物在g-25柱上纯化,用100mmnah2po4,50mmnacl,ph6.0-7.5缓冲液洗脱,得到12.8-18.1mg在14.4-15.5ml缓冲液中的偶联物化合物aa-01、aa-02、aa-03、aa-04、ba-01、ba-02、ba-03、ba-04、ba-05、ba-06、ba-07、ba-08、ba-09、ba-10、ba-11、ba-12、ba-13、ba-14、ba-15、ba-16、ca-02、ca-03、ca-04、ca-05、ca-06、ca-07、ca-08、ca-09、ca-10、ca-11、ca-12、da-01、da-02、da-03、da-04、da-05或da-06(收率75%~90%)。通过uplc-qtof质谱确定偶联物的药物/抗体比(dar),为3.1-4.2。通过sechplc(tosohbiosciences,tskgelg3000sw,7.8mm×30cm,0.5ml/min,100min)分析单体含量,为94-99%,sds-page谱图为单一谱带。偶联物结构如下所示: 其中n=2.0~4.5。 实施例340.与t-dm1对比,偶联物aa-01、aa-02、aa-03、aa-04、ba-01、ba-02、ba-03、ba-04、ba-05、ba-06、ba-07、ba-08、ba-09、ba-10、ba-11、ba-12、ba-13、ba-14、ba-15、ba-16、ca-02、ca-03、ca-04、ca-05、ca-06、ca-07、ca-08、ca-09、ca-10、ca-11、ca-12、da-01、da-02、da-03、da-04、da-05和da-06的体外细胞毒性评价。 用于细胞毒性测定的细胞系是人胃癌细胞系nci-n87,细胞在含有10%fbs的rpmi-1640中生长。测定时,将细胞(180μl,6000个细胞)加入到96孔板中的每个孔中,并在37℃,5%co2下温育24小时。接下来,在适当的细胞培养基里,用不同浓度的测试化合物(20μl)处理细胞(总体积,0.2ml)。对照孔含有细胞和培养基,但无测试化合物。将孔板在37℃和5%co2下温育120小时,然后向孔中加入mtt(5mg/ml)(20μl),并将孔板在37℃下孵育1.5小时。小心去除培养基,然后加入dmso(180μl),振荡15分钟,在490nm和570nm处测量吸光度,以620nm为参考。依照以下公式计算抑制率:抑制率%=[1-(分析值-空白对照值)/(控制值-空白对照值)]×100。 以ic50和ic90表示的细胞毒性结果: 实施例230.体内抗肿瘤活性(nci-n87异种移植肿瘤的balb/c裸鼠)。 在人胃癌n-87细胞系肿瘤异种移植模型上评估了偶联物ba-12,ba-14,ba-16,ca-03,ca-04,ca-05,ca-06,ca-07,ca-10,ca-11,ca-12,以及t-dm1的体内疗效。在五周龄的雌性balb/c裸鼠(104只动物)右肩下用在0.1ml无血清培养基中的n-87癌细胞(5×106个细胞/小鼠)进行皮下接种。肿瘤生长8天至平均大小130mm3。然后将动物随机分成13组(每组8只动物)。第一组小鼠用作对照组,注射磷酸缓冲盐水(pbs)。其它12组分别用偶联物ba-12,ba-14,ba-16,ca-03,ca-04,ca-05,ca-06,ca-07,ca-10,ca-11,ca-12和t-dm1静脉注射,剂量3mg/kg。剩余2组用偶联物c-3a和d-1a静脉注射,剂量3mg/kg。每4天测量一次肿瘤的三维尺寸,并使用公式:肿瘤体积=1/2(长×宽×高),计算肿瘤体积。同时还测量动物的体重。当满足下列任何一项标准时,处死小鼠:(1)体重减少超过处理前体重的20%,(2)肿瘤体积大于2000mm3,(3)病情严重无法进食或(4)皮肤坏死。如果肿瘤无法被感知,则认为小鼠是无肿瘤的。 试验结果绘制在图27中。所有12种偶联物都不会导致动物体重减轻。在第35天,由于肿瘤体积大于2000mm3且小鼠十分虚弱,处死对照组的动物。除了测试的ca-06以外,其余测试的12种偶联物均显示出比t-dm1更好的抗肿瘤活性。在化合物ca-04和ca-3组中的所有6/6动物在第14天至第30天完全没有可测量的肿瘤。相反,剂量为3mg/kg的t-dm1不能消除肿瘤。 权利要求书(按照条约第19条的修改) 1.一种含有2,3-二氨基琥珀酰基双连接子的偶联物,其特征在于具有(ia),(ib),(ic),(iia),(iib),(iic),(iiia),(iiib),(iiic),(iva),(ivb)和(ivc)的结构: 其中 代表单键; 代表可选为单键或可以缺省; 代表可选为单键,双键,或者可以缺省;n独立地为1到30; q是连接到r3和r4的细胞结合剂/分子,可以是目前已知的,或者即将成为已知的任何种类的分子,可与具有治疗意义或生物学修饰的细胞群的片段结合,复合或反应。优选地,细胞结合剂/分子是免疫治疗蛋白,抗体,单链抗体;与靶细胞结合的抗体片段;单克隆抗体;单链单克隆抗体;或结合靶细胞的单克隆抗体片段;嵌合抗体;与靶细胞结合的嵌合抗体片段;域抗体;与靶细胞结合的域抗体片段;模拟抗体的adnectins;darpins;淋巴因子;激素;维生素;增长因子;集落刺激因子;或营养转运分子(转铁蛋白);含超过四个氨基酸的结合肽,或蛋白质,或抗体,或附着在白蛋白,聚合物,树枝状大分子,脂质体,纳米颗粒,囊泡或(病毒)衣壳上的小的细胞结合分子或配体; drug1或/和drug2是细胞毒性分子/药剂是治疗药物/分子/试剂,或免疫治疗蛋白质/分子,或用于增强细胞结合或稳定细胞结合剂的功能分子,或细胞表面受体结合配体,或抑制细胞增殖分子;或用于监测,检测或研究细胞结合作用的分子。它也可以是免疫治疗化合物、化学治疗化合物的类似物或前药,或药学上可接受的盐,水合物或水合盐,或晶体,或光学异构体,外消旋体,非对映异构体或对映异构体,抗体(probody)或抗体(probody)片段,或sirna、dna分子,或细胞表面结合配体; x1和x2相同或不同,独立地选自nh、nhnh、n(r1)、n(r1)n(r2)、o、s、s-s、o-nh、o-n(r1)、ch2-nh、ch2-n(r1)、ch=nh、ch=n(r1)、s(o)、s(o2)、p(o)(oh)、s(o)nh、s(o2)nh、p(o)(oh)nh、nhs(o)nh、nhs(o2)nh、nhp(o)(oh)nh、n(r1)s(o)n(r2)、n(r1)s(o2)n(r2)、n(r1)p(o)(oh)n(r2)、os(o)nh、os(o2)nh、op(o)(oh)nh、c(o)、c(nh)、c(nr1)、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)nh、oc(nh)nh、oc(nr1)nh、nhc(o)nh、nhc(nh)nh、nhc(nr1)nh、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)n(r1)、oc(nh)n(r1)、oc(nr1)n(r1)、nhc(o)n(r1)、nhc(nh)n(r1)、nhc(nr1)n(r1)、n(r1)c(o)n(r1)、n(r1)c(nh)n(r1)、n(r1)c(nr1)n(r1);或c1-c6烷基;c2-c8烯基、杂烷基、烷基环烷基或杂环烷基;c3-c8芳基、芳烷基、杂环、碳环、环烷基、杂烷基环烷基、烷基羰基或杂芳基; y1、y2、z1和z2是相同或不同的官能团,独立地通过二硫化物,硫醚,硫酯,肽,腙,醚,酯,氨基甲酸酯,碳酸酯,胺(二级,三级或四级),亚胺,环杂烷基,杂芳基,烷氧基或酰胺键,连接至细胞结合分子q;y1、y2、z1和z2独立地具有以下结构:c(o)ch、c(o)c、c(o)ch2、arch2、c(o)、nh、nhnh、n(r1)、n(r1)n(r2)、o、s、s-s、o-nh、o-n(r1)、ch2-nh.ch2-n(r1)、ch=nh、ch=n(r1)、s(o)、s(o2)、p(o)(oh)、s(o)nh、s(o2)nh、p(o)(oh)nh、nhs(o)nh、nhs(o2)nh、nhp(o)(oh)nh、n(r1)s(o)n(r2)、n(r1)s(o2)n(r2)、n(r1)p(o)(oh)n(r2)、os(o)nh、os(o2)nh、op(o)(oh)nh、c(o)、c(nh)、c(nr1)、c(o)nh、c(nh)nh、c(nr1)nh、oc(o)nh、oc(nh)nh、oc(nr1)nh、nhc(o)nh、nhc(nh)nh、nhc(nr1)nh、c(o)nh、c(nr1)nh、oc(o)n(r1)、oc(nh)n(r1)、oc(nr1)n(r1)、nhc(o)n(r1)、nhc(nh)n(r1)、nhc(nr1)n(r1)、n(r1)c(o)n(r1)、n(r1)c(nh)n(r1)、n(r1)c(nr1)n(r1);或c1-c8烷基、c2-c8杂烷基、烷基环烷基、杂环烷基;c3-c8芳基、芳烷基、杂环、碳环、环烷基、杂环烷基、烷基羰基、杂芳基; r1、r2、r3和r4中的各个原子以所有可能的化学方式结合,比如形成亚烷基,亚烯基和亚炔基,醚,聚氧化烯,酯,胺,亚胺,多胺,肼,腙,酰胺,脲,氨基脲,卡巴肼,烷氧胺,氨基甲酸酯,氨基酸,肽,酰氧基胺,异羟肟酸,或上述组合。优选地,r1、r2、r3和r4相同或不同,独立地选自o、nh、s、nhnh、n(r5)、n(r3)n(r3’)、如式(och2ch2)por5、(och2ch-(ch3))por5、nh(ch2ch2o)pr5、nh(ch2ch(ch3)o)pr5、n[(ch2ch2o)pr5]-[(ch2ch2o)p’r5’]、(och2ch2)pcoor5、ch2ch2(och2ch2)pcoor5的聚乙烯氧基单,其中p和p’独立地是选自0至约1000的整数,或上述的组合;c1-c8烷基;c2-c8杂烷基、烷基环烷基、杂环烷基、酯、醚或酰胺;c3-c8芳基,芳烷基,杂环,碳环,环烷基,杂烷基环烷基,烷基羰基或杂芳基;或1~24氨基酸;其中r5和r5’独立地为h;c1-c8烷基;c2-c8杂烷基、烷基环烷基或杂环烷基;c3-c8芳基,芳烷基,杂环;c2-c8酯、醚或酰胺;或1~24氨基酸; 或r1、r2、r3和r4可任选地由下列一个或多个连接子组分构成:6-马来酰亚胺基己酰基(“mc”)、马来酰亚胺丙酰基(“mp”)、缬氨酸-瓜氨酸(“val-cit”或“vc”)、丙氨酸-苯丙氨酸(“ala-phe”或“af”)、对氨基芐氧基-羰基(“pab”)、4-硫代戊酰基(“spp”)、4-(n-马来酰亚胺甲基)环己烷-1酰基(“mcc”)、(4-乙酰基)氨基苯酰基(“siab”)、4-硫丁酰基(spdb)、4-硫-2-羟基磺酰基-丁酰基(2-sulfo-spdb),或含有1-8个天然或非天然氨基酸单的天然或非天然肽。天然氨基酸最优选自天冬氨酸、谷氨酸、精氨酸、组氨酸、赖氨酸、丝氨酸、苏氨酸、天冬酰胺、谷氨酰胺、半胱氨酸、硒代半胱氨酸、酪氨酸、苯丙氨酸、甘氨酸、脯氨酸、色氨酸和丙氨酸; 或r1、r2、r3和r4独立地可包含以下亲水结构之一: 其中是连接位点;x3、x4、x5、x6和x7独立地选自nh、nhnh、n(r5)、n(r5)n(r5’)、o、s、c1-c6烷基、c2-c6杂烷基、烷基环烷基或杂环烷基、c3-c8芳基、芳烷基、杂环、碳环、环烷基、杂环烷基、烷基羰基、杂芳基、或1~8个氨基酸;其中r5和r5’独立地为h、c1-c8烷基、c2-c8杂烷基、烷基环烷基或杂环烷基、c3-c8芳基、芳烷基、杂环、碳环、杂环烷基、烷基羰基或杂芳基、c1-c8酯、醚或酰胺;或具有式(och2ch2)p或(och2ch(ch3))p的聚乙烯氧基,其中p是0到约5000的整数,或其组合; 或r1、r2、r3、r4、y1、y2、z1和z2独立地含有自我毁灭或非自我毁灭的组分,肽单、腙键、二硫化物、酯、肟、酰胺或硫醚键。自我毁灭单包括,与对氨基芐基氨甲酰基(pab)电子结构相似的芳香化合物,例如2-氨基咪唑-5-甲醇的衍生物、杂环pab类似物、β-葡糖苷酸、以及邻或对氨基芐基缩醛; 自我毁灭型连接子组分具有以下结构之一: 其中(*)标记的原子是另外的间隔体或可断裂连接子单、或细胞毒性剂和/或结合分子(cba)的连接点;x1、y1、z2和z3独立地为nh、o或s;z1独立地为h、nhr5、or1、sr5、cox1r5,其中x1和r5如前文所定义;v为0或1;u1独立地为h、oh、c1-c6烷基,(och2ch2)n、f、cl、br、i、or5、sr5、nr5r5’、n=nr5、n=nr5、n=r5、nr5r5’、no2、sor5r5’、so2r5、so3r5、so3r5、oso3r5、oso3r5、pr5r5’、po5r5’、po2r5r5’、opo(or5)(or5′)或och2po(or5(or5(or5′)、其中,其中,r5和r5’独立选自h、c1-c8烷基、c2-c8烷基,烯基、杂烷基或氨基酸;c3-c8芳基、烷基、烷基、烷基、或氨基酸;c3-c8芳基、杂环、碳环、环烷基、杂环烷基、杂芳烷基、烷基羰基或糖苷;或药用阳离子盐; 非自我毁灭型连接子组分具有以下结构之一:*(ch2ch2o)r*; 其中(*)标记的原子是另外的间隔体或可释放的连接子单、或细胞毒性剂和/或结合分子的连接点;x1、y1、u1、r5、r5’如前文所定义;r为0~100;m和n独立地为0~20; 或r1、r2、r3和r4独立地包含可释放的连接子组分,其包含至少一个可在生理条件下被破坏的键,例如ph、酸、碱、氧化作用、代谢、生化或酶不稳定的键,包含以下结构: -(cr5r6)m(aa)r(cr7r8)n(och2ch2)t-、(cr5r6)m(cr7r8)n(aa)r(och2ch2)t-、(aa)r-(cr5r6)m(cr7r8)n(och2ch2)t-、(cr5r6)m(cr7r8)n(och2ch2)r(aa)t-、-(cr5r6)m-(cr7=cr8)(cr9r10)n(aa)t(och2ch2)r-、-(cr5r6)m(nr11co)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m(aa)t(nr11co)(cr9r10)n(och2ch2)r-、-(cr5r6)m(oco)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、-(cr5r6)m(co)(aa)t-(cr9r10)n(och2ch2)r-、-(cr5r6)m(nr11co)(aa)t(cr9r10)n(och2ch2)r-、-(cr5r6)m-(oco)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、-(cr5r6)m(co)(aa)t(cr9r10)n-(och2ch2)r-、-(cr5r6)m-苯基co(aa)t(cr7r8)n-、-(cr5r6)m-呋喃co(aa)t(cr7r8)n-、-(cr5r6)m-恶唑co(aa)t(cr7r8)n-、-(cr5r6)m-噻唑基co(aa)t(ccr7r8)n-、-(cr5r6)t-噻吩co(cr7r8)n-、-(cr5r6)t-咪唑co-(cr7r8)n-、-(cr5r6)t-吗啉co(aa)t-(cr7r8)n-、-(cr5r6)t哌嗪-co(aa)t-(cr7r8)n-、-(cr5r6)t-n甲基co(aa)t-(cr7r8)n-、-(cr5r)m-(aa)t苯基-、-(cr5r6)m-(aa)t呋喃、-(cr5r6)m-恶唑(aa)t、-(cr5r6)m-噻唑基(aa)t、-(cr5r6)m-噻吩-(aa)t-、-(cr5r6)m-咪唑(aa)t-、-(cr5r6)m-吗啉(aa)t-、-(cr5r6)m-哌嗪(aa)t-、-(cr5r6)m-n甲基哌嗪(aa)t-、k(cr5r6)m(aa)r(cr7r8)n(och2ch2)t-、k(cr5r6)m(cr7r8)n(aa)r(och2ch2)t-、k(aa)r-(cr5r6)m(cr7r8)n(och2ch2)t-、k(cr5r6)m(cr7r8)n(och2ch2)r(aa)t-、k(cr5r6)m-(cr7=cr8)(cr9r10)n(aa)t(och2ch2)r-、k(cr5r6)m(nr11co)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m(aa)t(nr11co)(cr9r10)n(och2ch2)r-、k(cr5r6)m(oco)(aa)t(cr9r10)n-(och2ch2)r-、k(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m(co)(aa)t-(cr9r10)n(och2ch2)r-、k(cr5r6)m(nr11co)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m-(oco)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m(ocnr7)(aa)t(cr9r10)n(och2ch2)r-、k-(cr5r6)m(co)(aa)t(cr9r10)n(och2ch2)r-、k(cr5r6)m-苯基co(aa)t(cr7r8)n-、k-(cr5r6)m-呋喃co(aa)t-(cr7r8)n-、k(cr5r6)m-恶唑co(aa)t(cr7r8)n-、k(cr5r6)m-噻唑基co(aa)t-(cr7r8)n-、k(cr5r6)t-噻吩co(cr7r8)n-、k(cr5r6)t咪唑-co-(cr7r8)n-、k(cr5r6)t吗啉co(aa)t(cr7r8)n-、k(cr5r6)t哌嗪-co(aa)t-(cr7r8)n-、k(cr5r6)t-n甲基co(aa)t(cr7r8)n-、k(cr5r)m(aa)t苯基、k-(cr5r6)m-(aa)t呋喃-、-k(cr5r6)m-恶唑(aa)t-、k(cr5r6)m-噻唑基(aa)t-、k(cr5r6)m-噻吩-(aa)t-、k(cr5r6)m-咪唑(aa)t-、k(cr5r6)m-吗啉(aa)t-、k(cr5r6)m-哌嗪(aa)t-、k(cr5r6)mn甲基哌嗪(aa)t-;其中aa、m和n定义如前文所描述;t和r独立地为0-100;r3、r4、r5、r6、r7和r8独立地选自h、卤化物、c1-c8烷基、c2-c8芳基、烯基、炔基、醚、酯、胺或酰胺,这些基团均可以被以下基团所取代:一个或多个卤素、cn、nr1r2、cf3、or1、芳基、杂环、s(o)r1、so2r1、-co2h、-so3h、-or1、-co2r1、-conr1、-po2r1r2、-po3h或p(o)r1r2r3;k是nr1、-ss-、-c(=o)-、-c(=o)nh-、-c(=o)o-、-c=nh-o-、-c=n-nh-、-c(=o)nh-nh-、o、s、se、b、het(c3-c8杂环或杂芳环),或含有1-20个相同或不同氨基酸的肽。 或者r1、r2、r3和r4独立地为具有1-18个碳原子的直链烷基,或具有式(och2ch2)p的聚乙烯氧基单,p=1~5000,或含有1~20个氨基酸单(l或d形式)的肽,或上述组合。 此外,y1、y2、r1、r2、r3、r4、z1或z2可独立地由以下一个或多个组分构成: 6-马来酰亚胺己酰胺基(mc)、马来酰亚胺基丙酰胺基(mp)、硫代马来酰胺基、硫代氨基氧代丁酸、硫代氨基氧代丁烯酸、缬氨酸瓜氨酸(val-cit)、丙氨酸苯丙氨酸(ala-phe)、赖氨酸苯丙氨酸(lys-phe)、赖氨酸丙氨酸(lys-ala),p-对氨基苄氧羰基(pab)、4-硫代戊酰基(spp)、4-硫代丁酰基(spdb),4-(n-马来酰亚胺甲基)环已烷基-1-酰基(mcc)、马来酰亚胺乙胺基(me)、4-硫代-2-羟基磺酰基丁酰基(2-磺酰-spdb)、芳基硫基(pys),(4-乙酰基)氨基苯甲酰基(siab)、氧基苄基硫基、氨基苄基硫基、二氧基苄硫基、二氨基苄硫基、氨基氧基苄硫基、烷氧基氨基(aoa)、亚乙基氧基(eo)、4-甲基-4-二硫代戊酰基(mpdp)三唑、二硫代、烷基磺酰基、烷基磺酰胺基、磺胺双酰胺基、磷酸二酰胺基、烷基膦酰胺酸基、次膦酸基、n-甲基烷基膦酰胺酸基、n,n’-二甲基膦酰胺酸基、烷基二膦酰胺基,肼、乙酰亚胺;肟、乙酰乙酰肼、氨基乙胺、氨基乙基-氨基乙基胺,和l-或d-,或含有1-20个氨基酸的天然或非天然肽;其中原子中间的连接键意味着它可以连接相邻的碳原子键;其中波浪线指另外键连接的位点; 或者,y1、y2、r1、r2、r3、r4、z1或z2可以独立地缺省,但是y1、y2、r1、r2、r3、r4、z1和z2不可以同时缺省。 2.如权利要求1中所述的偶联物,其特征在于具有式(i-01)、(i-02)、(i-03)、(i-04)、(i-05)、(i-06)、(i-07)、(i-08)、(i-09)、(i-10)、(i-11)、(i-12)、(i-13)、(i-14)、(i-15)、(i-16)、(i-17)、(i-18)、(i-19)、(i-20)、(i-21)、(i-22)、(i-23)、(ii-01)、(ii-02)、(ii-03)、(ii-04)、(ii-05)、(ii-06)、(ii-07)、(ii-08)、(ii-09)、(ii-10)、(ii-11)、(ii-12)、(ii-13)、(ii-14)、(ii-15)、(ii-16)、(ii-17)、(ii-18)、(iii-01)、(iii-02)、(iii-03)、(iii-04)、(iii-05)、(iii-06)、(iii-07)、(iii-08)、(iii-09)、(iii-10)、(iii-11)、(iii-12)、(iii-13)、(iii-14)、(iii-15)、(iii-16)、(iii-17)、(iii-18)、(iii-19)、(iii-20)、(iv-01)、(iv-02)、(iv-03)、(iv-04)、(iv-05)、(iv-06)、(iv-07)、(iv-08)、(iv-09)、(iv-10)、(iv-11)、(iv-12)、(iv-13)、(iv-14)、(iv-15)、(iv-16)、(iv-17)、(iv-18)、(iv-19)和(iv-20)的结构: 其中:drug1、drug2、n、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、drug1和drug2如前文所定义;此外,drug1和drug2其中之一独立地,可以缺省,但是不能同时缺省。 3.如权利要求2中所述的偶联物,由式(va)、(vb)、(vc)、(via)、(vib)、(vic)、(viia)、(viib)、(viic)、(viiia)、(viiib)和(viiic)所示的具有有高反应活性的立体异构体制备,其特征在于细胞毒性分子的两个或多个官能团可以同时或依次与化合物的lv1和/或lv2反应: 其中: 任选地是单键或双键或三键,或者可以缺省;当代表三键时,lv1和lv2同时缺省; drug1、drug2、n、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1和z2的定义与权利要求1中定义相同; lv1和lv2为相同或不同的反应官能团,这些官能团可以与细胞结合分子上的硫基、胺、羧酸、硒醇、酚或羟基发生反应。lv1和lv2独立地选自羟基(oh)、氟(f)、氯(cl)、溴(br)、碘(i)、硝基苯氧基、n-羟基琥珀酰亚胺(nhs)基、苯氧基、二硝基苯氧基、五氟苯氧基、四氟苯氧基、三氟苯氧基、二氟苯氧基、一氟苯氧基、五氯苯氧基、三氟甲磺酰基、咪唑基、二氯苯氧基、三氯苯氧基、四氯苯氧基、1-羟基苯并三唑基、甲苯磺酰基、甲磺酰基、2-乙基-5-苯基异恶唑-3’-磺酰基、酸酐或与其它酸酐作用形成的酸酐,例如乙酸酐、甲酸酐,或与多肽缩合试剂、mitsunobu反应试剂作用生成的中间体。缩合剂选自:1-乙基-(3-二甲基氨基丙基)碳二亚胺(edc)、二环己基碳二亚胺(dcc)、n,n’-二异丙基碳二亚胺(dic)、n-环己基-n’-(2-吗啉代-乙基)碳二亚胺甲基对甲苯磺酸盐(cmc或cme-cdi)、1,1′-羰基二咪唑(cdi)、氧-(苯并三唑-1-)基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tbtu)、n,n,n’,n’-四甲基-氧-(1h-苯并三唑-1-基)-六氟磷酸铵(hbtu)、(苯并三唑-1-基氧基)三(二甲基氨基)-六氟磷酸盐(bop)、(苯并三唑-1-基氧基)三吡咯烷基六氟磷酸盐(pybop)、氰基膦酸二乙酯(depc)、氯-n,n,n’,n’-四甲基甲脒六氟磷酸盐、1-[双(二甲基氨基)亚甲基]-1h-1,2,3-三唑并[4,5-b]吡啶3-氧六氟磷酸盐(hatu)、1-[(二甲氨基)(吗啉代)亚甲基]-1h-[1,2,3]三唑并[4,5-b]吡啶-1-鎓3-氧六氟磷酸盐(hdma)、2-氯-1,3-二甲基-咪唑六氟磷酸盐(cip)、六氟磷酸氯代吡咯烷酮鎓(pyclop)、氟-n,n,n’,n’-双(四亚甲基)甲脒六氟磷酸盐(btffh)、n,n,n’,n’-四甲基-s-(1-氧代-2-吡啶基)硫脲六氟磷酸盐、氧-(2-氧代-1(2h)吡啶基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tptu)、s-(1-氧代-2-吡啶基)n,n,n’,n’-四甲基硫脲四氟硼酸盐、氧-[(乙氧基羰基)-氰基甲基氨基]-n,n,n’,n’-六氟磷酸四甲基脲(hotu)、(1-氰基-2-乙氧基-2-氧代乙基氨基氧基)二甲氨基-吗啉代-六氟磷酸盐(comu)、氧-(苯并三唑-1-基)-n,n,n’,n’-双(四亚甲基)六氟磷酸盐(hbpyu)、n-芐基-n’-环己基-碳二亚胺(有或没有聚合物结合)、二吡咯烷基(n-琥珀酰亚胺基氧基)碳鎓六氟磷酸盐(hspyu)、氯二吡咯烷基六氟磷酸盐(pyclu)、2-氯-1,3-二甲基咪唑四氟硼酸盐(cib)、(苯并三唑-1-基氧基)二呱啶碳六氟磷酸盐(hbpipu)、氧-(6-氯苯并三唑-1-基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tctu)、溴代(二甲基氨基)-六氟磷酸盐(brop)、丙基膦酸酐(ppaca、)、2-吗啉代乙基异氰化物(mei)、n,n,n’,n’-四甲基-氧-(n-琥珀酰亚胺基)六氟磷酸盐(hstu)、2-溴-1-乙基-吡啶鎓四氟硼酸盐(bep)、氧-[(乙氧基羰基)氰基-亚甲基氨基]-n,n,n’,n’-四甲基脲四氟硼酸盐(totu)、4-(4,6-二甲氧基-1,3,5-三嗪-2-基)-4-甲基吗啉氯化物(mmtm、dmtmm)、n,n,n’,n’-四甲基-氧-(n-琥珀酰亚胺基)脲四氟硼酸(tstu)、o-(3,4-二氢-4-氧代-1,2,3-苯并三嗪-3-基)-n,n,n’,n’-四甲基脲四氟硼酸盐(tdbtu)、1,1′-(偶氮二羰基)-二呱啶(add)、二-(4-氯芐基)偶氮二羧酸酯(dcad)、偶氮二羧酸二叔丁酯(dbad)、偶氮二羧酸二异丙酯(diad)、偶氮二羧酸二乙酯(dead)。另外,lv1和lv2可以是酸酐,或与其它c1-c8酸酐作用形成的酸酐; 或lv1和lv2独立地选自卤化物(氟化物、氯化物、溴化物和碘化物)、甲磺酰基(甲磺酰基)、甲苯磺酰基(甲苯磺酰基)、三氟甲基磺酰基(三氟甲磺酸酯)、三氟甲基磺酸酯、硝基苯氧基、n-琥珀酰亚胺基氧基(nhs)、苯氧基;二硝基苯氧基;五氟苯氧基、四氟苯氧基、三氟苯氧基、二氟苯氧基、单氟苯氧基、五氯苯氧基、1h-咪唑-1-基、氯苯氧基、二氯苯氧基、三氯苯氧基、四氯苯氧基、n-(苯并三唑基)氧基、2-乙基-5-苯基异恶唑-3′-磺酰基、苯基恶二唑磺酰基(-砜-oda)、2-乙基-5-苯基异恶唑鎓-基、苯基恶二唑基(oda)、恶二唑基、不饱和碳(碳-碳、碳-氮、碳-硫、碳-磷、硫-氮、磷-氮、氧-氮或碳-氧之间的双键或三键)、或以下结构之一:二硫化物;卤代乙酰基;酰卤化物;n-羟基丁二酰亚胺酯基;马来酰亚胺基;单取代马来酰亚胺基;单取代丁二酰亚胺基;二取代丁二酰亚胺基;二取代丁二酰亚胺基;-cho醛基;乙烯磺酰基;丙烯酰基;2-(对甲氧基)乙酰基;2-(甲氧基)乙酰基;2-(硝基苯氧基)乙酰基;2-(二硝基苯酚氧基)乙酰基;2-(氟苯氧基)-乙酰基;2-(二氟苯氧基)-乙酰基;2-((三氟甲基)-磺酰氧基)乙酰基;酮或醛基;2-(五氟苯氧基)乙酰基;甲基砜麻黄二唑基(oda);酸酐、烷氧基氨基;叠氮基、炔基、或酰肼,其中x1’为f,cl,br,i或lv3;x2’是o,nh,n(r1)或ch2;r3独立地为h,芳基,杂芳基或芳香基团,其中一个或几个氢原子独立地被-r1,-卤素,-or1,-sr1,-nr1r2,-no2,-s(o)r1,-s(o)2r1或-coor1取代;lv3是离去基团,选自f、cl、br、i;硝基苯氧基;n-羟基琥珀酰亚胺基(nhs);苯氧基;二硝基苯氧基;五氟苯氧基;四氟苯氧基;二氟苯氧基;单氟苯氧基;五氯苯氧基;三氟甲磺酰基;咪唑基;二氯酚基;四氯苯氧基;1-羟基苯并三唑基;甲苯甲磺酰基;甲磺酰基;2-乙基-5-苯基异恶唑-3′-磺酰基,r1和r2如前文所定义。 4.如权利要求3所述的偶联物,其特征在于具有式(v-01)、(v-02)、(v-03)、(v-04)、(v-05)、(v-06)、(v-07)、(v-08)、(v-09)、(v-10)、(v-11)、(v-12)、(v-13)、(v-14)、(v-15)、(v-16)、(v-17)、(v-18)、(v-19)、(v-20)、(v-21)、(v-22)、(v-23)、(vi-01)、(vi-02)、(vi-03)、(vi-04)、(vi-05)、(vi-06)、(vi-07)、(vi-08)、(vi-09)、(vi-10)、(vi-11)、(vi-12)、(vi-13)、(vi-14)、(vi-15)、(vi-16)、(vi-17)、(vi-18)、(vii-01)、(vii-02)、(vii-03)、(vii-04)、(vii-05)、(vii-06)、(vii-07)、(vii-08)、(vii-09)、(vii-10)、(vii-11)、(vii-12)、(vii-13)、(vii-14)、(vii-15)、(vii-16)、(vii-17)、(vii-18)、(vii-19)、(vii-20)、(viii-01)、(viii-02)、(viii-03)、(viii-04)、(viii-05)、(viii-06)、(viii-07)、(viii-08)、(viii-09)、(viii-10)、(viii-11)、(viii-12)、(viii-13)、(viii-14)、(viii-15)、(viii-16)、(viii-17)、(viii-18)、(viii-19)、和(viii-20)所示的结构: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、drug1和drug2如前文所定义;x1和x1’独立地为h、f、cl、br、i、ots、oms、otf、n3、cho、-c=ch、-c≡c-、arc(=o)r1、c(=o)nhnh2、-o-nh2、硝基苯氧基、n-羟基琥珀酰亚胺(nhs)、苯氧基、二硝基苯氧基、五氟苯氧基、四氟苯氧基、二氟苯氧基、单氟苯氧基、五氯苯氧基、三氟甲磺酰基、咪唑基、二氯酚基、四氯苯氧基、1-羟基苯并三唑基、甲苯甲磺酰基、甲磺酰基,2-乙基-5-苯基异恶唑-3′-,酸酐或与其它酸酐作用形成的酸酐、例如乙酸酐、甲酸酐,o-nhs(on-氢琥珀酰亚胺)、o-咪唑、o-三唑、o-四唑、o-ar、o-arno2、o-ar(no2)2、o-arf4、o-arf3、o-arf5、o-arf2、o-arf、o-arcl4、o-arcl3、o-arcl5、o-arcl2、o-arcl、o-arso3h、o-aropo3h2、o-ar(no2)cooh、s-ar(no2)2cooh、o-吡啶、o-硝基苯氧基、o-二硝基苯氧基、o-五氟苯氧基、o-四氟苯氧基、o-三氟苯氧基、o-二氟苯氧基、o-氟苯氧基、o-五氯苯氧基、o-四氯苯氧基、o-三氯苯氧基、o-二氯苯氧基、o-氯苯氧基、o-吡啶、o-硝基吡啶、o-二硝基吡啶、o-c1-c8烷基、o-三氟甲磺酸盐、o-苯并三唑、s-ar、s-arno2、s-ar(no2)2、s-arf4、s-arf3、s-arf5、s-arf2、s-arf、s-arcl4、s-arcl3、s-arcl5、s-arcl2、s-arcl、s-arso3h、s-aropo3h2、s-ar(no2)cooh、s-ar(no2)2cooh、s-吡啶、ss-吡啶、s-硝基吡啶、s-二硝基吡啶、s-c1-c8烷基、ss-c1-c8烷基、s-三氟甲磺酸酯、s-苯并三唑、其中ar是c3-c8芳环;或与多肽缩合试剂生成的,或与mitsunobu反应偶联试剂生成的中间体分子。 5.如权利要求1所述的偶联物,由式(ix-01)、(ix-02)、(ix-03)、(ix-04)、(ix-05)、(ix-06)、(ix-07)、(ix-08)、(ix-09)、(ix-10)、(ix-11)、(ix-12)、(ix-13)、(ix-14)、(ix-15)、(ix-16)、(ix-17)、(ix-18)、(ix-19)、(ix-20)、(ix-21)、(ix-22)、(ix-23)、(x-01)、(x-02)、(x-03)、(x-04)、(x-05)、(x-06)、(x-07)、(x-08)、(x-09)、(x-10)、(x-11)、(x-12)、(x-13)、(x-14)、(x-15)、(x-16)、(x-17)、(x-18)、(x-19)、和(x-20)所示的高反应活性的化合物制得,其特征在于其特征在于细胞毒性分子的两个或多个官能团可以同时或依次与化合物的lv1和/或lv2反应: 其中:q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、lv1、lv2、lv1’、和lv2’如前文所定义;此外,drug1和drug2其中之一独立地,可以缺省,但是不能同时缺省。 6.如权利要求1所述的偶联物,由式(xi-01)、(xi-02)、(xi-03)、(xi-04)、(xi-05)、(xi-06)、(xi-07)、(xi-08)、(xi-09)、(xi-10)、(xi-11)、(xi-12)、(xi-13)、(xi-14)、(xi-15)、(xi-16)、(xi-17)、(xi-18)、(xii-01)、(xii-02)、(xii-03)、(xii-04)、(xii-05)、(xii-06)、(xii-07)、(xii-08)、(xii-09)、(xii-10)、(xii-11)、(xii-12)、(xii-13)、(xii-14)、(xii-15)、(xii-16)、(xii-17)、(xii-18)、(xii-19)、(xii-20)、(xii-21)、(xii-22)、(xii-23)和(xii-24)所示的高反应活性的化合物制得,其特征在于细胞毒性分子和细胞连接分子可以独立地,同时或依次与化合物反应: 其中q,x1,x2,y1,y2,r1,r2,r3,r4,r5,r5’,z1,z2,lv1,lv2,lv1’,lv2’,x1和x1’的定义同前文。 7.如权利要求1所述的偶联物,其中y1,y2,z1和z2与细胞结合剂/分子中一对巯基连接,将细胞结合剂的链间二硫键还原为巯基对的还原剂选自:二硫苏糖醇(dtt)、二硫赤藓糖醇(dte)、l-谷胱甘肽(gsh)、三(2-羧乙基)膦(tcep)、2-巯基乙胺(β-mea)或/和β-巯基乙醇(β-me、2-me)。 8.如权利要求1所述的偶联物,其中drug1或drug2选自: (1).化疗剂,选自于:a)烷基化剂,选自氮芥:氯苯那普,氯普那嗪,环磷酰胺,达喀尔巴嗪,雌二醇氮芥,异环磷酰胺,氮芥,盐酸二甲氧胺,氧化二氮芥,盐酸氨氯地平,麦考酚酸,卫矛醇,呱泊溴烷,新氮芥,苯芥胆甾醇,松龙苯芥,噻替呱,曲磷胺对,尿嘧啶;cc-1065和阿多来新、卡折来新、比折来新或其合成类似物;多卡霉素及其合成类似物,kw-2189或cbi-tmi、;苯并二氮二聚体或吡咯并苯二氮(pbd)二聚体,托美霉素二聚体,吲哚并苯并二氮杂二聚体,咪唑并苯并噻二氮杂二聚体,或恶唑烷并苯并二氮杂的二聚体;亚硝基脲:包括卡莫司汀,洛莫司汀,氯化梭菌素,福莫司汀,尼莫司汀,拉莫司汀;烷基磺酸盐:包括白苏芬、树苏芬、磺胺异丙磺胺和皮苏芬;三氮烯或达喀尔巴嗪;含铂化合物:包括卡铂,顺铂,奥沙利铂;吖丙啶类,苯并二氢吡喃酮,卡洛酮,美妥替派和乌雷多巴;乙烯亚胺和甲基三聚氰胺,包括六甲蜜胺,三亚乙基三胺,三乙基磷酰胺,三亚乙基硫代磷酰胺和三羟甲基甲基胺; b).植物生物碱:选自长春花生物碱,包括长春新碱,长春碱,长春地辛,长春瑞滨,去甲长春碱;紫杉醇类:包括紫杉醇,多西紫杉醇及其类似物;美登素类包括dm1、dm2、dm3、dm4、dm5、dm6、dm7、美登素、安沙霉素及其类似物);cryptophycin(包括cryptophycin1和cryptophycin8);埃博霉素,软珊瑚醇,迪莫利德,草苔虫内酯,海兔毒素,澳瑞斯汀,tubulysins,cephalostatin;pancratistatin;erbulins;sarcodictyin;海绵抑制素; c)dna拓扑异构酶抑制剂:选自依托泊苷替尼,包括9-氨基喜树碱、喜树碱、克立那托、多拉霉素、依托泊苷、磷酸依托泊苷、伊立替康、米托蒽醌、诺消灵、视黄酸(视黄醇)、替尼泊苷、拓扑替康、9-硝基喜树碱或rfs2000、丝裂霉素及其类似物; d)抗代谢物:选自抗叶酸剂(dhfr抑制剂,包括甲氨蝶呤、曲麦克特、二甲叶酸、蝶罗呤、氨喋呤(4-氨基苯甲酸)或其他叶酸类似物);imp脱氢酶抑制剂(包括麦考酚酸、噻唑呋林、利巴韦林、eicar);核糖核苷酸还原酶抑制剂(包括羟基脲、去铁胺);嘧啶类似物:尿嘧啶类似物(包括安西他滨、阿扎胞苷、6-氮尿嘧啶、卡培他滨(希罗达)、卡莫氟、阿糖胞苷、双脱氧尿苷、脱氧氟尿苷、依诺他滨、5-氟尿嘧啶、氟尿苷、ratitrexed(tomudex))和胞嘧啶类似物(包括阿糖胞苷,胞嘧啶阿拉伯糖苷,氟达拉滨);嘌呤类似物(包括硫唑嘌呤,氟达拉滨,巯嘌呤,硫胺素,硫鸟嘌呤);叶酸补充剂,弗洛林酸;和烟酰胺磷酸核糖基转移酶(nampt)的抑制剂; e)激素疗法剂:选自受体拮抗剂:抗雌激素(包括甲地孕酮,雷洛昔芬,他莫昔芬),lhrh兴奋剂(包括戈斯他林,醋酸亮丙瑞林);抗雄激素药(包括比卡鲁胺,氟他胺,卡鲁司酮,丙酸倍他雄酮,表雄甾醇,戈舍瑞林,亮丙瑞林,美替利定,尼鲁米特,睾内酯,曲洛司坦及其他雄激素抑制剂);维甲类化合物:维生素d3类似物(包括cb1093,eb1089,kh1060,胆钙化醇,麦角钙化甾醇);光动力疗法剂(包括维替泊芬,酞菁,光敏剂pc4,去甲氧基-竹红菌素a);细胞因子(干扰素-α,干扰素-γ,肿瘤坏死因子(tnf),含tnf的人蛋白); f)激酶抑制剂,选自bibw2992(抗-egfr/erb2),伊马替尼,吉非替尼,呱加他尼,索拉非尼,达沙替尼,舒尼替尼,厄洛替尼,尼洛替尼,拉帕替尼,阿西替尼,帕唑帕尼,凡德他尼,e7080(抗vegfr2),mubritinib,普纳替尼(ap24534),bafetinib(inno-406),bosutinib(ski-606),卡博替尼,维莫德吉,iniparib,鲁索利替尼,cyt387,阿西替尼,tivozanib,索拉非尼,贝伐单抗,西妥昔单抗,曲妥珠单抗,雷珠单抗,帕尼单抗,伊斯平斯; g)聚(adp-核糖)聚合酶(parp)抑制剂,选自奥拉帕里、尼拉帕里、依尼帕里、塔拉佐帕里、维利帕里、维利帕里、cep9722(cephalon)、e7016(eisai)、bgb-290(beigene)、3-氨基苯甲酰酰胺; h)抗生素:选自烯二炔类抗生素(选自加利车霉素、加利车霉素γ1、δ1、α1和β1,达因霉素,包括达因霉素a和脱氧米霉素,埃斯培拉霉素,卡塔尔霉素,c-1027,maduropeptin,或新卡嗪奥斯汀和相关色蛋白烯二炔抗生素),aclacinomysins,放线菌素,安曲霉素,重氮丝氨酸,博来霉素,卡诺霉素,卡拉霉素,洋红霉素,嗜癌素,色霉素,达金霉素,柔红霉素,去柔红霉素,6-重氮-5-氧代-l-去甲亮氨酸,阿霉素,吗啉-阿霉素,氰基吗啉-阿霉素,2-吡咯啉阿霉素和脱氧柔红霉素,表柔比星,阿柔比星,伊达比星,马可霉素,nitomycin,霉酚酸,诺加霉素,橄榄霉素,peplomycin,potfiromycin,嘌呤霉素,奎拉霉素,罗道霉素,链黑霉素,链脲霉素,杀结核菌素,乌苯美司,净司他丁,佐柔比星; i)聚酮化合物(番荔素),bullatacin和bullatacinone;吉西他滨,环氧酶素和卡菲偌米布,硼替佐米,沙利度胺,来那度胺,pomalidomide,tosedostat,zybrestat,plx4032,sta-9090,stimuvax,allovectin-7,xegeva,provenge,yervoy,异戊二烯化抑制剂和洛伐他汀,多巴胺能神经毒素(选自星形孢菌素),放线菌素(包含放线菌素d,更生霉素),鹅膏毒素,博莱霉素(包括博来霉素a2,博莱霉素b2,培洛霉素),蒽环类抗生素,包括柔红霉素,阿霉素(亚德里亚霉素),伊达比星,表柔比星,佐柔比星,米托蒽醌,mdr抑制剂(或维拉帕米),ca2+atp酶抑制剂(或毒胡萝卜素),组蛋白去乙酰酶抑制剂(伏立诺他,罗米地辛,帕比司他,丙戊酸,mocetinostat(mgcd0103),belinostat,pci-24781,恩替诺特,sb939,resminostat,givinostat,ar-42,cudc-101,萝卜硫素,曲古抑菌素a);塞来昔布,格列酮类,表没食子儿茶素没食子酸酯,双硫仑,salinosporamidea;抗肾上腺药物,选自:氨鲁米特,米托坦,曲洛司坦,醋葡醛内酯,醛磷酰胺,氨基乙酰丙酸,安吖啶,阿拉伯糖苷,bestrabucil,比生群,edatraxate,defofamine,美可辛,地吖醌,依氟鸟氨酸(dfmo),elfomithine,依利醋铵,依托格鲁,硝酸镓,胞嘧啶,羟基脲,伊班膦酸盐,香菇多糖,氯尼达明,米托胍腙,米托蒽醌,莫呱达醇,二胺硝吖啶,喷司他丁,蛋氨氮芥,吡柔比星,鬼臼酸,2-乙肼,甲基苄肼;呱嗪二酮丙烷;根霉素;西佐;螺环锗;细格孢氮杂酸;三亚胺醌;三氯三乙胺;单端孢霉烯(包括t-2毒素,疣孢菌素a,杆孢菌素a和anguidine),聚氨酯,sirna,反义药物; 2)自身免疫疾病药物:环孢菌素,环孢菌素a,氨基己酸,硫唑嘌呤,溴隐亭,苯丁酸氮芥,氯喹,环磷酰胺,皮质类固醇(包括安西奈德,倍他米松,布地奈德,氢化可的松,氟尼缩松,丙酸氟替卡松,氟可龙达那唑,地塞米松,曲安奈德,二丙酸倍氯米松),dhea,依那西普,羟基氯喹,英夫利昔单抗,美洛昔康,甲氨蝶呤,麦考酚酸酯,泼尼松,西罗莫司,他克莫司; 3)抗感染性疾病药物,包括: a)氨基糖苷类:阿米卡星,阿司米星,庆大霉素(奈替米星,西索米星,异帕米星),潮霉素b,卡那霉素(阿米卡星,阿贝卡星,氨基脱氧卡那霉素,地贝卡星,妥布霉素),新霉素(framycetin,巴龙霉素,核糖霉素),奈替米星,壮观霉素,链霉素,妥布霉素,甲基姿苏霉素; b)酰胺醇类:迭氮氯霉素,氯霉素,氟苯尼考,甲砜霉素; c)安沙霉素:格尔德霉素,除莠霉素; d)碳青霉烯类:比阿培南,多利培南,厄他培南,亚胺培南/西司他丁,美罗培南,帕尼培南; e)头孢烯:碳头孢烯(洛拉卡比),头孢乙腈,氯氨苄青霉素,头孢拉定,头孢羟氨,头孢洛宁,头孢噻啶,头孢噻吩或头孢金素,头孢氨苄,头孢来星,头孢孟多,头孢匹林,羟胺唑头孢菌素,氟唑头孢菌素,孢西酮,唑啉头孢菌素,头孢拉宗,头孢卡品,头孢达肟,头孢吡,头孢克肟,头孢西丁,头孢罗齐,头孢甲氧环烯胺,头孢替唑,头孢呋辛,头孢克肟,头孢地尼,头孢托仑,头孢吡,头孢他美,头孢甲肟,头孢地嗪,头孢尼西,头孢呱酮,头孢雷特,头孢噻肟,噻乙胺唑头孢菌素,头孢唑兰,头孢氨苄,头孢咪唑,头孢匹胺,头孢匹罗,头孢泊肟,头孢罗齐,头孢喹诺,头孢磺啶,头孢他啶,头孢特仑,头孢布腾,头孢噻林,头孢唑肟,头孢吡普,头孢曲松,头孢呋辛,头孢唑南,头霉素(头孢西丁,头孢替坦,头孢氰唑),氧(碳)头孢烯(氟氧头孢,拉氧头孢); f)糖肽:博来霉素,万古霉素(奥利万星,特拉万星),替考拉宁(达巴万星),雷莫拉宁; g)甘氨酰环素:如替加环素; h)β-内酰胺酶抑制剂:青霉烷(舒巴坦,他唑巴坦),氧青霉烷(克拉维酸); i)林可酰胺:克林霉素,林可霉素; j)脂肽:达托霉素,a54145,钙依赖性抗生素(cda); k)大环内酯类:阿奇霉素,克霉素,克拉霉素,地红霉素,红霉素,氟雷霉素,交沙霉素,酮内酯(泰利霉素,塞红霉素),麦迪霉素,米卡霉素,竹桃霉素,利福霉素(异烟肼、利福平,利福布丁,利福喷汀),罗匹霉素,罗红霉素,大观霉素,螺旋霉素,他克莫司(fk506),醋竹桃霉素,泰利霉素; l)单环胺:氨曲南,替吉莫南; m)恶唑烷酮类:利奈唑胺; n)青霉素类:阿莫西林,氨苄青霉素(匹氨西林,海洛西林,巴氨西林,氨苄青霉素,阿霉素),阿替代西林,阿洛西林,苄青霉素,苄星青霉素苄青霉素,苄星青霉素苯氧甲基青霉素,克洛西林,普鲁卡因青霉素(美替西林),美洛西林,甲氧西林,萘夫西林,苯唑西林,醋甲西林,青霉素,非奈西林,苯氧基甲基青霉素,呱拉西林,氨苄西林,磺苯西林,替莫西林,替卡西林; o)多肽:杆菌肽,粘菌素,多粘菌素b; p)喹诺酮类:阿拉曲沙星,巴洛沙星,环丙沙星,克林沙,达氟沙星,二氟沙星,依诺沙星,恩诺沙星,加雷沙星,加替沙星,吉米沙星,格帕沙星,卡诺曲伐沙星,左氧氟沙星,洛美沙星,麻保沙星,莫西沙星,那氟沙星,诺氟沙星,奥比沙星,氧氟沙星,培氟沙星,曲伐沙星,格帕沙星,西他沙星,司帕沙星,替马沙星,托沙星,曲伐沙星; q)链阳性菌素:普那霉素,奎奴普丁/达福普汀; r)磺胺类:氨芐磺胺,偶氮磺胺,磺胺嘧啶,磺胺甲异唑、磺胺酰亚胺、磺胺吡啶、磺胺异恶唑、甲氧苄啶、磺胺甲恶唑(复方磺胺甲恶唑); s)类固醇抗菌药物:如夫西地酸; t)四环素类:强力霉素,金霉素,氯米西环素,地美环素,雷莫昔林,美西环素,美他环素,米诺环素,土霉素,潘美环素,吡咯烷甲基四环素,四环素,甘氨酰环素(如替加环素); u)其他类型的抗生素:番荔枝素,胂凡纳明,细菌萜醇抑制剂(杆菌肽),danal/ar抑制剂(环丝氨酸),dictyostatin,圆皮海绵内酯,软珊瑚醇,埃博霉素,乙胺丁醇,依托泊苷,法罗培南,夫西地酸,呋喃唑酮,异烟肼,laulimalide,甲硝唑,莫匹罗星,nam合成抑制剂(例如磷霉素),呋喃妥因,紫杉醇,普兰西霉素,吡嗪酰胺,奎奴普丁/达福普汀,利福平,他唑巴坦替硝唑,乌菊花素; 4)抗病毒药物: a)侵入/融合抑制剂:阿帕韦洛,马拉韦罗,vicriviroc,gp41(恩夫韦肽),pro140,cd4(艾巴利珠单抗); b)整合酶抑制剂:雷特格韦,elvite-gravir,globoidnana; c)成熟抑制剂:bevirimat,vivecon; d)神经氨酸酶抑制剂:奥司他韦,扎那米韦,帕拉米韦; e)核苷和核苷酸:阿巴卡韦,阿昔单韦,阿德福韦,阿莫西韦,阿昔单抗,溴夫定,西多福韦,克拉夫定,地塞米松,去羟肌苷(ddi),elvucitabine,恩曲他滨(ftc),恩替卡韦,泛昔洛韦,氟拉西林(5-fu),3’-氟取代的2’,3’-脱氧核苷类似物,包括3’-氟-2’,3’-双脱氧胸苷(flt)和3’-氟-2’,3’-双脱氧鸟苷(flg),福米韦生,9-鸟嘌呤,碘苷,拉米夫定(3tc),1-核苷(包括β-1-胸苷和β-1-2′-脱氧胞苷),喷昔洛韦,racivir,利巴韦林,迪替丁,司他夫定(d4t),塔利巴韦林(viramidine),替比夫定,替诺福韦,三氟尿苷伐昔洛韦,缬更昔洛韦,扎西他滨(ddc),齐多夫定(azt); f)非核苷类:金刚烷胺,阿替吡啶,卡普韦林,二芳基嘧啶(依曲韦林,rilpivirine),地拉夫定,二十二烷醇,乙米韦林,依法韦仑,膦甲酸(磷酰基甲酸),咪喹莫特,聚乙二醇干扰素,洛韦胺,洛德腺苷,甲吲噻腙,奈韦拉平,nov-205,长效干扰素α,鬼臼毒素,利福平,金刚乙胺,瑞喹莫德(r-848),醋胺金刚烷; g)蛋白酶抑制剂:安普那韦,阿扎那韦,boceprevir,darunavir,福萨那韦,印地那韦,洛匹那韦,奈非那韦,普来可那立,利托那韦,沙奎那韦,telaprevir(vx-950),替拉那韦; h)其它类型的抗病毒药物:抗体酶,阿比朵尔,calanolidea,ceragenin,氰维林-n,二芳基嘧啶,表没食子儿茶素没食子酸酯(egcg),膦甲酸,格里菲辛,taribavirin(viramidine),羟基脲,kp-1461,米替福新,普来可那立,混成抑制剂,利巴韦林,seliciclib; (5).放射性同位素,可以选自(放射性核素)3h、11c、14c、18f、32p、35s、64cu、68ga、86y、99tc、111in、123i、124i、125i、131i、133xe、177lu、211at、或213bi。 (6).发色团分子,能够吸收紫外线、荧光、红外光、近红外光、可见光;黄色素、红细胞、虹彩色素、白细胞、黑色素和蓝绿色素的一类或一个亚类、荧光分子吸收光后再发光的荧光化学物质。视觉光转导分子、荧光团分子、发光分子、萤光素化合物。非蛋白质有机荧光团,选自:氧杂蒽衍生物(包括荧光素、罗丹明、俄勒冈绿、伊红和德克萨斯红);花青衍生物(包括花青、吲哚羰花青、氧杂花青、硫代花青和部花青);方酸衍生物和环取代的方酸、包括seta、setau和square染料;萘衍生物(包括丹酰和氟硅酸钠衍生物);香豆素衍生物;恶二唑衍生物(包括吡啶基恶唑、硝基苯并恶唑和苯并恶二唑);蒽衍生物(包括蒽醌类、包括draq5、 draq7和cytrak橙);芘衍生物(包括级联蓝等);恶嗪衍生物(包括尼罗红、尼罗蓝、甲酚紫、恶嗪170等);吖啶衍生物(包括黄醇黄素、吖啶橙、吖啶黄等);芳基甲胺衍生物(包括金胺、结晶紫、孔雀石绿)和四吡咯衍生物(卟吩、酞菁、胆红素)。生色分子选自以下荧光化合物的任何类似物和衍生物:cf染料、draq和cytrak探针、bodipy、alexafluor、dylightfluor、atto和tracy、fluoprobes、abberiordyes、dy和megastokesdyes、sulfocy染料、hilytefluor、seta、setau和squaredyes、quasar和calfluordyes、surelightdyes(apc、rpepercp、phycobilisomes)、apc、apcxl、rpe、bpe、别藻蓝蛋白(apc)、氨基胭脂蛋白、apc-cy7偶联物、bodipy-fl、cascadeblue、cy2、cy3、cy3.5、cy3b、cy5、cy5.5、cy7、f荧光素、fluorx、羟基香豆素、丽丝胺罗丹明b、萤光黄、me-甲氧基香豆素、nbd、pacificblue、pacificorange、pe-cy5偶联物、pe-cy7偶联物、percp、r-藻红蛋白(pe)、red613、seta-555-叠氮化物、seta-555-dbco、seta-555-nhs、seta-580-nhs、seta-680-nhs、seta-780-nhs、seta-apc-780、seta-percp-680、seta-r-pe-670、setau-380-nhs、setau-405-马来酰亚胺、setau-405-nhs、setau-425-nhs、setau-647-nhs、texasred、tritc、trured、x-rhodamine、7-aad(7-氨基放线菌素d、cg-选择性的)、吖啶橙、色霉素a3、cytrak橙(redexcitationdark)、dapi、draq5、draq7、溴化乙锭、hoechst33258、hoechst33342、lds751、光辉霉素、碘化丙啶(pi)、sytox蓝、sytox绿、sytox橙、噻唑橙、to-pro:菁染料单体、toto-1、to-pro-1、toto-3、to-pro-3、yoseta-1、yoyo-1;荧光化合物:包括dcfh(2’、7′-二氯二氢荧光素、氧化形式)、dhr(二氢罗丹明123、氧化形式、光催化氧化)、fluo-3(am酯,ph>6)、fluo-4(am酯,ph7.2)、indo-1(am酯,低/高钙(ca2+))、snarf(ph6/9)、别藻蓝蛋白(apc)、amcyan1(四聚体、clontech)、asred2(四聚体、clontech)、azamigreen(单体)、azurite、b-藻红蛋白(bpe)、cerulean、cypet、dsred单体(clontech)、dsred2(“rfp”)、ebfp、ebfp2、ecfp、egfp(弱二聚体)、emerald(弱二聚体)、eyfp(弱二聚体)、gfp(s65a突变)、gfp(s65c突变)、gfp(s65l突变)、gfp(s65t突变)、gfp(y66f突变)、gfp(y66h突变)、gfp(y66w突变)、gfpuv、hcred1、j-red、katusha、kusabiraorange(单体、mbl)、mcfp、mcherry、mcitrine、midoriishicyan(二聚体、mbl)、mkate(tagfp635、单体)、mkeima-red(单体)、mko、morange、mplum、mraspberry、mrfp1(单体)、mstrawberry、mtfp1、mturquoise2、p3(藻胆体复合物)、多甲藻黄素-叶绿素-蛋白质复合物(percp)、r-phycoerythrin(rpe)、t-sapphire、tagcfp(二聚体)、taggfp(二聚体)、tagrfp(二聚体)、tagyfp(二聚体)、tdtomato(tandem二聚体)、topaz、turbofp602(二聚体)、turbofp635(二聚体)、turbogfp(二聚体)、turborfp(二聚体)、turboyfp(二聚体)、venus、wildtypegfp、ypet、zsgreen1(四聚体)、zsyellow1(四聚体)及其衍生物。 (7).细胞结合配体或受体激动剂,可以选自:叶酸衍生物、谷氨酸尿素衍生物、生长抑素及其类似物(选自奥曲肽(sandostatin)和兰瑞肽(somatuline))、芳香磺酰胺、aromaticsulfonamides、垂体腺苷酸环化酶激活肽(pacap)(pac1)、血管活性肠肽(vip/pacap)(vpac1,vpac2)、α-黑素细胞刺激激素(α-msh)、胆囊收缩素(cck)/胃泌素受体激动剂、蛙皮素(选自pyr-gln-arg-leu-gly-asn-gln-trp-ala-val-gly-his-leu-met-nh2)/胃泌素释放肽(grp)、神经降压素受体及其受体亚型(ntr1,ntr2,ntr3)、物质p(nk1受体)配体、神经肽y(y1–y6)、归巢肽包括rgd(arg-gly-asp),ngr(asn-gly-arg),二聚和多聚环状rgd肽(选自crgdfv),taasgvrsmh和ltlrwvglms(硫酸软骨素蛋白多糖ng2受体)和f3肽、细胞穿透肽(cpps)、肽激素,选自促黄体激素释放激素(lhrh)激动剂和拮抗剂,和促性腺激素释放激素(gnrh)激动剂,通过靶向卵泡刺激素(fsh)和黄体生成素(lh)起作用,以及睾酮产物,选自布舍瑞林(pyr-his-trp-ser-tyr-d-ser(otbu)-leu-arg-pro-nhet)、戈那瑞林(pyr-his-trp-ser-tyr-gly-leu-arg-pro-gly-nh2)、戈舍瑞林(pyr-his-trp-ser-tyr-d-ser(otbu)-leu-arg-pro-azgly-nh2)、组氨瑞林(pyr-his-trp-ser-tyr-d-his(n-苯基)-leu-arg-pro-nhet)、醋酸亮丙瑞林(pyr-his-trp-ser-tyr-d-leu-leu-arg-pro-nhet)、那法瑞林(pyr-his-trp-ser-tyr-2nal-leu-arg-pro-gly-nh2)、曲普瑞林(pyr-his-trp-ser-tyr-d-trp-leu-arg-pro-gly-nh2)、德舍瑞林、阿巴瑞克(ac-d-2nal-d-4-氯-d-3-(3-吡啶基)ala-ser-(n-me)tyr-d-asn-leu-异丙基-lys-pro-d-ala-nh2)、西曲瑞克(ac-d-2nal-d-4-chloro-phe-d-3-(3-pyridyl)ala-ser-tyr-d-cit-leu-arg-pro-d-ala-nh2)、地加瑞克(ac-d-2nal-d-4-chlorophe-d-3-(3-吡啶基)ala-ser-4-氨基phe(l-hydroorotyl)-d-4-氨基phe(氨基甲酰基)-leu-异丙基lys-pro-d-ala-nh2)和加尼瑞克(ac-d-2nal-d-4-chlorophe-d-3-(3-吡啶基)ala-ser-tyr-d-(n9,n10-二乙基)-homoarg-leu-(n9,n10-二乙基)-homoarg-pro-d-ala-nh2),模式识别受体(prrs),选自toll受体(tlrs)、c型凝集素和nodlike受体(nlrs)、降钙素受体激动剂、整合素受体及其受体亚型(选自αvβ1、αvβ3、αvβ5、αvβ6、α6β4、α7β1、αlβ2、αiibβ3)激动剂(选自grgdspk,环(rgdfv)(l1)及其衍生物[环(-n(me)r-gdfv)、环(r-sar-dfv)、环(rg-n(me)d-fv)、环(rgd-n(me)f-v)、环(rgdf-n(me)v-)(cilengitide)]、纳米抗体(vhh的衍生物(骆驼ig))、域抗体(dab、vh或vl域的衍生物)、双特异性t细胞engager(bite、双特异性双抗体)、双亲和重新定位(dart,双特异性双抗体)、四价串联抗体(tandab,二聚双特异双抗体)、anticalin(lipocalins的衍生物)、adnectins(10thfn3(fibronectin))、设计的锚蛋白重复蛋白(darpins)、avimers、egf受体和vegf受体激动剂。(8).药学上可接受的盐,酸或其衍生物,水合物或水合盐、或晶体结构、或任何上述药物的旋光异构体,外消旋物,非对映异构体或对映异构体。 9.如权利要求1所述的偶联物,其中drug1或drug2是发色团分子,用于检测,监测或研究细胞结合分子的相互作用和/或功能,和/或偶联物与靶细胞的相互作用。 10.如权利要求1所述的偶联物,其中drug1或drug2是聚亚烷基二醇[包含聚(乙二醇),聚(丙二醇),环氧乙烷或环氧丙烷的共聚物或其类似物],用于延长细胞结合分子在哺乳动物中的半衰期。 11.如权利要求1所述的偶联物,其中drug1或drug2是细胞结合配体,细胞受体激动剂或细胞受体结合分子,用作靶向导体/导向器以将偶联物递送至恶性细胞,或用于调节或共刺激期望的免疫应答或改变信号传导途径。 12.如权利要求1或2中任一项所述的偶联物,其中drug1或drug2选自tu-bulysin、美登素、紫杉烷类、cc-1065类似物、柔红霉素和多柔比星化合物、毒伞肽(包括鹅膏毒素)、indolecarboxamide、苯并二氮卓二聚体(例如吡咯并苯二氮杂卓(pbd)、托美霉素、氨茴霉素、吲哚并苯并二氮、咪唑并苯并噻二氮杂卓或恶唑烷并苯并二氮杂卓的二聚体)、加利车霉素类和烯二炔类抗生素、放线菌素、氮丝菌素、博来霉素、表柔比星、他莫昔芬、伊达比星、多拉司汀、澳瑞斯汀(例如mmae、mmaf、澳瑞斯汀pye、澳瑞斯汀tp、澳瑞斯汀2-aq、6-aq、eb(aeb)、efp(aefp)和它们的同系物)、多卡霉素、甲氨蝶呤,thiotepa,长春碱,长春新碱,hemasterins,nazumamides,microginins,radiumumins,altobactins,microsclerodermins,theonellamides,esperamicins,艾日布林,烟酰胺磷酸核糖基转移酶(nampt),rna,sirna,sirna抑制因子及其类似物和衍生物、药学上可接受的盐、酸、衍生物、水合物或水合盐、或晶体结构;或任何上述药物的旋光异构体、外消旋物、非对映异构体或对映异构体。 13.如权利要求1、2、8、9、10、11、或12中所述的偶联物,其中细胞结合剂/分子选自抗体、蛋白质、抗体、纳米抗体、维生素(包括叶酸)、肽、高分子胶束、脂质体、脂蛋白基药物载体、纳米颗粒药物载体、树枝状聚合物,以及涂附在细胞结合配体上的上述分子或颗粒,或上述物质的组合。 14.如权利要求1、2、8、9、10、11、12或13中任一项所述的偶联物,其中细胞结合剂/分子选自抗体,抗体样蛋白,完整抗体(多克隆抗体、单克隆抗体、抗体二聚体、抗体多聚体)或多特异性抗体(选自双特异性抗体、三特异性抗体或四特异性抗体),单链抗体,与靶细胞、单克隆抗体、单链单克隆抗体结合的抗体片段,与靶细胞结合的单克隆抗体片段,嵌合抗体,与靶细胞结合的嵌合抗体片段,域抗体,与靶细胞结合的域抗体片段,表面修饰抗体,单链表面修饰抗体,或与靶细胞结合的表面修饰抗体片段,人源化抗体或表面修饰抗体,人源化单链抗体,或与靶细胞结合的人源化抗体片段,抗独特型(抗-id)抗体,cdr,双抗体,三抗体,四抗体,微抗体,前抗体,前抗体片段,小免疫蛋白(sip),淋巴因子,激素,维生素,生长因子,菌落刺激因子,营养转运分子,大分子量蛋白,经抗体或大分子量蛋白质修饰的纳米颗粒或聚合物分子。 15.如权利要求1、2、8、9、10、11、12、13或14中任一项所述的偶联物,其中细胞结合剂/分子是能够抗肿瘤细胞、病毒感染细胞、微生物感染细胞、寄生虫感染细胞、自身免疫细胞、活化细胞、骨髓细胞、活化t细胞、b细胞或黑素细胞或者任何表达以下一种抗原或受体的细胞:cd2、cd2r、cd3、cd3gd、cd3e、cd4、cd5、cd6、cd7、cd8、cd8a、cd8b、cd9、cd10、cd11a、cd11b、cd11c、cd12、cd12w、cd13、cd14、cd15、cd15s、cd15u、cd16、cd16a、cd16b、cd17、cdw17、cd18、cd19、cd20、cd21、cd22、cd23、cd24、cd25、cd26、cd27、cd28、cd29、cd30、cd31、cd32、cd33、cd34、cd35、cd36、cd37、cd38、cd39、cd40、cd41、cd42、cd42a、cd42b、cd42c、cd42d、cd43、cd44、cd44r、cd45、cd45ra、cd45rb、cd45ro、cd46、cd47、cd47r、cd48、cd49a、cd49b、cd49c、cd49e、cd49f、cd50、cd51、cd52、cd53、cd54、cd55、cd56、cd57、cd58、cd59、cd60、cd60a、cd60b、cd60c、cd61、cd62e、cd62l、cd62p、cd63、cd64、cd65、cd65s、cd66、cd66a、cd66b、cd66c、cd66d、cd66e、cd66f、cd67、cd68、cd69、cd70、cd71、cd72、cd73、cd74、cd74、cd75、cd75s、cd76、cd77、cd78、cd79、cd79a、cd79b、cd80、cd81、cd82、cd83、cd84、cdw84、cd85、cd86、cd87、cd88、cd89、cd90、cd91、cd92、cdw92、cd93、cd94、cd95、cd96、cd97、cd98、cd99、cd99r、cd100、cd101、cd102、cd103、cd104、cd105、cd106、cd107、cd107a、cd107b、cd108、cd109、cd110、cd111、cd112、cd113、cdw113、cd114、cd115、cd116、cd117、cd118、cd119、cdw119、cd120a、cd120b、cd121a、cd121b、cdw121b、cd122、cd123、cdw123、cd124、cd125、cdw125、cd126、cd127、cd128、cdw128、cd129、cd130、cd131、cdw131、cd132、cd133、cd134、cd135、cd136、cdw136、cd137、cdw137、cd138、cd139、cd140a、cd140b、cd141、cd142、cd143、cd144、cd145、cdw145、cd146、cd147、cd148、cd149、cd150、cd151、cd152、cd153、cd154、cd155、cd156a、cd156b、cdw156c、cd157、cd158a、cd158b、cd159a、cd159b、cd159c、cd160、cd161、cd162、cd162r、cd163、cd164、cd165、cd166、cd167、cd167a、cd168、cd169、cd170、cd171、cd172a、cd172b、cd172g、cd173、cd174、cd175、cd175s、cd176、cd177、cd178、cd179、cd180、cd181、cd182、cd183、cd184、cd185、cd186、cdw186、cd187、cd188、cd189、cd190、cd191、cd192、cd193、cd194、cd195、cd196、cd197、cd198、cdw198、cd199、cdw199、cd200、cd200a、cd200b、cd201、cd202、cd202b、cd203、cd203c、cd204、cd205、cd206、cd207、cd208、cd209、cd210、cdw210、cd211、cd212、cd213a1、cd213a2、cd214、cd215、cd216、cdw217、cdw218a、cdw218b、cd219、cd220、cd221、cd222、cd223、cd224、cd225、cd226、cd227、cd228、cd229、cd230、cd231、cd232、cd233、cd234、cd235a、cd235ab、cd235b、cd236、cd236r、cd237、cd238、cd239、cd240、cd240ce、cd240d、cd241、cd242、cd243、cd244、cd245、cd246、cd247、cd248、cd249、cd250、cd251、cd252、cd253、cd254、cd256、cd257、cd258、cd259、cd260、cd261、cd262、cd263、cd264、cd265、cd266、cd267、cd268、cd269、cd270、cd271、cd272、cd273、cd274、cd275、cd276(b7-h3)、cd277、cd278、cd279、cd280、cd281、cd282、cd283、cd284、cd285、cd286、cd287、cd288、cd289、cd290、cd291、cd292、cdw293、cd294、cd295、cd296、cd297、cd298、cd299、cd300a、cd300c、cd300e、cd301、cd302、cd303、cd304、cd305、cd306、cd307、cd308、cd309、cd310、cd311、cd312、cd314、cd315、cd316、cd317、cd318、cd319、cd320、cd321、cd322、cd323、cd324、cdw325、cd326、cdw327、cdw328、cdw329、cd330、cd331、cd332、cd333、cd334、cd335、cd336、cd337、cdw338、cd339、4-1bb、5ac、5t4(滋养层糖蛋白、tpbg、5t4、wnt激活的抑制因子1或waif1)、腺癌抗原、ags-5、ags-22m6、激活素受体样激酶1、afp、akap-4、alk、α-整合素、αvβ6、氨基肽酶n、淀粉样蛋白β、雄激素受体、血管生成素2、血管生成素3、膜联蛋白a1、炭疽毒素保护性抗原、抗转铁蛋白受体、aoc3(vap-1)、b7-h3、炭疽芽孢杆菌、baff(b细胞活化因子)、b淋巴瘤细胞、bcr-abl、bombesin、boris、c5、c242抗原、ca125(碳水化合物抗原125、muc16)、ca-ix(或caix、碳酸酐酶9)、calla、canag、canislupusfamiliarisil31、碳酸酐酶ix、心肌肌球蛋白、ccl11(c-c基序趋化因子11)、ccr4(c-c趋化因子受体4型、cd194)、ccr5、cd3e(ε)、cea(癌胚抗原)、ceacam3、ceacam5(癌胚抗原)、cfd(因子d)、ch4d5、胆囊收缩素2(cck2r)、cldn18(claudin-18)、结块因子a、cripto、fcsf1r(集落刺激因子1受体、cd115)、csf2(集落刺激因子2、粒细胞-巨噬细胞集落刺激因子(gm-csf))、ctla4(细胞毒性t淋巴细胞相关蛋白4)、ctaa16.88肿瘤抗原、cxcr4(cd184)、c-x-c趋化因子受体4型、环状adp核糖水解酶、细胞周期蛋白b1、cyp1b1、巨细胞病毒、巨细胞病毒糖蛋白b、达比加群、dll3(δ样配体3)、dll4(δ样配体4)、dpp4(二肽基肽酶4)、dr5(死亡受体5)、大肠杆菌志贺毒素型pe-1、大肠杆菌志贺毒素型pe-2、ed-b、egfl7(含egf样结构域的蛋白质7)、egfr、egfrii、egfrviii、内皮糖蛋白(cd105)、内皮素b受体、内毒素、epcam(上皮细胞粘附分子)、epha2、episialin、erbb2(表皮生长因子受体2)、erbb3、erg(tmprss2ets融合基因)、大肠杆菌、etv6-aml、fap(成纤维细胞活化蛋白α)、fcgr1、甲胎蛋白、纤维蛋白ii、β链、纤连蛋白额外结构域-b、folr(叶酸受体)、叶酸受体α、叶酸水解酶、fos相关抗原1、呼吸道合胞病毒f蛋白、卷曲受体、岩藻糖基gm1、gd2神经节苷脂、g-28(细胞表面抗原glyvolipid)、gd3独特型、globoh、磷脂酰肌醇蛋白聚糖3、n-羟乙酰神经氨酸、gm3、gmcsf受体α链、生长分化因子8、gp100、gpnmb(跨膜糖蛋白nmb)、gucy2c(鸟苷酸环化酶2c、鸟苷酸环化酶c(gc-c)、肠鸟苷酸环化酶、鸟苷酸环化酶c受体、热稳定肠毒素受体)、热休克蛋白、血凝素、乙型肝炎表面抗原、乙型肝炎病毒、her1(人表皮生长因子受体1)、her2、her2/neu、her3(erbb-3)、igg4、hgf/sf(肝细胞生长因子/散射因子)、hhgfr、hiv-1、组蛋白复合物、hla-dr(人类白细胞抗原)、hla-dr10、hla-drb、hmwmaa、人绒毛膜促性腺激素、hngf、人分散因子受体激酶、hpve6/e7、hsp90、htert、icam-1(细胞间粘附分子1)、独特型、igf1r(igf-1、胰岛素样生长因子1受体)、ighe、ifn-g、influezahemag-glutinin、ige、igefc区、ighe、白细胞介素(il-1、il-2、il-3、il-4、il-5、il-5、il-6、il-6r、il-7、il-8、il-9、il-9、il-10、il-11、il-12、il-13、il-13、il-15、il-17、il-17、il-17a、il-18、il-19、il-20、il-20、il-21、il-22、il-23、il-27、il-27、或il-28)、il31ra、ilgf2(胰岛素样生长因子2)、整合素(α4、αiibβ3、αvβ3、αvβ3、α4β7、α7、α5β1、α5β7、α5β1、α5β7、α5β8、il-α6β4、α7β7、αllβ3、α5β5、αvβ5)、干扰素γ诱导蛋白、itga2、itgb2、kir2d、lck、le、legumain、lewis-y抗原、lfa-1(淋巴细胞功能相关抗原1、cd11a)、lhrh、lingo-1、脂磷壁酸、liv1a、lmp2、lta、mad-ct-1、mad-ct-2、mage-1、mage-2、mage-3、magea1、magea3、mage4、mart1、mcp-1、mif(巨噬细胞移动抑制因子或糖基化抑制因子(gif))、ms4a1(跨膜4域亚家族a成员1)、msln(间皮素)、muc1(粘蛋白1、细胞表面相关(muc1)或多形上皮粘蛋白(pem))、muc1-klh、muc16(ca125)、mcp1(单核细胞趋化蛋白1)、melana/mart1、ml-iap、mpg、ms4a1(跨膜4域亚家族a)、mycn、髓鞘相关糖蛋白、肌肉生长抑制素、na17、narp-1、nca-90(粒细胞抗原)、nectin-4(asg-22me)、ngf、神经凋亡调节蛋白酶1、nogo-a、notch受体、nucleolin、neu癌基因产物、ny-br-1、ny-eso-1、ox-40、oxldl(氧化低密度脂蛋白)、oy-tes1、p21、p53非突变体、p97、page4、pap、抗-(n-羟乙酰神经氨酸)的互补位、pax3、pax5、pcsk9、pdcd1(pd-1、程序性细胞死亡蛋白1、cd279)、pdgf-rα(α型血小板衍生生长因子受体)、pdgfr-β、pdl-1、plac1、plap样睾丸碱性磷酸酶、血小板衍生生长因子受体β、磷酸钠共转运蛋白、pmel17、聚唾液酸、蛋白酶3(pr1)、前列腺癌、ps(磷脂酰丝氨酸)、前列腺癌细胞、铜绿假单胞菌、psma、psa、psca、狂犬病病毒糖蛋白、rhd(rh多肽1(rhpi)、cd240)、恒河猴因子、rankl、rantes受体(ccr1、ccr3、ccr5)、rhoc、ras突变体、rgs5、robo4、呼吸道合胞病毒、ron、肉瘤易位断点、sart3、硬骨素、slamf7(slamfamilymember7)、selectinp、sdc1(syndecan1)、sle(a)、somatomedinc、sip(鞘氨醇-1-磷酸)、生长抑素、精子蛋白17、ssx2、steap1(前列腺的六种跨膜上皮抗原1)、steap2、stn、tag-72(肿瘤相关糖蛋白72)、survivin、t-cellreceptor、tcell跨膜蛋白、tem1(肿瘤内皮标志物1)、tenb2、腱生蛋白c(tn-c)、tgf-α、tgf-β(转化生长因子β)、tgf-β1、tgf-β2(转化生长因子β2)、tie(cd202b)、tie2、tim-1(cdx-014)、tn、tnf、tnf-α、tnfrsf8、tnfrsf10b(肿瘤坏死因子受体超家族成员10b)、tnfrsf13b(肿瘤坏死因子受体超家族成员13b)、tpbg(滋养层糖蛋白)、trail-r1(肿瘤坏死凋亡诱导配体受体1)、trailr2(死亡受体5(dr5))、肿瘤相关钙信号转导2、肿瘤特异性糖基化muc1、tweak受体、tyrp1(糖蛋白75)、trop-2、trp-2、酪氨酸酶、vcam-1(cd106)、vegf、vegf-a、vegf-2(cd309)、vegfr-1、vegfr2或波形蛋白、wt1、xage1或表达任何胰岛素生长因子受体或任何表皮生长因子受体的细胞。 16.如权利要求15所述的肿瘤细胞,选自淋巴瘤细胞、骨髓瘤细胞、肾细胞、乳腺癌细胞、前列腺癌细胞、卵巢癌细胞、结直肠癌细胞、胃癌细胞、鳞状癌细胞、小细胞肺癌细胞、非小细胞肺癌细胞、睾丸癌细胞、恶性细胞或任何因不受控制的、快速生长和分裂而引起癌症的细胞。 17.如权利要求1所述的偶联物,其中drug1或drug2是发色分子,选自于以下结构ac01、ac02、ac03、ac04、ac05、ac06、andac07、ac08、ac09、ac010、和ac11: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、n的定义与前文相同;r12和r12’独立地为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、o(ch2ch2o)pch2ch2nhso3h、nh(ch2ch2o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh-ar-cooh、nh-ar-nh2,其中p=0-5000,aa是氨基酸,(aa)n包含了相同或不同的天然或非天然氨基酸,n=1-30。 18.如权利要求1所述的偶联物,其中drug1或drug2是tubulysin类似物,选自于以下结构t01、t02、t03、t04、t05、t06、t07、t08、t09、t10、t11、t12、t13、t14、t15、t16、t017、t18、t19、t20、t21、t22和t23: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2、和n的定义如前文所述;y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;mab为抗体,优选地为单克隆抗体;r12为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、nhoh、nhor1、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nhso3h、nh(ch2ch2o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh(ch2ch2nh)pch2ch2nh2、nh(ch2ch2s)pch2ch2nh2、nh(ch2ch2nh)pch2ch2oh、nh(ch2ch2s)pch2ch2oh、nh-r1-nh2、或nh(ch2ch2o)pch2ch2nhpo3h2、其中aa为1-8个氨基酸;n为1-20;p为1-5000;r1、r1’、r2、r3、r4和r5独立地为h、c1-c8直链或支链烷基、酰胺或胺;c2-c8芳基、烯基、炔基、杂芳基、杂烷基、烷基环烷基、酯、醚、杂环烷基或酰氧基胺;或含有1-8个氨基酸的肽或(och2ch2)p或(och2ch(ch3))p、其中p是1到约5000的整数;两个r:r1r2、r2r3、r1r3或r3r4可以形成烷基、芳基、杂芳基、杂烷基或烷基环烷基的3~8环状;x3是h、ch3、ch2ch3、c3h7或x1’r1’,其中x1’是nh、n(ch3)、nhnhnh、o或s;r1’为h或c1-c8直链或支链烷基、芳基、杂芳基、杂烷基、烷基环烷基或酰氧基胺;r3’为h或c1-c6直链或支链烷基;z3为h、coor1、nh2、nhr1、or1、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1、o-糖苷(葡萄糖苷、半乳糖苷、甘露糖苷、葡萄糖醛酸苷/葡糖苷酸、阿洛糖苷、果糖苷等)、nh糖苷、s-糖苷或ch2糖苷;m1和m2独立地是h、na、k、ca、mg、nh4或nr1r2r3。 19.如权利要求1所述的偶联物,其中drug1或drug2是加利车霉素类似物,选自于以下结构c01和c02: 其中q、x1x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1。 20.如权利要求1所述的偶联物,其中drug1或drug2是美登素生物碱类似物,选自于以下结构my01、my02、my03、my04、my05、my06、my07和my08: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文;优选地x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1。 21.如权利要求1,其中drug1或drug2紫杉烷类似物,选自于以下结构tx01,tx02和tx03: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义同前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o) nhnhc(o)和c(o)nr1。 22.如权利要求1,其中drug1或drug2是cc-1065类似物和/或多卡霉素类似物,选自于以下结构cc01、cc02、cc03、cc04、cc05、cc06和cc07: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;q优选地为单克隆抗体;z3是h、po(om1)(om2)、so3m1、ch2po(om1)(om2)、ch3n(ch2ch2)2nc(o)-、o(ch2ch2)2nc(o)-、r1或糖苷。 23.如权利要求1所述偶联物,其中drug1或drug2是柔红霉素或多柔比星同系物,选自于以下结构da01、da02、da03、da04、da05、da06、da07、da08、da09、da10和da11: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义如前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;r12为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、nhoh、nhor1、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nh-so3h、nh(ch2ch2o)pch2ch2nh-so3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2-ch2nhpo3h2、nh(ch2ch2o)pch2-ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh(ch2ch2nh)pch2-ch2nh2、nh(ch2ch2s)pch2ch2nh2、nh(ch2ch2nh)pch2ch2oh、nh(ch2ch2s)pch2-ch2oh、nh-r1-nh2、或nh(ch2ch2o)pch2ch2nhpo3h2。 24.如权利要求1所述的偶联物,其中drug1或drug2是澳瑞斯汀或多拉司汀类似物,选自于以下结构au01、au02、au03、au04、au05、au06、au07、au08、au09、au10、au11、au12、au13、au14、au15、au16、au17、au18、au19、au20、au21、au22、au23、au24、au25、au26、和au27: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义同前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;r12是oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、nhoh、nhor1、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nh-so3h、nh(ch2ch2o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2-ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2ch2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、nh(ch2ch2nh)pch2-ch2nh2、nh(ch2ch2s)pch2ch2nh2、nh(ch2ch2nh)pch2ch2oh、nh(ch2ch2s)pch2-ch2oh、nh-r1-nh2或nh(ch2ch2o)pch2ch2nhpo3h2,其中aa为1-8个氨基酸;p为1-5000;q优选为单克隆抗体;r1、r2、r3、r4和r5独立地为h,c1-c8直链或支链烷基,芳基,杂芳基,杂烷基,烷基环烷基,酯,醚,酰胺,胺,杂环烷基或酰氧基胺;或含有1-8个氨基酸的肽,或具有式(och2ch2)p或(och2ch(ch3))p的聚乙烯基氧单,其中p是1至约5000的整数。两个r:r1r2,r2r3,r1r3或r3r4可形成烷基,芳基,杂芳基,杂烷基或烷基环烷基的3~8个成员环;x3为h,ch3或x1’r1’,其中x1’为nh,n(ch3),nhnh,o或s,r1’是h或c1-c8直链或支链烷基,芳基,杂芳基,杂烷基,烷基环烷基,酰氧基胺;r3’是h或c1-c6直链或支链烷基;z3’是h、coor1、nh2、nhr1、or1、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1、或o-糖苷(葡糖苷、半乳糖苷、甘露糖苷、葡糖苷酸/葡糖苷酸、阿洛糖苷、果糖苷等)、nh糖苷、s-糖苷或ch2糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 25.如权利要求1所述的偶联物,其中drug1或drug2是苯并二氮卓二聚体,选自以下结构pb01、pb02、pb03、pb04、pb05、pb06、pb07、pb08、pb09、pb10、pb11、pb12、pb13、pb14、pb15、pb16、pb17、pb18、pb19、pb20、pb21、pb22、pb23、pb24、pb25、pb26、pb27、pb28、pb29、pb30、pb31和pb32: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;r1、r2、r3、r1’、r2’和r3’独立地为h、f、cl、=o、=s、oh、sh、c1-c8直链或支链烷基、芳基、烯基、杂芳基、杂烷基、烷基环烷基、酯(coor5or–oc(o)r5)、醚(or5)、酰胺(conr5)、氨基甲酸酯(oconr5)、胺(nhr5、nr5r5′)、杂环烷基或酰氧基胺(-c(o)nhoh、-onhc(o)r5),含20种天然或非天然氨基酸的多肽,或如式(och2ch2)p或(och2ch(ch3))p的聚乙烯氧基单,其中p是1至约5000的整数。两个r:r1r2、r2r3、r1r3、r1’r2’、r2’r3’或r1’r3’可独立形成烷基、芳基、杂芳基、杂烷基或烷基环烷基的3~8个环;x3和y3独立地为n、nh、ch2或cr5、其中r5、r6、r12和r12’独立地为h、oh、nh2、nh(ch3)、nhnh2、cooh、sh、oz3、sz3、f、cl、或c1-c8直链或支链烷基、芳基、杂芳基、杂烷基、烷基环烷基、酰氧基胺;z3为h、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1或o-糖苷(葡萄糖苷、半乳糖苷、甘露糖苷、葡糖苷酸/葡糖苷酸、阿洛糖苷、果糖等)、nh-糖苷、s-糖苷或ch2-糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 26.如权利要求1所述的偶联物,其中drug1或drug2是鹅膏毒肽及其类似物,选自于以下结构am01、am02、am03、am04、am05、am06、am07、am08和am09: 其中x1、x2、q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh,nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、chc(o)nh-nhc(o)、c(o)nr1或缺省;r7、r8和r9独立地为h、oh、or1、nh2、nhr1、c1-c6烷基或缺省;y2为o、o2、nr1、nh或缺省;r10是ch2、o、nh、nr1,nhc(o)、nhc(o)nh、nhc(o)o、oc(o)o、c(o)、oc(o)、oc(o)(nr1)、(nr1)c(o)(nr1)、c(o)r1或缺省;r11为oh、nh2、nhr1、nhnh2、nhnhcooh、o-r1-cooh、nh-r1-cooh、nh-(aa)ncooh、o(ch2ch2o)pch2ch2oh、o(ch2ch2o)pch2ch2nh2、nh(ch2ch2o)pch2ch2nh2、nr1r1’、o(ch2ch2o)pch2ch2cooh、nh(ch2ch2o)pch2-ch2cooh、nh-ar-cooh、nh-ar-nh2、o(ch2ch2o)pch2ch2nhso3h、nh(ch2ch2-o)pch2ch2nhso3h、r1-nhso3h、nh-r1-nhso3h、o(ch2ch2o)pch2ch2nhpo3h2、nh(ch2ch2o)pch2ch2nhpo3h2、or1、r1-nhpo3h2、r1-opo3h2、o(ch2ch2o)pch2c-h2opo3h2、or1-nhpo3h2、nh-r1-nhpo3h2、或nh(ch2ch2o)pch2ch2nhpo3h2其中aa为1-20个氨基酸;n和m1独立地为1-30;p为1-5000;z3为h、oh、coor1、nh2、nhr1、or1、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1或o-糖苷(葡萄糖苷,半乳糖苷,甘露糖苷,葡糖苷/葡糖苷酸,阿洛糖苷,果糖苷等)nh糖苷、s-糖苷或ch2-糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 27.如权利要求1所述的偶联物,其中drug1或drug2是喜树碱及其衍生物,选自以下结构cp01、cp02、cp03、cp04、cp05和cp06: 其中q、x1,x2,y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)、c(o)nr1或缺省;z3为h、oh、coor1、nh2、nhr1、or1、ch3、conhr1、nhcor1、ocor1、op(o)(om1)(om2)、och2op(o)(om1)(om2)、oso3m1、r1、或o-糖苷(葡萄糖苷、半乳糖苷、甘露糖苷、葡糖醛酸苷/葡糖醛酸苷、阿洛糖苷、果糖苷等)、nh-糖苷、s-糖苷或ch2-糖苷;m1和m2独立地为h、na、k、ca、mg、nh4、nr1r2r3。 28.如权利要求1所述的偶联物,其中drug1或drug2是艾日布林及其衍生物,选自于以下结构eb01,和eb02: 其中q、x1、x2、y1、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选地,x1、x2、y1和y2独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)、c(o)nr1或缺省。 29.如权利要求1所述的偶联物,其中drug1或drug2是烟酰胺磷酸核糖基转移酶抑制剂,选自于以下结构np01,np02,np03,np04,np05,np06,np07,np08和np09: 其中q、x1、x2、y1、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;x5为f、cl、br、i、oh、or1、r1、opo3h2、oso3h、nhr1、ocor1、nhcor1;优选地,x1、x2、y1和y2为独立地为o、n、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)、c(o)nr1或缺省。 30.如权利要求1或10所述的偶联物,其中drug1或drug2是聚亚烷基二醇类似物,选自以下结构pg01、pg02和pg03: 其中q、x1、x2、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义与前文相同;优选地y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;p为1-5000;r1和r3与上述r1定义相同,且优选地r1和r3为独立地h、oh、och3、ch3、或oc2h5。 31.如权利要求1所述的偶联物,其中drug1或drug2是细胞结合配体或细胞受体激动剂及其类似物,选自以下结构:lb01(叶酸偶联物)、lb02(pmsa配体偶联物)、lb03(pmsa配体偶联物)、lb04(pmsa配体偶联物)、lb05(生长抑素偶联物)、lb06(生长抑素偶联物)、lb07(奥曲肽、生长抑素类似物偶联物)、lb08(兰瑞肽、生长抑素类似物偶联物)、lb09(伐普肽(sanvar)、生长抑素类似物偶联物)、lb10(caix配体偶联物)、lb11(caix配体偶联物)、lb12(胃泌素释放肽受体(grpr)、mba偶联物)、lb13(促黄体激素释放激素(lh-rh)配体和gnrh偶联物)、lb14(促黄体激素释放激素(lh-rh)和gnrh配体偶联物)、lb15(gnrh拮抗剂、abarelix偶联物)、lb16(钴胺素、维生素b12类似物偶联物)、lb17(钴胺素、维生素b12类似物偶联物)、lb18(αvβ3整联蛋白受体、环状rgd五肽偶联物)、lb19(vegf受体的异二价肽配体偶联物)、lb20(神经髓质素b偶联物)、lb21(g蛋白偶联受体蛙皮素偶联物)、lb22(类toll受体tlr2偶联物)、lb23(雄激素受体偶联物)、lb24(αv整合素受体西仑吉肽/环(-rgdfv-)偶联物)、lb25(利福布汀类似物偶联物)、lb26(利福布汀类似物偶联物)、lb27(利福布汀类似物偶联物)、lb28(氟氢可的松偶联物)、lb29(地塞米松偶联物)、lb30(丙酸氟替卡松偶联物)、lb31(丙酸倍氯米松偶联物)、lb32(曲安奈德偶联物)、lb33(泼尼松偶联物)、lb34(泼尼松龙偶联物)、lb35(甲基强的松龙偶联物)、lb36(倍他米松偶联物)、lb37(伊立替康类似物偶联物)、lb38(克唑替尼类似物偶联物)、lb39(硼替佐米类似物偶联物)、lb40(卡菲佐米类似物偶联物)、lb41(卡菲佐米类似物偶联物)、lb42(亮丙瑞林类似物偶联物)、lb43(曲普瑞林类似物偶联物)、lb44(克林霉素偶联物)、lb45(利拉鲁肽类似物偶联物)、lb46(索马鲁肽类似物偶联物)、lb47(瑞他帕林类似物偶联物)、lb48(indibulin类似物偶联物)、lb49(长春碱类似物偶联物)、lb50(利西那肽类似物偶联物)、lb51(奥希替尼类似物偶联物)、lb52(核苷类似物偶联物)、lb53(厄洛替尼类似物偶联物)和lb54(拉帕替尼类似物偶联物): 其中y5、是n、ch、c(cl)、c(ch3)、或c(coor1);r1是h、c1-c6烷基、c3-c8芳基; 其中x1、x2、q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、c(o)nhnhc(o)和c(o)nr1;x3为ch2、o、nh、nhc(o)、nhc(o)nh、c(o)、oc(o)、oc(o)(nr3)、r1、nhr1、nr1、c(o)r1或缺省;x4为h、ch2、oh、o、c(o)、c(o)nh、c(o)n(r1)、r1、nhr1、nr1、c(o)r1或c(o)o;x5为h、ch3、f、或cl;m1和m2为独立的h、na、k、ca、mg、nh4、nr1r2r3;r6为5′-脱氧腺苷、me、oh、或cn。 32.如权利要求1所述的偶联物,其中细胞毒性分子是dna,rna,mrna,小干扰rna(sirna),微rna(mirna),或与piwi相互作用rnas(pirna),偶联物选自以下结构si-1: 其中q、y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n的定义如前文所述;优选地,x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)和c(o)nr1;是单链或双链的dna、rna、mrna、sirna、mirna或pirna。 33.权利要求1、5、6、12、13、14、15、16、17、18、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35或36中任一项所述的偶联物,其中细胞连接分子/剂选自于igg抗体,单克隆抗体,或igg类抗体蛋白质,具有st1、st2、st3、st4、st5、或st6的结构,其通过轻重链之间的二硫键,或重链之间上部二硫键,或重链之间下部二硫键被还原产生的一对巯基,特异性偶联: 其中y1、y2、r1、r2、r3、r4、r5、r5’、z1、z2和n定义同前文所述;优选的x1、x2、y1和y2独立地为o、nh、nhnh、nr5、s、c(o)o、c(o)nh、oc(o)nh、oc(o)o、nhc(o)nh、nhc(o)s、oc(o)n(r1)、n(r1)c(o)n(r1)、ch、ch2、c(o)nhnhc(o)和c(o)nr1;m1、m2、m3和m4独立地为1-30。 34.如权利要求33所述的偶联物,当含有相同或不同本发明中的双键连接子的细胞毒性分子,依次地,逐步地与细胞结合分子偶联时,在细胞结合分子的不同偶联位点上连接的药物(或细胞毒性分子)和m1可以是不同的。 35.如权利要求33或34中任一项所述的偶联物,其中drug选自tubulysin、美登素、紫杉烷类、cc-1065类似物、柔红霉素和多柔比星化合物、毒伞肽(包括鹅膏毒素)、indolecarboxamide、苯并二氮卓二聚体、吡咯并苯二氮杂卓(pbd)二聚体、托美霉素二聚体、氨茴霉素二聚体、吲哚并苯并二氮二聚体、咪唑并苯并噻二氮杂卓、恶唑烷并苯并二氮杂卓的二聚体、加利车霉素类和烯二炔类抗生素、放线菌素、氮丝菌素、博来霉素、表柔比星、他莫昔芬、伊达比星、多拉司汀、澳瑞斯汀(包括甲基澳瑞斯汀、mmae、mmaf、澳瑞斯汀pye、澳瑞斯汀tp、澳瑞斯汀2-aq、6-aq、eb(aeb)、efp(aefp)和它们的同系物)、多卡霉素、格尔德霉素、hsp90抑制剂、烟酰胺磷酸核糖基转移酶抑制剂、centanacycin、甲氨喋呤、噻替派、长春地辛、长春新碱、erbulins,、半米塔林、nazumamides、微晶蛋白、放射敏素、streptonigtin、sn38或其它喜树碱类似物或降解物、alterobactin、microsclerodermins、theonellamides、esperamicin、pnu-及其类似物和衍生物、药学上可接受的盐、酸、衍生物、水合物或水合盐;或晶体结构;或任何上述药物的旋光异构体、外消旋物、非对映异构体或对映异构体;或权利要求8所述的细胞毒性分子/化合物。 36.如权利要求3所述的化合物,具有如a-01、a-02、a-03、a-04、b-01、b-02、b-03、b-04、b-05、b-06、b-07、b-08、b-09、b-10、b-11、b-12、b-13、b-14、b-15、b-16、c-01、c-02、c-03、c-04、c-05、c-06、c-07、c-08、c-09、c-10、c-11、c-12、d-01、d-02、d-03、d-04、d-05、d-06、pg-04、97、98、116、125、129、133、135、157a、157b、157c、157d、157e、157f、162、163、235a、235b、235c、236a、236b、236c、238a、238b、238c、255、256、258a、258b、258c、260、262、267、271、272、274、276、278、282、284、286、287、306、309、314、318和325的结构: 37.如权利要求1所述的偶联物,具有如aa-01、aa-02、aa-03、aa-04、ba-01、ba-02、ba-03、ba-04、ba-05、ba-06、ba-07、ba-08、ba-09、ba-10、ba-11、ba-12、ba-13、ba-14、ba-15、ba-16、ca-02、ca-03、ca-04、ca-05、ca-06、ca-07、ca-08、ca-09、ca-10、ca-11、ca-12、da-01、da-02、da-03、da-04、da-05或da-06、99、117、126、130、136、158a、158b、158c、158d、158e、158f、164、237a、237b、237c、239a、239b、239c、257、259、261、263、268、273、275、277、279、283、285、288、307、310、315、319和326的结构: 其中m1,和n与权利要求1中的定义相同;mab是抗体;交叉键表示它可以连接两个原子中的任何一个。 38.一种药物组合物,其包含治疗有效量的,权利要求1、2、8、9、10、11、12、13、14、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、或37、中的任一偶联物,和药学上可接受的盐,载体,稀释剂或辅料,或偶联物的组合物,以治疗癌症、感染或自身免疫性疾病。 39.如权利要求38所述的药物组合物,其以液体制剂形式或以冻干制剂形式存在,包括以重量计的,0.01%-99%的权利要求1、2、8、9、10、11、12、13、14、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、或37、中一种或多种偶联物,0.0%-20.0%的一种或多种多醇;0.0%-2.0%的一种或多种表面活性剂;0.0%-5.0%的一种或多种防腐剂;0.0%-30%的一种或多种氨基酸;0.0%-5.0%一种或多种抗氧化剂;0.0%-0.3%的一种或多种金属螯合剂;0.0%-30.0%的一种或多种缓冲盐,用于将制剂的ph调节至4.5至8.5;以及0.0%-30.0%的一种或多种等渗剂,用于在复溶后施用于患者时,将渗透压调节在250至350mosm之间。 其中多醇选自果糖、甘露糖、麦芽糖、乳糖、阿拉伯糖、木糖、核糖、鼠李糖、半乳糖、葡萄糖、蔗糖、海藻糖、山梨糖、松三糖、棉子糖、甘露醇、木糖醇、赤藓糖醇、麦芽糖醇、乳糖醇、赤藓糖醇、苏糖醇、山梨糖醇、甘油或l-葡萄糖酸盐及其金属盐; 其中表面活性剂选自聚山梨酸酯20、聚山梨酸酯40、聚山梨酸酯65、聚山梨酸酯80、聚山梨酸酯81或聚山梨酸酯85、泊洛沙姆、聚(环氧乙烷)-聚(环氧丙烷)、聚乙烯-聚丙烯、triton;十二烷基硫酸钠(sds))、月桂基硫酸钠;辛基钠糖苷;十二烷基、肉豆蔻酰基、亚油基或硬脂基磺基甜菜碱;十二烷基、肉豆蔻酰基、亚油基或硬脂基肌氨酸;亚油酸、肉豆蔻基或十六烷基甜菜碱;月桂酰胺基丙基、椰油酰胺基丙基-、亚油酰胺基丙基-、豆蔻酰氨基丙基-、棕榈酰丙基-丙基或异硬脂酰胺基丙基-甜菜碱(月桂酰胺基丙基);肉豆蔻酰丙基-、棕榈酰胺基丙基或-异硬脂酰胺基丙基-二甲基胺;甲基椰油酰基-钠或甲基油基-甲基十二烷基磺酸钠;十二烷基甜菜碱-、椰油酰胺基丙基甜菜碱和椰油两性甘氨酸酯;或异硬脂基乙基亚胺基乙醇硫酸盐;聚乙二醇、聚丙二醇,以及乙烯和丙二醇的共聚物; 其中的防腐剂选自苯甲醇、十八烷基二甲基苄基氯化铵、六甲基氯化铵、苯扎氯铵、苄索氯铵、苯酚、丁基和芐基醇、对羟基苯甲酸烷基酯、对羟基苯甲酸甲酯或对羟基苯甲酸丙酯、邻苯二酚、间苯二酚、环己醇、3-戊醇或间甲酚 其中氨基酸选自精氨酸、胱氨酸、甘氨酸、赖氨酸、组氨酸、鸟氨酸、异亮氨酸、亮氨酸、丙氨酸、甘氨酸谷氨酸或天冬氨酸; 其中抗氧化剂选自抗坏血酸、谷胱甘肽、胱氨酸或甲硫氨酸; 其中螯合剂选自edta或egta; 其中缓冲盐选自柠檬酸、抗坏血酸、葡萄糖酸、碳酸、酒石酸、琥珀酸、乙酸或邻苯二甲酸的钠、钾、铵或三羟基乙基氨基盐;tris或氨丁三醇的盐酸、磷酸或硫酸盐;精氨酸、甘氨酸、甘氨酰甘氨酸或组氨酸的乙酸盐、氯化物、磷酸盐、硫酸盐或琥珀酸盐; 其中等渗剂选自甘露醇、山梨醇、乙酸钠、氯化钾、磷酸钠、磷酸钾、柠檬酸三钠或氯化钠。 40.如权利要求38或39所述的药物组合物,其特征在于以液体或冻干制剂的形式保存在西林瓶,瓶,预填充注射器或预填充自动注射器中。 41.如权利要求1、2、8、9、10、11、12、13、14、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、或37、所述的偶联物,或权利要求38或39所述的药物组合物,具有体外,体内或离体细胞杀伤活性。 42.如权利要求38或39所述的药物组合物,其与化疗剂,放射治疗,免疫治疗剂,自身免疫失调剂,抗感染剂或其他偶联物同时给药,以协同治疗或预防癌症、自身免疫性疾病或传染性疾病。 43.如权利要求42所述的协同剂,选自以下一种或几种药物:阿巴西普、abemaciclib、乙酸阿比特龙、abraxane、阿杜卡奴单抗、对乙酰氨基酚/氢可酮、阿卡替尼、阿杜卡奴单抗、阿达木单抗、adxs31-142、adxs-her2、阿法替尼二马来酸盐、阿地白介素、阿乐替尼、阿伦单抗、艾力替尼、alitretinoin、ado-trastuzumabemtansine、安非他明/右旋安非他明、阿那曲唑、apatinib、阿立哌唑、蒽环类药物、阿立哌唑、atazanavir、阿特朱单抗、阿托伐他汀、avelumab、avxs-101、axicabtageneciloleucel、阿西替尼、贝利司他、bcg-live、贝伐单抗、贝沙罗汀、blinatumomab、硼替佐米、波舒替尼、本妥昔单抗、布格替尼、布地奈德、布地奈德/福莫特罗、丁丙诺啡、byl719(α特异性pi3k抑制剂)、卡巴他赛、卡博替尼、卡马替尼、卡培他滨、卡非佐米、嵌合抗原受体工程t(car-t)细胞、塞来昔布、色瑞替尼、西妥昔单抗、西奥罗尼、西达本胺、环孢素、cinacalcet、克唑替尼、考比替尼、cosentyx、克唑替尼、tisagenlecleucel、达比加群、达拉菲尼、达卡巴嗪、达利珠单抗、达科替尼、达托霉素、达拉木单抗、darbepoetinalfa、darunavir、达沙替尼、denileukindiftitox、地诺单抗、depakote、dexlansoprazole、dexmethylphenidate、地塞米松、l-3、4-二羟基苯基丙氨酸、dinutuximab、阿法链道酶、强力霉素、度洛西汀、德卫利昔、度伐鲁单抗、依托珠单抗、emicizumab、emtricibine/利匹韦林/替诺福韦、地索普西富马酸、恩曲他滨/替诺福韦/依非韦伦、依诺肝素、恩沙替尼、恩杂鲁胺、易吡替尼、阿法依伯汀、厄洛替尼、埃索美拉唑、eszopiclone、依那西普、依维莫司、依西美坦、依维莫司、艾塞那肽er、依泽替米贝、依泽替米贝/辛伐他汀、法米替尼、非诺贝特、非戈替尼、非格司亭、芬戈莫德、氟马替尼、丙酸氟替卡松、氟替卡松/沙美特罗、呋喹替尼、氟维司群、gazyva、吉非替尼、醋酸格拉替雷、醋酸戈舍瑞林、gsk(bcma-adc)、henatinib、埃克替尼、伊马替尼、替伊莫单抗、依鲁替尼、埃克替尼、艾代拉里斯、异环磷酰胺、英夫利昔单抗、咪喹莫特、immunocyst、immunobcg、iniparib、门冬胰岛素、地特胰岛素、甘精胰岛素、赖脯胰岛素、干扰素α、干扰素α-1b、干扰素α-2a、干扰素α-2b、干扰素β、干扰素β1a、干扰素β1b、干扰素γ-1a、拉帕替尼、易普利姆玛、异丙托溴铵/沙丁胺醇、伊沙唑米、卡努玛、莱地鲁单伉、醋酸兰瑞肽、来那度胺、来那度胺、甲磺酸乐伐替尼、来曲唑、左旋甲状腺素、左旋甲状腺素、利多卡因、利奈唑胺、利拉鲁肽、lisdexamfetamine、ln-144(肿瘤浸润淋巴细胞)、lorlatinib、德立替尼/delitinib、美金刚、甲氧基聚乙二醇epoetin-beta、哌醋甲酯、美托洛尔、曲美替尼、美西他滨/利匹韦林/替诺福韦、莫达非尼、莫米松、mycidac-c、霉酚酸、耐昔妥珠单抗、诺拉替尼、尼罗替尼、尼拉帕尼、尼沃鲁单抗、奥法木单抗、奥比曲妥珠单抗、奥瑞珠单抗、奥拉帕尼、奥美沙坦、奥美沙坦/氢氯苯噻哒嗪、奥马珠单抗、omega-3脂肪酸乙酯、oncorine、奥司他韦、奥希替尼、羟考酮、奥扎莫德、帕波克利、帕利珠单抗、帕尼单抗、帕比司他、帕唑帕尼、派姆单抗、pd-1抗体、pd-l1抗体、培美曲塞、帕妥珠单抗、吡非尼酮、肺炎球菌结合疫苗、泊马度胺、普瑞巴林、proscavax、普萘洛尔、普喹替尼、吡咯替尼、喹硫平、雷贝拉唑、氯化镭223、雷洛昔芬、raltegravir、雷莫芦单抗、雷珠单抗、瑞戈非尼、瑞博西尼、瑞莎珠单抗、利妥昔单抗、利伐沙班、罗米地辛、罗苏伐他汀、磷酸鲁索替尼、沙丁胺醇、索凡替尼、索马鲁肽、sevelamer、西地那非、司妥昔单抗、西莫替尼、西帕替尼/cipatinib、辛波莫德、sipuleucel-t、西他列汀、西他列汀/二甲双胍、solifenacin、索兰珠单抗、索尼吉布、索拉非尼、磺胺替尼、舒尼替尼、他克莫司、tacrimus、他达那非、他莫昔芬、甲磺酸达拉非尼、talimogenela-herparepvec、talazoparib、特拉瑞韦、talazoparib、替莫唑胺、替西罗莫司、替奈普酶、替诺福韦/恩曲他滨、富马酸替诺福韦酯、睾酮凝胶、替加卡托/依伐卡托、沙利度胺、theliatinib、ticebcg、噻托溴铵、tisagenlecleucel、托珠单抗、托瑞米芬、曲美替尼、曲妥珠单抗、曲贝替定(海鞘素743)、曲美替尼、替西木单抗、trifluridine/tipiracil、维甲酸、乌帕替尼、uro-bcg、优特克单抗、valoctocogeneroxaparvovec、缬沙坦、veliparib、凡德他尼、威罗菲尼、维特克拉、维莫德吉、索凡替尼、伏立诺他、阿柏西普、zostavax及其类似物、衍生物、药学上可接受的盐、载体、稀释剂或其辅料,或以上的组合。
2024最新激活全家桶教程,稳定运行到2099年,请移步至置顶文章:https://sigusoft.com/99576.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌侵权/违法违规的内容, 请联系我们举报,一经查实,本站将立刻删除。
文章由激活谷谷主-小谷整理,转载请注明出处:https://sigusoft.com/26629.html