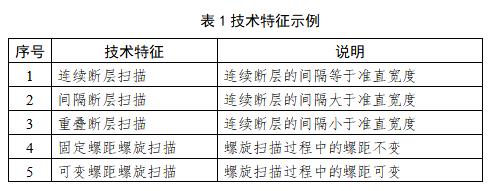
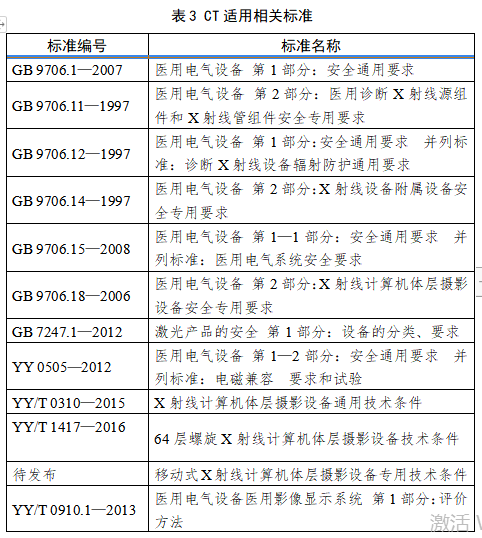
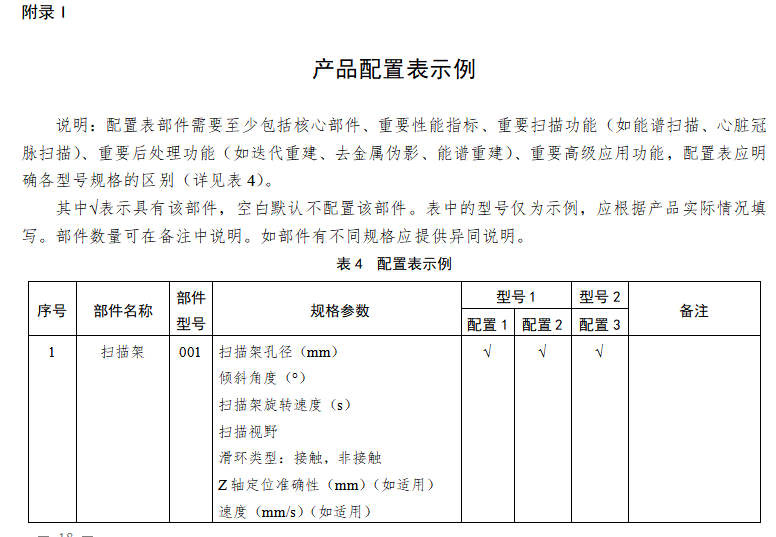
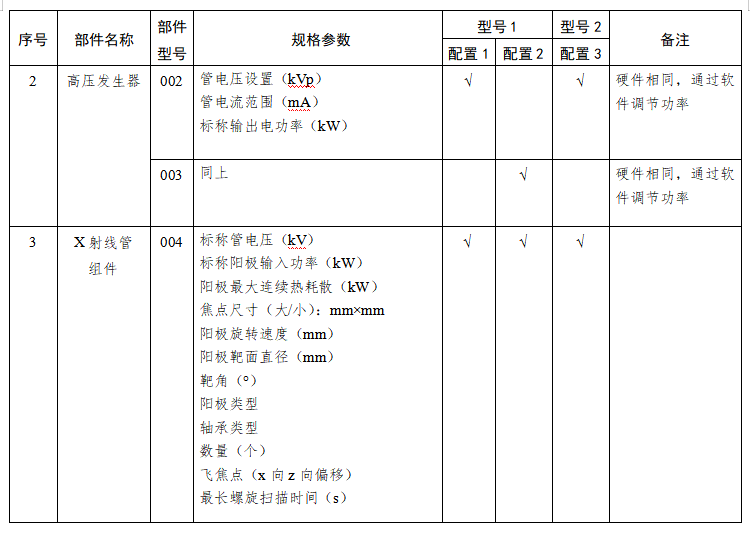
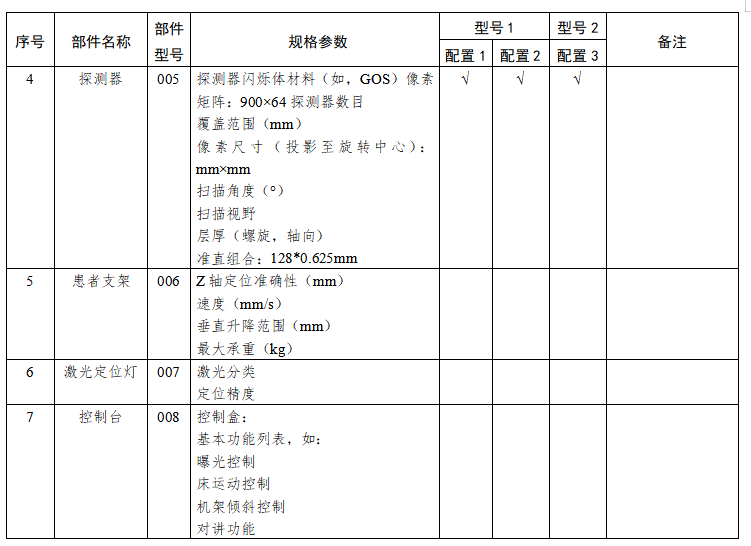
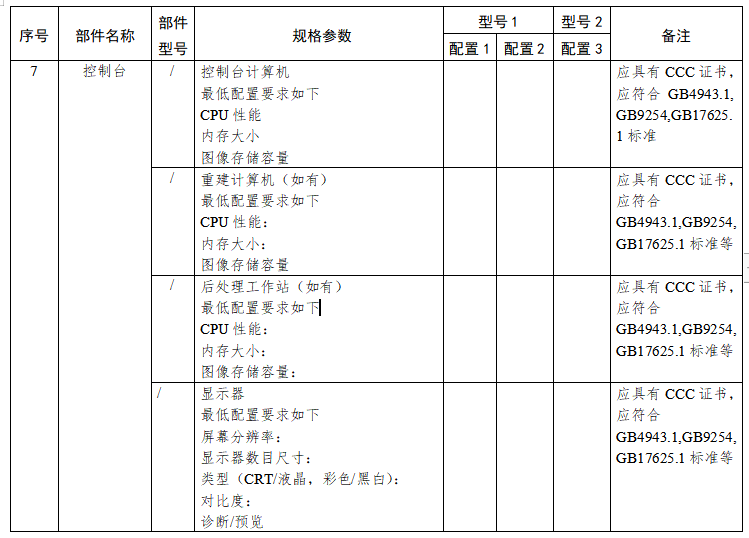
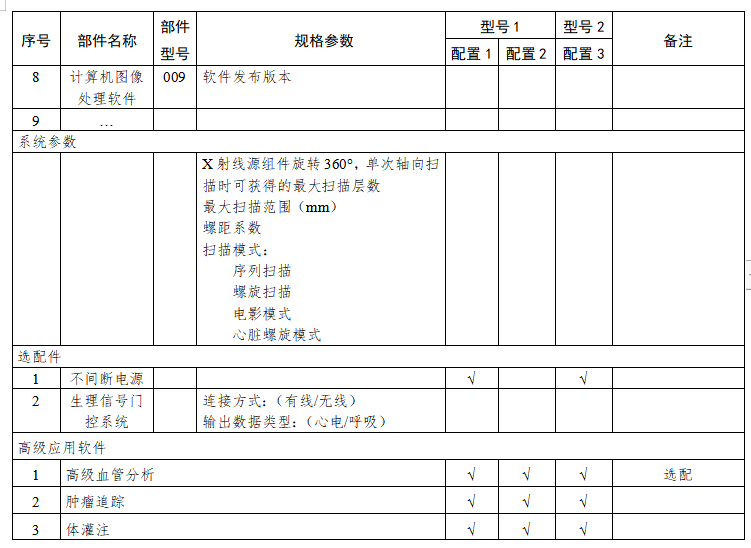
X射线计算机体层摄影设备注册技术审查指导原则 西格玛医学 本指导原则是对X射线计算机体层摄影设备的一般要求,注册申请人应依据具体产品的特性对注册申报资料的内容进行充实和细化。注册申请人还应依据具体产品的特性确定其中的内容是否适用,若不适用,需具体阐述其理由及相应的科学依据。 本指导原则是对注册申请人和审查人员的指导性文件,但不包括注册审批所涉及的行政事项,亦不作为法规强制执行,如果有能够满足相关法规要求的其他方法,也可以采用,但是需要提供详细的研究资料和验证资料。应在遵循相关法规的前提下使用本指导原则。本指导原则是在现行法规和标准体系以及当前认知水平下制定的,随着法规和标准的不断完善,以及科学技术的不断发展,本指导原则相关内容也将进行适时的调整。 一、适用范围 本指导原则适用于X射线计算机体层摄影设备(以下简称CT)。参考《医疗器械分类目录》(国家食品药品监督管理总局公告2017年第104号),产品属于子目录06—医用成像器械,一级产品类别为02—X射线计算机体层摄影设备(CT),二级产品类别为01—X射线计算机体层摄影设备(CT),按第三类医疗器械管理。 二、产品综述资料 (一)概述 X射线计算机体层摄影设备根据安装方式及预期用途不同,可划分为移动式CT、固定式CT、车载CT。根据设计原理不同,可划分为单源CT和双源CT,普通CT和能谱CT。 (二)产品描述 1.描述产品工作原理 2.描述产品结构组成(如适用) (1)应描述系统所有组件及附件。应提供系统布置图,说明扫描间、操作间、设备间的设备分布。应提供图示,标识主要部件,图文标识顺序应一致。 (2)应提供系统框图。 (3)应描述各部件、选件、附件工作原理、主要功能及相互关系;应描述不同规格的部件(如有)的异同。可提供必要的实物图、拆解图、剖视图。 a.管组件应说明内部关键组件。 b.高压发生器应说明高压整流逆变的原理。 c.扫描架应提供剖视图,说明内部关键组件。 d.准直系统、探测器及数据系统应提供拆解图及尺寸图、原理框图。 e.控制系统应提供框图及必要注释,说明控制架构。 f.选配硬件应提供图示,说明附加功能及与基本组成的相互关系。 g.软件组件应提供厂家声称的临床高级应用功能的描述,如心脏分析、高级血管分析、结肠分析、肿瘤追踪、体灌注、脑灌注、脑导航、肺结节评估、肺密度、齿科应用、钙化积分、仿真内窥镜、能谱分析、肝脏分析、肺分析、4D 分析、骨密度分析等。 h.附件包括定位辅助附件和非医疗附件(如系统模体、卷纸架、桌椅、家具、附件柜等),非医疗附件无需申报注册。 3.应提供系统供电连接框图来说明主要部件的电路连接关系,如配电盘(如有)、电源分配机柜或单(如有)、稳压电源(如有)、不间断电源(如有)、机架、病床、控制台、扫描控制盒等电路连接关系。 4.关键部件规格描述,按照附录I提供。 5.设备技术特征描述 应包括重要的扫描功能(如能谱扫描、心脏冠脉扫描)、重要后处理功能(如迭代重建、去金属伪影、能谱重建)的描述,包括不限于表1的内容。申报产品新的技术特征应注明。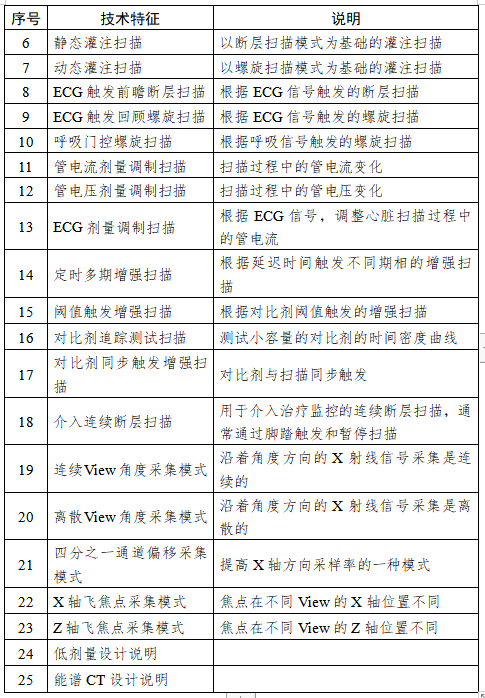










2024最新激活全家桶教程,稳定运行到2099年,请移步至置顶文章:https://sigusoft.com/99576.html
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌侵权/违法违规的内容, 请联系我们举报,一经查实,本站将立刻删除。 文章由激活谷谷主-小谷整理,转载请注明出处:https://sigusoft.com/20372.html